
Politechnika Warszawska
Wydział Inżynierii Środowiska
Uzdatnianie wody do celów przemysłowych
„Zmiękczanie i dekarbonizacja wody na jonitach”
Grupa: ZWiOŚ 1
Zespół 1:
Diana Usarek
Carlos Pyrcz
Joanna Stochowska
Piotr Zapałowski
Łukasz

1. Wstęp teoretyczny
Zmiękczenie i dekarbonizacja wody na jonitach opiera się na wykorzystaniu zjawiska
wymiany jonów pomiędzy substancją stałą (jonitem) a otaczającym ją roztworem
(uzdatnianą wodą). Ważne jest aby zachodzący proces był odwracalny i powodował
znacznych zmian w strukturze ciała stałego. Jonity dzielimy w zależności od rodzaju
usuwanych z wody jonów na: kationity (wymieniają kationy) i anionity (wymieniają
aniony). Ze względu na rodzaj grup funkcyjnych kationity dzielimy na: słabo kwaśne
(usuwają kationy związane z resztami słabych kwasów) oraz silnie kwaśne (usuwają
wszystkie kationy związane z resztami kwasów). Anionity dzielimy na: słabo
zasadowe (usuwają reszty mocnych kwasów) i silnie zasadowe (usuwają reszty
wszystkich kwasów).
Zmiękczanie wody polega na usuwaniu z niej jonów wapnia i magnezu. W tym celu
stosuje się kationit silnie kwaśny w cyklu sodowym. W wyniku wymiany kationów z
wody na jon sodowy powstaje wodorowęglan sodu, który przy wysokim ciśnieniu i
temperaturze rozkłada się na NaOH i CO
2
, odpowiedzialne za pienienie się wody
oraz korozję.
Dekarbonizacja wody polega na usunięciu związanego dwutlenku węgla poprzez
użycie kationitu w cyklu wodorowym. W wyniku zachodzących reakcji powstają silne
kwasy mineralne oraz znaczne ilości CO
2
. Dwutlenek węgla usuwany jest w wyniku
odgazowania, natomiast kwaśny odczyn wody neutralizowany jest poprzez
zmieszanie strumieni wody z kationitów pracujących odpowiednio w cyklu sodowym i
wodorowym.
2. Cel i zakres ćwiczenia
Celem ćwiczenia było przebadanie przebiegu procesu zmiękczania i dekarbonizacji
wody na kationitach sodowym i wodorowym pracujących w układzie równoległym
oraz ustalenie stosunku zmieszania strumieni cieczy z obu jonitów.
Zakres ćwiczenia obejmował:
Przeprowadzenie procesu zmiękczania oraz dekarbonizacji wody w zadanych
warunkach
Analizę właściwości wody przed i po uzdatnianiu
Ustalenie odpowiedniego stosunku w celu uzyskania zadanych parametrów
3. Metodyka
Proces wymiany jonowej prowadzony był na dwóch kationitach pracujących
równolegle w cyklu sodowym i wodorowym przy ustalonej prędkości filtracji 5 [m/h].
W surowej oraz uzdatnionej wodzie oznaczano: twardość, zasadowość, kwasowość
ogólną i mineralną i pH.
Na podstawie uzyskanych wyników obliczono stopień wymieszania odcieków z
kationitów w celu uzyskania wartości wymaganych dla wody do celów
przemysłowych. Zmieszaną wodę doprowadzono do wrzenia w celu odpędzenia
CO
2
.
4. Otrzymane wyniki
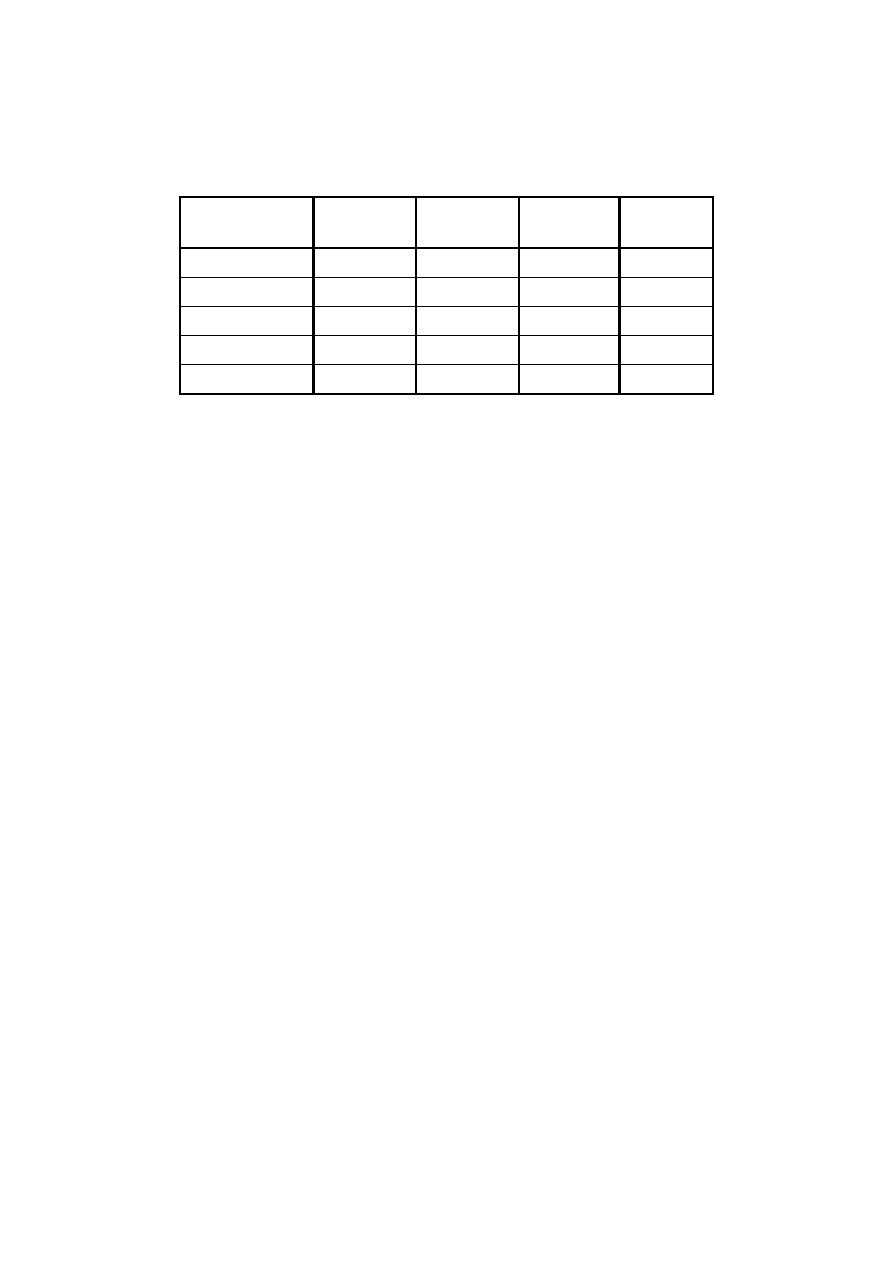
Otrzymane wyniki przedstawiono w postaci tabelarycznej:
Oznaczany
wskaźnik
Jednostka
Woda
surowa
Kt
Na+
Kt
H+
Twardość
[mval/l]
6,00
0,00
0,00
Zasadowość
[mval/l]
3,60
3,25
0,00
Kwasowość og.
[mval/l]
0,50
0,60
5,10
Kwasowość min.
[mval/l]
-
-
4,50
pH
[-]
7,02
7,21
2,67
Stopień wymieszania strumieni cieczy po kationitach obliczono z następującego
układu równań:
+
= 0,2
∙
−
∙
=
∙ 0,2
Gdzie:
- V
1
- objętość próbki po kationicie pracującym w cyklu sodowym [ml]
- V
2
- objętość próbki po kationicie pracującym w cyklu wodorowym [ml]
- Z- zasadowość po kationicie pracującym w cyklu sodowym [mval/l]
- K
min
- kwasowość
po kationicie pracującym w cyklu wodorowym [mval/l]
-
x- założona zasadowość w wodzie po zmieszaniu strumieni cieczy [mval/l]
Przy założeniu x=0,5[mval/l] otrzymano następujące objętości wymieszania:
= 0,13 = 130
= 0,07 = 70
Dla wody po wymieszaniu w powyższym stosunku uzyskano następujące wyniki
badań:
pH=5,62
zasadowość = 0,7[mval/l]
twardość= 0 [mval/l]
Po odpędzeniu CO
2
z wody po wymieszaniu pH wynosi 6,5.
5. Analiza wyników. Wnioski.
Uzyskane podczas badań wyniki porównano z wartościami wymaganymi dla wody do
celów przemysłowych:
Twardość = 0
[mval/l]
Zasadowość
(0,3 ÷ 1,0)
[mval/l]
pH
(6,5 ÷ 9,0)

Analiza wyników:
kationit pracujący w cyklu sodowym:
twardość wody uzyskała wartość 0 [mval/l]
co świadczy o pełnej skuteczności
w usunięciu jonów wapnia i magnezu
zasadowość utrzymuje się na podobnym poziomie. Zmienia się rodzaj
zasadowości, ponieważ w wyniku pojawienia się wodorowęglanu sodu
(NaHCO
3
) pojawiła się zasadowość alkaliczna.
kationit pracujący w cyklu sodowym nie wpływa w sposób znaczący na zmianę
kwasowości ogólnej
nie odnotowujemy kwasowości mineralnej, ponieważ pH znajduje się w
zakresie 4,5-8,3
ponieważ kwasowość oraz zasadowość pozostają na porównywalnym
poziomie, nie odnotowuje się zmiany pH
kationit pracujący w cyklu wodorowym:
twardość wody uzyskała wartość 0 [mval/l]
co świadczy o pełnej skuteczności
w usunięciu jonów wapnia i magnezu
kwasowość mineralna wrasta (z 0 do 4,5), ponieważ po kationicie wodorowym
pojawiają się silne kwasy mineralne: kwas solny i kwas siarkowy
kwasowość ogólna wzrasta, w wyniku pojawienia się kwasów mineralnych
w wyniku znacznego wzrostu kwasowości oraz spadku pH poniżej wartości
4,5, nie odnotowujemy występowania zasadowości
pH spada w znacznym stopniu (z 7,02 do 2,67), ponieważ następuje wymiana
kationów z wody na jony H
+
oraz powstają silne kwasy mineralne
woda powstała w wyniku wymieszania cieczy po kationitach:
w wyniku wymiany jonowej na kationicie pracującym w cyklu sodowym jak i
na kationicie pracującym w cyklu wodorowym uzyskano spadek twardości do
0[mval/l], dlatego w wodzie po zmieszaniu twardość również nie występuje co
odpowiada wymaganiom stawianym wodzie na cele przemysłowe
po zmieszaniu wody z obu kationitów w obliczonych proporcjach uzyskaliśmy
wartość zasadowości 0,7[mval/l] mieszczącą się w przedziale wymaganym dla
wody przeznaczonej na cele przemysłowe
pH zmieszanej cieczy wynosi 5,62 i nie mieści się w wymaganym przedziale
(6,5-9,0). Po odpędzeniu CO
2
pH wzrasta do 6,5 spełniając wymagania
stawianym wodzie na cele przemysłowe
Wnioski:
Zmiękczanie wody zarówno na kationicie pracującym w cyklu sodowym jak i
wodorowym ma wysoką skuteczność (w warunkach laboratoryjnych uzyskaliśmy
całkowite usunięcie twardości). Zastosowanie pojedynczego kationitu nie pozwala
jednakże na uzyskanie parametrów wymaganych dla wód wykorzystywanych w
celach przemysłowych. Osiągnięcie odpowiedniego stopnia uzdatnienia wymaga

zastosowania układu równoległego kationitów ze zmieszaniem odcieków w
odpowiednich proporcjach. Dopiero tak wymieszana i odgazowana nadaje się do
wykorzystania w celach przemysłowych.
Woda uzdatniona zgodnie z opisem zawartym w metodyce spełnia wymogi stawiane
wodzie używanej do celów przemysłowych.
Wyszukiwarka
Podobne podstrony:
3 Zmiekczanie wody
Zmiękczanie wody, Studia, Studia
Wzory zmiękczania wody, Materiały - Biotechnologia
CIclack zmiękczacz wody
grochulska segal,systemy odnowy wody, zmiękczanie wody metodami strąceniowymi
Wzory - zmiekczanie wody 1 , chemia techniczna nieorganiczna
3 Zmiekczanie wody metoda termiczna
zmiękczanie wody fosforanem trójsodowym, Ścieki przemysłowe, Sprawozdania- Scieki przemysłowe
Zmiekczanie wody, bio, Chemia, Biofizyka, Toksykologia, Wykład PWrocławska
Dekarbonizacja wody i zmiękczanie w wymienniku sodowym
Technologia wody zmiękczanie
Ujecia wody
Ruchy wody morskiej i wody podziemne
GEOLOGIA 3 wody podziemne
zbiornik wody czystej, dezynfekcja
więcej podobnych podstron