
Ćwiczenia z Geochemii Ogólnej
PROJEKT 2
Wykonali:
Łukasz Kielar
Damian Krupa
248081
254492
Gr. 3DIŚ3
Gr. 3DIŚ3
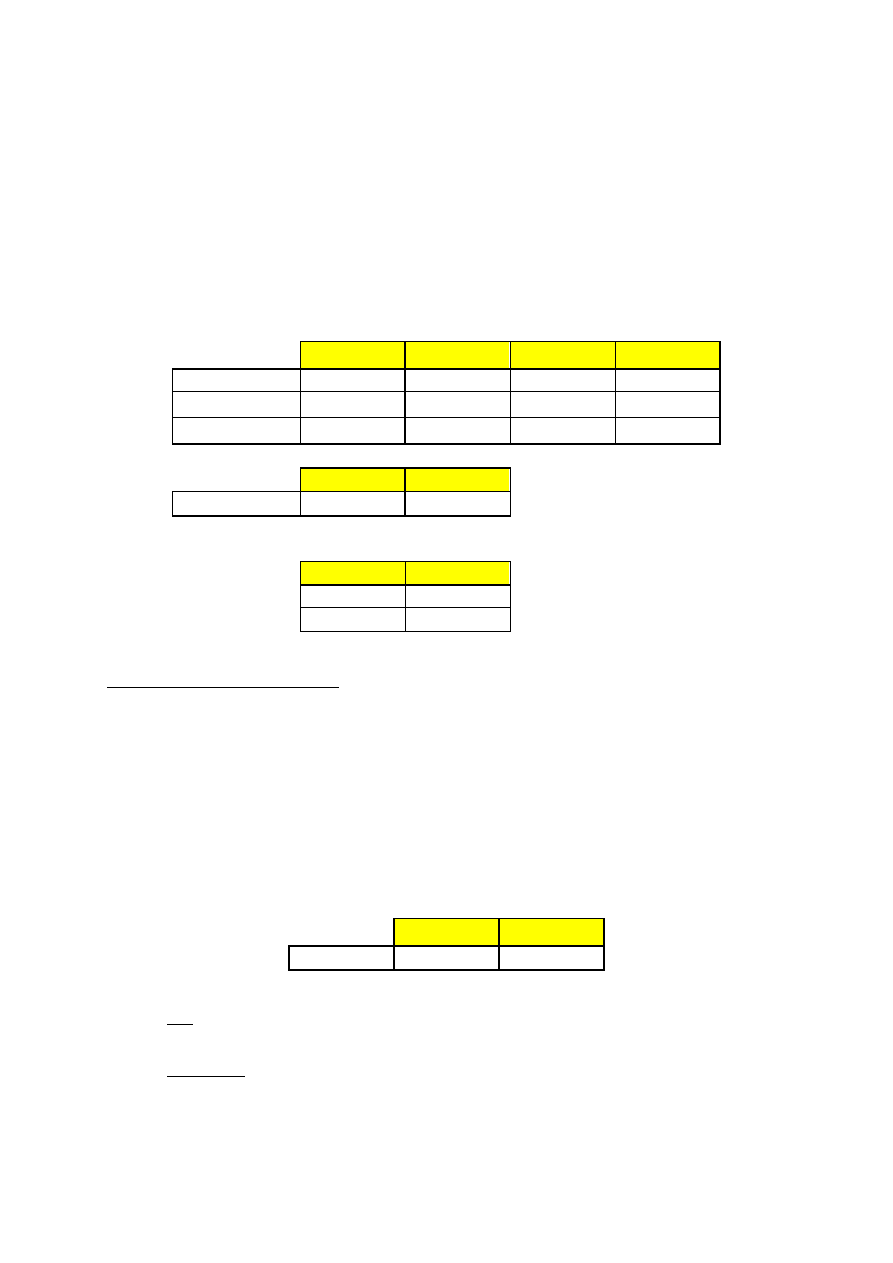
2
Ćwiczenie 1.
Dostałeś w spadku działkę budowlaną w okolicach Polkowic. Teren jest częściowo uzbrojony – jest
kanalizacja, ale wodę musisz mieć swoją. Zamawiasz studnię wierconą, która kosztuje Cię dość sporo bo
zwierciadło wód gruntowych okazało się tam głęboko. Podobno, jak twierdzi sąsiad, „to przez te kopalnie
pod nami”. Z przerażeniem myślisz, że Twoja woda może pochodzić z poziomu piaskowców
kruszconośnych bogatych w pirotyn. Zanim wyślesz próbkę do analizy na żelazo postanawiasz policzyć ile
żelaza byłoby w wodzie, gdyby była ona w równowadze z pirotynem.
a)
Czy pirotyn jest trwałym minerałem w reakcji rozpuszczania?
↔
+
Przyjmujemy temperaturę (T)=25
o
C oraz ciśnienie (p)=1 atm.
δG
o
[cal/mol]
δG
o
[J/mol]
δH
o
[cal/mol]
δH
o
[J/mol]
Pirotyn FeS
-24000
-100414,21
-23900
-99995,82
Fe
2+
-18850
-78866,99
-21300
-89117,61
S
2+
19253,52
80555,29
7887,23
32999,58
[J/mol*K]
[cal/mol*K]
R (stała gazowa)
8,314
1,987
Przelicznik jednostek
[J]
[cal]
1
0,23901
4,184
1
Wartość energii swobodnej (G
o
)
∆
= ∆
ó
− ∆
ó
= ∆
!
+ ∆
"
# − ∆
! "
∆
= 102102,51 [J mol
⁄
]
Reakcja ma tendencję do samorzutnego zachodzenia w lewo, co oznacza że pirotyn (FeS) w
warunkach normalnych jest minerałem trwałym.
b)
Oblicz stałą równowagi K
eq
(równa w tym wypadku stałej rozpuszczalności K
sp
) w temperaturze wody
ze studni po ogrzaniu do temperatury pokojowej równej 25
o
C.
[
o
C]
[K]
T
25
298,15
0
1
= 2
∆3
45
[−]
0
1
= 2
678678,96
:,;6<∗8>:,69
[−]
0
1
= 1,29 ∗ 10
6:
= 10
6@,:>
[−]

3
c)
Czy w temperaturze pokojowej w warunkach normalnych nastąpi wytrącanie galeny z wody
studziennej, w której stężenia jonów wynoszą odpowiednio:
[mol/dm
3
]
[Fe
2+
]
10
-7
[S
2-
]
10
-6,5
AB =
BCD
0
"E
[−]
Gdzie: SI – wskaźnik nasycenia roztworu,
IAP – iloczyn jonowy obliczany na podstawie aktywności substancji biorących udział w reakcji,
K
SP
– stała równowagi reakcji dla danych warunków.
AB =
[Fe
2+
][S
2−
]
0
"E
AB =
10
−7
∗ 10
−6,5
10
6@,:>
AB = 24,55 ∗ 10
;
= 10
<,;>
[−]
Wskaźnik nasycenia roztworu jest większy od 1, co mówi nam o tym, że roztwór jest nasycony i
nastąpi wytrącanie pirotynu z wody studziennej.
4
Ćwiczenie 2.
Na podstawie otrzymanych wyników analiz chemicznych dwóch próbek wód:
•
przedstaw wyniki analizy w mmol/dm
3
,
•
oblicz błąd analizy na podstawie bilansu ładunków,
•
oblicz twardość [mval/dm
3
] oraz nazwij wodę z uwagi na twardość ogólną,
•
przedstaw wyniki graficznie na diagramie Pipera.
Ponadto:
•
Wodę powierzchniową zaklasyfikuj do odpowiedniej klasy czystości oraz sprawdź czy jej skład
chemiczny pozwala na wykorzystanie do celów pitnych (Rozporządzenie Ministra Zdrowia z
29.03.2007 r. i 20.04.2010 r.). Jeśli nie, to jakie składniki/parametry o tym decydują?
•
Sprawdź, czy skład chemiczny wody „mineralnej” pozwala na nazwanie jej wodą mineralną, a jeśli
tak, to uzupełnij jej nazwę.
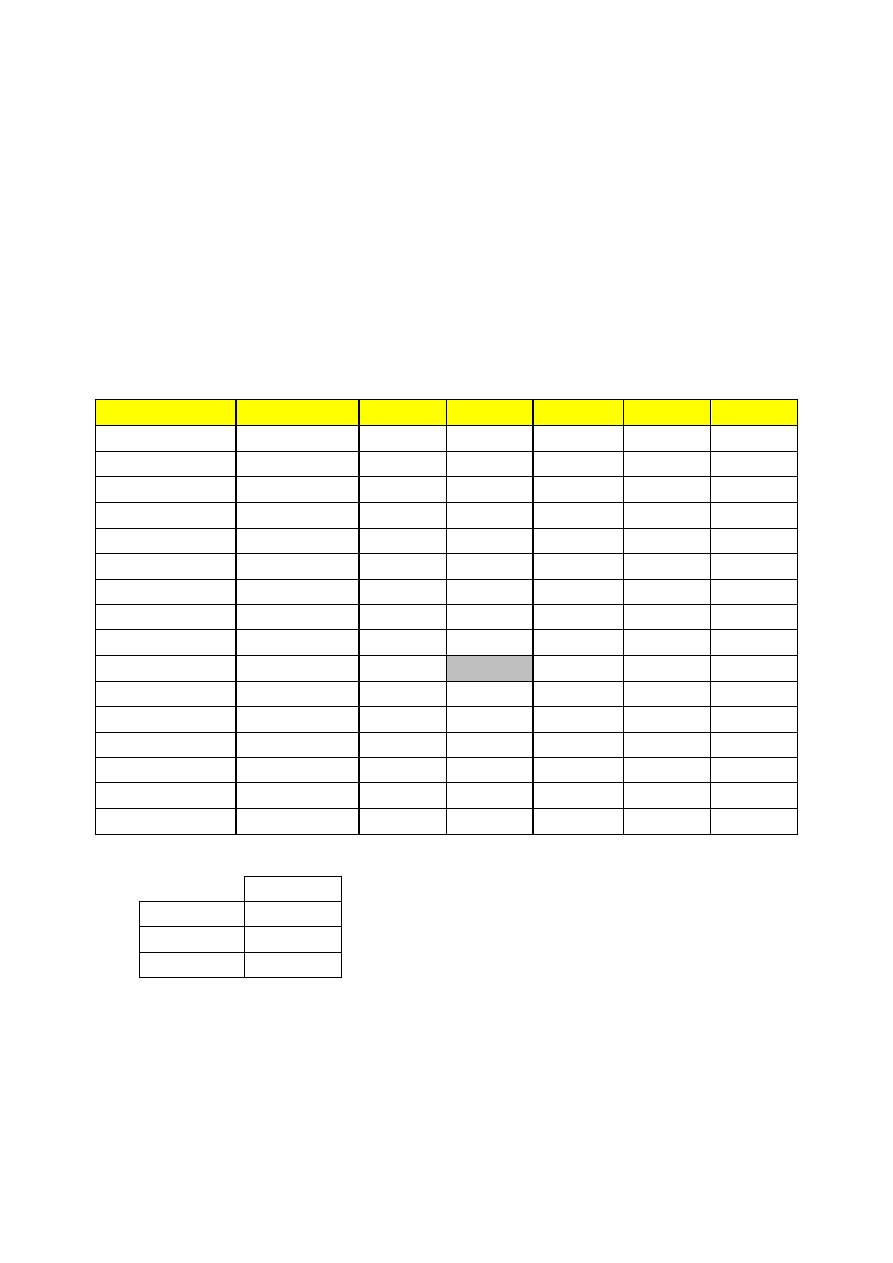
1)
Woda nr 1
Składnik
Masa molowa Ładunek
mg/dm
3
mmol/dm
3
mval/dm
3
Klasa
Ca
2+
40,08
2
62,00
1,547
3,094
II
Mg
2+
24,31
2
13,80
0,568
1,135
I
Na
+
22,99
1
14,70
0,639
0,639
-
K
+
39,10
1
2,40
0,061
0,061
-
HCO
3
-
61,02
1
259,60
4,254
4,254
-
SO
4
2-
96,07
2
24,50
0,255
0,510
I
Cl
-
35,45
1
2,80
0,079
0,079
I
PO
4
3-
94,97
3
0,40
0,004
0,013
III
NO
3
-
62,01
1
8,01
0,129
0,129
II
NH
4
+
18,05
1
0,67
0,037
0,037
II
Li
+
6,94
1
0,01
0,001
0,001
-
Fe
2+
55,85
2
0,15
0,003
0,005
II
Mn
2+
54,94
2
0,038
0,001
0,001
I
Sr
2+
87,62
2
0,60
0,007
0,014
-
ChZT-Cr
-
-
4,24
-
-
I
BZT
5
-
-
1,70
-
-
I
Bilans jonowy:
[mval/dm
3
]
∑K
4,989
∑A
4,985
suma
9,974
Gdzie: ∑K – suma kationów,
∑A – suma anionów.
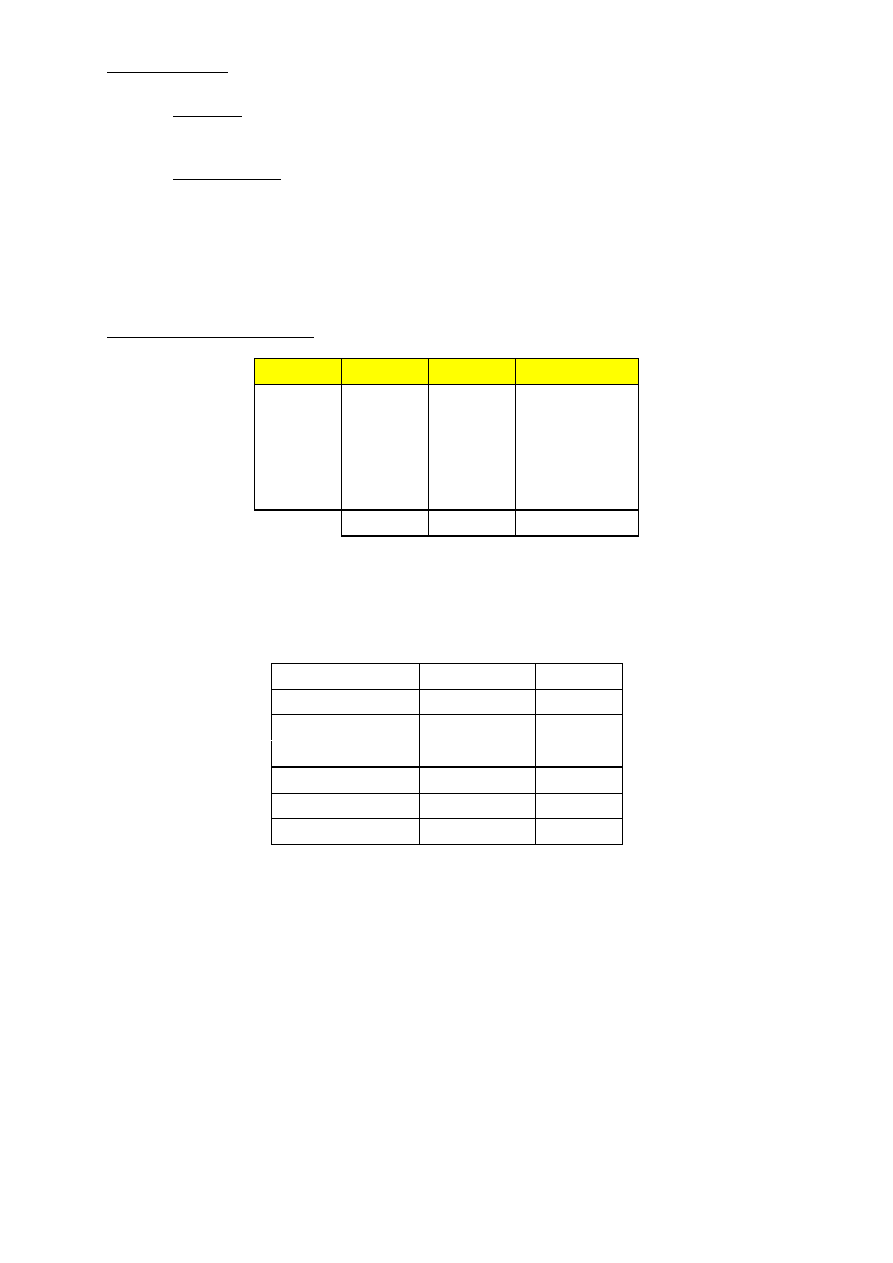
5
Błąd analizy (x):
L =
∑K − ∑A
∑K + ∑A
∗ 100 [%]
L =
4,989 − 4,985
4,989 + 4,985
∗ 100
L = 0,04 %
Dopuszczalny błąd względny dla analizy wody powierzchniowej nr 1 mieści się w granicach błędu.
Analiza została wykonana poprawnie.
Twardość wody (mval/dm
3
):
Kation
Mnożnik mval/dm
3
Twardość [
o
N]
Ca
2+
0,04990
3,094
8,663
Mg
2+
0,08224
1,135
3,178
Sr
2+
0,02282
0,014
0,038
Fe
2+
0,03581
0,005
0,015
Mn
2+
0,07281
0,003
0,008
suma
4,251
11,902
Interpretując wyniki na twardość dla próbki wody powierzchniowej nr 1 można stwierdzić, że woda
należy do średnio twardych.
Obliczenia do diagramu Pipera
Ca
2+
3,094
62,76
Mg
2+
1,135
23,03
Na
+
0,639
14,21
K
+
0,061
SO
4
2-
0,510
10,53
HCO
3
-
4,254
87,84
Cl
-
0,079
1,63
Analizowana przez nas woda tylko w jednym przypadku przekracza określone
rozporządzeniami wartości dopuszczalne. Mianowicie NH
4
+
nieznacznie odbiega od przyjętej
wartości (0,5 mg/L). Może to świadczyć o świeżym zanieczyszczeniu miejscowym, np.
nielegalne odprowadzenie gnojowicy do rzeki. Woda powinna być przeanalizowana ponownie
za jakiś czas. W tym momencie woda nie odpowiada normom. Wartości ChZT-Cr i BZT
5
są w
normach co oznacza, że jest bardzo niewiele mikroorganizmów obecnych w wodzie. Z uwagi
na poziom fosforanów, wodę można zakwalifikować do III klasy jakości wód
powierzchniowych (wody zadowalającej jakości).
6
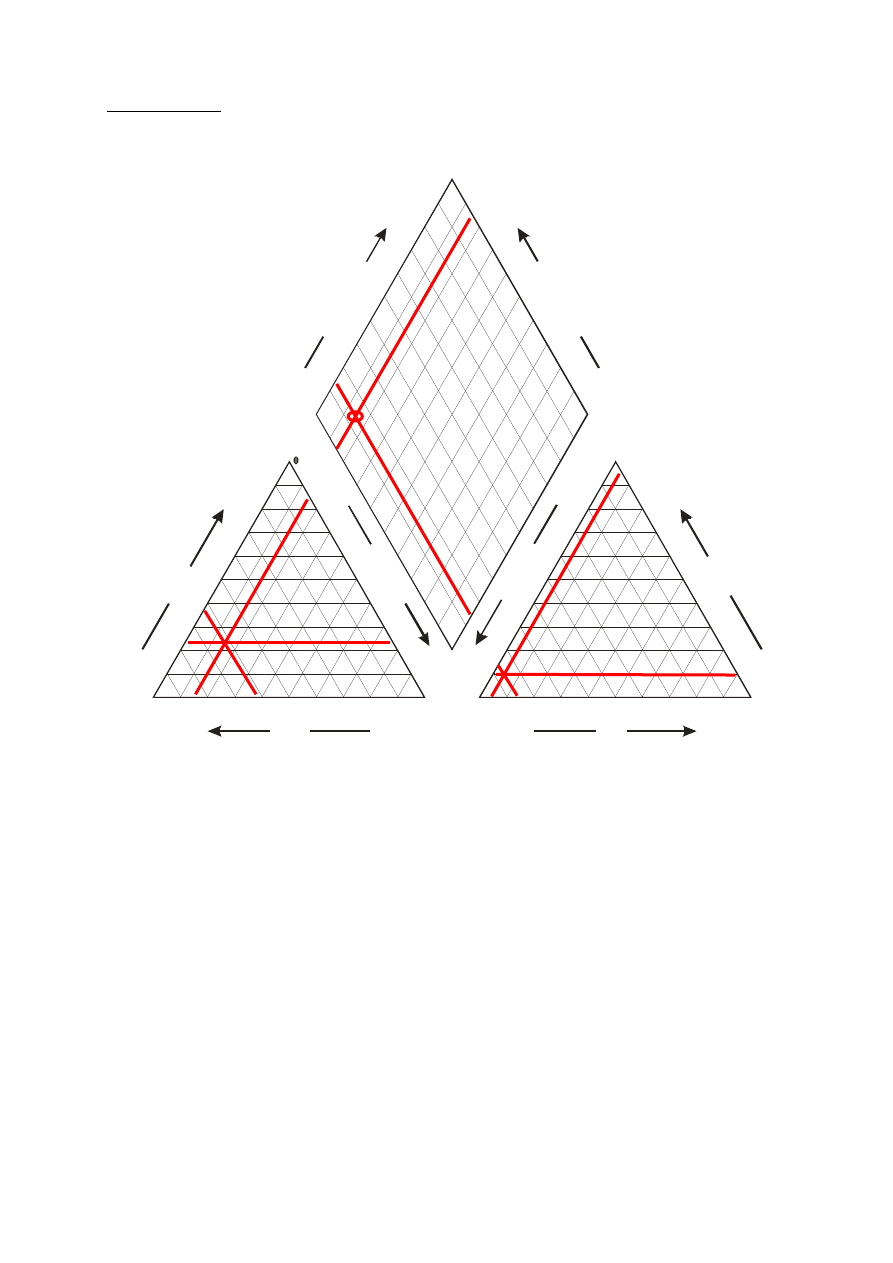
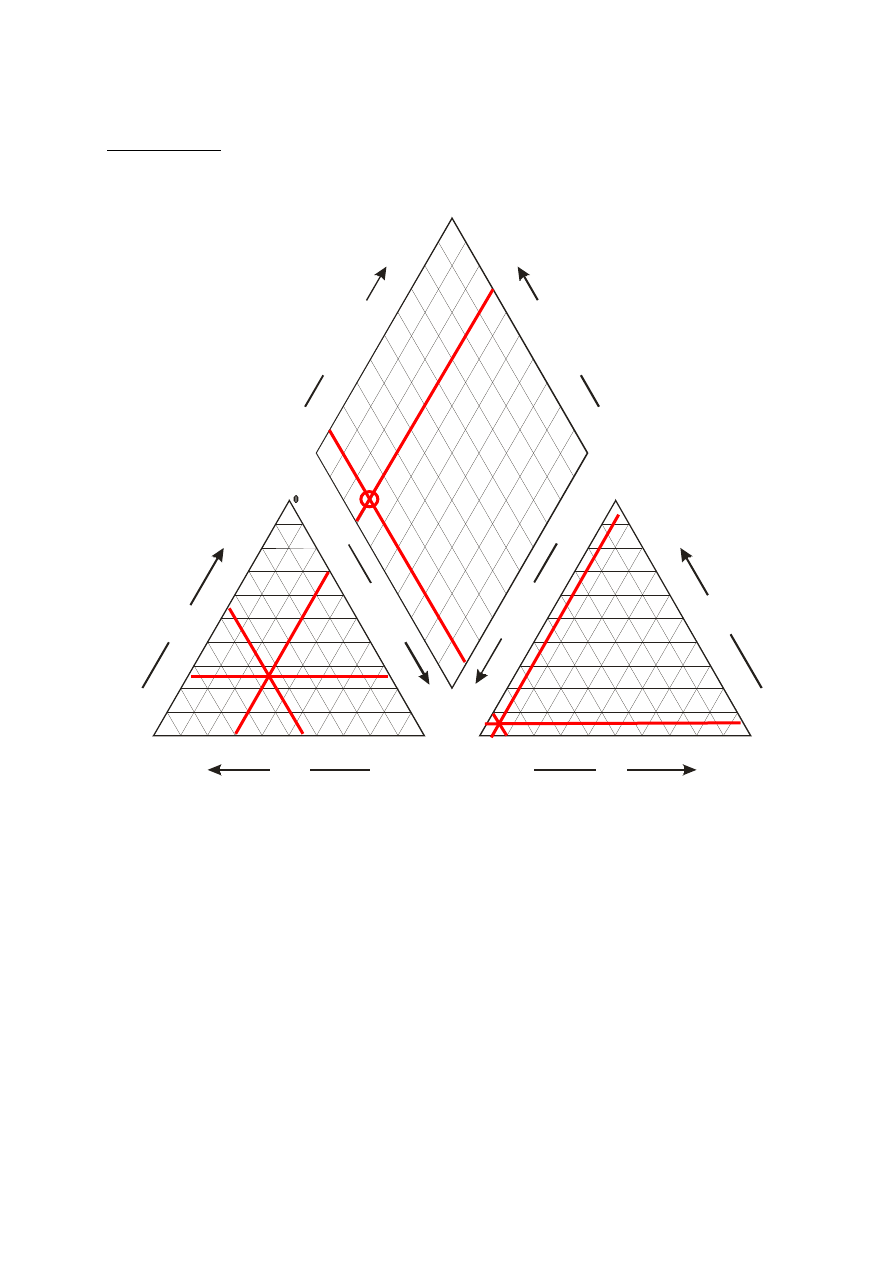
Diagram Pipera
0
0
0
0
0
20
20
20
20
20
20
40
40
40
40
40
40
60
60
60
60
60
60
80
80
80
80
80
80
100
100
100
100 100
0
0
20
20
40
40
60
60
80
80
100
100
100
Ca
Cl
M
g
S
O
+
C
l
4
C
a
+
M
g
S
O
4
N
a
+
K
H
C
O
3
7
2)
Woda nr 2
Powierzchniowa Masa molowa Ładunek
mg/dm
3
mmol/dm
3
mval/dm
3
Klasa
Ca
2+
40,08
2
41,31
1,031
2,061
I
Mg
2+
24,31
2
13,19
0,543
1,085
I
Na
+
22,99
1
29,96
1,303
1,303
-
K
+
39,10
1
1,28
0,033
0,033
-
HCO
3
-
61,02
1
278,00
4,556
4,556
-
SO
4
2-
96,07
2
13,63
0,142
0,284
I
Cl
-
35,45
1
7,00
0,197
0,197
I
PO
4
3-
94,97
3
0,10
0,001
0,003
I
NO
3
-
62,01
1
8,29
0,134
0,134
II
NH
4
+
18,05
1
0,69
0,038
0,038
II
Li
+
6,94
1
0,04
0,006
0,006
-
Fe
2+
55,85
2
0,19
0,003
0,007
II
Mn
2+
54,94
2
0,047
0,001
0,002
I
Sr
2+
87,62
2
0,43
0,005
0,010
-
ChZT-Cr
-
-
28,28
-
-
III
BZT
5
-
-
11,31
-
-
IV
Bilans jonowy:
[mval/dm
3
]
∑K
4,545
∑A
5,174
suma
9,719
Gdzie: ∑K – suma kationów,
∑A – suma anionów.
Błąd analizy (x):
L =
∑K − ∑A
∑K + ∑A
∗ 100 [%]
L =
4,545 − 5,174
4,545 + 5,174
∗ 100
L = −6,47 %
Dopuszczalny błąd względny dla analizy wody powierzchniowej nr 2 nie mieści się w granicach
błędu, który w tym przypadku wynosi 2-5 %. Analiza nie została prawidłowo wykonana i należałoby
ją powtórzyć.
8
Twardość wody (mval/dm
3
):
Kation
Mnożnik
mval/dm
3
Twardość [
o
N]
Ca
2+
0,04990
2,061
5,772
Mg
2+
0,08224
1,085
3,037
Sr
2+
0,02282
0,010
0,027
Fe
2+
0,03581
0,007
0,019
Mn
2+
0,07281
0,003
0,010
suma
3,166
8,865
Interpretując wyniki na twardość dla próbki wody powierzchniowej nr 2 można stwierdzić, że woda
należy do wód miękkich.
Obliczenia do diagramu Pipera
Ca
2+
2,061
45,99
Mg
2+
1,085
24,21
Na
+
1,303
29,80
K
+
0,033
SO
4
2-
0,284
5,63
HCO
3
-
4,556
90,45
Cl
-
0,197
3,92
Analizowana przez nas woda tylko w jednym przypadku przekracza określone
rozporządzeniami wartości dopuszczalne. Mianowicie NH
4
+
nieznacznie odbiega od przyjętej
wartości (0,5 mg/L). Może to świadczyć o świeżym zanieczyszczeniu miejscowym, np.
nielegalne odprowadzenie gnojowicy do rzeki. Woda powinna być przeanalizowana ponownie
za jakiś czas. W tym momencie woda nie odpowiada normom. Wartości ChZT-Cr i BZT
5
są
znacznie podwyższone w porównaniu do wody powierzchniowej nr 1. Można wnioskować, że
jest bogata w liczne mikroorganizmy, co w dalszym etapie może doprowadzić do eutrofizacji
tej wody. Wartości Mn
2+
oraz Fe
2+
są zbliżone do granicznych, lecz ich nie przekraczają. Z
uwagi na poziom ChZT-Cr oraz BZT
5
, wodę można zakwalifikować do IV klasy jakości wód
powierzchniowych (wody niezadowalającej jakości).
9
Diagram Pipera
0
0
0
0
0
20
20
20
20
20
20
40
40
40
40
40
40
60
60
60
60
60
60
80
80
80
80
80
80
100
100
100
100 100
0
0
20
20
40
40
60
60
80
80
100
100
100
Ca
Cl
M
g
S
O
+
C
l
4
C
a
+
M
g
S
O
4
N
a
+
K
H
C
O
3
Wyszukiwarka
Podobne podstrony:
projekty 3 id 400866 Nieznany
kse projekt id 252149 Nieznany
projekt29 id 400291 Nieznany
projektMOS id 400412 Nieznany
projektowanie 2 id 400443 Nieznany
Projekt 7 A id 398367 Nieznany
projekt0002 id 400180 Nieznany
Projekt 6 id 397770 Nieznany
Omowienie projektu id 335352 Nieznany
PROJEKT 5 id 398124 Nieznany
GW PROJEKT F id 197909 Nieznany
projekt 4 i 5 id 398318 Nieznany
GEOCHEMIA IZOTOPOW id 187948 Nieznany
Mechana projekt2 id 290480 Nieznany
projekt 1 3 id 397964 Nieznany
Projekt3 id 400307 Nieznany
projekt 0 1 id 397933 Nieznany
projekt 3 id 398252 Nieznany
Geochemia Wyklady id 187963 Nieznany
więcej podobnych podstron