
1.
Napisz wynik reakcji Michaela dla poni
ż
szego przykładu. Nazwij substraty.
CH
3
NO
2
O
O
O
2
N
+
1. EtO
-
Na
+
2. H
3
O
+
nitrometan 3-buten-2-on
2.
Na przykładzie acetonu zapisz mechanizm reakcji kondensacji aldolowej.
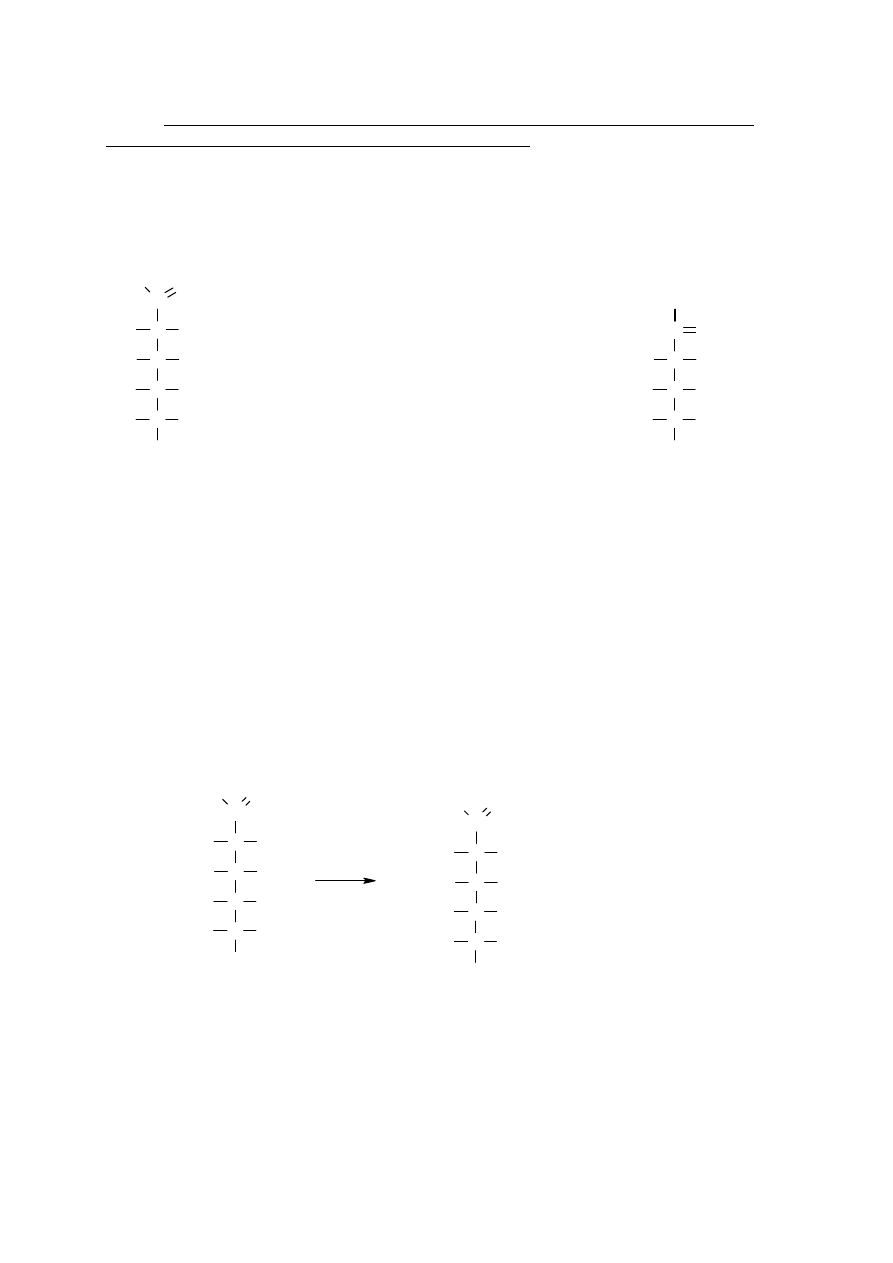
3.
Czym ró
ż
ni
ą
si
ę
aldozy od ketoz? Zapisz wzorami po jednym przykładzie i
podaj sposób ich rozró
ż
niania na drodze chemicznej.
Przykład aldozy Przykład ketozy
(glukoza- aldoheksoza) (fruktoza-ketoheksoza)
C
C
C
C
C
CH
2
OH
H
O
OH
H
OH
OH
H
O
H
H
H
CH
2
OH
C
C
C
C
CH
2
OH
H
OH
OH
O
H
H
H
O
Ró
ż
nica mi
ę
dzy aldoz
ą
a ketoz
ą
Wyst
ę
puje ró
ż
nica w charakterze grupy karbonylowej: aldozy posiadaj
ą
grup
ę
aldehydow
ą
, a ketozy ketonow
ą
.
Rozró
ż
nienie na drodze chemicznej
Reakcj
ą
pozwalaj
ą
c
ą
odró
ż
ni
ć
aldozy od ketoz jest reakcja z buforowanym wodnym
roztworem Br
2
. Reakcja ta jest specyficzna dla aldoz (utleniaj
ą
si
ę
do kwasu
aldonowego), a ketozy nie ulegaj
ą
utlenieniu przez wodny roztwór Br
2
Reakcja z Br
2
na przykładzie glukozy, która utlenia si
ę
do kwasu D-
glukarowego:
O
C
C
C
C
C
CH
2
OH
H
OH
H
OH
OH
H
O
H
H
H
O
C
C
C
C
C
CH
2
OH
O
H
OH
H
OH
OH
H
O
H
H
H
Br
2
, H
2
O
pH=6

4.
Dla D-glukozy napisz reakcje tworzenia form cyklicznych i zaznacz pozycj
ę
anomeryczn
ą
.
5.
Napisz reakcj
ę
zmydlania dowolnego tluszczu.
6.
Co to s
ą
mydła? Jak si
ę
je otrzymuje i na czym polegaj
ą
wła
ś
ciwo
ś
ci pior
ą
ce
(myj
ą
ce) mydła?
7.
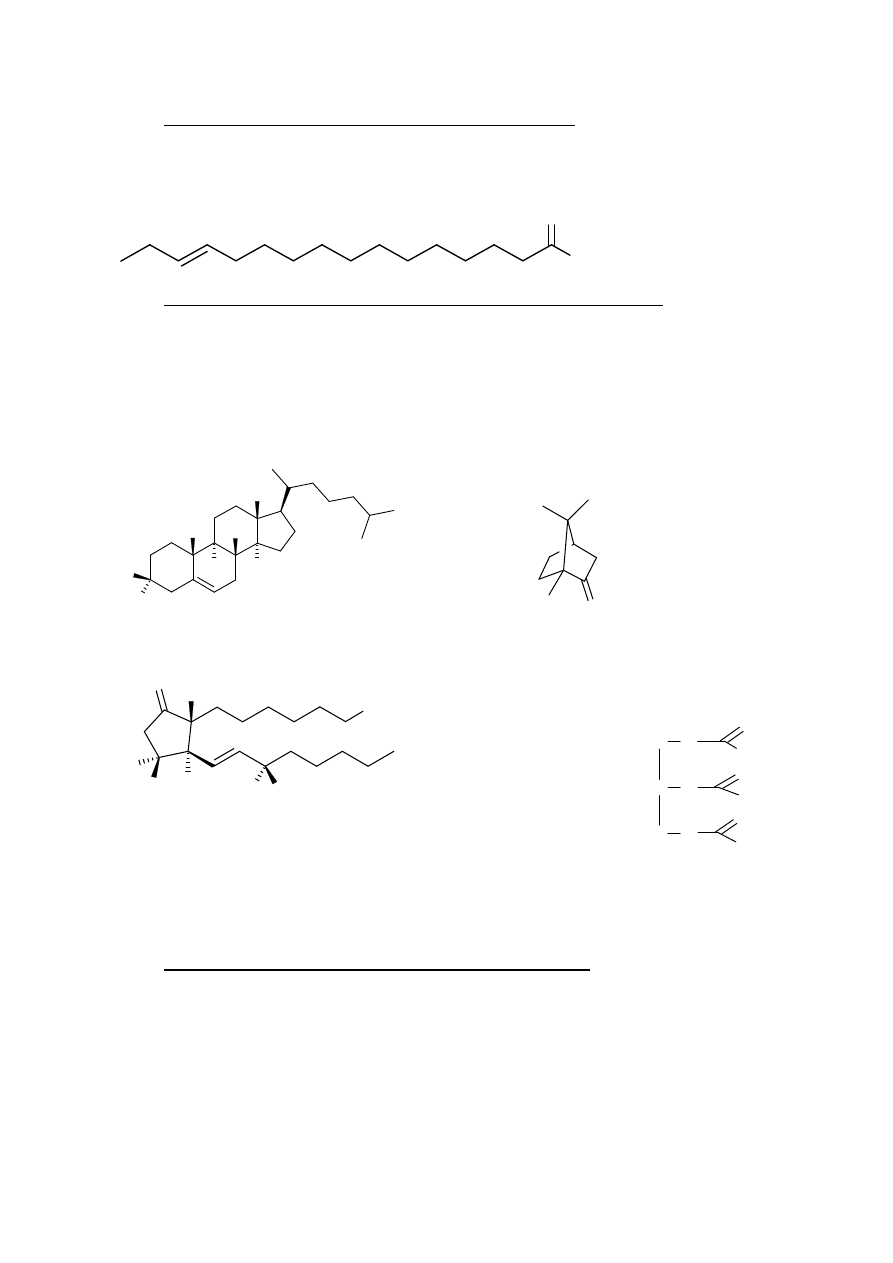
Co oznacza okre
ś
lenie kwas tluszczowy omega-3 ?
W kwasie tłuszczowym ostatni atom w
ę
gla w ła
ń
cuchu jest oznaczany symbolem
omega. Omega 3 oznacza,
ż
e pierwsze wi
ą
zanie podwójne znajduje si
ę
przy 3
atomie w
ę
gla licz
ą
c od atomu omega.
OH
O
ω
8.
Jakie zwi
ą
zki zaliczamy do lipidów, napisz odpowiednie wzory.
Lipidami nazywamy naturalne organiczne cz
ą
steczki o nieznacznej rozpuszczalno
ś
ci
w wodzie, izolowane z komórek lub tkanek przez ekstrakcj
ę
niepolarnymi
rozpuszczalnikami organicznymi takimi jak np. eter czy chloroform. Przykładami
lipidów s
ą
: tłuszcze, oleje, woski, prostaglandyny, steroidy, terpenoidy, wiele
spo
ś
ród witamin i hormonów oraz wi
ę
kszo
ść
niebiałkowych składników błon
komórkowych.
O
H
CH
3
CH
3
H
H
H
H
cholesterol
O
kamfora
O
H
H
O
H
H
H
H
O
CO
2
H
prostaglandyna E
1
C
H
2
C
H
C
H
2
O
O
O
R
R'
O
R''
O
O
tłuszcz zwierz
ę
cy- triester
(R, R', R''= ła
ń
cuchy C
11
-C
19
)
9.
Jaka wa
ż
na cecha odró
ż
nia w
ę
glowodany od lipidów.
W
ę
glowodany, tak jak lipidy, to organiczne zwi
ą
zki chemiczne składaj
ą
ce si
ę
z
atomów w
ę
gla, wodoru i tlenu. S
ą
to zwi
ą
zki zawieraj
ą
ce jednocze
ś
nie liczne grupy
hydroksylowe, karbonylowe oraz czasami mostki półacetalowe. W
ę
glowodany
mo
ż
emy podzieli
ć
na: cukry proste (monosacharydy), oligosacharydy, wielocukry
(polisacharydy) Najpowszechniejszym przykładem w
ę
glowodanów jest glukoza:
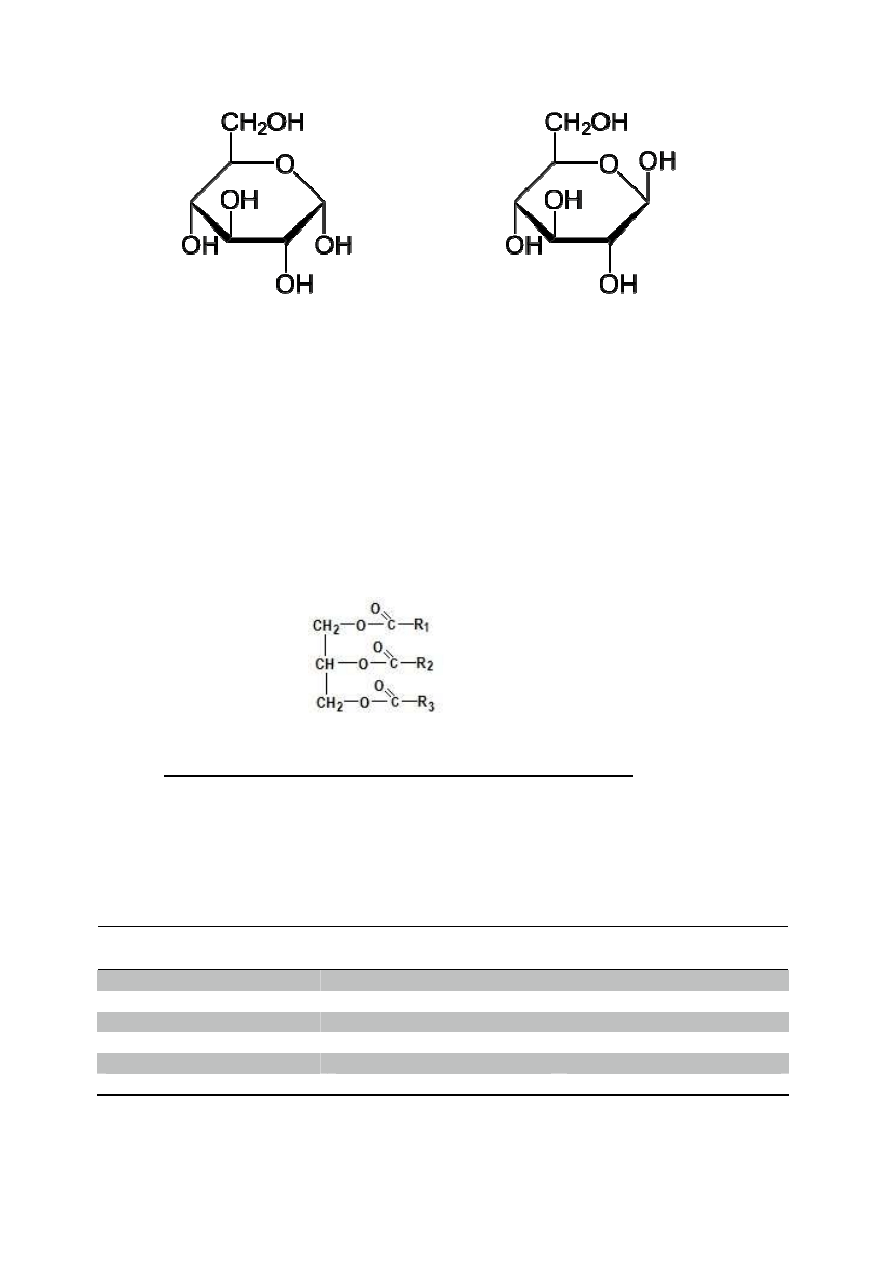
Ze wzgl
ę
du na obecno
ść
licznych grup –OH w
ę
glowodany bardzo dobrze
rozpuszczaj
ą
si
ę
w wodzie – w przeciwie
ń
stwie do lipidów.
Lipidami nazywamy naturalnie wyst
ę
puj
ą
ce organiczne cz
ą
steczki o nieznacznej
rozpuszczalno
ś
ci w wodzie, izolowane z komórek i tkanek przez ekstrakcj
ę
niepolarnymi rozpuszczalnikami organicznymi. Przykładami lipidów s
ą
tłuszcze, oleje,
woski, wiele witamin i hormonów. Zbudowane s
ą
z atomów w
ę
gla, wodoru, tlenu oraz
innych pierwiastków, np. azotu czy fosforu. S
ą
to zwi
ą
zki składaj
ą
ce si
ę
z alkoholi
zestryfikowanych z resztami kwasów tłuszczowych lub kwasów tłuszczowych wraz z
innymi zwi
ą
zkami chemicznymi. Ze wzgl
ę
du na budow
ę
nie rozpuszczaj
ą
si
ę
w
wodzie, natomiast dobrze rozpuszczaj
ą
si
ę
w rozpuszczalnikach niepolarnych.
Tłuszcze mo
ż
emy podzieli
ć
na: ro
ś
linne i zwierz
ę
ce lub nasycone i nienasycone lub
stałe i ciekłe.
Ogólny wzór tłuszczu:
10.
Podaj podział terpenów. Jaka reguła ma tu zastosowanie?
Terpeny klasyfikuje si
ę
zale
ż
nie od liczby jednostek izoprenowych, które zawieraj
ą
.
Tak wi
ę
c monoterpeny to 10-w
ę
glowe substancje biosyntezowane z dwóch jednostek
izoprenowych, seskwiterpeny s
ą
to 15-w
ę
glowe cz
ą
steczki powstałe z trzech
jednostek izoprenowych itd.
Liczba atomów w
ę
gla
Liczba
jednostek
izoprenowych
Klasyfikacja
10
2
monoterpen
15
3
seskwiterpen
20
4
diterpen
25
5
sesterterpen
30
6
triterpen
40
8
tetraterpen
α-D-glukopiranoza
β-D-glukopiranoza
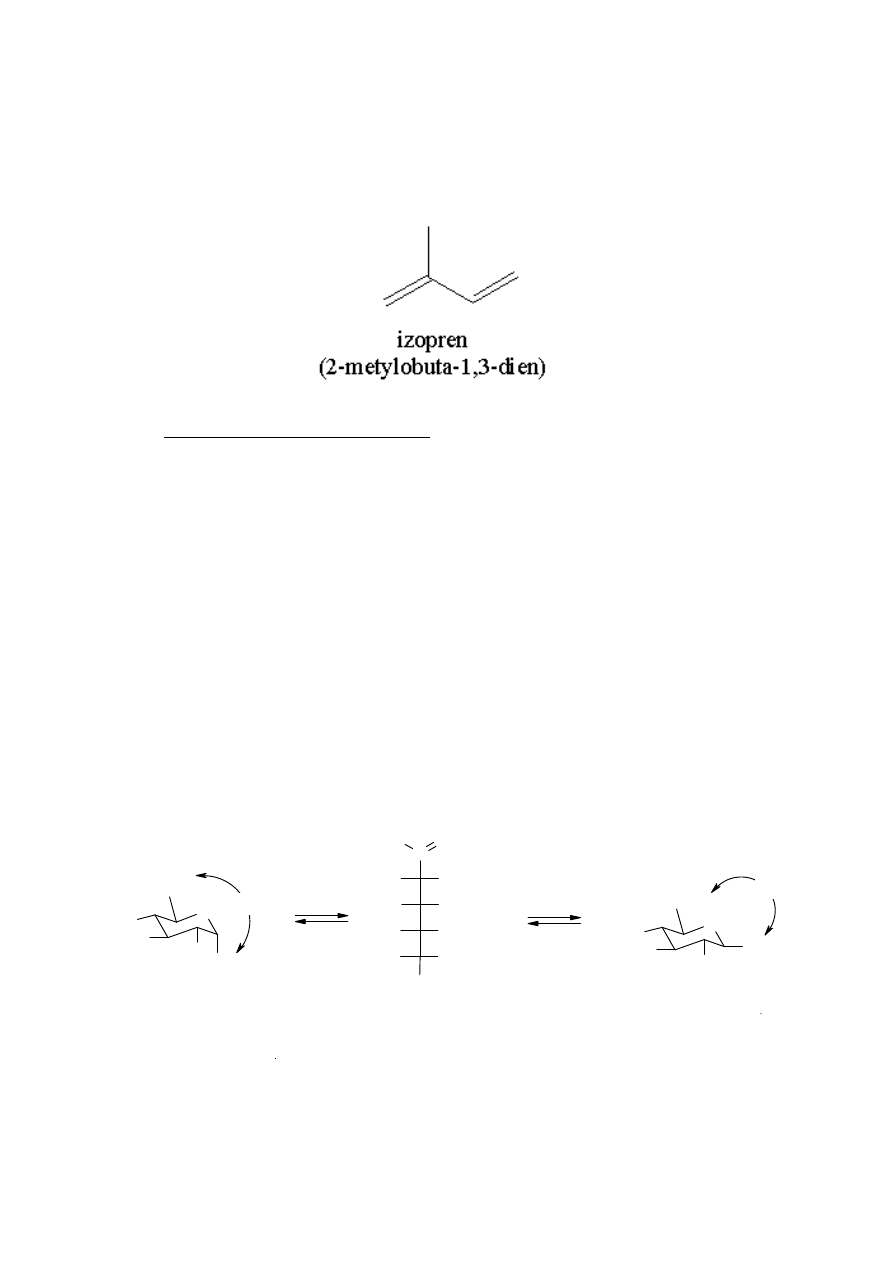
Ma tu zastosowanie reguła izoprenowa. Zgodnie z t
ą
reguł
ą
terpeny mog
ą
by
ć
rozpatrywane jako produkty kolejnego ł
ą
czenia według mechanizmu „głowa do
ogona” jednostek izoprenowych (2-metylobuta-1,3-dienowych). Atom w
ę
gla C1
nazywamy „głow
ą
” jednostki izoprenowej, a atom w
ę
gla C4 jest „ogonem”.
11.
Co oznacza poj
ę
cie mutarotacja?
Mutarotacja– polega na zmianie warto
ś
ci liczbowej k
ą
ta skr
ę
cania
płaszczyzny
ś
wiatła spolaryzowanegoprzechodz
ą
cego przez roztwory substancji
ulegaj
ą
cych epimeryzacji. W przypadku sacharydów spowodowana jest stopniowym
przechodzeniem anomeru
α
w
β
. Jest wynikiem tautomerycznych równowag,
ustalaj
ą
cych si
ę
w roztworach cukrów (np. w stanie równowagi roztwór wodny D-
glukozy zawiera 35,5% formy
α
i 64,5% formy
β
). (Przewaga formy
β
-D-glukozy
wynika st
ą
d,
ż
e odmiana ta jest korzystniejsza energetycznie, gdy
ż
w konformacji
krzesłowej wszystkie podstawniki s
ą
w pozycjach ekwatorialnych). Mutarotacja jest
zjawiskiem, wyst
ę
puj
ą
cym u wi
ę
kszo
ś
ci sacharydów (nie wyst
ę
puje np. w
roztworze sacharozy, gdy
ż
w tym disacharydzie oba anomeryczne atomy w
ę
gla s
ą
zablokowane wi
ą
zaniem O-glikozydowym). Jest charakterystyczna dla cukrów
redukuj
ą
cych.
Mutarotacja przebiega przez odwracalne otwarcie pier
ś
cienia ka
ż
dego z anomerów
do otwartoła
ń
cuchowego aldehydu, a nast
ę
pnie zachodzi ponowne zamkni
ę
cie
pier
ś
cienia.
O
O
H
O
H
OH
OH
CH
2
OH
C
13
CH
2
OH
OH
H
H
O
H
OH
H
OH
H
O
H
O
O
H
O
H
OH
OH
CH
2
OH
trans
cis
α
-D-glukopiranoza
β
-D-glukopiranoza
C1
„głowa”
C3
C2
C4
„ogon”
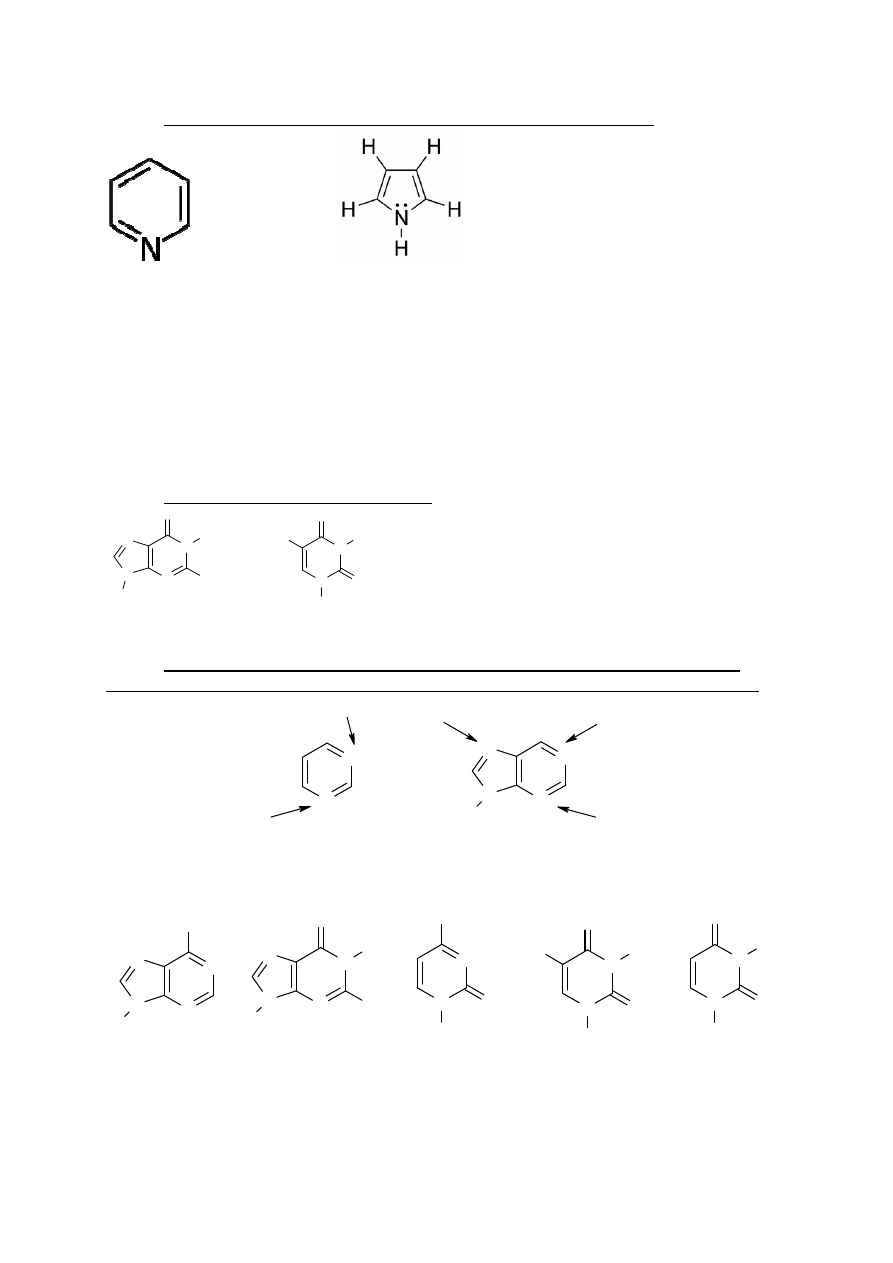
12.
Wyja
ś
nij, dlaczego pirydyna jest mocniejsz
ą
zasad
ą
ni
ż
pirol?
Pirydyna
pirol
Pirol jak i pirydyna maj
ą
woln
ą
par
ę
na atomie azotu . W pirolu wolna para jest
wykorzystana do stworzenia układu aromatycznego , pirydyna ma układ aromatyczny
wi
ę
c para na azocie zostaje nie wykorzystana i to ona
ś
wiadczy o wi
ę
kszej
zasadowo
ś
ci pirydyny nad pirolem.
13.
Napisz wzór guaniny oraz tyminy.
N
N
N
N
O
H
NH
2
H
guanina ( G )
N
N
O
O
C
H
3
H
H
tymina ( T )
14.
Napisz wzór pirymidyny i puryny oraz zaznacz pozycje zasadowe w tych
zwi
ą
zkach. Napisz wzory co najmniej 2 zasad wchodz
ą
cych w skład nukleotydów.
N
N
N
N
H
NH
2
N
N
N
N
H
O
NH
2
H
N
N
NH
2
H
O
N
N
O
H
C
H
3
O
H
N
N
O
H
O
H
N
N
pirymidyna
1
2
3
4
5
6
N
N
N
N
H
puryna
1
2
3
4
5
6
7
8
9
Zasady purynowe i pirymidynowe
adenina (A)
DNA
RNA
guanina (G)
DNA
RNA
cytozyna (C)
DNA
RNA
tymina (T)
DNA
uracyl (U)
RNA
zasadowe
zasadowe
zasadowe
zasadowe
zasadowe
15.
Napisz wzory i nazwij zwi
ą
zki heterocykliczne zawieraj
ą
ce azot i/lub tlen o 3,
5 i 6 atomach w pier
ś
cieniu.
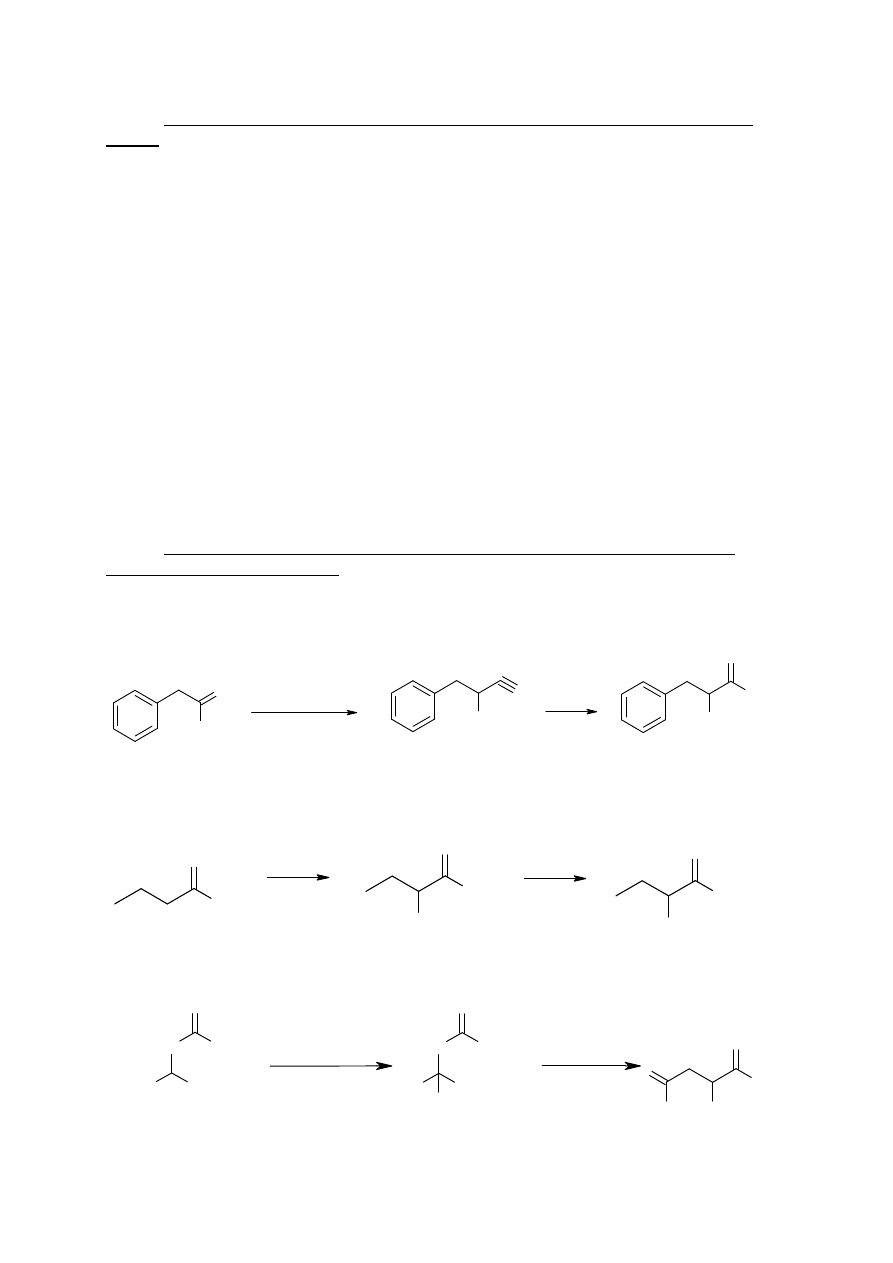
16.
Jakim elementem struktury ró
ż
ni
ą
si
ę
rybonukleotydy od
deoksyrybonukleotydów?
Ró
ż
ni
ą
si
ę
one jedn
ą
zasad
ą
(tymina - uracyl). Jak tak
ż
e obecno
ś
ci
ą
grupy
hydroksylowej w przypadku cukru w rybonukleotydzie.
17.
Napisz wzory odpowiednich rybonukleotydów zawieraj
ą
cych adenin
ę
oraz
uracyl.
18.
Na dowolnych przykładach napisz co najmniej 3 reakcje (ró
ż
ne metody)
otrzymywania aminokwasów.
Synteza Streckera
O
H
NH
4
Cl / KCN
OH
2
N
NH
2
H
3
O+
NH
2
OH
O
Reakcja Hela- Wolharda- Zieli
ń
skiego
OH
O
Br
2
PBr
3
OH
Br
O
NH
3
NH
2
OH
O
Synteza przez acetamidomalonian etylu
N
O
CH
3
CO
2
Et
EtO
2
C
EtONa
BrCH
2
CO
2
Et
N
O
Ch
3
CO
2
Et
EtO
2
C
CH
2
CO
2
Et
H
3
O+
Temp
O
OH
NH
2
OH
O
Redukcyjne aminowanie
α
-oksokwasów
OH
O
O
NH
3
NaBH
4
OH
O
NH
2
19.
Co to jest punkt izoelektryczny aminokwasu? Definicja.
W roztworze kwasowym, czyli przy niskim pH, cz
ą
steczka aminokwasu jest
protonowana i wyst
ę
puje głównie jako kation. W roztworze zasadowym, przy
wysokim pH, aminokwas traci proton i wyst
ę
puje głównie jako anion
. Po
ś
rednie pH,
przy którym istnieje dokładna równowaga mi
ę
dzy form
ą
kationow
ą
i anionow
ą
aminokwasu i wyst
ę
puje on jedynie jako oboj
ę
tny, dipolowy jon obojnaczy
nazywamy punktem izoelektrycznym, pI, aminokwasu.
20.
Na czym polega proces elektroforezy?
Elektroforeza to metoda separacji makrocz
ą
steczek. Pod wpływem przyło
ż
onego
napi
ę
cia cz
ą
steczki te, obdarzone ładunkiem elektrycznym, w
ę
druj
ą
w polu
elektrycznym. Pr
ę
dko
ść
przemieszczania zale
ż
y od ładunku makrocz
ą
steczki, jej
rozmiaru, kształtu, a tak
ż
e oporów ruchu
ś
rodowiska. Technika ta jest najcz
ęś
ciej
stosowana do rozdzielenia DNA i jego analizy w
ż
elu, a tak
ż
e do rozdzielania RNA
czy białek.
Wyró
ż
nia si
ę
dwa rodzaje
ż
eli:
ż
ele agarozowe i
ż
ele poliakrylamidowe
Aparaty do elektroforezy:
aparat i
ż
el poziomy –
ż
el umieszcza si
ę
poziomo; nalewamy do zbiornika
odpowiedni bufor i przykładamy napi
ę
cie – to wywołuje migracj
ę
DNA (ma ładunek
ujemny) od elektrody ujemnej (katody) do elektrody dodatniej (anody);
aparat pionowy – stosuje si
ę
go głównie do rozdziału w
ż
elach poliakrylamidowych;
ż
el umieszcza si
ę
pionowo; od góry i od dołu
ż
elu s
ą
zbiorniki z buforem; kierunek
migracji jest od elektrody ujemnej do elektrody dodatniej.
Rozdział elektroforetyczny zale
ż
y od kilku czynników:
konformacji DNA;
R O
R O
R O
H
3
NCHCOH
H
3
NCHCO
H
3
NCHCO
+
_
+
+
_
H
3
O
-
OH
niskie pH
(protonowany)
wysokie pH
zdeprotonowany
pH
punkt izoelektryczny
(neutralny jon obojnaczy)

wielko
ś
ci DNA – im wi
ę
ksze, tym wolniej migruje w
ż
elu;
st
ęż
enia agarozy;
przyło
ż
onego napi
ę
cia;
rodzaju buforu.
Przed nało
ż
eniem próby DNA w
ż
el podbarwiamy prób
ę
barwnikiem
ś
ledz
ą
cych, np.
bł
ę
kit bromofenolowy, który w
ę
druje w tym samym kierunku co DNA, z pr
ę
dko
ś
ci
ą
tak
ą
jak około 1.000 par zasad. Do barwnika
ś
ledz
ą
cego dodaje si
ę
tak zwany
roztwór obci
ąż
aj
ą
cy. Najcz
ęś
ciej jest to st
ęż
ony roztwór mocznika lub sacharozy albo
fikol 400. Czynnik obci
ąż
aj
ą
cy powoduje,
ż
e próbka opada na dno studzienki
(kanału), wypychaj
ą
c z niej bufor na zewn
ą
trz.
Wyniki rozdziału elektroforetycznego obserwuje si
ę
po wybarwieniu DNA bromkiem
etydyny i wizualizacji w
ś
wietle UV przy długo
ś
ci fali
α
= 260 nm (maksimum
absorpcji dla DNA).
ś
el mo
ż
na sfotografowa
ć
przy zastosowaniu odpowiedniego
filtra.
Rys. Schemat przebiegu procesu elektroforezy (
ź
ródło: wikipedia.pl, domena
publiczna).
ś
el agarozowy z uformowanymi w nim trzema studzienkami (S) na próbki.
Wstrzykni
ę
cie markera DNA (wzorzec masowy) do pierwszej studzienki.
Wprowadzenie badanych próbek do drugiej i trzeciej studzienki.
Przyło
ż
enie napi
ę
cia. DNA porusza si
ę
w kierunku anody ze wzgl
ę
du na posiadany
ładunek ujemny.
Małe fragmenty DNA poruszaj
ą
si
ę
szybko przez
ż
el, du
ż
e fragmenty DNA – powoli.
Normalnie DNA nie jest widoczny w trakcie tego procesu, dlatego do próbki DNA
dodawany jest barwnik.
21.
Podaj definicje reakcji pericyklicznych oraz wyja
ś
nij znaczenie nast
ę
puj
ą
cych
oznacze
ń
[2+2], [2+4], itp.
Reakcje pericykliczne s
ą
to reakcje w których tworzenie nowych wiazan i zrywanie
starych zachodzi równocze
ś
nie w cyklicznym stanie przej
ś
ciowym, podczas reakcji
nie tworz
ą
si
ę
produkty po
ś
rednie. Oznaczenia te charakteryzuja reakcje

cykloaddycji- reakcje mi
ę
dzycz
ą
steczkowe, w których 2 cz
ą
steczki ulegaj
ą
addycji ,
tworz
ą
c cykliczny produkt. Cyfry w nawiasie oznaczaja ilo
ść
elektronów pi bior
ą
cych
udział w reakcji. 2+2 pomi
ę
dzy dwoma alkenami(produktem jest cyklobutan lub
pochodne), 4+2 dien + dienofil-r. Dielsa-Aldera(produktem jest cykloheksen lub
pochodne).
22.
Opisz krótko (ilustruj
ą
c dowolnymi równaniami reakcji) nast
ę
puj
ą
ce procesy:
a) cykloaddycja [4+2] Dielsa-Aldera
b) przegrupowanie [3,3] Claisena
Wyszukiwarka
Podobne podstrony:
bazy danych druga id 81754 Nieznany (2)
Czesc ogolna id 128706 Nieznany
druga id 142797 Nieznany
czesc ia id 127263 Nieznany
czesc iva id 127272 Nieznany
02 KSIEGA DRUGA id 362764 Nieznany (2)
G1 PW D Czesc opisowa 1 id 1853 Nieznany
pas czesc 4b id 349723 Nieznany
czesc iiia id 127268 Nieznany
Czesc VI id 127283 Nieznany
czesc iia id 127266 Nieznany
bazy danych druga id 81754 Nieznany (2)
Czesc ogolna id 128706 Nieznany
II czesc id 209842 Nieznany
Czesc 1 id 128659 Nieznany
Druga katedra poznanska id 1428 Nieznany
naklejk czesc 2 id 313324 Nieznany
druga zasada id 142854 Nieznany
czesc dolna bebna id 127252 Nieznany
więcej podobnych podstron