1
Temat ćwiczenia:
Ogniwa metanolowo – powietrzne i etanolowo - powietrzne
Konspekt
Ćwiczenie
nr 4
Wydział, rok:
Grupa:
nr zespołu:
Data wykonania
ćwiczenia:
Ocena
Nazwisko i imię
Odpowiedź:
Wykonanie ćwiczenia:
Końcowa:
1.
2.
Główne elementy układu:
1.
Dwa ogniwa paliwowe metanolowo – powietrzne;
2.
Ogniwo paliwowe etanolowo – powietrzne w zestawie z odbiornikiem energii w postaci silnika ze śmigłem
3.
zestaw indykatorów – papierków lakmusowych oraz skala ph
4.
Zestaw przewodów;
5.
Dwa multimetry;
6.
Odbiornik z możliwością regulacji rezystancji;
7.
metanol 3% (mas.)
8.
miernik temperatury wraz z czujnikiem
9.
suszarka
1. Wprowadzenie
Ogniwa metanolowo – powietrzne (DMFC: Direct - Methanol Fuel Cell), będące
przedmiotem niniejszego ćwiczenia, należą do ogniw polimerowych. To ostatnie określenie
stanowi swego rodzaju skrót myślowy. Ściślej mówiąc, ogniwa paliwowe polimerowe
posiadają polimerową membranę, umieszczoną pomiędzy elektrodami, na których
powierzchni zachodzą reakcje utleniania i redukcji, warunkujące wystąpienie siły
elektromotorycznej.
Obecnie najpopularniejszym typem z w/w grupy jest ogniwo zasilane wodorem. W
tym przypadku polimerowa membrana – elektrolit, stanowi barierę między anodą i katodą, w
obrębie której odbywa się transport protonów. Źródłem kationów jest reakcja utleniania
przebiegająca na anodzie(-). Uwolnione w jej wyniku elektrony przepływają przez obwód
zewnętrzny do katody, gdzie następuje redukcja tlenu i powstawanie, z udziałem
przemieszczających się przez membranę protonów, końcowego produktu reakcji – wody.
Ogniwo badane w niniejszym ćwiczeniu jest podobne do opisanego powyżej, jednak
tu paliwem umożliwiającym generację energii elektrycznej jest roztwór metanolu. Reakcje
elektrodowe przebiegają właściwie przy udziale cząsteczek tlenu, wody i metanolu.
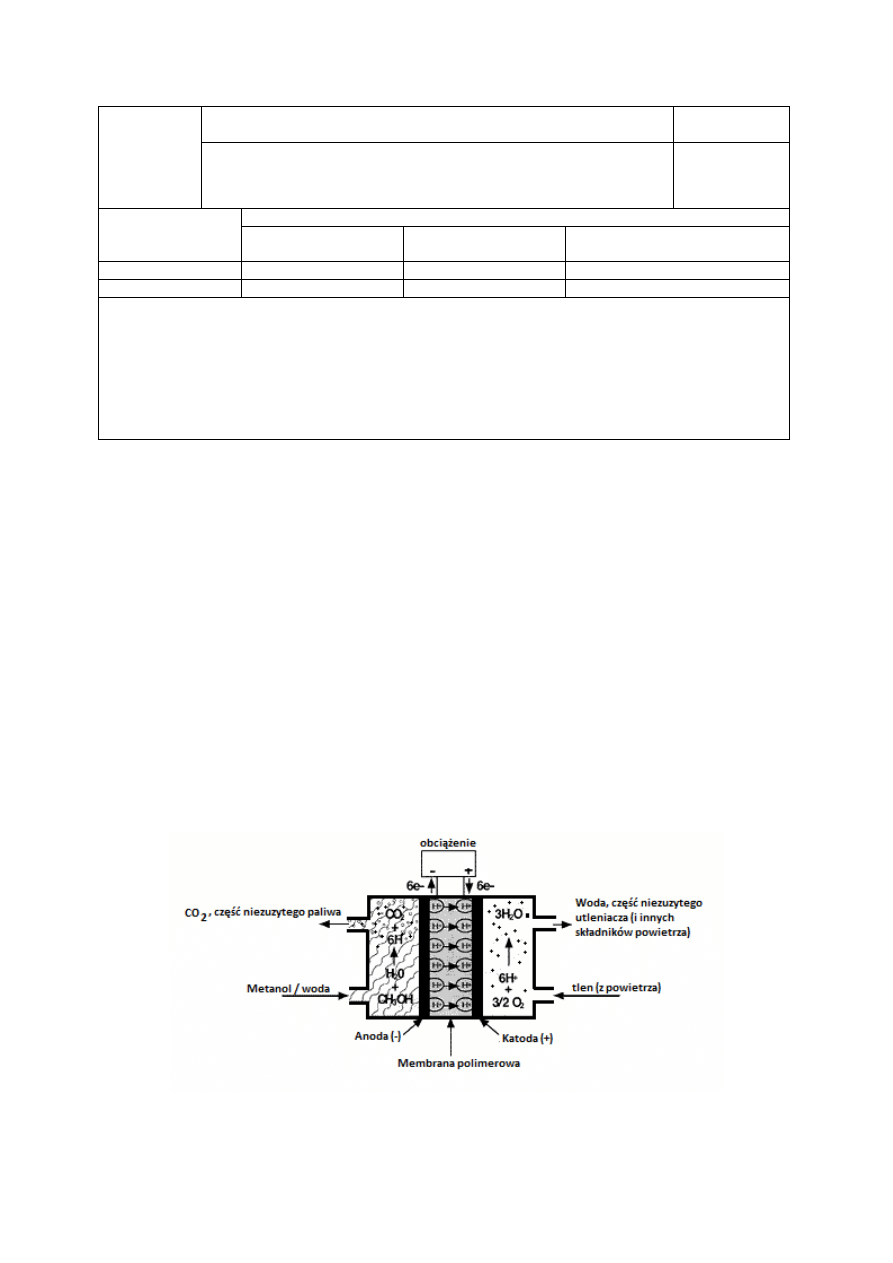
Rys. 1. Schemat ogniwa DMFC.
Na katodzie z otoczenia zostają zaabsorbowane cząsteczki tlenu, na anodzie natomiast
cząsteczki metanolu i wody z dostarczonego paliwa. Tlen podlega procesowi jonizacji,

2
podczas gdy na anodzie dochodzi do rozpadu wody i alkoholu metylowego. Protony powstałe
na elektrodzie ujemnej przemieszczają się przez polimerową membranę na katodę (jony CO
2+
i O
2-
migrują wzdłuż anody), gdzie następuje rekombinacja jonów do cząsteczek wody.
Naturalnie produktem wydzielającym się na anodzie jest dwutlenek węgla.
Reakcje elektrodowe przebiegają jak poniżej:
na anodzie:
CH
3
OH + H
2
O CO
2
+ 6H
+
+ 6e
-
(1)
na katodzie:
1,5O
2
+ 6H
+
+6 e
-
3H
2
O
(2)
sumarycznie:
CH
3
OH + 1,5O
2
CO
2
+ 2H
2
O
(3)
Teoretyczna ilość energii elektrycznej, jaką możemy uzyskać wykorzystując ogniwo
paliwowe metanolowo – powietrzne to 5 kWh/dm
3
. Oczywiście praktyczne osiągnięcie takich
wartości nie jest możliwe ze względu na ograniczone sprawności ogniw DMFC dochodzące
do ok. 35%.
Ogniwo paliwowe, do zasilenia którego wykorzystuje się etanol jest zbudowane
dokładnie tak samo jak omówione powyżej. Można zauważyć także wyraźną analogię
zachodzących w czasie pracy ogniwa reakcji utleniania – redukcji:
na anodzie:
C
2
H
5
OH CH
3
CHO + 2H
+
+ 2e
-
(4)
C
2
H
5
OH + H
2
O CH
3
COOH + 4H
+
+ 4e
-
(5)
C
2
H
5
OH + 3H
2
O 2CO
2
+ 12H
+
+ 12e
-
(6)
Na katodzie:
4H
+
+ 4e
-
+ O
2
2H
2
O
(7)
Produkty uzyskiwane w wyniku reakcji na anodzie są wynikiem niezupełnego
utlenienia alkoholu etylowego. Łatwo zauważyć, że w wyniku pracy ogniwa środowisko
w przestrzeni reakcyjnej anody zakwasza się.
Wykonanie ćwiczenia
1.1. Ustalenie wartości napięcia spoczynkowego ogniw
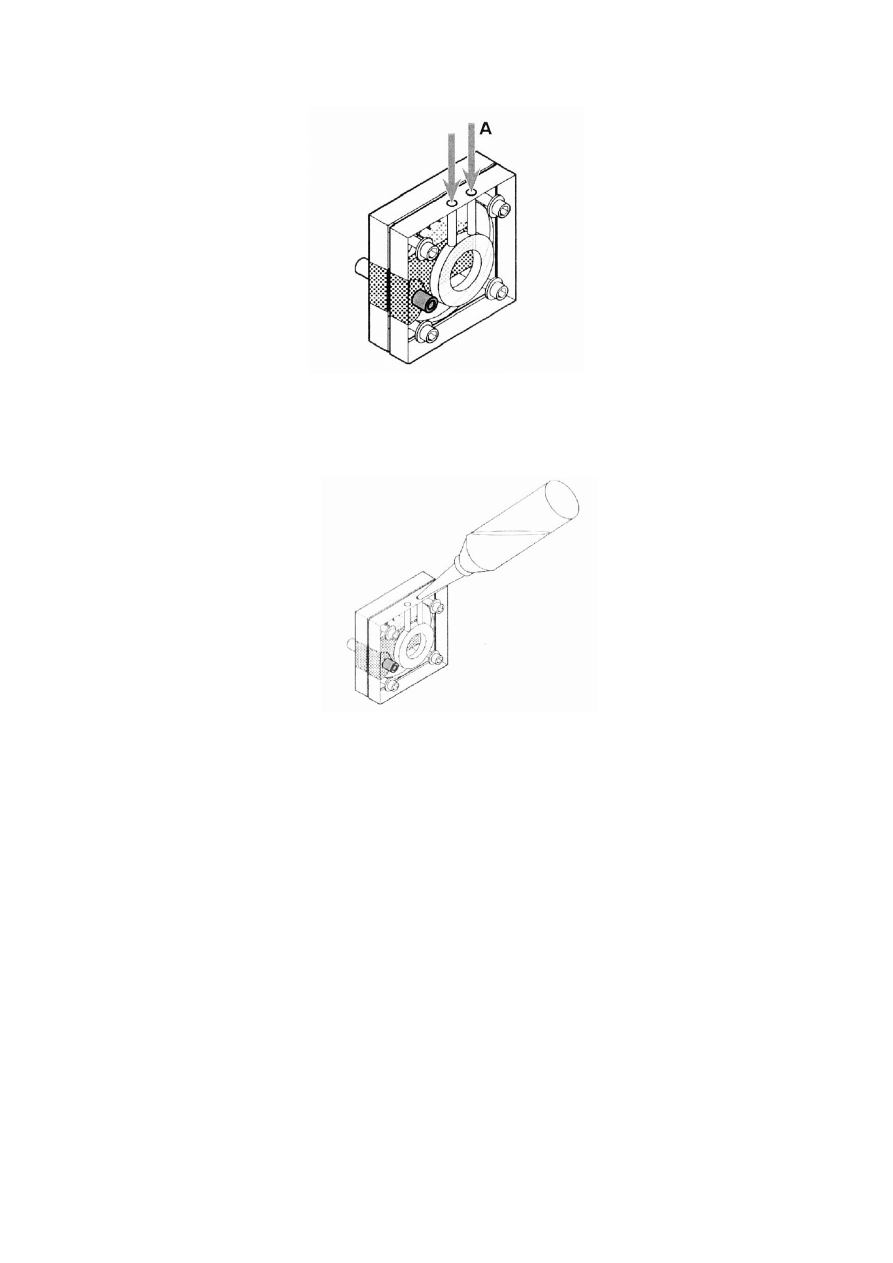
a) Do napełniania/opróżniania ogniwa służą otworki, na rys. 2 oznaczone literą „A”.
Sprawdź czy w ogniwach nie ma resztek wody pozostałych po poprzednim
eksperymencie. Jeżeli tak usuń wodę strzykawką lub plastikową butelką (poprzez
przepłukanie powietrzem lub wyssanie wody).
3
Rys. 2.
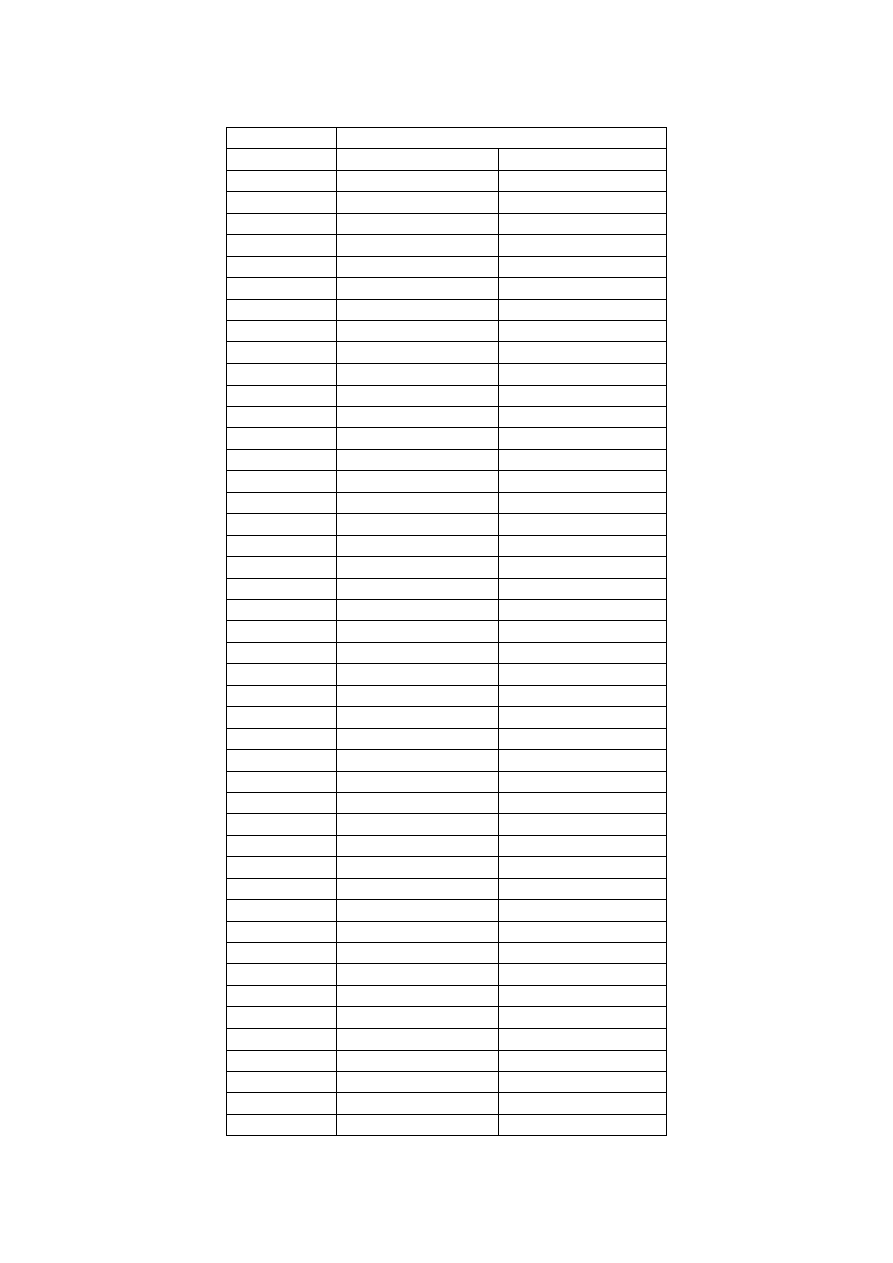
b) Napełnij zbiorniczki dwóch ogniw 3% roztworem metanolu, zgodnie z rys. 3.
Rys. 3.
c) Dołącz do obu ogniw multimetry, ustaw odpowiednie zakresy napięcia stałego.
d) Wykonuj pomiary co 30s dla obu ogniw paliwowych, do czasu, kiedy kolejne 5
pomiarów będzie różnić się nie więcej niż wartość rzędu 0,005V.
e) Wyniki notuj w tabeli 1.
Opracowanie wyników:
a) Na wykresie U = f(t) przedstaw przebieg krzywych napięcia dla obu badanych ogniw.
b) Na podstawie ustabilizowanych wartości napięcia określ wartość napięcia
spoczynkowego badanych ogniw (oblicz średnią wartość z tych pomiarów).
4
Tabela 1. Ustalenie wartości napięcia spoczynkowego ogniw paliwowych DMFC.
Czas [.....]
Napięcie [.....]
Ogniwo 1
Ogniwo 2
U
sp
:
5
1.2. Wyznaczenie krzywej mocy ogniw paliwowych DMFC w różnych układach
pracy
a) Opróżnij zbiorniczki ogniw – paliwo wlej do słoika znajdującego się w zlewie,
onaczonego etykietą „zlewki metanolu”.
b) Przepłukaj wnętrze ogniw wodą destylowaną a następnie przedmuchaj powietrzem
(z wykorzystaniem plastikowej butelki lub strzykawki).
c) Napełnij ogniwa świeżym roztworem metanolu i podłącz je do woltomierzy tak,
jak w części 1.1.
d) Obserwuj przyrost napięcia do czasu ustabilizowania się jego wartości (ok. 5 minut).
e) Zanotuj stabilne wartości napięć (porównaj je z napięciem spoczynkowym
zmierzonym w części 1.1., uwagi uwzględnij przy opracowaniu wniosków
z ćwiczenia).
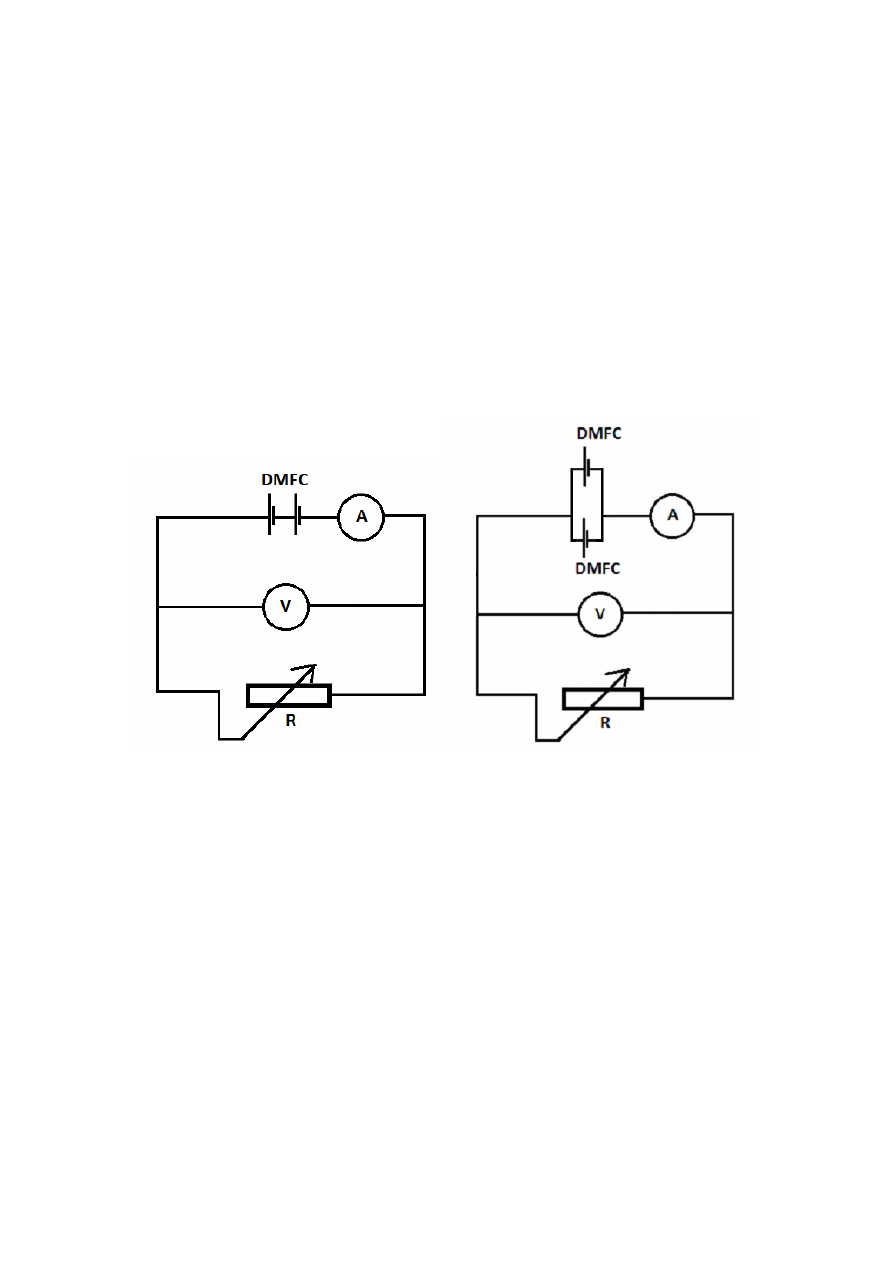
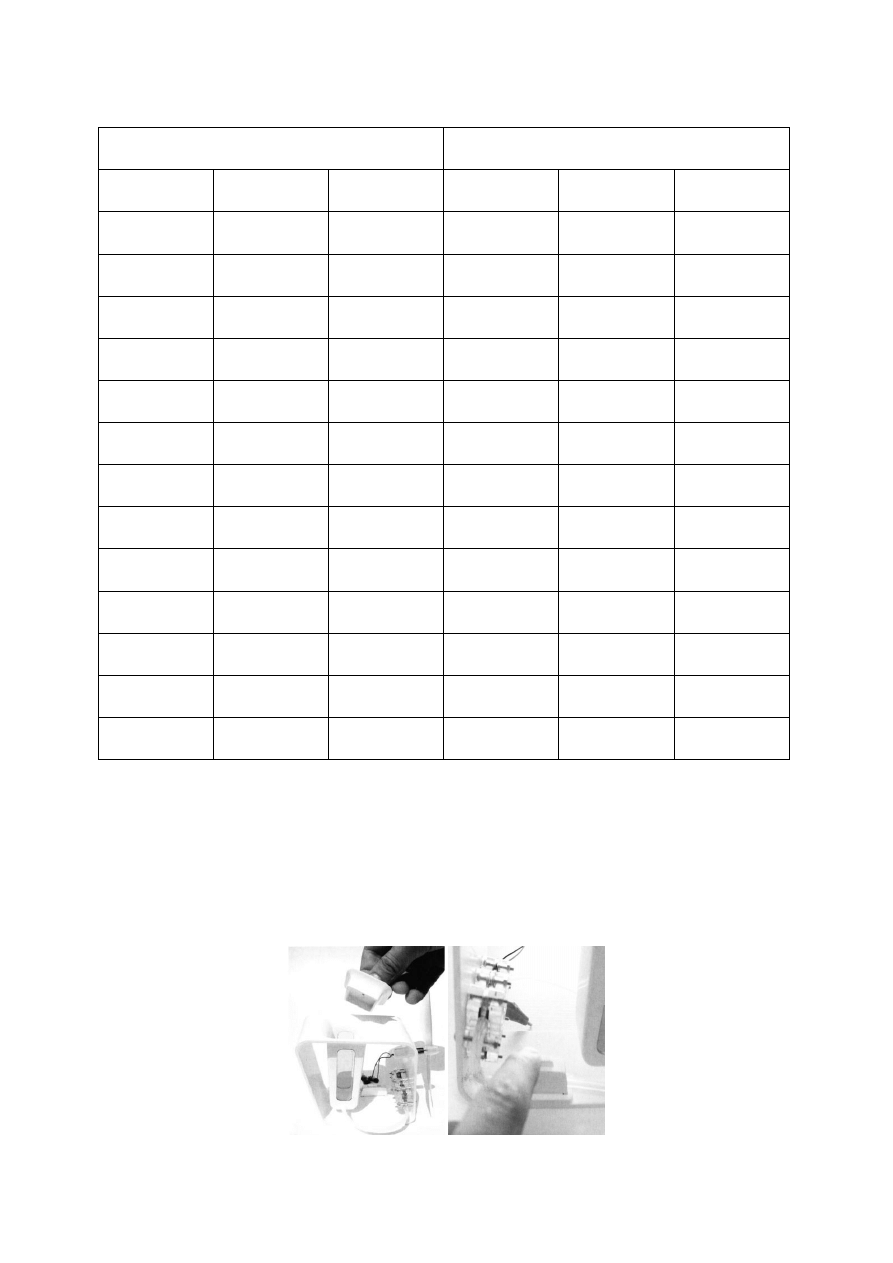
f) Połącz układ pomiarowy zgodnie z rysunkiem 4a.
Rys. 4. Układy pomiarowe do badania zależności mocy od natężenia prądu dla ogniw
pracujących w konfiguracji szeregowej (a) i równoległej (b).
g) Dla kolejnych wartości rezystancji odczytuj wartości napięcia i natężenia prądu. Po
zmianie rezystancji każdorazowo odczekaj ok. pół minuty zanim dokonasz odczytów.
h) Wyniki zapisuj w tabeli 2.
i) Po zakończeniu pomiarów rozłącz układ i dla schematu z rys. 4b postępuj zgodnie z
punktami f – h.
j) Zużyte paliwo wlej do słoika znajdującego się w zlewie, onaczonego etykietą „zlewki
metanolu”.
Opracowanie wyników:
a) Na podstawie danych z tabeli 2 oblicz moc dla zadanych obciążeń.
b) Wykreśl krzywe zależności P = f(I) dla konfiguracji szeregowej i równoległej
połączenia ogniw w jednym układzie współrzędnych.
c) Porównaj krzywe, uwagi uwzględnij podczas opracowania wniosków z ćwiczenia.
a)
b)
6
Tab. 2. Dane pomiarowe - wyznaczenie charakterystyk P = f(I)
Połączenie ogniw szeregowe
Połączenie ogniw rónoległe
U [.....]
I [.....]
P [.....]
U [.....]
I [.....]
P [.....]
1.3. Badanie wpływu warunków zewnętrznych na efektywność pracy ogniwa
zasilanego etanolem.
a) Do zbiorniczka zestawu ogniwa zasilanego etanolem (rys. 5. a) nalej trochę wody
destylowanej (ok. 1/3 objętości). Ustaw wylot wężyka tak, by krople wody mogły
kapać do podstawionego naczynia lub zlewu, otwórz zaworek przesuwając
przełącznik w prawo (rys. 5. b) i przepłukuj wodą układ przez ok. 2 minuty.
Rys. 5. Zestaw ogniwa zasilanego etanolem wraz z odbiornikiem energii.
a)
b)
7
b) Wylej resztę wody i jeszcze przez chwilę zostaw zaworek w pozycji otwartej, by
resztki wody mogły zostać usunięte z układu. Następnie zamknij zaworek
c) Napełnij zbiorniczek 60 ml 10% roztworu etanolu.
d) Dołącz do wyprowadzeń elektrycznych ogniwa woltomierz (silniczek ze śmigłem
odłączony). Przez 5 minut co 30s odczytuj wartość wskazywanego przez miernik
napięcia. Wyniki zapisuj w tabeli 3.
Tab. 3.
T [.....]
U [.....]
e) Porównaj zmiany napięcia z odczytami z części 1.1. ćwiczenia – komentarz
uwzględnij we wnioskach.
f) Dołącz do ogniwa odbiornik w postaci silniczka ze śmigłem. Przez 5 min, co 30s
zapisuj w tabeli 4 wartość napięcia dla ogniwa pracującego pod obciążeniem.
g) Po upływie 5 minut poproś prowadzącego o pomoc w zamontowaniu czujnika
temperatury na mierzonym ogniwie.
h) Ogrzewaj ogniwo suszarką (sprawdź dłonią, czy suszarka nie znajduje się zbyt blisko
ogniwa – ogrzewanie nie może być zbyt gwałtowne) do osiągnięcia przez nie
temperatury 55ºC. W tym czasie, co 1K odczytuj wartość napięcia. Dane zapisuj w
tabeli 5.
i) Po osiągnięciu maksymalnej temperatury zakończ ogrzewanie, dokonaj jeszcze ok. 10
pomiarów podczas stygnięcia ogniwa.
j) Otwórz zaworek spustowy i pozwól, by kilka kropel roztworu spadło do podłożonego
naczynia, następnie nasącz zużytym paliwem papierek lakmusowy. Drugi koniec
papierka zanurz w roztworze znajdującym się w zbiorniczku paliwa. Porównaj barwę
końców papierka (użyj także skali pH), uwagi uwzględnij we wnioskach.
Opracowanie wyników:
a) Sporządź wykres dla danych zawartych w tabeli 3.
b) Sporządź wykres zależności U = f(t) dla ogniwa pracującego pod obciążeniem.
8
c) Sporządź wykres zależności U = f(T)
d) Oszacuj pH zużytego paliwa.
Tab. 4. Napięcie ogniwa zasilanego etanolem pracującego pod obciążeniem
T [.....]
U [.....]
Tab. 5. Napięcie ogniwa zasilanego etanolem pracującego pod obciążeniem
w zależności od temperatury
T [ºC]
U [.....]

9
Wyszukiwarka
Podobne podstrony:
ogniwo metanolowe by Slupski, Energetyka AGH, semestr 5, V Semestr, Konwersja Energii, LABORKI, Ćwi
Ćwiczenie 4 Ogniwo Paliwowe Metanolowo Powietrzne Sprawozdanie
ogniwo metanolowe by Slupski, Energetyka AGH, semestr 5, V Semestr, Konwersja Energii, LABORKI, Ćwi
Ćwiczenie 4 Ogniwo Paliwowe Metanolowo Powietrzne Obliczenia I Wykres
Ogniwo paliwowe metanolowo - powietrzne, Energetyka AGH, semestr 5, V Semestr, Konwersja Energii, L
Ogniwa paliwowe metanolowe
Ogniwa paliwowe metanolowe
ogniwo paliwowe 3
ogniwo paliwowe
Ogniwo paliwowe odwracalne Instrukcja
ogniwo paliwowe1, Szkoła, Politechnika 1- 5 sem, politechnika, rok 2, sem 4
ogniwo paliwowe
Instrukcja cwiczenie 3 ogniwo D Nieznany
ogniwo paliwowe(1), Polibuda, IV semestr, el en
ogniwo paliwowe, Polibuda, IV semestr, el en
Sprawko ogniwo paliwowe, Polibuda, IV semestr, el en
sprawko ogniwo paliwowe
więcej podobnych podstron