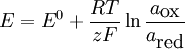Utlenianie – reakcja chemiczna, w której atom przechodzi z niższego na wyższy stopień utlenienia (co jest równoważne z oddaniem elektronów).
Nazwa ta ma charakter umowny, gdyż każdej reakcji utlenienia musi towarzyszyć reakcja
redukcji. Łącznie takie procesy nazywa się reakcjami redoks.
Redukcja (inna nazwa elektronacja) to proces, w trakcie którego atom lub ich grupa
przechodzi z wyższego na niższy stopień utlenienia.
Każdej redukcji musi towarzyszyć utlenienie. Łącznie takie procesy nazywa się reakcjami
redoks.
Elektroda - końcowy element niektórych układów lub urządzeń elektrycznych, przewodnik
elektryczny wysyłający ładunek elektryczny lub przyjmujący go z otoczenia, albo kształtujący pole elektrostatyczne w swoim otoczeniu.
Elektrody pierwszego rodzaju
Potencjał elektrodowy elektrod pierwszego rodzaju jest wynikiem wysyłania lub
przyjmowania przez metal jonów dodatnich z roztworu elektrolitu. Elektrody pierwszego
rodzaju są więc odwracalne względem kationów.
Przykładem takich elektrod są znane już nam, elektroda cynkowa i miedziana, a także
elektroda węglowa, która jest odwracalna względem jonów wodorowych.
Elektrody drugiego rodzaju
Elektrody drugiego rodzaju składają się z metalu, jego trduno rozpuszczalnej soli oraz
elektrolitu zawierającego aniony wchodzące w skład trudno rozpuszczalnej soli.
Elektroda redox – potencjal tworzy się dzieki reakcji redox na elektrodach
Elektroda chinhydronowa - półogniwo zbudowane z elektrody platynowej zanurzonej w
roztworze równomolowym chinonu i hydrochinonu zwanym chinhydronem.
Elektroda chinhydronowa jest odwracalna względem jonów hydroniowych i jest elektrodą
redoks, na której cząstkową reakcją potencjałotwórczą jest wymiana elektronów i protonów
między chinonem a hydrochinonem wg reakcji:
Potencjał standardowy, standardowy potencjał półogniwa, E° – siła elektromotoryczna
ogniwa zbudowanego z odwracalnego półogniwa badanego, zawierającego jony o
jednostkowej aktywności, oraz elektrody wodorowej, której potencjał przyjmuje się za równy 0 we wszystkich temperaturach, aby było możliwe określenie potencjału badanej elektrody
(lewa strona na schematach). Jeśli badana elektroda jest anodą, to jej potencjał jest ujemny, jeśli natomiast jest katodą to jej potencjał jest dodatni. Potencjał standardowy rozumiany jest również jako wkład elektrody do standardowej siły elektromotorycznej ogniwa.
Szereg napięciowy metali (inaczej szereg elektrochemiczny, szereg aktywności metali) to
zestawienie pierwiastków chemicznych o własnościach metalicznych, według ich potencjału
standardowego E0. Punktem odniesienia dla tego zestawienia jest elektroda wodorowa, której potencjał standardowy przyjmuje się umownie za zero.
Równanie "ernsta – podstawowa zależność elektrochemiczna wyrażająca równowagowy
potencjał elektrody (E) względem jej potencjału standardowego (E0) i stężenia substancji
biorących udział w procesie elektrodowym.
Ogólna postać równania:
Potencjał wydzielania jest to
potencjał elektrody, który należy przekroczyć, aby uzyskać mierzalny przebieg danej
reakcji
elektrodowej:
nadpotencjał (nadnapięcie), chem. różnica między potencjałem elektrody, przez którą płynie prąd elektr. i jej potencjałem w obwodzie otwartym (potencjałem spoczynkowym); miara
polaryzacji elektrody.
Najprostsze w budowie jest historyczne ogniwo Volty. Składa się ono z dwóch płytek,
wykonanych z różnych metali, zanurzonych w roztworze elektrolitu. Rozważmy typowy
przykład: w roztworze kwasu siarkowego (VI) zanurzone są płytki cynkowa i miedziana.
Ponieważ z rozcieńczonym roztworem takiego kwasu reaguje tylko cynk, płytka z tego
metalu pokrywa się szybko pęcherzykami wodoru, wypływającymi ku górze. Na płytce
miedzianej nie obserwuje się żadnych przejawów reakcji chemicznej. Tak więc, w układzie
zachodzi reakcja cynku z kwasem, według równania:
•
Przykłady ogniw
Pierwotne wtórne stężeniowe
Wyszukiwarka
Podobne podstrony:
Chemia Bionie wyk1
chemia powt
Wykład Chemia kwantowa 11
wyklad z czwartku chemia fizycz dnia19 marca
chemia(1) 3
Chemia węglowodory
Chemia organiczna czesc I poprawiona
ERGONOMIA chemia
chemia organiczna wykład 6
Chemia wyklad I i II (konfiguracja wiÄ…zania Pauling hybrydyzacja wiazania pi i sigma)
Chemia procesu widzenia
Chemia R cje chemiczne
Chemia materiałów V
Wykład 9 CHEMIA ORGANICZNA
CHEMIA NIEORGANICZNA 2
Chemia
więcej podobnych podstron