Chemia – zajmuje się składem substancji, przemianami materii w niej
zachodzącymi oraz zależnościami pomiędzy zmianami składu i zmianami
energii.
CHEMIA
CHEMIA
CHEMIA
CHEMIA
CHEMIA
ANALITYCZNA
FIZYCZNA
NIEORGANICZNA
ORGANICZNA
Chemia analityczna zajmuje się technika wykrywania składu materii.(jakie
atomy, jak uformowane w skupiskach, jaka konfiguracja przestrzenna?).
Chemia fizyczna zajmuje się ogólnymi prawami, które rządzą zachowaniem się
materii. (od czego zależy konfiguracja przestrzenna atomów i jak zmienia się w
czasie, jakie są siły napędowe, które wytwarzają poszczególne substancje proste
i złożone).
Chemia nieorganiczna zajmuje się związkami wszystkich znanych do tej pory
pierwiastków.
Chemia organiczna koncentruje się wyłącznie na związkach węgla.
Chemia powstała około 500 lat temu w okresie tajemniczych osiągnięć alchemii
i była początkowo dziedziną nauki doświadczalną. Główne zainteresowanie
kierowano wówczas na wykrycie nowych receptur takich jak na przykład
pozyskiwanie metali z Ziemi, jak przemienić ołów w złoto, jak otrzymać
lekarstwo z roślin. Receptury gromadzono, a chemia stawała się coraz bardziej
abstrakcyjna. Ówcześni myśliciele byli zaciekawieni skąd pochodzą ogólne
wzorce obserwacji i zaczęli tworzyć modele rzeczywistej struktury. Obecnie
chemia znajduje w połowie drogi między biologia a fizyką. Podobnie jak
biologia chemia stara się usystematyzować zaobserwowane dotąd układy
Podobnie do fizyki chemia próbuje tłumaczyć zaobserwowane prawa
zachowania się materii na podstawie kilku prostych zasad stosowanych do
cząstek prostych..
Współcześnie jak większość nauk chemia zaczyna obejmować dyscypliny
pokrewne. Pojawia się, więc dziedziny badań badania międzydyscyplinarnych.
Np. biochemia, zajmująca się reakcjami chemicznymi zachodzącymi w żywych
organizmach.
Oprócz dziedzin badawczy współcześnie istnieje dość prężnie rozwijająca się
chemia teoretyczna, w której zjawiska chemiczne opisuje się za pomocą
wyrafinowanych metod matematycznych.
Ciekawym dziwem chemii i stosunkowo młodym jest chemia ciała stałego
obejmuja chemie i fizykę i opisuje właściwości fizyczne zachodzące w iele
stałym (np. przewodność elektryczną).
Materia ma masę i zajmuje przestrzeń. Może występować w trzech stanach
skupienia.
Stan stały charakteryzuje się utrzymaniem kształtu, postaci i objętości próbki,
niezależnie od kształtu pojemnika.
Stan ciekły charakteryzuje się zachowaniem objętości. Nie utrzymuje kształtu,
przyjmuje kształt pojemnika.
Stan gazowy charakteryzuje się tym, że próbka nie zachowuje ani kształtu, ani
objętości. Rozszerza się w celu wypełnienia całego zbiornika.
Faza jest to obszar lub obszary próbki oznaczające się tym samym zbiorem
właściwości.
Pierwiastek chemiczny to według pierwotnej definicji substancja, której nie da
się chemicznymi sposobami rozłożyć na prostsze substancje. Po rozwinięciu się
teorii atomowej materii okazało się, że pierwiastki to po prostu substancje
składające się z atomów o tej samej liczbie protonów w jądrze (liczbie
atomowej). Pierwiastki uszeregowane według ich wzrastającej liczby atomowej
tworzą układ okresowy pierwiastków.
Cząsteczka - grupa atomów trwale ze sobą połączona wiązaniami chemicznymi.
Związek chemiczny to zbiór atomów, które są trwale połączone wiązaniami
chemicznymi. Najmniejszą porcją związku chemicznego jest cząsteczka.
Cząsteczki mogą, ulegać przemianom tylko na skutek pękania i/lub
powstawania wiązań.
Przez związek rozumie się ssubstancję zespolona z dwóch lub więcej atomów,
która nie zmienia składu procentowego poszczególnych pierwiastków podczas
częściowej mazany stanu .
Prawo stałości składu, prawo stosunków stałych – fundamentalne prawo
chemiczne odnoszące się do składu związków chemicznych. Mówi ono, że
każdy związek ma stały skład ilościowy, niezależnie od sposobu, w jaki został
otrzymany. Zostało po raz pierwszy sformułowane w 1799 roku przez Josepha
Louisa Prousta. Jest jednym z odkryć w dziedzinie chemii prowadzących do
powstania teorii atomistycznej budowy materii.
"
Mieszanina to połączenie dwóch, lub więcej pierwiastków, które zachowują
swoje właściwości. Rodzaje mieszanin:
Mieszaniny jednorodne to mieszaniny, w których nie da się rozróżnić
składników składających się na mieszaninę.
Mieszaniny niejednorodne, to mieszaniny, których składniki można
odróżnić za pomocą oczu i prostych narzędzi optycznych.
Różnica między mieszaniną a związkiem, gdy podgrzejemy roztwór jego skład
procentowy ulegnie zmianie gdyż tworzące go substancje maja inne właściwości
fizyczne, skraplanie powietrza.
Atom (z gr. atomos, niepodzielny) - najmniejszy, niepodzielny metodami
chemicznymi składnik materii.
Atomy składają się z jądra i otaczających to jądro elektronów. W jądrze
znajdują się z kolei protony i neutrony. Jądro jest kilkadziesiąt tysięcy razy
mniejsze od całego atomu skupia ono w sobie praktycznie całą masę atomu,
gdyż proton i neutron są o ok. 2000 razy cięższe od elektronu. Protony i
neutrony mają w przybliżeniu taką samą masę. Neutrony są cząstkami
obojętnymi elektrycznie, protony noszą ładunek dodatni, zaś elektrony ujemny.
W każdym atomie w stanie podstawowym liczba protonów i elektronów jest
jednakowa. Wartość ładunku elektrycznego protonów i elektronów jest także
jednakowa, więc atomy jako całość są obojętne elektrycznie. O właściwościach
atomów decyduje głównie liczba protonów w jądrze atomowym, atomy o takiej
samej liczbie protonów w jądrze należą do tego samego pierwiastka
chemicznego. Rozmiary atomów nie są dokładnie określone z powodów
kwantowych, zależą od rodzaju atomu i innych czynników, są rzędu 10-10 m.
Masa w przedziale 10-27–10-25 kg.
Elektron to trwała cząstka elementarna będąca jednym z elementów atomu.
Elektrony znajdują się w atomach poruszając się wokół jądra atomowego w
obszarach zwanych powłokami otaczającymi jądro atomowe. Ujemny ładunek
elektronów zobojętnia dodatni ładunek zawarty w jądrze. Elektrony w mogą
występować w stanie wolnym(np. w przewodniku), co znaczy, że mają zdolność
swobodnego ruchu wewnątrz jego objętości. Jeżeli elektrony po przyłożeniu
napięcia elektrycznego zaczną się poruszać w uporządkowany sposób, to pojawi
się prąd elektryczny.
Proton to cząstka występująca w jądrach atomowych. Przyjmuje się, że proton
posiada elementarny (niepodzielny), dodatni ładunek elektryczny, zapisywany
jako +1e.
Neutron to cząstka występująca w jądrach atomowych. Jest obojętny
elektrycznie. Stabilizuje jądro atomowe oddzielając od siebie dodatnio
naładowane protony.
Jądro atomowe to centralna część atomu zbudowana z jednego lub więcej
protonów i neutronów, zwanych nukleonami. Jądro stanowi bardzo niewielki
ułamek objętości całego atomu w stanie podstawowym, jednak to w jądrze
skupiona jest prawie cała masa.
Oznaczanie
Jądra atomowe oznacza się takim samym symbolem, jak pierwiastek chemiczny
odpowiadający temu jądru, dodatkowo na dole umieszcza się liczbę atomową
(Z), a u góry liczbę masową (A), dla przykładu jądro atomowe o 11 protonach i
13 neutronach, jest jądrem atomu sodu i oznaczamy je symbolem:
24 Na
11
Jon to atom lub cząsteczka, która ma nadmiar lub niedomiar elektronów w
stosunku do protonów. Obojętne elektrycznie atomy i cząsteczki związków
chemicznych posiadają równą liczbę elektronów i protonów, jony zaś są
elektrycznie naładowane dodatnio lub ujemnie.
Jony naładowane dodatnio nazwa się kationami, zaś ujemnie anionami.
Prawo okresowości własności pierwiastków są periodycznie zależne od ich mas
atomowych. (Mendelejew ok. 1869 r.).
Nie zawarł jednak w swoim prawie określenia długości tych okresów. Swoje
założenia Mendelejew opierał na prawie triad W. Doebereinera i prawie oktaw
A. R. Newlanda.
Dymitr Mendelejew z Rosji i Lothar Meyer z Niemiec są uważania za tych,
którzy nie zależnie od siebie odkryli prawo okresowości. Masy atomowe
zaczęto wyznaczać 1803 r. Zauważono, że występują pewne regularności w
zachowaniu się pierwiastków, w przypadku gdy uszeregowano jej w kolejności
wzrastających liczb atomowych. Np. wapń (40) stront (88) i bar (137)
zauważono, iż masa strontu –środkowego- jest mniej więcej średnią różnicą
asymetryczną mas dwóch pozostałych, podobnie dla chloru (35,5), bromu 980) i
jodu(127) – prawo triad. Gdy nastąpił postęp w badaniach chemicznych oraz
gdy odkryto i scharakteryzowano więcej pierwiastków w 1864 r. Jon Newlands
stwierdził, że właściwości, co ósmego pierwiastka SA powtórzeniem
właściwości pierwszego – prawo oktaw. Jednym ze szczególnych osiągnięć
było zwrócenie uwagi na trzy luki w jego uszeregowaniu pierwiastków i
przepowiedzenie właściwości pierwiastków, których odkrycie wypełni luki, a
nawet właściwości związków zawierających te pierwiastki. Było to jedynie
kwestią krótkiego czasu odkrycie brakujących pierwiastków galu, skandu i
germanu wiedziano, co należy szukać.




















































































































































































































Z obecnej postaci układu okresowego wynika, że pierwiastki uszeregowane w
kolejności wzrastających liczb atomowych wykazuja okresowe powtarzające
się właściwości.
Układ okresowy pierwiastków jest to zestawienie wszystkich pierwiastków
chemicznych w postaci rozbudowanej tabeli, uporządkowane według ich
rosnącej liczby atomowej, grupujące pierwiastki według ich cyklicznie Reakcja
chemiczna to każdy proces w wyniku, którego następuje zrywanie i/lub
powstawanie nowych wiązań chemicznych. Reakcje dzielą się na:
Reakcja prosta, to inaczej mówiąc prosty akt zerwania lub powstania
jednego wiązania chemicznego.
Zn + S → ZnS
Reakcje złożone, w których dochodzi jednocześnie do rozpadu jednych
wiązań i powstania drugich.
Rodzaje reakcji złożonych:
reakcja addycji - czyli inaczej reakcja dodawania - w wyniku tej
reakcji reagująca cząsteczka ulega powiększeniu o jakiś atom lub grupę
atomów,
SO3 + H2O → H2SO4
reakcja substytucji - czyli inaczej reakcja podstawienia - w wyniku tej
reakcji w cząsteczce następuje wymiana jakiegoś atomu lub ich grupy.
NaOH + HCl → NaCl + H2O
reakcja eliminacji - czyli inaczej reakcja oderwania - w wyniku tej
reakcji od cząsteczki odrywa się jakiś atom lub grupa atomów i nic innego
się w to miejsce nie przyłącza.
Mol - jednostka liczności materii legalna w układzie SI.
Jeden mol jest to liczność materii, mającej taką samą liczbę cząstek ile jest
atomów zawartych w 12 gramach izotopu węgla 12C. W jednym molu znajduje
się 6,0221367(36) × 1023 cząsteczek, atomów, jonów, elektronów, innych
cząstek lub zespołów takich cząstek. Liczba ta jest nazywana liczbą Avogadro.
Masa atomowa (niepopr. cięż ar atomowy) - liczba określająca ile razy jeden
reprezentatywny atom danego pierwiastka chemicznego jest cięższy od 1/12
izotopu 12C, przy czym pod pojęciem 'reprezentatywnego atomu' rozumie się
atom o średnim ciężarze wyliczony proporcjonalnie ze wszystkich stabilnych
izotopów danego pierwiastka, ze względu na ich rozpowszechnienie na Ziemi.
Izotopy - to atomy, które posiadają tę samą liczbę protonów, ale różnią się
liczbą neutronów. Izotopy różnią się masą atomową, ale należą do jednego
pierwiastka i mają niemal identyczne własności chemiczne.
Ze względu na różnicę mas atomowych izotopy mają jednak różne niektóre
własności fizyczne, przy czym różnice te są tym większe im większy jest rozrzut
ich mas względem siebie. Różnice w masach atomowych izotopów powodują,
że w formie czystej mają one inną gęstość, temperaturę wrzenia, topnienia i
sublimacji. Różnice te rozciągają się także na związki chemiczne o różnym
składzie izotopowym.
Różnica mas izotopów powoduje też występowanie niewielkich różnic w ich
reaktywności. Nie ma ona wpływu na kierunek reakcji chemicznych w których
one uczestniczą, ale wpływa na szybkość tych reakcji. Zjawisko to nazwa się
efektem izotopowym i wykorzystuje się w badaniu mechanizmów reakcji
chemicznych. Te niewielkie różnice w szybkości reakcji wywołują zmiany w
składzie izotopowym związków chemicznych powstających w różnych
reakcjach, zjawisko to wykorzystywane jest ostatnio do rozróżniania czy węgiel
zawarty w danym związku chemicznym brał udział reakcji fotosyntezy.
Izotopy dzielą się na:
•
trwałe (nie ulegają samorzutnej przemianie na izotopy innych
pierwiastków),
•
nietrwałe zwane izotopami promieniotwórczymi (ulegają samorzutnej
przemianie na inne izotopy zazwyczaj innego pierwiastka).
Występowanie izotopów komplikuje nieco obliczenia chemiczne (zobacz:
stechiometria), powodując, że masy atomowe i co za tym idzie masy
cząsteczkowe nie są liczbami całkowitymi, lecz liczbami z ułamkiem.
Izotopy nie mają oddzielnych nazw z wyjątkiem izotopów wodoru, oznacza się
je symbolem pierwiastka chemicznego z liczbą masową u góry po lewej stronie,
np. 208Pb
Wiązanie chemiczne według klasycznej definicji to każde trwałe połączenie
dwóch atomów. Wiązania chemiczne powstają na skutek uwspólnienia dwóch
lub więcej elektronów pochodzących bądź z jednego, bądź z obu łączących się
atomów lub przeskoku jednego lub więcej elektronów z jednego atomu na atom
i utworzenia w wyniku tego tzw. pary jonowej.
Wiązania chemiczne można podzielić na kilka rodzajów:
Wiązanie atomowe powstaje między dwoma jednakowymi atomami (np.:
dwoma atomami wodoru).
Wiązanie kowalencyjne powstaje między dwoma atomami, których
wzajemna różnica ładunku jąder jest bliska 0. Elektrony uwspólnione
tworzące wiązanie są przesunięte w stronę jednego z atomów, co powoduje,
że wiązanie wykazuje większy ładunek ujemny po stronie jednego z atomów
i mniejszy po stronie drugiego. Powoduje to, że wiązanie to ma cechy
małego magnesu (tzw. własności dipolowe). Wiązania kowalencyjne można
jeszcze podzielić na zwykle, w których uwspólniane elektrony pochodzą w
równej liczbie od obu atomów oraz na wiązania koordynacyjne.
Wiązanie jonowe powstaje między dwoma atomami, których wzajemna
różnica elektroujemności jest bardzo duża. Elektrony zamiast się uwspólnić
przeskakują na stałe do jednego z atomów.
Wiązanie wodorowe formalnie rzecz biorąc nie jest wiązaniem
chemicznym, w tym sensie, że nie powstaje ono na skutek wymiany
elektronów i jest zwykle dużo mniej trwałe od "prawdziwych" wiązań,
Podstawą obecnych poglądów dotyczących struktury i własności atomów jest
koncepcja że
Materia pochłania i emituje energie promienistą nie w sposób ciągły, lecz w
porcjach zwanych kwantami.
Energia jednego kwantu równa jest
E = h ⋅υ
gdzie: h = stała Plancka (6,62 · 10-34 J·s = 6,62 10-27 erg·s)
υ = częstość promieniowania [s-1]
Wymiar h odpowiada wielkości zwanej w fizyce działaniem: h jest najmniejsza
porcja czyli elementarnym kwantem.
W atomie siła przyciągania elektrycznego pomiędzy jądrem naładowanym
dodatnio a elektronem naładowanym ujemnie jest proporcjonalna do ładunku
jądra razy ładunek elektronu podzielna do przez kwadrat odległości miedzy
nimi.
Z ⋅ e2
v2
K ⋅
=
r2
r
gdzie: K = stala uniwersalna 8,98·109 N·m2·C-2.
Ze = jadrododatniego ładunku
e = ładunek elektronu
r =promień
v = prędkość
Niels Bohr w 1913 roku przedstawiła pierwszą teorię budowy atomu,
przynajmniej dla przypadku atomu wodoru (lib wodoropodobnych )tj
jednoelektrodowych jonów innych pierwiastków. Powiązał w swej teorii model
Rutheforda z koncepcjami kwantowymi Planka i Einsteina oraz uwzględnił
wyniki badań widm atomowych.
Teoria Bobra oparta jest na postulatach, które można sformułować następująco:
1. Elektron porusza się wokół jądra po orbitach stacjonarnych tj. takich, że z
ruchem tym nie związana jest żadna zmiana energii atomu. Spośród
nieskończenie wielu orbit dopuszczalnych w modelu klasycznym
stacjonarne są tlko, dla których spełniony jest warunek kwantowy:
h
m ⋅ v ⋅ r = n
e
π
2
gdzie: me = masa elektronu
v = prędkość liniowa elektronu
r = promień orbity
n = dowolna liczba naturalna –główna liczba kwantowa
2. Emisja albo absorcja promieniowania zachodzi na skutek przeskoku
elektronu z jednej orbity stacjonarnej, na której energia jego wynosi E2,
na inną, której odpowiada energia E1. Częstość emitowanego albo
absorbowanego promieniowania jest uwarunkowana tylko różnicą tych
energii i wynika z wzoru:
h ⋅υ = E − E
2
1
Z warunku kwantowego wynika, ze moment pędu jest ograniczony do
przybierania wartości, które są całkowitymi wielokrotnościami wartości
h/2π. Każda z tych wartości musi odpowiadać dozwolonemu stanowi atomu.
Odpowiednie dopuszczalne wartości dla r można po przekształceniach
równań warunku kwantowego i siły przyciągania. Można otrzymać zależność
zw Promień Bohra:
2
n
r =
a
0
Z
gdzie:a0 = łączy wszystkie stałe h2/(4π2Kme2)
Z tego równania wynika, że jedynymi dopuszczalnymi wartościami dla
promienia drogi elektronu SA wartości proporcjonalne do kwadratu liczby
całkowitej n podzielonej przez liczbę atomową Z.
Ponieważ w powyższym wyprowadzeniu nie uwzględniono sił odpychania
miedzy elektronami w tym samym atomie równanie to można stosować
jedynie w przypadku oddziaływania jądra i jednego elektronu.
W rzeczywistości promień drogi elektronu w atomie nie da się obserwować
doświadczalnie. Natomiast stany energetyczne atomu lub raczej różnice
pomiędzy stanami energetycznymi można obserwować doświadczalnie. W
modelu Bohra można obliczyć energie elektronu jako sumę energii
kinetycznej i potencjalnej.
1
2
KZe2
E =
mv −
2
r
podstawiając za masę i prędkość wcześniej wyliczone wartości:
otrzymujemy:
2
KZ e
E = −
2
2n a0
Wstawiając do tego równania różne wartości n = 1,2,3,4,5.. otrzymamy
wartości energii odpowiadające różnym dopuszczalnym stanom jednego
elektron u w atomie.
Rys. 4.12.
Promień elektronowy wzrasta wraz ze wzrostem wartości n. Elektrony
mające wartość n=1 znajdują się najbliżej jądra; określamy je jako znajdujące
się w warstwie K, orbicie K lub powłoce K. Elektrony, które maja wartość
N=2 znajdują się nieco dalej od jądra i określamy je jako znajdujące się w
warstwie L, na orbicie L czyli na orbicie wyższej. Wyższe orbity lub wyższe
poziomy energetyczne odnoszą się również do zewnętrznych poziomów
energetycznych. Oznaczenia literowe K,L,M,N… początkowo wprowadzili
badacze w spektorskpii rentgenowskiej. Gdyż przenoszenie elektronów z
warstw zewnętrznych do warstwy K jest związane z emisja promieniowania
rentgenowskiego.
Teoria Bobra opisuje dokładnie obserwowane widma atomowe dla atomu
wodoru. Wprowadzając pewne udoskonalenia dla zrównoważenia wpływów
spowodowanych przez zjawisko odpychania elektron-elektron, teorie Bobra
można rozszerzyć na inne pierwiastki. Jednak model Bobra ma kilka
poważnych niedociągnięć, wskutek czego wprowadzono bardziej wyszukana
teorie budowy atomu.
Modle Bobra wyjaśniał regularności w widmach liniowych, lecz także
umożliwiał racjonalne wytłumaczenie okresowego powtarzania się
właściwości chemicznych pierwiastków. Elektrony mają dostępne ściśle
określone poziomy energetyczne. Załóżmy ponadto, że maksymalna liczba
elektronów na każdym poziomie energetycznym atomu jest również
ograniczona i zgodnie z założeniem Bobra wynosi 2n2. Dla n=1 wynosi 2,
dla n=2 wynosi 8, dla n=3 wynosi 18 .
Warstwa każdorazowo zapełniona, gdy ma 2, 8, 18, 32… elektronów.
Właściwości chemiczne zależą głównie od liczby elektronów na najbardziej
zewnętrznym poziomie energetycznym, ograniczenie populacji do 2n2
prowadzi automatycznie do okresowego powtarzania się tej samej liczby
elektronów w powłoce zewnętrznej i stąd powtarzania się tych samych
właściwości.
Jednym ze słabych punktów teorii Bobra jest to, że nie wyjaśnia ona
dlaczego ruchy elektronów są ograniczone tylko do pewnych orbit. Bohr
zakładał, że moment pędu jest kantowy i nie tłumaczył dlaczego.
De Broglie możliwe wyjaśnienie kwantowej natury elektronów. Zasugerował
że każda poruszająca się cząstka ma falową naturę podobna do światła. De
Broglie podał następujący wzór na długość fali 9fali materii):
h
λ = mv
gdzie: h – stała Plancka
mv – moment cząstki
Po przekształceniach otrzymujemy warunek kwantowy Bohra.
Z koncepcji fali wynika że elektron nie można dokładnie zlokalizować.
Zamiast traktować elektron jak oddzielna cząstkę wprowadzno pojecie fali.
Zagadnienie to, wspólne dla cząstek o małej masie matematycznie opracował
Heisenberg. W słynnym twierdzeniu zwanym zasada nieoznaczoności.
Zasada nieoznaczonośći (Heisenberg 1927 r.)
Nie jest możliwe jednoczesne dokładne zmierzenie położenia cząstki i pędu.
Niepewność tą można wyrazić, mówiąc, że nieoznaczoność położenia cząstki
razy nieoznaczoność pędu jest rzędu stałej Plancka h. Im dokładniej staramy
się określić pęd lub położenie cząstki tym większa jest niepewność
oznaczania innych zmiennych.
Ponieważ nie można wykreślić torów dla elektronów w atomach najlepiej
jest mówić o prawdopodobieństwie znalezienia się elektronu w określonym
miejscu atomu. Obliczenie tego rodzaju prawdopodobieństwa jest bardzo
zawikłanym zagadnieniem matematycznym,.
Prawdopodobieństwo znalezienia się elektronu można określić jako rozkład
prawdopodobieństwa. Istnieją trzy sposoby przedstawienia rozkładu.
Prawdopodobieństwa. Rys. 415. Na rysunku a prawdopodobieństwo
znalezienia się elektronu
Rzeczywistości elektrony wykonują bardzo skomplikowane ruchy z dużą
prędkością.
Obszar, w którym prawdopodobieństwo przebywania elektronu przybiera
znaczne wartości, wypełnia jak gdyby „chmura prawdopodobieństwa”, którą
nazywamy chmurą elektronową. Każdym punkcie tej chmury elektron
znajduje się względnie często. Im częściej się tam znajduje tym, tym chmura
jest gęściejsza. Możemy, więc chmurę elektronową traktować jako elektron
rozmazany w przestrzeni. Chmura elektronowa jest pewnym sposobem
przedstawiania orbitalu.
Klasyczna elektronowa teoria budowy cząsteczek nie rozróżnia stanów w
jakich może znajdować się elektron, podczas gdy mechanika kwantowa
wykazała, że np. elektrony s zachowują się odmiennie niż elektrony p, w
szczególności mają chmury elektronowe odmiennych kształtów.
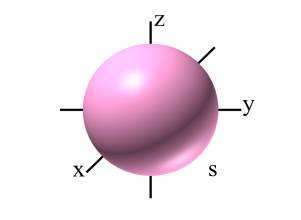
Chmury elektronów s mają zawsze symetrię sferyczną: tzn., że we
wszystkich kierunkach prawdopodobieństwo znalezienia elektronu w danej
odległości od jądra jest jednakowe. Chmura elektronu s jest zawsze kulista.
Dla wyższych wartości głównej liczby kwantowej istnieją wewnątrz chmury
elektronem elektronów s współśrodkowe obszary o bardzo małej gęstości
prawdopodobieństwa, chmura zawsze pozostaje kulista.
rys. orbital s
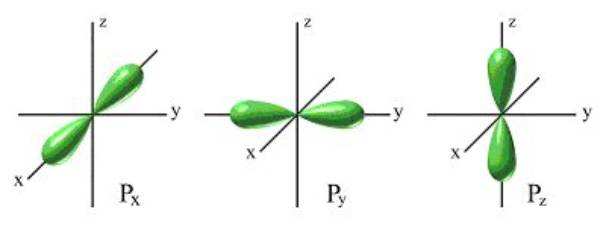
Chmury elektronów p mają kształt przestrzennej ósemki.
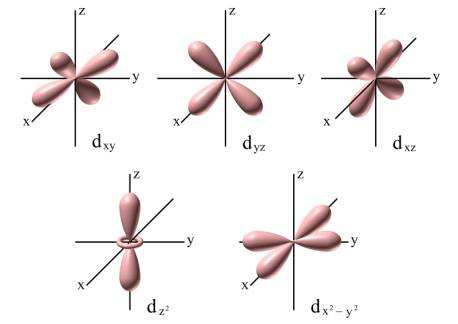
rys. orbital p
rys orbital d
W wiązaniach kowalencyjnych przeważnie uczestniczą elektrony s i p,
ograniczymy się do rozpatrzenia ich chmur elektronowych. .
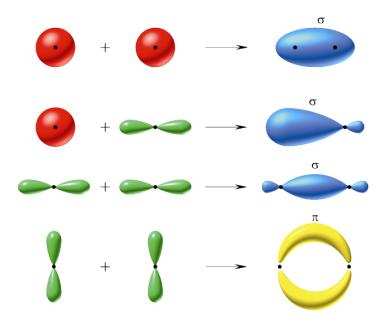
Wiązanie kowalencyjne powstaje wówczas, gdy chmura niesparowanego
elektronu jednego atomu i chmura niesparowanego elektronu drugiego atomu
przenikają się (nakładają) nawzajem.
Najprostszy typ wiązania kowalencyjnego – jest to wiązanie za
pośrednictwem pary s-s. Atom nie może mieć więcej niż jeden niesparowany
elektron s. We wszystkich kierunkach od jądra właściwości chmury tego
elektronu są jednakowe: żaden kierunek nie jest wyróżniony. Jeżeli więc w
dowolnym kierunku chmura kulista niesparowanego elektronu s natrafi na
tka chmurę elektronu innego atomu, wytworzy się wiązanie s-s,
przedstawione schematycznie. Cząsteczka wodoru. H-H.
Wiążące orbitale δ i π.
Wyszukiwarka
Podobne podstrony:
Zagadnienia - ogólnie, I ROK, II SEMESTR, Chemia Fizyczna
Chemia Bionie wyk1
chemia powt
02a URAZY CZASZKOWO MÓZGOWE OGÓLNIE 2008 11 08
Wykład Chemia kwantowa 11
wyklad z czwartku chemia fizycz dnia19 marca
chemia(1) 3
Chemia węglowodory
Chemia organiczna czesc I poprawiona
ERGONOMIA chemia
chemia organiczna wykład 6
Chemia wyklad I i II (konfiguracja wiÄ…zania Pauling hybrydyzacja wiazania pi i sigma)
Chemia procesu widzenia
Chemia R cje chemiczne
Chemia materiałów V
więcej podobnych podstron