ĆWICZENIE 6
Kwasy karboksylowe to związki organiczne zawierające grupę COOH. Niższe kwasy
karboksylowe (nasycone i nienasycone) są ciekłe, wyższe (powyżej C12) są ciałami stałymi.
Kwasy od C1 do C3 mają silny ostry zapach i rozpuszczają się w wodzie w dowolnym stosunku, a powyżej C4 pozbawione są zapachu i ich rozpuszczalność w wodzie maleje.
Kwasy powyżej C12 są praktycznie nierozpuszczalne w wodzie. Kwasy aromatyczne są bardzo trudno rozpuszczalne w zimnej wodzie. Kwasy karboksylowe rozpuszczone w wodzie
wykazują odczyn kwasowy, co może stanowić potwierdzenie ich obecności w analizowanej próbce związku. Reagują również z roztworami zasad i z NaHCO3. Kwasy w odróżnieniu od
fenoli reagują z tym odczynnikiem z wydzieleniem gazowego CO2. W analizie jakościowej kwasów wykorzystywane są reakcje zachodzące w obrębie grupy karboksylowej takie jak reakcje bezpośrednio związane z kwasowym wodorem – próba ze wskaźnikiem, próba jodan-jodek lub reakcja estryfikacji kwasu alkoholem. Wykorzystywane są także reakcje związane są z indywidualnymi właściwościami różnych rodzajów kwasów.
W probówkach opisanych numerami 1, 2, 3 znajdują się związki organiczne zawierające w swojej budowie ugrupowanie karboksylowe, a zatem mogą to być:
a) Kwasy (nasycone, nienasycone lub aromatyczne)
b) Fenolokwasy
c) Hydroksykwasy
d) Kwasy wielokarboksylowe
e) Na podstawie wykonanych prób analitycznych należy przyporządkować probówkę do
odpowiedniej grupy węglowodorów.
Rodzaj substancji
Reakcje charakterystyczne
Wynik próby
Reakcja z fenoloftaleiną,
Odbarwianie roztworu fenoloftaleiny
Kwas alifatyczny
Reakcja z NaHCO 3
Wydzielanie pęcherzyków gazu
Reakcja z FeCl3
Powstawanie czerwone zabarwienia
Reakcja z fenoloftaleiną,
Odbarwianie roztworu fenoloftaleiny
Kwas aromatyczny
Reakcja z NaHCO 3
Wydzielanie pęcherzyków gazu
Reakcja nitrowania
Powstaje żółte zabarwienie
Kwas aromatyczny z
Reakcje z fenoloftaleiną,
Odbarwianie roztworu fenoloftaleiny
grupą hydroksylową
NaHCO3
Wydzielanie pęcherzyków gazu
Reakcja z FeCl3
Powstaje fioletowe zabarwienie
Reakcje z fenoloftaleiną,
Odbarwianie roztworu fenoloftaleiny
Kwas alifatyczny z
NaHCO3
Wydzielanie pęcherzyków gazu
grupą hydroksylową
Reakcja z KMnO4
Odbarwianie roztworu KMnO4
Reakcja z fenoloftaleiną,
Odbarwianie roztworu fenoloftaleiny
Kwas
NaHCO3 lub FeCl3
Wydzielanie pęcherzyków gazu
dikarboksylowy
Reakcja z rezorcyną
Powstawanie barwy niebieskiej
OGÓLNE PRÓBY WYKRYWANIA KWASU KARBOKSYLOWEGO
Próba z wodorowęglanem sodu – NaHCO3
Próba z wodorowęglanem sodu pozwala odróżnić kwasy karboksylowe od fenoli.
RCOOH + NaHCO3 → RCOONa + CO2↑+ H2O
ArOH + NaHCO3 → brak objawów reakcji
Wykonanie:
Do probówki dodaje się około 1 cm3 5% roztworu NaHCO3 i kroplę lub 0.01g substancji badanej. Wydzielanie się pęcherzyków CO2 wskazuje na obecność kwasu.
Próba ze wskaźnikiem uniwersalnym
Do przeprowadzenia tej próby używa się wodnego roztworu badanego kwasu i papierka uniwersalnego. Do związków nierozpuszczalnych w wodzie należy najpierw dodać kilka kropli alkoholu lub acetonu a następnie dopiero wody. Równolegle przygotowuje się próbę kontrolną z wodą i użytym rozpuszczalnikiem.
Wykonanie:
0, 1 cm3 lub 0,05 g badanej substancji rozpuszcza się na szkiełku zegarkowym w około 1 cm 3
wody destylowanej. Do przygotowanego roztworu zanurza się papierek wskaźnikowy i odczekuje minutę. Porównanie zabarwienie papierka ze wzorcową skalą barw
odpowiadających określonemu zakresowi pH dostarcza informacji o charakterze badanej substancji.
Próba z fenoloftaleiną
Związki o charakterze kwasowym odbarwiają zasadowy roztwór fenoloftaleiny.
Wykonanie:
Na szkiełku zegarkowym umieszcza się jedną kroplę 0,01M NaOH, jedną kroplę etanolowego
roztworu fenoloftaleiny i 4 krople wody, a następnie 4 krople lub niewielką ilość dobrze sproszkowanej badanej substancji. Odbarwienie fenoloftaleiny potwierdza charakter kwasowy badanego związku.
Próba jodan - jodek
Próba jodan – jodek wykonywana jest do identyfikacji słabych kwasów. Podczas
przeprowadzania reakcji jodan – jodek w obecność kwasu powstaje wolny jod, który powoduje niebieskie zabarwienie skrobi.
5I- + IO -
3 + 6H+ = 3H2O + 3I2
Wykonanie:
Do probówki zawierającej około 5mg badanej substancji lub dodaje się (nasycony roztwór w 2 kroplach etanolu) zadaje się w probówce 2 kroplami 2% roztworu KI i 2 kroplami 4%
roztworu KIO3. Probówkę zamyka się zwitkiem waty i ogrzewa przez minutę we wrzącej łaźni wodnej. Po oziębieniu dodaje się 4 krople 0.1% roztworu skrobi. W obecności kwasów powstaje wolny jod, który zabarwia skrobię na kolor fioletowy lub fioletowoniebieski.
REAKCJE DLA KWASÓW MONOKARBOKSYLOWYCH
1. Próba na kwas mrówkowy
Kwas mrówkowy w odróżnieniu od pozostałych kwasów karboksylowych posiada
właściwości redukujące.
Wykonanie:
Do probówki zawierającej około 1 ml roztworu kwasu mrówkowego dodaje się kilka kropli roztworu sublimatu (HgCl2) i ogrzewa we wrzącej łaźni wodnej do pojawienia się białego osadu kalomelu (Hg2Cl2).
2. Próba na właściwości redukujące kwasu mrówkowego
W wyniku utleniania kwasu mrówkowego otrzymuje się kwas węglowy, który rozkłada się do
ditlenku węgla i wody.
+
H
KMnO4/H
O
CO2 + H2O
HO
Wykonanie:
Do próbówki zawierającej około 1 cm3 kwasu mrówkowego dodaje się 2 cm3 nasyconego roztworu KMnO4 i 1 cm3 2M H2SO4. Widoczne wydzielanie CO2 na zimno potwierdza obecność kwasu mrówkowego.
3. Próba na właściwości redukujące kwasu mrówkowego
Wykonanie:
Do próbówki zawierającej około 0,5 cm3 1% roztworu AgNO3 dodaje się 0,5 cm3 kwasu mrówkowego i lekko ogrzewa. Pojawienie się szarego osadu srebra potwierdza obecność kwasu mrówkowego
Wykrywanie kwasu octowego
Podobnie jak kwas mrówkowy , propionowy tak i kwas octowy dają pozytywną reakcję z FeCl3. Pod wpływem tego odczynnika w obecności wymienionych kwasów powstaje
czerwone zabarwienie roztworu.
H C
H C
3 NaOH
H C
3
3
3
+
FeCl3
O
3+
O
3
O
Na
Fe
-
O
H
-
O
O
3
Wykonanie:
Do około 0,2 cm3 badanej substancji dodaje się 2 cm3 wody destylowanej. Otrzymany roztwór zobojętnia się 10% NaOH, a następnie dodaje kilka kropli 10% FeCl3 i porównuje zabarwienie z równocześnie przygotowaną próbą kontrolną. Do przygotowania próby kontrolnej używa się tych samych składników z pominięciem badanej substancji.
REAKCJE KWASÓW AROMATYCZNYCH
Reakcja kwasu benzoesowego z chlorkiem żelaza (III).
Wykonanie:
Do probówki wlewa się 2 cm3 roztworu kwasu benzoesowego i dodaje 2 krople 0,5 M
roztworu NaOH celem zobojętnienia roztworu wobec papierka wskaźnikowego. Następnie dodaje się kroplami 1 cm3 1%roztworu FeCl3. Powstaje jasno pomarańczowy galaretowaty osad benzoesanu żelaza.
Wykrywanie pierścienie aromatycznego
UWAGA! Próbę wykonać pod digesterium. Reakcja może zachodzić gwałtownie -
zachować ostrożność, wykonywać w ostateczności.
Związki zawierające pierścień aromatyczny ulegają reakcji nitrowania w środowisku kwaśnym tworząc żółte nitrowe pochodne.
Wykonanie:
Do próbówki odmierza się około 0,5cm3 roztworu badanego, dodaje około 0,5cm3 stężonego
HNO3 a następnie kilka kropel stężonego H2SO4. Zawartość probówki bardzo ostrożnie ogrzewać. Pojawienie się żółtego zabarwienia potwierdza obecność pierścienia
aromatycznego.
REAKCJE KWASÓW DIKARBOKSYLOWYCH
Próba na wykrywanie kwasu szczawiowego – reakcja z rezorcyną
Kwasy 1,2 – dikarboksylowe oraz ich pochodne (estry, bezwodniki, imidy) reagują z rezorcyną w obecności stężonego kwasu siarkowego (VI). Powstają wówczas barwniki typu fluoresceiny.
Wykonanie:
Do probówki zawierającej 1 cm3 wodnego roztworu kwasu szczawiowego wrzuca się 2-3
kryształki rezorcyny. Całość miesza aż do rozpuszczenia rezorcyny. Następnie ostrożnie po ściance probówki wkrapla się 1cm3 stęż. H2SO4. Powstanie niebieskiego pierścienia
potwierdza obecność kwasu szczawiowego.
Próba na wykrywanie kwasu szczawiowego – utlenianie za pomocą KMnO4
Oznaczanie kwasu szczawiowego opiera się na reakcji, w której manganian(VII) w
środowisku kwasu siarkowego(VI) utlenia jony szczawianowe do ditlenku węgla:
2MnO -
2-
4 + 5C2O4 + 16H+ = 2Mn2+ + 10CO2 + 8H2O
W wyniku tej reakcji obserwuje się odbarwienie dodawanych porcji titranta. Na początku
przebieg reakcji jest powolny. Dopiero po upływie czasu niezbędnego do powstania jonów
manganu (II), które katalizują reakcje utleniania jonów szczawianowych, obserwuje się
wzrost szybkości reakcji analitycznej.
Wykonanie:
Do probówki wprowadza się 0,5 cm3 wodnego roztworu badanej substancji (kwasu
szczawiowego) i 1,5 cm3 16% H2SO4 i kilka kropel 1% KMnO4. Całość ogrzewa do temperatury 700C. kwasu. W przypadku obecności kwasu szczawiowego następuje
odbarwienie roztworu KMnO4.
Rozkład kwasu szczawiowego
Wykonanie:
0,1 g substancji ogrzewa się w suchej probówce. W przypadku kwasu szczawiowego
następuje rozkład z wydzieleniem HCOOH i CO2. Obecność powstałego kwasu mrówkowego
można wykryć za pomocą wcześniej podanych metod.
Izomeryzacja kwasu maleinowego do kwasu fumarowego
Kwas maleinowy ma konfigurację cis (Z), łatwo tworzy bezwodnik kwasowy i rozpuszcza się w wodzie . Kwas fumarowy ma konfigurację trans (E) i nie tworzy bezwodnika kwasowego.
W przeciwieństwie do kwasu maleinowego jest trudno rozpuszczalny w wodzie.
Wykonanie:
Do kolby o poj. 50 ml zaopatrzonej w chłodnicę zwrotną wprowadza się około 0,5 g kwasu
maleinowego rozpuszczonego w 5 cm3 ciepłej wody destylowanej i dodaje 1 cm3 stężonego
kwasu solnego. Całość ogrzewa się do łagodnego wrzenia w przez 30 min. W trakcie reakcji z roztworu reakcyjnego wypadają kryształki kwasu fumarowego. Roztwór pozostawia się do
ostygnięcia w temp. pokojowej. Wydzielony kwas fumarowy sączy się na lejku Buchnera i
przemywa 100cm3 zimnej wody. Osad pozostawia się do wysuszenia Otrzymany produkt
można identyfikować na podstawie temperatury topnienia (kwas fumarowy topi się przy 286-2870C).
PRÓBA NA HYDROKSYKWASY
Próba Uffelmana na wykrywanie kwasu mlekowego
Próba Uffelmana polega na wiązaniu przez kwas mlekowy żelaza zawartego w odczynniku Uffelmana (roztwór fenolu z dodatkiem chlorku żelaza( III)). W wyniku reakcji fenolu z FeCl3 powstaje fenolan żelaza(III) o fioletowym zabarwieniu. W obecności kwasu mlekowego fioletowe zabarwienie przechodzi w żółte, gdyż powstaje mleczan żelaza. Próba ta stosowana jest do wykrywania kwasu mlekowego w soku żołądkowym. Podobna reakcja zachodzi z kwasem solnym.
Wykonanie:
Do probówki wlewa się około 1 cm3 1% roztworu fenolu dodaje jedną kroplę roztworu 1%FeCl3. Do zabarwionego na kolor fioletowy roztworu dodaje kilka kropel badanego roztworu kwasu mlekowego. Barwa fioletowa zmienia się na żółtą. Równolegle wykonuje się analogiczną próbę, używając zamiast kwasu mlekowego kwasu solnego. W tym przypadku nastąpi odbarwienie roztworu, lecz nie wystąpi żółte zabarwienie roztworu.
Utlenianie kwasu mlekowego
W wyniku utleniania hydroksykwasu otrzymuje się ketokwas, który analogicznie do ketonów reaguje z fenylohydrazyną, tworząc fenylohydrazony – ciała o wysokiej temperaturze topnienia, trudno rozpuszczalne. Dzięki temu służą one do wyodrębniania ketonów z mieszanin innych związków.
Wykonanie:
W kolbce stożkowej umieszcza się 0,5 cm3 kwasu mlekowego, dodaje 1 kroplę fenoloftaleiny i zobojętnia 0,5 M roztworem NaOH. Następnie dodaje się 12 cm3 1% roztworu KMnO4 i kolbkę odstawia na około 20 minut. Kwas mlekowy utlenia się w tych warunkach do kwasu
pirogronowego, a fioletowa barwa KMnO4 zanika. Zawartość kolby przesącza się na lejku Buchnera, przesącz wykorzystuje się do dalszej analizy.
Wykrywanie obecności kwasu pirogronowego:
Do otrzymanego przesączu ,zawierającego kwas pirogronowy, w ilości 3 cm3 dodaje się 0,5 cm3
roztworu chlorowodorku fenylohydrazyny. Z roztworu wytrąca się żółty osad fenylohydrazonu kwasu pirogronowego.
NaOH
CH3
CH
COOH
CH
C
3
COOH + H
KMnO
2O
4
OH
O
CH3
CH3
C
O + H
C
N
+ H
2N
NH
NH
2O
COOH
COOH
Próba na kwas salicylowy – próba z FeCl3
Wykonanie:
Kilka kryształków kwasu salicylowego rozpuszcza się w 1 cm3 wody i dodaje 3-4 krople roztworu 1% FeCl3. Podobnie jak w roztworze fenoli pojawienie się fioletowego zabarwienia, które nie zmienia się po dodaniu 1 cm3 etanolu potwierdza obecność fenolokwasu.
Próba na kwas salicylowy – próba z CaO
Kwas salicylowy ogrzewany z CaO rozkłada się do fenolu i CO2
O
OH
CaO/ temp.
OH
+ CaCO3
OH
Wykonanie:
W suchej probówce ogrzewa się około 0,5 g badanej substancji z około 0,5 g CaO.
Powstawanie charakterystycznego dla fenoli zapachu potwierdza obecność kwasu
salicylowego. Dodatkowo otrzymany fenol można identyfikować w reakcji z FeCl3.
Próba na kwas acetylosalicylowy – próba z FeCl3
Kwas acetylosalicylowy należy poddać reakcji hydrolizy a następnie przeprowadzić próbę z FeCl3
Wykonanie:
0,1 g badanej substancji wraz z kilkoma cm3 wody ogrzewa się do wrzenia w ciągu 1 min. Do ochłodzonego roztworu dodaje się 3-4 kropli 3% FeCl3 Powstanie ciemnofioletowego zabarwienia potwierdza pośrednio obecność kwasu acetylosalicylowego.
REAKCJE NA NIENASYCONE KWASY KARBOKSYLOWE - NIENASYCONE
KWASY TŁUSZCZOWE
Przyłączanie halogenu do nienasyconych kwasów tłuszczowych
Jod (lub inne halogeny) łatwo przyłączają się w miejscu podwójnego wiązania, w wyniku czego brunatny roztwór jodu odbarwia się i powstaje bezbarwny halogenokwas.
Wykonanie:
Do 3 kropli oliwy (lub nienasyconego kwasu karboksylowego) dodaje się kroplami odczynnik Hubla (roztwór jodu i chlorku rtęci(II) w alkoholu). Płyn odbarwia się po pewnym czasie w temperaturze pokojowej lub natychmiast po ogrzaniu. Potwierdza to obecność nienasyconego kwasu tłuszczowego.
Utlenianie wiązań podwójnych w nienasyconych kwasach tłuszczowych
Wiązania podwójne łatwo ulegają utlenieniu pod wpływem utleniaczy, a także chociaż znacznie wolniej, pod wpływem tlenu atmosferycznego. Cząsteczka kwasu tłuszczowego, w miejscu podwójnego wiązania, ulega rozbiciu na dwie cząsteczki zawierające grupy aldehydowe. Reakcja ta zachodzi podczas jełczenia tłuszczów, a gromadzące się aldehydy nadają im przykry smak i zapach.
Wykonanie:
Do probówki zawierającej kilka kropli oliwy dodaje się 1 cm3 roztworu 5% Na2CO3 celem rozpuszczenia badanej substancji. Po rozpuszczeniu oliwy wkrapla się 2%KMnO4.
Odbarwienie dodanego roztworu KMnO4 potwierdza obecność wiązań wielokrotnych.
Analiza spektralna kwasów karboksylowych i ich niektórych pochodnych
1. Spektroskopia w podczerwieni (IR)
Obszar widma w podczerwieni obejmujący 1870-1600 cm-1 ma szczególne znaczenie w badaniach spektroskopowych wszystkich związków posiadających wiązanie C=O (także kwasów karboksylowych i ich pochodnych). Położenie pasma absorpcyjnego wiązania C=O
jest zależne od czynników wewnątrzcząsteczkowych i oddziaływań międzycząsteczkowych.
W porównaniu z pasmami ketonów i aldehydów, sygnały grupy C=O kwasu karboksylowego
ma często znacznie większe natężenie, ponadto kwasy wykazują absorpcję także w innych obszarach widma wskutek obecności grupy hydroksylowej w grupie karboksylowej.
Estry charakteryzują się wstępowaniem charakterystycznych pasm absorpcyjnych wiązań C=O oraz C– O (szczegółowe wartości w tabelce).
W przypadku amidów, oprócz charakterystycznego pasma absorpcji C=O występują pasma drgań N–H. Amidy pierwszorzędowe dają dwa pasma blisko 3350 i 3180 cm-1, natomiast amidy drugorzędowe jedno pasmo w okolicy 3300 cm-1.
Charakterystyczne pasma absorpcyjne w IR kwasów karboksylowych i ich pochodnych:
Charakterystyczne
Grupa związków
Rodzaj drgań
pasma absorpcji (cm-1)
O–H rozciągające (wolna
3550-3500
O–H)
O–H rozciągające
kwasy karboksylowe, kwasy
3300-2500
(związana O–H); szerokie
sulfonowe
pasmo
O–H rozciągające poza
955-890
płaszczyzną deformacyjne
1725-1700
nasycone kwasy alifatyczne
1700-1680
kwasy aromatyczne
1740-1715
α-halogenokwasy
1750-1735
estry alifatyczne nasycone
estry
α-
i
β-nienasycone
i
1730-1715
aromatyczne
1800-1770
estry fenylowe i winylowe
1755-1740
α-ketoestryiα-diestry
ok. 1825
β-laktony
C=O rozciągające
1780-1760
nasycone γ-laktony
1750-1735
δ-laktony
ok. 1690
amidy I-rzędowe w rozcieńczonym
roztworze
ok. 1650
amidy I-rzędowe w fazie stałej
1700-1665
amidy II-rzędowe w
rozcieńczonym roztworze
1680-1630
amidy II-rzędowe w fazie stałej
1670-1630
amidy III-rzędowe
1735-1700
uretany
1815-1785
halogenki kwasowe
1320-1210
kwasy karboksylowe
C–O rozciągające
1300-1000
estry
3540-3480
amidy I-rzędowe, wolna N–H
3420-3380
3360-3320
amidy I-rzędowe, związana N–H
3220-3180
N–H rozciągające
3460-3420
amidy II-rzędowe, wolna N–H
3330-3070
amidy II-rzędowe, związana N–H
3300
sulfonamidy (jedno lub dwa pasma)
1640-1500
amidy I i II-rzędowe
N–H zginające
1415-1300
kwasy sulfonowe, siarczany
O=S=O rozciągające
1200-1120
2. Spektroskopia magnetycznego rezonansu jądrowego
a) 1H-NMR
Szczególną cechą widma 1H-NMR kwasu karboksylowego jest sygnał piku protonu grupy karboksylowej w obszarze 10-13 ppm. Ponadto charakterystyczną pozycję mają sygnały protonów węgli w otoczeniu grupy karboksylowej.
W przypadku amidów sygnał protonu grupy amidowej jest mało charakterystyczny i zależy od zarówno od budowy cząsteczki jak i od czynników zewnętrznych np. temperatury, rodzaju rozpuszczalnika.
Charakterystyczne wartości położenia sygnałów:
Przesunięcie chemiczne (ppm)
Proton
10,0-13,0
R–COOH(kwasy karboksylowe)
R–CH–COOH (kwasy karboksylowe)
2,1-2,5
R–CH–COOR (estry)
–CH–CO–NH– (amidy)
3,5-4,8
R–COO–CH– (estry)
5,0-9,0
R(CO) –NH(amidy)
2,2-2,9
R(CO) –N–CH(amidy)
b) 13C-NMR
Charakterystyczne wartości położenia sygnałów:
Przesunięcie chemiczne (ppm)
Węgiel
155-185
C=O (kwasy karboksylowe, estry,
amidy, bezwodniki)
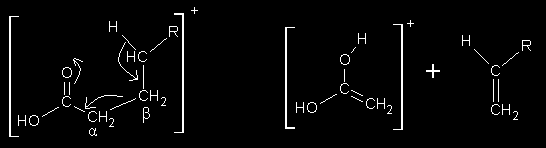
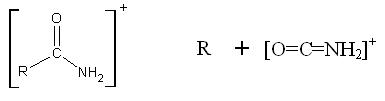
4. Spektrometria masowa (MS)
W widmie masowym kwasów karboksylowych występuje jon molekularny, którego
intensywność uzależniona jest od rodzaju kwasu. W przypadku kwasów aromatycznych, pik
jonu macierzystego charakteryzuje się przeważnie dużą intensywnością.
Charakterystycznymi pikami rozpoznawczym są:
- powstające w wyniku rozpadu wiązań utworzonych przez węgiel grupy karboksylowej:
• [M+–17] = [M+–OH],
• [M+–45] = [M+–COOH];
- powstający w wyniku rozerwania wiązania β względem grupy C=O (w kwasach
alifatycznych) tzw. przegrupowanie McLafferty’ego:
• [M+–60] = [M+–CH3COOH];
m/e=60
Biorąc pod uwagę powyższe drogi rozpadu kwasów karboksylowych charakterystycznymi pikami mającymi znaczenie diagnostyczne są także: m/e=45 oraz m/e=60.
Dla kwasów aromatycznych charakterystycznym jonem jest [Ar–C≡O]+, który daje
przykładowo pik m/e=105 dla [C6H5–C≡O]+.
Dla estrów kwasów karboksylowych charakterystyczny jest pik jonu [R–C=O]+, powstałego w wyniku oderwania grupy alkoksylowej. Inną częstą drogą fragmentacji jest oderwanie grupy alkilowej pochodzącej od kwasu co skutkuje powstaniem jonu [R–O-C=O]+.
Fragmentacja amidów zachodzi zazwyczaj analogicznie do kwasów karboksylowych.
Przykładowo dla amidów pierwszorzędowych charakterystyczny jest pik m/e=44.
m/e=44
oznacza na rysunkach wolny rodnik