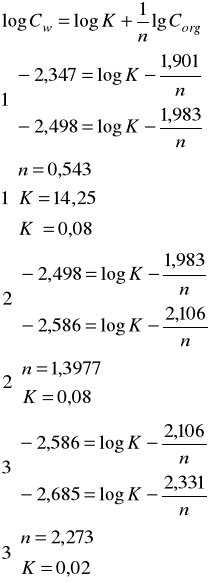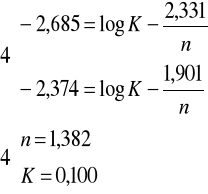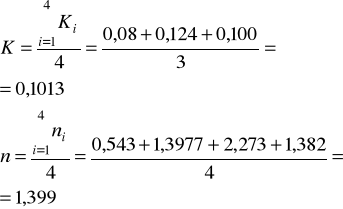Nr 6
SPRAWOZDANIE Z ĆWICZENIA
W LABORATORIUM CHEMII FIZYCZNEJ
Wydział: Chemii Spożywczej i Biotechnologii
Semestr III
Tomasz Florczak
Ćwiczenie nr 34
Temat: Oznaczanie stałej podziału kwasu benzoesowego w układzie woda- benzen (woda -toluen)
Celem ćwiczenia jest wyznaczenie współczynnika podziału kwasu benzoesowego pomiędzy dwie niemieszające się ciecze- wodę i benzen. Miareczkując zasada kwas benzoesowy zawarty w fazie wodnej można wyznaczyć stężenie równowagowe kwasu w fazie organicznej.
Współczynnik podziału wyznaczamy korzystając z prawa Nernsta. Prawo to mówi, że jeżeli do układu dwu niemieszających się cieczy A i B dodamy trzeci składnik rozpuszczający się w obydwu cieczach to po ustaleniu równowagi, podzieli się on pomiędzy fazy ciekłe tak, że stosunek jego stężeń molowych w obu fazach będzie w stałej temperaturze wielkością stałą. Zależność ta wynika z równości potęcjałów chemicznych składnika rozpuszczanego w obu fazach:
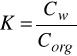
Jeżeli masa cząsteczkowa się zmienia na skutek procesów zachodzących w roztworach pisujemy wzór następująco:
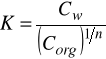
Przy czym n oznacza liczbę wskazującą ile razy masa substancji rozpuszczonej jest większa od masy cząsteczkowej tej substancji rozpuszczonej w pierwszym rozpuszczalniku.
Po zlogarytmowaniu otrzymujemy:
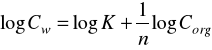
Nr próbki |
Objętość ługu
[ml] |
Stężenie wyjściowe
[mol/dm3] |
Objętość ługu
[ml] |
Stężenie równowagowe w fazie wodnej
[mol/dm3] |
Stężenie równowagowe w fazie organ.
[mol/dm3] |
|
|
1 |
31,8 |
1,685e-2 |
8,1 |
4,293e-3 |
1,256e-2 |
-2,374 |
-1,901 |
2 |
25,6 |
1,357e-2 |
6 |
3,18e-3 |
1,039e-2 |
-2,498 |
-1,983 |
3 |
19,7 |
1,044e-2 |
4,9 |
2,597e-3 |
7,843e-3 |
-2,586 |
-2,106 |
4 |
12,7 |
6,731e-3 |
3,9 |
2,067e-3 |
4,664e-3 |
-2,685 |
-2,331 |
5 |
6,5 |
3,445e-3 |
|
|
|
|
|
Z poniżej zamieszczonego wykresu obliczam stałe K i n:
|
|
Wnioski:
Badana oznaczania stałej podziału kwasu benzoesowego w układzie woda -toluen daje wartości przbliżone. Liczba n wydaje się być prawidłowa mimo iż dwa wyniki odbiegają od pozostałych jednakże ich średnia artmetyczna daje wartość zbliżoną do wyliczonej. Przy wyznaczaniu współczynnika podziału Nernsta jedna wartość znacznie odbiegała od pozostałych w związku z czym postanowiłem ją odrzucić jako błedną. Wyszła ona zbyt wysoka co według mojego zdania było spowodowane znacznym błędem w liczbie n.Podkreśla to fakt , że licząc wsp. K dla wartości średniej n otrzymana wartość wydaje się być sensowna. Jednakże trudno jest mi się ustosunkować co do prawdziwości otrzymanego wyniku. Biorąc pod uwagę dokładność z jaką starałem się wykonać doświadczenie, powinien on oscylować wokół wartości prawdziwej.
-1,9 -2 -2,1 -2,2 -2,3 -2,4
-2,4
-2,5
-2,6
-2,7
logCorg
logCw
logCw=f(logCorg)
Wyszukiwarka