09.04.2003 |
xx |
Grupa 3 |
Ćwiczenie nr 3 |
MIARECZKOWANIE SPEKTROFOTOMETRYCZNE |
Ocena: |
Prowadzący: |
xxx |
|
Uwagi: |
||
Cel ćwiczenia:
Celem ćwiczenia było ilościowe oznaczenie w otrzymanej próbce zawartości jonów Cu2+ metodą spektrofotometrycznego miareczkowania mianowanym roztworem EDTA.
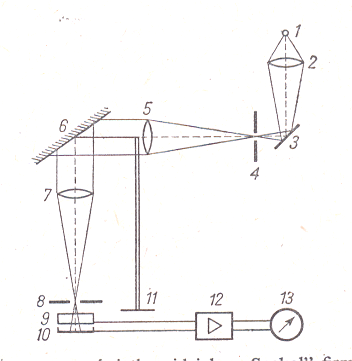
Schemat optyczny spektrofotometru „SPEKOL”:
Wykonanie ćwiczenia:
Otrzymaną do analizy próbkę zawierającą jony Cu2+, uzupełniono w kolbie miarowej na 100 cm3 wodą destylowaną do kreski (otrzymano roztwór A).
W celu wybrania właściwej do miareczkowania długości fali wykonano krzywe absorpcji substancji miareczkowanej i produktu reakcji. W tym celu w suchych zlewkach o pojemności ok. 50 cm3 sporządzono następujące roztwory:
roztwór B - 5 cm3 roztworu Cu2+ z kolby A,
10 cm3 buforu amonowego o pH = 10
roztwór C - 5 cm3 roztworu Cu2+ z kolby A
10 cm3 buforu amonowego o pH = 10
10 cm3 0,02 M roztworu EDTA
Do spektrofotometru SPEKOL zamontowano przystawkę EK i wyznaczono krzywe absorpcji roztworów B i C. Do pomiarów użyto kiuwet o grubości 1 cm. Jako odnośnika użyto wody destylowanej. Pomiary przeprowadzono dla długości fal od 550 - 750 nm w odstępach co 10 nm.
Na podstawie otrzymanych wyników (Tabela 1) narysowano krzywe absorpcji roztworów B i C (wykres 1 i wykres 2) i wybrano długość fali, przy której wykonano miareczkowanie.
Tabela 1.
Absorbancja roztworów B i C w zakresie długości fal 550 - 750 nm.
λ[nm] |
A dla roztworu B |
A dla roztworu C |
550 |
0,225 |
0,000 |
560 |
0,285 |
0,015 |
570 |
0,300 |
0,015 |
580 |
0,320 |
0,020 |
590 |
0,330 |
0,030 |
600 |
0,355 |
0,040 |
610 |
0,458 |
0,070 |
620 |
0,395 |
0,075 |
630 |
0,390 |
0,090 |
640 |
0,385 |
0,105 |
650 |
0,375 |
0,120 |
660 |
0,360 |
0,130 |
670 |
0,345 |
0,140 |
680 |
0,325 |
0,150 |
690 |
0,305 |
0,155 |
700 |
0,285 |
0,165 |
710 |
0,270 |
0,165 |
720 |
0,250 |
0,165 |
730 |
0,240 |
0,165 |
740 |
0,225 |
0,165 |
750 |
0,220 |
0,165 |
Uwaga: Na wykresie 1 nie zaznaczono punktu dla λ = 610 nm (A = 0,458), ponieważ odbiega on znacznie od pozostałych wyników (błąd pomiaru).
Na podstawie sporządzonych wykresów wybrano długość fali, która wyniosła: λ = 620 nm.
Przy tej długości fali wykonano miareczkowanie.
Wykonanie miareczkowania:
Zamontowano przystawkę do miareczkowania Ti. Ustawiono wybraną długość fali (λ = 620 nm). W kiuwecie umieszczono wodę destylowaną i nastawiono czułość tak, aby absorbancja odnośnika wynosiła 0 (T = 100%). Przystąpiono do miareczkowania otrzymanej próbki Cu2+. Do kiuwety pomiarowej odmierzono dokładnie 5 cm3 próbki Cu2+ (pobranej pipetą z kolby A) i 10 cm3 buforu amonowego o pH = 10. Do biurety o poj. 10 cm3 wlano mianowany 0,0190 M roztwór EDTA i umieszczono ją w uchwycie przystawki Ti. Włączono mieszadło magnetyczne i miareczkowano dodając z biurety roztwór EDTA porcjami po 0,5 cm3. Po dodaniu każdej porcji titranta mierzono absorbancję roztworu. Miareczkowanie prowadzono tak długo, aż otrzymano kilka identycznych wartości absorbancji.
Miareczkowanie powtórzono trzykrotnie dla identycznie przygotowanych próbek.
Wyniki miareczkowań zestawiono w tabeli 2.
Tabela 2.
Wyniki miareczkowania spektrofotometrycznego trzech próbek Cu2+ mianowanym 0,0190 M roztworem EDTA dla długości fali 620 nm.
V [ml] |
(Vo+Vt)/Vo |
A1 |
A2 |
A3 |
A1 ⋅ (Vo+Vt)/Vo |
A2 ⋅ (Vo+Vt)/Vo |
A3 ⋅ (Vo+Vt)/Vo |
0,0 |
1,0000 |
0,800 |
0,800 |
0,810 |
0,800 |
0,800 |
0,810 |
0,5 |
1,0333 |
0,710 |
0,720 |
0,740 |
0,734 |
0,744 |
0,765 |
1,0 |
1,0667 |
0,630 |
0,640 |
0,660 |
0,672 |
0,683 |
0,704 |
1,5 |
1,1000 |
0,540 |
0,550 |
0,590 |
0,594 |
0,605 |
0,649 |
2,0 |
1,1333 |
0,455 |
0,470 |
0,510 |
0,516 |
0,533 |
0,578 |
2,5 |
1,1667 |
0,385 |
0,400 |
0,440 |
0,449 |
0,467 |
0,513 |
3,0 |
1,2000 |
0,315 |
0,340 |
0,375 |
0,378 |
0,408 |
0,450 |
3,5 |
1,2320 |
0,250 |
0,270 |
0,310 |
0,308 |
0,333 |
0,382 |
4,0 |
1,2667 |
0,220 |
0,225 |
0,255 |
0,279 |
0,285 |
0,323 |
4,5 |
1,3000 |
0,215 |
0,225 |
0,245 |
0,280 |
0,293 |
0,319 |
5,0 |
1,3333 |
0,210 |
0,220 |
0,240 |
0,280 |
0,293 |
0,320 |
5,5 |
1,3667 |
0,205 |
0,210 |
0,240 |
0,280 |
0,287 |
0,328 |
6,0 |
1,4000 |
0,200 |
0,210 |
0,235 |
0,280 |
0,294 |
0,329 |
6,5 |
1,4333 |
0,200 |
0,210 |
0,230 |
0,287 |
0,301 |
0,330 |
7,0 |
1,4667 |
0,195 |
0,200 |
0,225 |
0,286 |
0,293 |
0,330 |
7,5 |
1,5000 |
0,190 |
0,200 |
0,220 |
0,285 |
0,300 |
0,330 |
8,0 |
1,5333 |
0,190 |
0,200 |
0,215 |
0,291 |
0,307 |
0,330 |
5. Opracowanie wyników:
W otrzymanych wynikach miareczkowania skorygowano błąd rozcieńczania, mnożąc każdy wynik przez iloraz
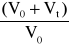
, gdzie:
Vo - objętość początkowa = 15 cm3,
Vt - objętość kolejnych porcji titranta.
Skorygowane wyniki miareczkowania zamieszczono w tabeli 2.
Na podstawie tabeli 2 sporządzono wykresy krzywych miareczkowania dla poszczególnych próbek (wykresy 3, 4 i 5, skorygowane wartości absorbancji).
Z otrzymanych wykresów odczytano punkty końcowe miareczkowania dla poszczególnych miareczkowań. Wynoszą one odpowiednio:
PK1 = 3,7 cm3
PK2 = 3,8 cm3
PK3 = 4,0 cm3
PKśr = 3,83 cm3
d) Obliczono masę Cu2+ w badanej próbce: Vk = 100 cm3, Vp = 5 cm3, W = ![]()
![]()
=![]()
= 0,0946 g
Wniosek: Otrzymana próbka zawierała 0,0946 g Cu2+.
1
1 - źródło światła
2 - kondensor
3 - zwierciadło
4 - przesłona wejściowa
5, 7 - soczewki achromatyzujące
6 - siatka dyfrakcyjna
8 - przesłona wyjściowa
9 - kiuweta z badanym roztworem
10 - fotoogniwo selenowe
11 - skala długości fal do nastawiania siatki
dyfrakcyjnej
12 - wzmacniacz tranzystorowy
13 - przyrząd pomiarowy
Wyszukiwarka