Metody rozdzielania i oczyszczania substancji chemicznych.
I. Ekstrakcja
Polega na wydzieleniu jednego z kilku składników z mieszaniny substancji stałych lub ciekłych za pomocą odpowiednio dobranych rozpuszczalników. Proces ten nie powinien powodować zmian chemicznych ekstrahowanej substancji.
Rozpuszczalnik nie może reagować ani z substancją ekstrahowaną ani innymi znajdującymi się w mieszaninie. Należy dobierać taki rozpuszczalnik który rozpuszcza tylko żądany składnik a pozostałych nie rozpuszcza. Rozpuszczalnik powinien być czysty i po odparowaniu nie może pozostawić żadnych pozostałości.
Ekstrakcję przeprowadza się w temperaturze pokojowej lub w temperaturze wrzenia rozpuszczalnika. Na ogół stosuje się rozpuszczalnik o niskiej temperaturze wrzenia: eter etylowy, eter izopropylowy, eter naftowy, benzyna, chloroform itp. Ekstrakcja ma zastosowanie przede wszystkim do rozdzielania substancji organicznych. Do ekstrahowania substancji nieorganicznych jako rozpuszczalnika stosuje się najczęściej wode.
Metody ekstrakcji:
Ekstrakcja z roztworów
Nie jest procesem ciągłym i wykonuje się je w rozdzielaczach
Ekstrakcja z mieszaniny substancji stałych
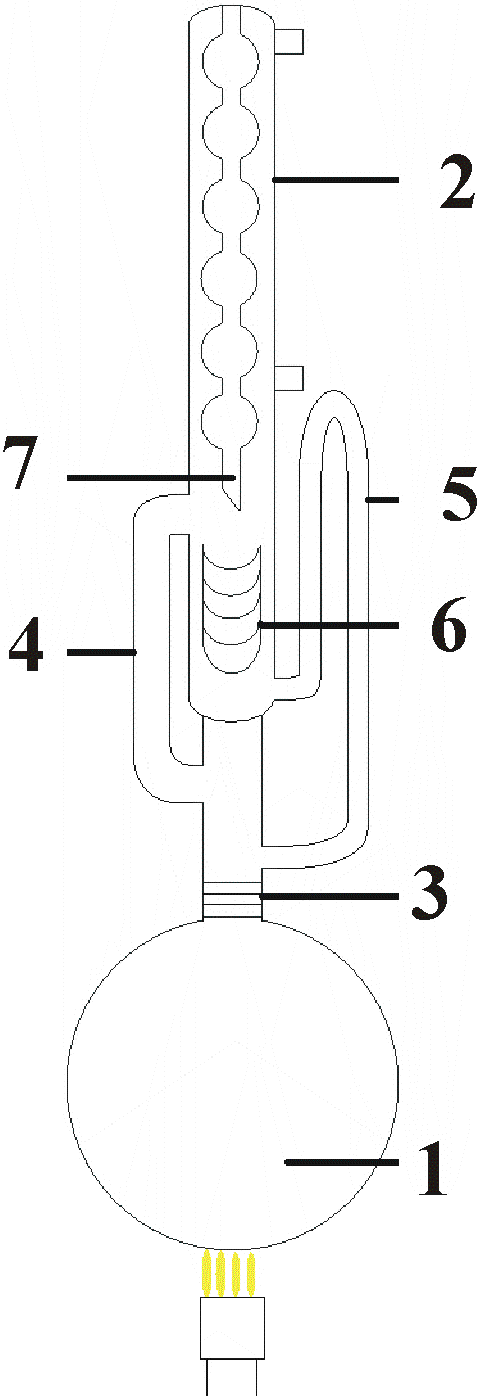
Jest to proces ciągły i wykonuje się go w specjalnym aparacie Soxhleta. Aparat Soxhleta składa się z kolby, ekstraktora i chłodnicy kulkowej. Części aparatu powinny być połączone za pomocą szlifów co zapewnia szczelność układów.
Środkowa część aparatu tzw. ekstraktor połączona jest szczelnie szklanymi rurkami z kolbą. Przez szerszą rurkę pary rozpuszczalnika przechodzą z kolby do ekstraktora, węższa służy do odprowadzania roztworu z ekstraktora powrotem do kolby. Substancje stałej nie miesza się bezpośrednio w ekstraktorze lecz w specjalnej gilzie wykonanej z porowatego materiału lub z grubej bibuły filtracyjnej.
Wadą ekstrahowania w aparacie Soxheta jest długotrwałe ogrzewanie substancji znajdującej się w kolbie.
Legenda do rysunku Aparatu Soxhleta:
1. Kolba z rozpuszczalnikiem; 2. Chłodnica kulkowa; 3. Połączenie na szlif; 4. Rurka szersza; 5. Rurka węższa; 6. Gilza; 7.Ekstraktor.
II. Sublimacja
Polega na ogrzewaniu substancji stałej i przeprowadzenie jej w stan gazowy a następnie przez oziębienie par ponownie w stan stały z pominięciem stanu ciekłego. Metodę tą stosuje się do oczyszczania oraz do wydobywania z mieszaniny substancji która przechodząc w gaz nie topi się np.: jod, naftalen, bezwodnik ftalowy.
Temperatura sublimacji musi być niższa od temperatury topnienia oraz od temperatury rozkładu danej substancji.
Stosując sublimacje do oczyszczania można osiągnąć duży stopień czystości. Poprzez sublimacje można też oddzielać od takich zanieczyszczeń od których jest trudno je rozdzielić np. przez krystalizacje.
Ze względu na to że niewiele substancji sublimuje metodę tą stosuje się rzadko.
III. Krystalizacja
Jest najczęstszy stosowany sposób oczyszczania substancji stałej.
Polega ono na wykorzystaniu różnej rozpuszczalności substancji i jej zanieczyszczeń w odpowiednio dobranym rozpuszczalniku.
Etapy przeprowadzania krystalizacji:
Substancje rozpuszcza się w gorącym rozpuszczalniku.
Otrzymany roztwór przesącza się na gorąco oddzielając w ten sposób substancje od nierozpuszczalnych zanieczyszczeń.
Otrzymany przesącz oziębia się pod zimną wodą, celem wykrystalizowania substancji z roztworu.
Otrzymane kryształki odsącza się i suszy.
Dobór rozpuszczalnika zależy od właściwości rozpuszczanej substancji. Powinien spełniać następujące warunki:
- Nie powinien reagować ze substancją.
- Powinien dobrze rozpuszczać na gorąco a źle na zimno
- Zanieczyszczenia powinny być praktycznie nierozpuszczalne
- Oczyszczana substancja powinna łatwo z niego krystalizować
- Powinien być łatwy do usuwania z powierzchni kryształów
IV. Destylacja
Jest to metoda rozdziału składników cieczy. Polega ona na przeprowadzeniu ich w stan pary poprzez ogrzanie do temperatury wrzenia, a następnie na oziębieniu, skropleniu i zebraniu w postaci destylatów.
W laboratoriach analitycznych destylacja stosowana jest do:
- rozdzielania mieszanin ciekłych
- oznaczania składu mieszanin ciekłych
- identyfikacja ciekłych substancji organicznych
- oczyszczanie cieczy
- określenia stopnia oczyszczenia związków chemicznych
Rozdzielenie mieszaniny jest tym łatwiejsze im większa jest różnica temperatur wrzenia jej składników. Temperatura wrzenia pod określonym ciśnieniem (760ml Hg) jest wielkością stałą dla danego związku chemicznego.
Metody destylacji:
1) Destylacja zwykła
Przeprowadza się wówczas gdy cieczy nie grozi rozkład w temperaturze wrzenia i gdy temperatura ta nie jest zbyt wysoka. Aparat do destylacji tej składa się z: kolby destylacyjnej, chłodnicy, odbieralnika, termometru i źródła ciepła. Aby zapobiec przegrzaniu cieczy do kolby dodaje się nieco potłuczonej porcelanki tzw.szamotki.
2) Destylacja frakcyjna
Polega na zbieraniu poszczególnych frakcji do oddzielnych odbiorników. Każda frakcja ma inną temperaturę wrzenia. Konieczna jest ciągła kontrola temperatury (np. destylacja frakcyjna ropy naftowej).
3) Destylacja próżniowa
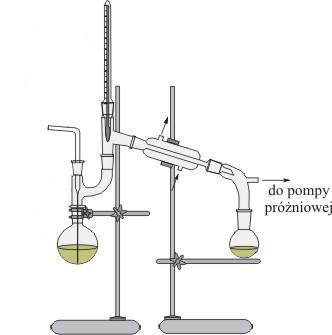
Stosowana jest do rozdzielania cieczy które są nietrwałe w wyższych temperaturach. W takich przypadkach stosuje się rozrzedzenie par w temperaturze. Stosując rozrzedzenie par w destylacji do wartości ok. 10-20 mm Hg uzyskuje się obniżenie temperatury wrzenia o 80-100ºC. Rozrzedzenie tego rzędu stosuje się przy użyciu pompki wodnej. Chcąc uzyskać większe rozrzedzenie stosuje się specjalne pompki olejowe.
Warunkiem przeprowadzenia tego typu destylacji jest szczelność aparatury. W porównaniu do poprzedniej metody zestaw destylacyjny należy zwiększyć o manometr, kolbę próżniową i pompkę wodną.
4) Destylacja z parą wodną
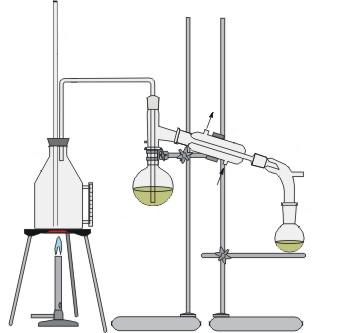
Stosowana jest do wydzielania z mieszaniny ciekłej składników nie mieszających się z wodą. Warunkiem jest jednak aby składnik ten był lotny z parą wodną. Zestaw aparatury należy uzupełnić w kociołek do wytwarzania pary wodnej
Ćwiczenie 1
Sublimacja naftalenu.
Około 0,5 g naftalenu wsypać do czystej zlewki, przykryć ją szczelnie parowniczką z zimną wodą. Zlewkę ogrzewać mikropalniczkiem i opisać obserwowane zjawisko.
Obserwacje: Na ściankach zlewki osadzają się maleńkie kryształki. Na spodzie parowniczki osadziły się opiłkowate kryształki które stworzyły „choineczki”
Ćwiczenie 2
Ekstrakcja jodu z płynu Lugola.
Przygotować sprzęt i odczynniki: rozdzielacz, zlewkę, chloroform, płyn Jugola (I w KI).
Wykonanie:
Do rozdzielacza wlać 5 cm³ płynu Jugola (I w KI) i 5 cm³ chloroformu. Zawartość rozdzielacza wstrząsnąć przez chwile po czym odstawić celem rozdzielenia faz. Dolną warstwę zlać do zlewki ( warstwa chloroformu z I (jodem)). Czynność powtarzać celem całkowitego wyekstrahowania I z KI.
Kolory substancji:
KI - jest bezbarwny
płyn Jugola - brunatny
I - fioletowe kryształki
Ćwiczenie 3
Destylacja roztworu ![]()
1) Zamontuj zestaw do destylacji zwykłej.
2) Do kolby dodaj roztwór ![]()
i dodaj szamotki (potłuczonej porcelanki)
3) Kolbe ogrzewaj , prowadź proces destylacji i zbierz w odbieralniku 20 ml wody destylowanej.
4
Wyszukiwarka
Podobne podstrony:
Podstawowe pojęcia i prawa chemiczne, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
Podstawowe czynności laboratoryjne, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
AJ Identyfikacja kationów III grupy, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
ChO w Rodzaje izomerii, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
Podział stanowisk pracy – mycie i znakowanie szkła, ~FARMACJA, I rok, chemia (ciul wie co), Semestr
AJ Wykrywanie anionów I-VI grupy – analiza kontrolna, ~FARMACJA, I rok, chemia (ciul wie co), Semest
R.Rodzaje stężeń roztworów, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
Reakcje Redox cd, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
AJ Wykrywanie soli - analiza kontrolna, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
Alkohole i fenole, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
R.Mieszanie i rozcieńczanie roztworów procentowych, ~FARMACJA, I rok, chemia (ciul wie co), Semestr
Węglowodory, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
R.Sporządzanie roztworów molowych, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
Budowa oraz obsługa wag technicznych i analitycznych, ~FARMACJA, I rok, chemia (ciul wie co), Semest
Rodzaj wiązań, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
Klasyfikacja związków nieorganicznych, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
Reakcje Redox, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
Podstawowy sprzęt laboratoryjny, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
AJ Podział anionów na grupy analityczne. Reakcje I i i II gr, ~FARMACJA, I rok, chemia (ciul wie co)
więcej podobnych podstron