PK WIiTCh GR . 24 Zespół nr 8
|
Ćwiczenie: 3 |
Data : 22.03.2001
|
1. Janusz Budzowski 2. Łukasz Krężel |
Temat: Wyznaczanie ciepła parowania cieczy z pomiarów prężności pary metodą izoteniskopową. |
Ocena: |
Część teoretyczna.
Temperatura wrzenia jest to temperatura, w której prężność pary nad roztworem równa jest ciśnieniu zewnętrznemu.
Pomiaru prężności pary dokonuje się zazwyczaj dwoma metodami:
a) dynamiczną, w której ustala się w aparaturze określone ciśnienie pary nasyconej, a następnie mierzy się temperaturę wrzenia pod tym ciśnieniem;
b) statyczną, w której przy ustalonej temperaturze mierzymy prężność pary nasyconej. Pomiaru dokonujemy dla różnych temperatur. Metodę tą nazywamy też izoteniskopową.
Rys. Schemat aparatury próżniowej do izoteniskopowego pomiaru prężności pary cieczy:
A - manometr rtęciowy, B - zbiornik buforowy, C - izoteniskop, D - naczynko termostatowe,
E - rurka kapilarna, F - mały zbiornik buforowy, G - chłodnica
Opis wykonania ćwiczenia:
Do zbiorniczka K i manometru M izoteniskopu nalewamy toluenu, tak aby jego poziom był w przyblizeniu taki jak na powyższym rysunku. Zanurzamy izoteniskop w naczynku termostatowym, włączamy obieg wody chłodzącej i ustalamy pierwszą temperaturę pomiarową. Przy zamkniętych kranach 1 i 3 oraz otwartym kranie 2 włączamy pompę, a nastepnie wolno otwieramy kran 1, tak aby słup rtęci w manometrze rtęciowym opadał z nieznaczą szybkością. Przy pewnym ciśnieniu przez toluen w manometrze M izoteniskopu zaczną przedostawać się banieczki powietrza znad poziomu toluenu do zbiorniczka K. Przez regulację kranu 1 można szybkość przedostawania się banieczek ustalić na nieznacznym poziomie. Proces odpowietrzania prowadzimy około 5 minut. Po odpowietrzeniu zbiorniczka K odcinamy próżnię przez zakręcenie kranu 1, wpuszczamy do aparatury niewielką ilość powietrza przez chwilowe otwarcie kranu 3, co spowoduje zmniejszenie „rzucania” toluenu w manometrze M. Kolejne otwarcia kranu 3 doprowadzają do wyrównania się poziomów toluenu w manometrze M. Oznacza to, że cisnienie pary nasyconej nad toluenem w zbiorniczku K jest równe ciśnieniu powietrza w aparaturze. To ostatnie odczytujemy na manometrze rtęciowym, jako różnicę poziomów rtęci w milimetrach. Analogicznie postepujemy przy kolejnych temperaturach. Jeżeli jednak w trakcie wyrównywania poziomów toluenu w manometrze M pęcherzyk powietrza przedostanie się do zbiorniczka K, pomiar rozpoczyna się od początku.
Część obliczeniowa.
W ćwiczeniu wyznaczamy ciepło parowania toluenu:
- masa molowa M=92.14 g/mol
- temperatura wrzenia Twrz=110.62 *C
- gęstość d=0.866÷0.867 g/cm3
- entalpia parowania w temp. wrzenia ΔHwrz=43.47 kJ/mol
Pomiaru dokonaliśmy dla 4 różnych temperatur:
Lp |
T[K] 314 |
T[K] 324 |
T[K] 336 |
T[K] 344 |
|
p [mmHg] |
p [mmHg] |
p [mmHg] |
p [mmHg] |
1 |
62 |
65 |
119 |
210 |
2 |
62 |
65 |
118 |
170 |
3 |
69 |
- |
- |
165 |
4 |
pśred = 62 |
pśred = 65 |
pśred = 118,5 |
pśred = 167,5 |
Ciśnienia pisane kursywą są obarczone zbyt dużym błędem i nie biorę ich do obliczeń.
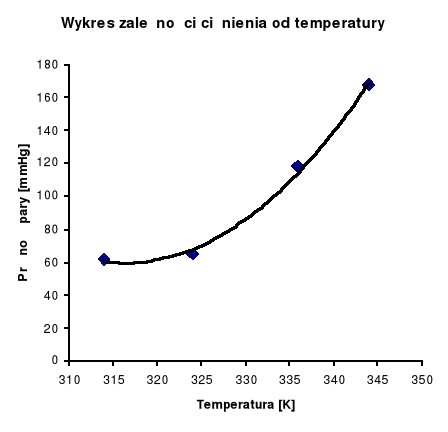
Obliczenia na podstawie równania Clausiusa-Clapeyrona:
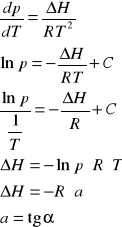
a-kąt nachylenia prostej
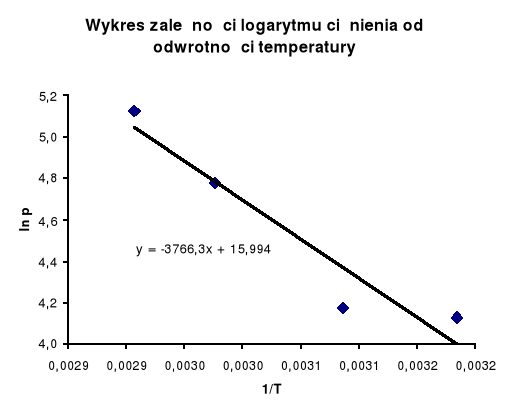
Z regresji liniowej powyższego wykresu odczytujemy kąt nachylenia prostej, którego tangens jest równy współczynnikowi kierunkowemu prostej wykresu.
a = -3766,3
DH = -8,314 * (-3766,3)
DH = 31,313 kJ/mol
Wnioski
Wartość tablicowa ΔH toluenu wynosi 33.32kJ/mol, nasza wyznaczona 31.313kJ/mol, daje to w rezultacie błąd rzędu 6%.Na błąd złożyć się mogło kilka powodów (niedokładnie odczytywana: temperatura, różnica poziomów rtęci w U-rurce, niezbyt dobrze oczyszczony po innej substancji izoteniskop, a także przedostanie się pęcherzyków powietrza do zbiorniczka z toluenem).
Wyszukiwarka