65 3
Odpowiedz
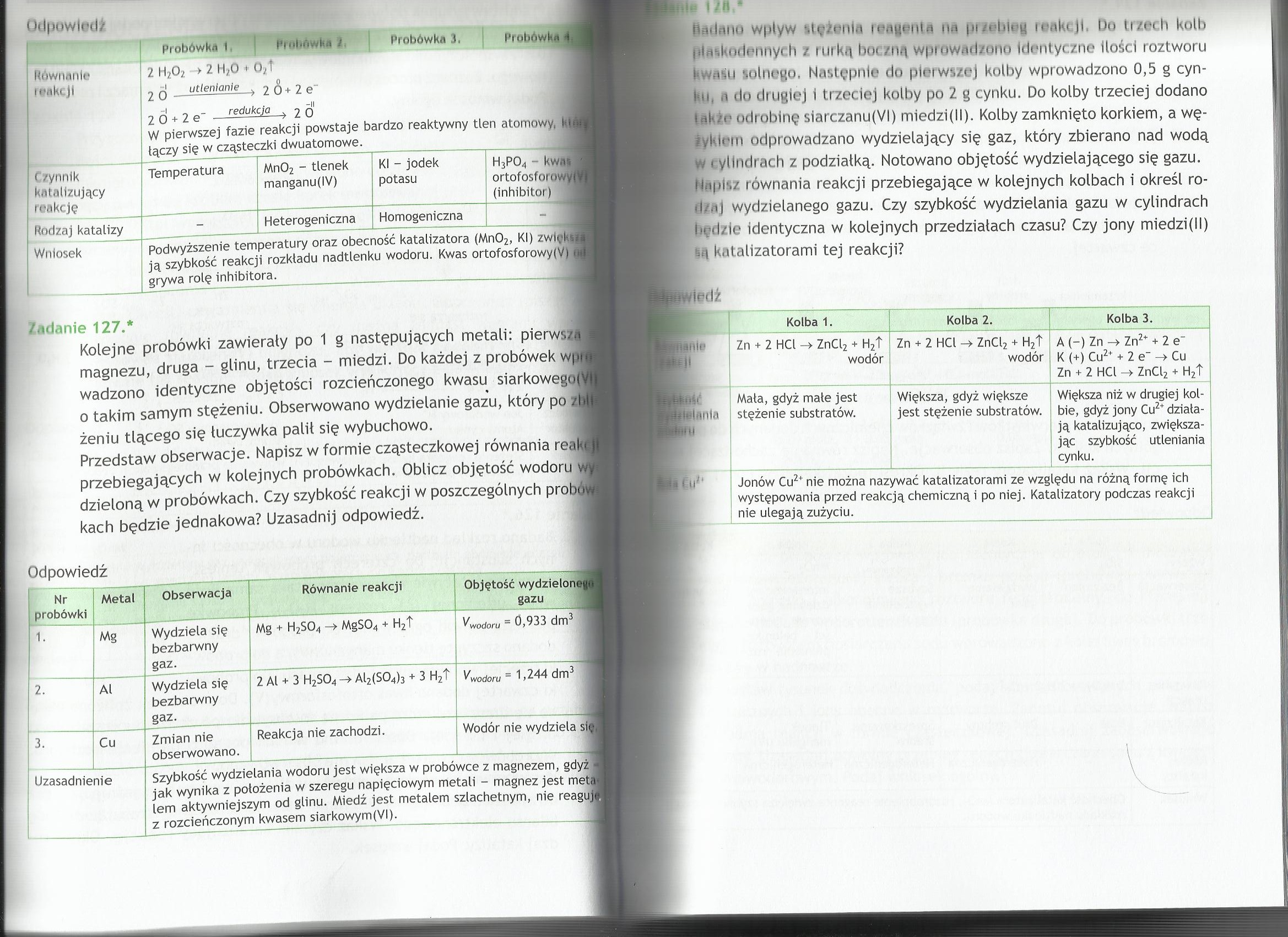
Równanie
i pakt jl
Probówka 3,
Pinbńwka
W pierwszej fazie reakcji powstaje bardzo reaktywny tlen atomowy,
|
Czynnik katalizujący rwkcję |
Temperatura |
Mn02 - tlenek manganu(IV) |
KI - jodek potasu |
H3P04 kwas ortofosfomwy (inhibitor) |
|
Rodzaj katalizy |
- |
Heterogeniczna |
Homogeniczna |
- ] |
|
- Wniosek |
Podwyższenie temperatury oraz obecność katalizatora (Mn02, KI) zwfUs | |||
ją szybkość reakcji rozkładu nadtlenku wodoru. Kwas ortofosforowy^) grywa rolę inhibitora.
'adanie 127.*
Kolejne probówki zawierały po 1 g następujących metali: pierws/j| magnezu, druga - glinu, trzecia - miedzi. Do każdej z probówek vv| wadzono identyczne objętości rozcieńczonego kwasu siarkowego^ o takim samym stężeniu. Obserwowano wydzielanie gazu, który po Ą żeniu tlącego się łuczywka palił się wybuchowo.
Przedstaw obserwacje. Napisz w formie cząsteczkowej równania reakj przebiegających w kolejnych probówkach. Oblicz objętość wodoru w dzieloną w probówkach. Czy szybkość reakcji w poszczególnych probóy kach będzie jednakowa? Uzasadnij odpowiedź.
Odpowiedź
|
Nr probówki |
Metal |
Obserwacja |
Równanie reakcji |
Objętość wydzielonej gazu |
|
1. |
Mg |
Wydziela się bezbarwny gaz. |
Mg + H2S04 MgS04 + H2t |
Vwodoru = 0,933 dm3 |
|
2. |
Al |
Wydziela się bezbarwny gaz. |
2 Al + 3 H2S04 Al2(S04)3 + 3 H2t |
^wodoru ~ 1,244 dm3 |
|
3. |
Cu |
Zmian nie obserwowano. |
Reakcja nie zachodzi. |
Wodór nie wydziela sii, |
|
Uzasadnienie |
Szybkość wydzielania wodoru jest większa w probówce z magnezem, gdyż jak wynika z położenia w szeregu napięciowym metali - magnez jest meta lem aktywniejszym od glinu. Miedź jest metalem szlachetnym, nie reaguj z rozcieńczonym kwasem siarkowym(VI). | |||
latu» wpływ nla ir.nyphU l f©8kej!. Do tf/ftch kólb
pin\\-oiItMinyi h / rurką hm /ną wpiow.irj/ona identyczne Ilości roztworu i • mi solnego. Następnie do plerws/ej kolby wprowadzono 0,5 § cynii!. a do drugiej i trzeciej kolby po 2 g cynku. Do kolby trzeciej dodano takie odrobinę siarczanu(VI) miedzi(ll). Kolby zamknięto korkiem, a wę-Md«-m odprowadzano wydzielający się gaz, który zbierano nad wodą w - yl mdi ach z podziałką. Notowano objętość wydzielającego się gazu. Napis/ równania reakcji przebiegające w kolejnych kolbach i określ ro-d-aj wydzielanego gazu. Czy szybkość wydzielania gazu w cylindrach bed/ie identyczna w kolejnych przedziałach czasu? Czy jony miedzi(II) katalizatorami tej reakcji?
vi«dż
Kolba 1.
Kolba 2.
Kolba 3.
wodór
Zn + 2 HCl-> ZnCl2 + H2T A (-) Zn -wodór K (+) Cu2+
Zn + 2 HCl -» ZnCl2 + H2T
A (-) Zn -> Zn2+ + 2e'
K (+) Cu2+ + 2 e" -> Cu Zn + 2 HCl -> ZnCl2 + H2t

Mata, gdyż matę jest Większa, gdyż większe Większa niż w drugiej kol-
stężenie substratów. jest stężenie substratów, bie, gdyż jony Cu2+ działa-
ją katalizująco, zwiększając szybkość utleniania cynku.
Jonów Cu2+ nie można nazywać katalizatorami ze względu na różną formę ich występowania przed reakcją chemiczną i po niej. Katalizatory podczas reakcji nie ulegają zużyciu.

Wyszukiwarka
Podobne podstrony:
141 2 Odpowiedź Równanie reakcji Al4C3 + 12Hft W^ ą AlCt, * i CH4T (metan) Sposób zbierania gazu P
06 (ODPOWIEDZI) 52 3. Równania, nierówności i ich układy 43. Największą liczbą spełniającą równanie
SNV32559 Dokonaj: - analizy zadania (schemat, bilans ?), • napisz odpowiednie równ
• komputerów i cyfrowych nośników danych (65 odpowiedzi) • broni
—^(mirł) = p/ + L su dl j=iM. Równanie) wektorowe (a) odpowiadaj 3 równaniom
56 (58) ISTQB Advanced Level - Test Manager sample exam - version 2012Pytanie 56 z 65 &n
57 (60) ISTQB Adwanced Level - Test Manager sample exam - wersion 2012Pytanie 57 z 65 &n
58 (53) ISTQB Aduanced Leuel - Test Manager sample exam - version 2012 Pytanie 58 z 65 Odpowiedź:
59 (51) ISTQB Advanced Level - Test Manager sample exam - version 2012Pytanie 59 z 65 &n
5 (704) ISTQB Advanced Level - Test Manager sample exam - wersion 2012Pytanie 5 z 65 &nb
61 (49) ISTQB Aduanced Leuel - Test Manager sample exam - version 2012 Pytanie 61 z 65 Odpowiedź:
63 (48) ISTQB Advanced Level - Test Manager sample exam - version 2012Pytanie 63 z 65 &n
65 (45) ISTQB Aduanced Leuel - Test Manager sample exam - uersion 2012Pytanie 65 z 65 &n
6 (636) ISTQB Advanced Level - Test Manager sample exam - version 2012Pytanie 6 z 65 &nb
CCF20120509�060 244 Część II. Rozwiązania i odpowiedzi b. Równania różniczkowe torów poruszania się
27 (191) ISTQB Adwanced Level - Test Manager sample exam - wersion 2012Pytanie 27 z 65 &
więcej podobnych podstron