
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego
Wyznaczanie entalpii parowania wody na podstawie pomiaru temperaturowego
współczynnika prężności pary
ćwiczenie nr 33
o
p
r
a
c
o
w
a
ł
a
d
r
J
.
W
o
ź
n
i
c
k
a
Zakres zagadnień obowiązujących do ćwiczenia
1. Druga zasada termodynamiki.
2. Równanie Clausiusa
−
Clapeyrona. Wyprowadzenie i interpretacja.
3. Równowaga: ciecz
−
para.
4. Budowa, działanie i zastosowanie ebuliometru oraz termometru Beckmanna.
Literatura
1. Praca zbiorowa pod red. Woźnickiej J. i Piekarskiego H.,
Ć
w
i
c
z
e
n
i
a
l
a
b
o
r
a
t
o
r
y
j
n
e
z
c
h
e
m
i
i
f
i
z
y
c
z
n
e
j
, Wydawnictwo UŁ, Łódź 2005.
2. Sobczyk L., Kisza A., Gatner K., Koll A.,
E
k
s
p
e
r
y
m
e
n
t
a
l
n
a
c
h
e
m
i
a
f
i
z
y
c
z
n
a
, PWN,
Warszawa 1982.
3. Brdička R.,
P
o
d
s
t
a
w
y
c
h
e
m
i
i
f
i
z
y
c
z
n
e
j
, PWN, Warszawa 1970.
4. Praca zbiorowa pod red. Basińskiego A.,
C
h
e
m
i
a
f
i
z
y
c
z
n
a
,
PWN, Warszawa 1980.
5. Sobczyk L., Kisza A.,
C
h
e
m
i
a
f
i
z
y
c
z
n
a
d
l
a
p
r
z
y
r
o
d
n
i
k
ó
w
, PWN, Warszawa 1977.
6. Szarawara J.,
T
e
r
m
o
d
y
n
a
m
i
k
a
c
h
e
m
i
c
z
n
a
, WNT, Warszawa 1985.
7. Atkins P. W.,
C
h
e
m
i
a
f
i
z
y
c
z
n
a
, Wydawnictwo Naukowe PWN, Warszawa 2001.
8. Buchowski H., Ufnalski W.,
G
a
z
y
,
c
i
e
c
z
e
,
p
ł
y
n
y
,
WNT, Warszawa 1994.
2
Celem ćwiczenia jest wyznaczenie molowej entalpii i entropii parowania wody na
podstawie pomiaru temperaturowego współczynnika prężności pary.
Układ pomiarowy
W omawianym ćwiczeniu, pomiaru prężności pary nasyconej dokonuje się
metodą dynamiczno – recyrkulacyjną
.
W metodzie tej, po ustaleniu się określonego
ciśnienia pary nasyconej, mierzy się temperaturę, przy której współistnieją pod danym
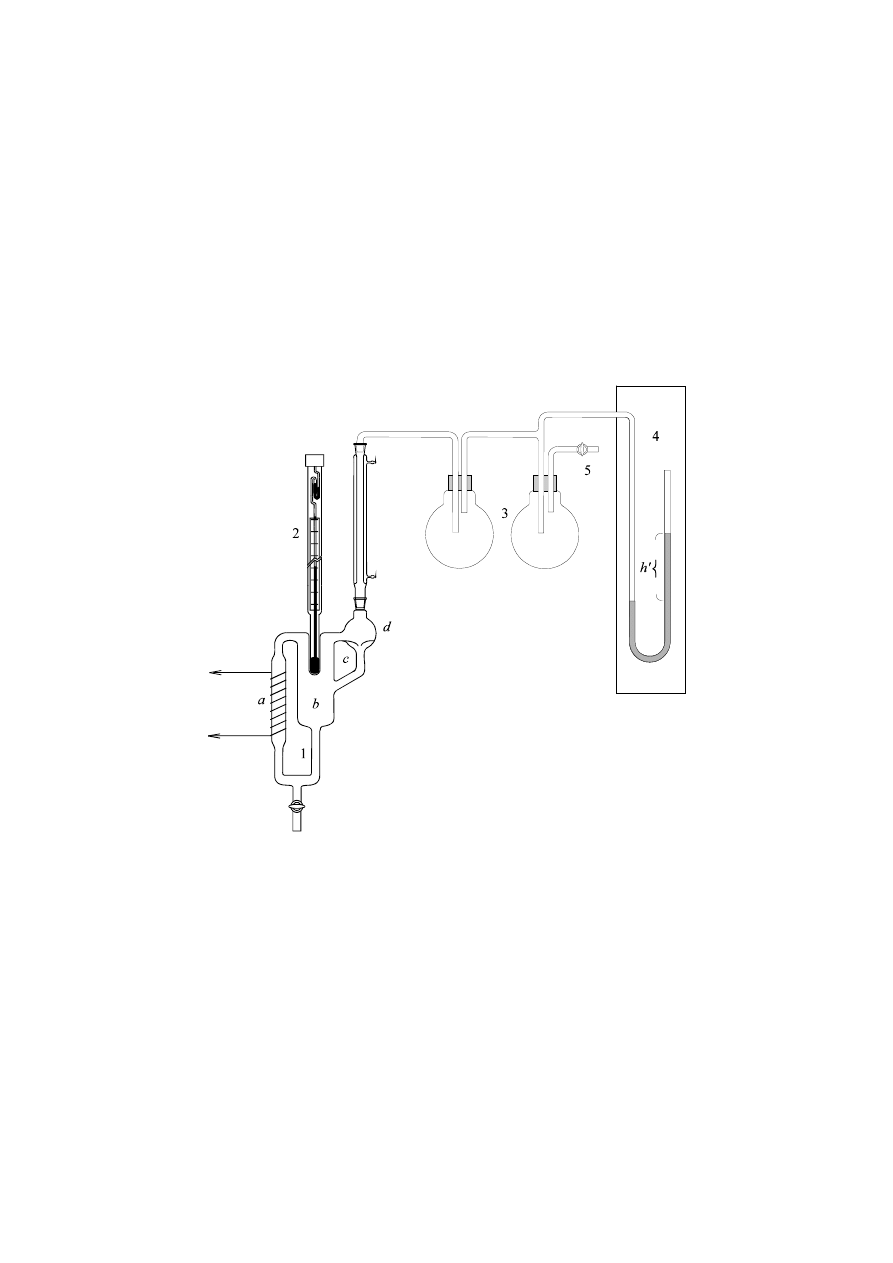
ciśnieniem fazy ciekła i gazowa (Rys. 1).
Rys. 1. Układ do pomiaru temperaturowego współczynnika prężności pary
Aparatura do pomiaru temperaturowego współczynnika prężności pary składa się
z ebuliometru (1) zaopatrzonego w różnicowy termometr Beckmanna (2) i połączonego
ze zbiornikiem powietrza (3). Zbiornik powietrza zmniejsza wahania ciśnienia
pochodzące od nierównomiernego wrzenia cieczy w ebuliometrze w czasie pomiaru.
Cała aparatura jest szczelna i może być w niej utrzymywane dowolne ciśnienie, którego
wartość w milimetrach słupa wody odczytuje się na manometrze (4). Nadciśnienie
(rozumiane jako ciśnienie wyższe od ciśnienia atmosferycznego) oraz podciśnienie
(ciśnienie niższe od atmosferycznego), uzyskuje się w układzie wdmuchując lub wycią-

3
gając powietrze ze zbiornika przy pomocy gruszki przez kran (5). Stan równowagi
termodynamicznej ciecz
−
para można zrealizować w ebuliometrze Świętosławskiego
(1). Konieczność konstrukcji tego typu aparatów wynika stąd, że miernika temperatury
−
termometru Beckmanna (2), nie można zanurzyć ani do wrzącej cieczy, ani umieścić
w fazie gazowej. Gniazdo termometryczne powinno być opłukiwane strumieniem cieczy
i pary, pozostających w stanie równowagi termodynamicznej. W ebuliometrze, szklany
pojemnik
a
owinięty jest drutem oporowym w celu doprowadzenia cieczy do wrzenia.
Tworząca się para i porywana przez nią wrząca ciecz są wyrzucane na ścianki gniazda
termometrycznego
b
wypełnionego rtęcią. Ciecz spływa z powrotem przez rurkę
c
do
zbiorniczka
a
.
Pewne ilości pary przedostają się do chłodnicy, gdzie ulegają skropleniu.
Skroplona ciecz spływa boczną rurką przez tzw. kroplomierz
d
, dający możliwość
obserwacji szybkości wrzenia cieczy. Jeżeli wrzenie cieczy odbywa się zbyt gwałtow-
nie, to wskazania termometru są zawyżone. Zbyt słabe ogrzewanie cieczy prowadzi do
zaniżonych wskazań temperatury. Intensywność grzania powinna być dostosowana do
typu ebuliometru oraz rodzaju cieczy. W przypadku ebuliometru używanego w naszym
laboratorium, z kroplomierza powinno spływać około 10 kropel wody w ciągu minuty.
Jak wcześniej wspomniano, do pomiaru temperatury wrzenia stosuje się różnico-
wy termometr Beckmanna (Rys. 2), przeznaczony do dokładnych pomiarów niewielkich
zmian temperatury. Skala termometru obejmująca tylko 5 stopni
(deg) daje możliwość
odczytu temperatury z dużą dokładnością:
±
0,01 stopnia, zaś przy użyciu lupy
±
0,002
stopnia. Punkt na skali, w którym zatrzymuje się rtęć w termometrze Beckmanna nie
wskazuje temperatury ani w stopniach Celcjusza ani Kelwina. Jest to punkt względny,
w odniesieniu, do którego możemy mierzyć jedynie zmiany temperatury układu.
W
y
z
n
a
c
z
o
n
e
p
r
z
y
u
ż
y
c
i
u
t
e
r
m
o
m
e
t
r
u
B
e
c
k
m
a
n
n
a
r
ó
ż
n
i
c
e
t
e
m
p
e
r
a
t
u
r
y
w
s
t
o
p
n
i
a
c
h
(
d
e
g
)
s
ą
r
ó
w
n
e
w
a
r
t
o
ś
c
i
o
m
r
ó
ż
n
i
c
t
e
m
p
e
r
a
t
u
r
y
w
y
r
a
ż
o
n
y
m
w
o
C
l
u
b
w
K
.
Termometru Beck-
manna można używać do badań w różnym zakresie temperatury dzięki temu, że jest on
zaopatrzony w dwa zbiorniki rtęci: górny i dolny, połączone wyskalowaną rurką
kapilarną. W zależności od interesującego nas zakresu pewną ilość rtęci można
przelewać ze zbiorniczka górnego do dolnego lub odwrotnie. Czynność tę nazywa się
nastawianiem termometru.

4
Odczynniki chemiczne i sprzęt laboratoryjny:
woda podwójnie destylowana,
lupa, gruszka gumowa.
Wykonanie ćwiczenia i przedstawienie wyników pomiarów
N
a
p
i
ę
c
i
e
n
a
a
u
t
o
t
r
a
n
s
f
o
r
m
a
t
o
r
z
e
u
s
t
a
l
a
p
r
o
w
a
d
z
ą
c
y
z
a
j
ę
c
i
a
.
N
i
e
n
a
l
e
ż
y
o
p
r
ó
ż
n
i
a
ć
e
b
u
l
i
o
m
e
t
r
u
.
W
o
d
a
p
o
d
w
ó
j
n
i
e
d
e
s
t
y
l
o
w
a
n
a
,
k
t
ó
r
ą
j
e
s
t
n
a
p
e
ł
n
i
o
n
y
e
b
u
l
i
o
m
e
t
r
n
i
e
m
u
s
i
b
y
ć
w
y
m
i
e
n
i
a
n
a
p
r
z
e
d
w
y
k
o
n
a
n
i
e
m
k
a
ż
d
e
g
o
d
o
ś
w
i
a
d
c
z
e
n
i
a
.
E
b
u
l
i
o
m
e
t
r
ł
a
t
w
o
u
l
e
g
a
u
s
z
k
o
d
z
e
n
i
u
,
a
j
e
g
o
n
a
p
r
a
w
a
j
e
s
t
t
r
u
d
n
a
i
k
o
s
z
t
o
w
n
a
.
1. Badaną ciecz
−
wodę doprowadzić w ebuliometrze do wrzenia pod ciśnieniem
atmosferycznym
b
.
Kran jest wówczas otwarty.
2. Po ustaleniu się procesu wrzenia, przy pomocy lupy na termometrze Beckmanna,
odczytać wartość temperatury wrzenia wody
τ
b
pod ciśnieniem
b
.
W rzeczywistości,
jest to punkt wrzenia odczytany w stopniach (deg), któremu w dalszej części
opracowania ćwiczenia przypisze się wartość temperatury w skali bezwzględnej
T
b
.
3. Na barometrze umieszczonym w laboratorium odczytać ciśnienie atmosferyczne
b
[Pa] odpowiadające temperaturze
τ
b
.
4. Poprzez wdmuchiwanie lub wyciąganie powietrza przy pomocy gruszki gumowej,
zmieniać co 10 mm wartość ciśnienia panującego w układzie i po ustaleniu się stanu
równowagi, dokonać odczytu wysokości słupa wody
h
'
z dokładnością
±
0,5 mm
H
2
O oraz odpowiadającej mu temperatury
τ
(punktu wrzenia). Wartość
h
'
określona
jest różnicą poziomów cieczy manometrycznej (wody). Dokonać co najmniej 10
pomiarów
h
'
oraz
τ
dla nadciśnienia i podciśnienia.
Opracowanie i dyskusja wyników pomiarów
1. Wartości
h
'
odczytane na manometrze w mm H
2
O, przeliczyć na mm Hg,
a następnie na Pa pamiętając, że:
ρ
H2O H2O
h
=
ρ
Hg
Hg
h
;
h
H2O
,
h
Hg
−
wysokości słupa wody i rtęci, gęstości obu cieczy:
ρ
H2O
= 1
⋅
10
3
kg m
-3
;
ρ
Hg
= 13,6
⋅
10
3
kg m
-3
, 760 mm Hg = 1 atm = 1,013
⋅
10
5
Pa.
2. Obliczone wartości
p
'
[Pa]
d
l
a
n
a
d
c
i
ś
n
i
e
n
i
a
d
o
d
a
j
e
s
i
ę
do ciśnienia barometrycz-
nego
b
i uzyskuje się
p
=
b
+
p
'
.
D
l
a
p
o
d
c
i
ś
n
i
e
n
i
a
o
d
e
j
m
u
j
e
s
i
ę
p
'
od
b
:
p
=
b
–
p
'
.
5
Otrzymuje się w ten sposób wartości prężności pary
p
w funkcji temperatury
τ
w odniesieniu do wszystkich punktów eksperymentalnych.
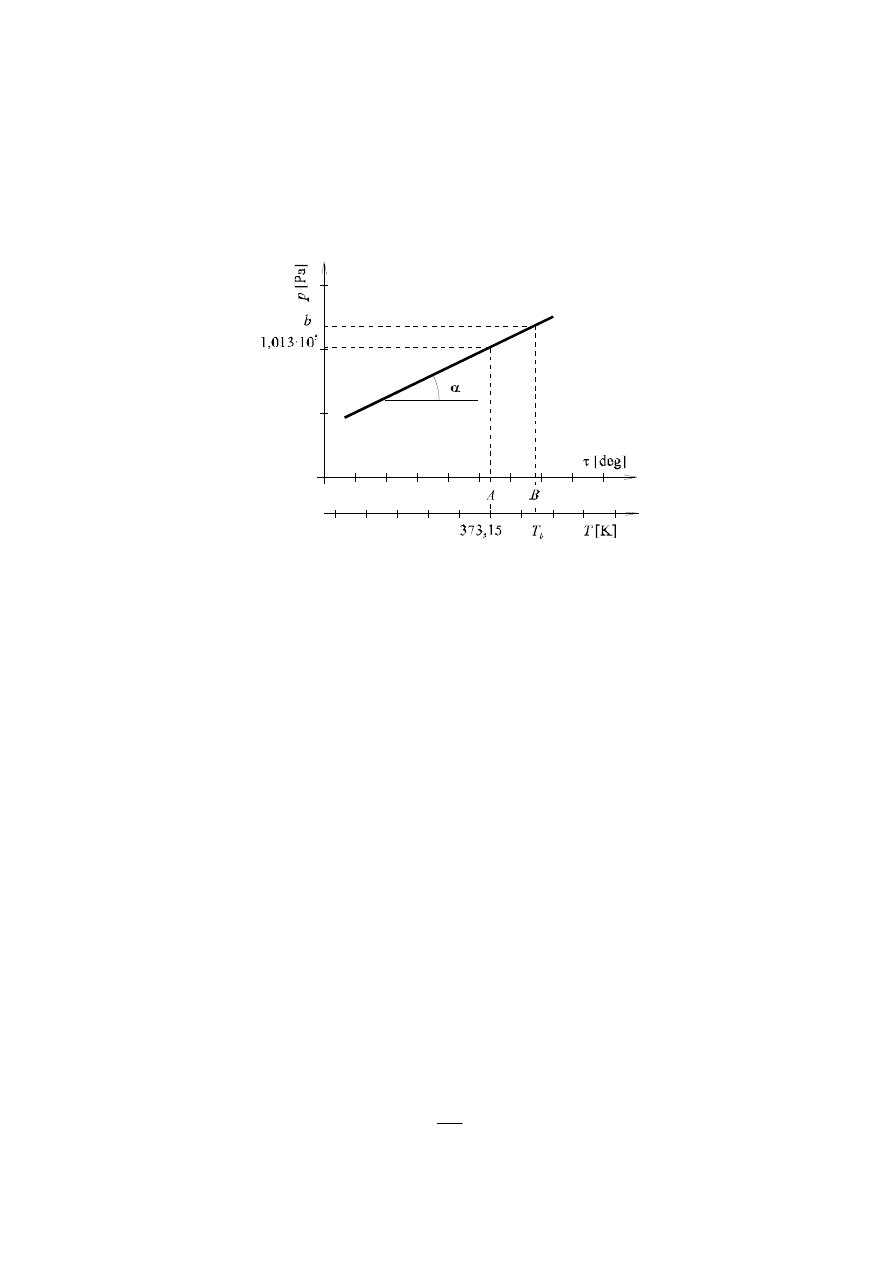
3. Na papierze milimetrowym sporządzić wykres zależności
p
=
f
(
τ
) wg rysunku 2.
Proponuje się przyjąć skale: 1 cm
→
0,05 deg; 4 cm
→
1000
Pa.
Rys. 2. Doświadczalnie uzyskana zależność prężności pary od temperatury
4. Z uwagi na to, że do obliczenia
∆
H
p
a
r
z równania Clausiusa
−
Clapeyrona niezbędna
jest wartość temperatury wrzenia wody
T
b
w warunkach ciśnienia barometrycznego
b
, należy każdej wartości
τ
przyporządkować bezwzględną wartość temperatury
T
w skali Kelwina. W tym celu należy:
– na dodatkowo wykreślonej osi
T
, równoległej do osi
τ
(Rys. 2), zaznaczyć
temperaturę wrzenia wody
T
n
t
w
= 373,15 K odpowiadającą ciśnieniu normalnemu
1,013
⋅
10
5
Pa (punkt A na rysunku).
– znając położenie punktu A, opisać oś temperatury
T
zachowując tę samą skalę co
w przypadku
τ
, czyli: 1 cm
→
0,05 K. Wartości
T
(odczytane z dokładnością
±
0,05 K) i odpowiadające poszczególnym punktom
τ
,
zamieścić w tabeli wyników.
5. Posługując się wykresem
p
=
f
(
T
) odczytać temperaturę wrzenia wody
T
b
(punkt B
na rysunku 2), odpowiadającą ciśnieniu atmosferycznemu
b
w danych warunkach
eksperymentalnych. Uzyskaną wartość
T
b
należy podstawić do równania Clausiusa
−
Clapeyrona w dalszej części opracowywania wyników doświadczenia.
6. Korzystając z wykresu
p
=
f
(
T
), obliczyć metodą graficzną wartość temperaturo-
wego współczynnika prężności pary
d
d
g
r
a
f
p
T
. W badanym zakresie ciśnienia oraz
6
temperatury:
d
d
p
T
=
∆
∆τ
p
=
∆
∆
p
T
=
tg
α
.
.
Współczynnik ten należy obliczyć również
metodą najmniejszych kwadratów
d
d
p
T
n
u
m
.
Do obliczeń należy stosować tę
ostatnią wartość.
7. Wiedząc, że molowe objętości wody w stanie pary
β
i cieczy
α
wynoszą:
V
m
β
= 30, 062
⋅
10
-3
m
3
mol
-1
;
V
m
α
= 0, 019
⋅
10
-3
m
3
mol
-1
obliczyć zmianę objętości molowej wody w procesie parowania
∆
V
m
=
V
m
β
−
V
m
α
.
8. Obliczyć molową entalpię parowania
∆
H
p
a
r
z równania Clausiusa
−
Clapeyrona:
∆
H
p
a
r
=
d
d
p
T
T
b
∆
V
m
9. Obliczyć molową entropię parowania wody w warunkach doświadczenia:
∆
S
p
a
r
=
p
a
r
b
H
T
∆
i porównać z wartością
∆
S
p
a
r
wynikającą z reguły Troutona.
10. Przeprowadzić dyskusję uzyskanych wyników doświadczalnych. Do sprawozdania
dołączyć czytelny wykres wykonany na papierze milimetrowym.
Tabele wyników pomiarów i obliczeń
N
a
d
c
i
ś
n
i
e
n
i
e
nr pomiaru
h
'
[mm H
2
O]
P
'
[Pa]
p
=
b
+
p
'
[Pa]
τ
[deg]
T
[K]
1.
.
10.
P
o
d
c
i
ś
n
i
e
n
i
e
nr pomiaru
h
'
[mm H
2
O]
P
'
[Pa]
p
=
b
−
p
'
[Pa]
τ
[deg]
T
[K]
1.
.
10.
b
[Pa]
τ
b
[deg]
T
b
[K]
∆
V
m
[m
3
mol
-1
]
d
d
p
T
g
r
a
f
[Pa K
-1
]
d
d
p
T
n
u
m
[Pa K
-1
]
∆
H
p
a
r
[J mol
-1
]
∆
S
p
a
r
[J mol
-1
K
-1
]
Wyszukiwarka
Podobne podstrony:
26 33 id 31365 Nieznany (2)
laoboratorium skory 33 id 26334 Nieznany
3 33 id 32911 Nieznany (2)
33 id 35668 Nieznany
gameLO net Bonus 33 id 185830 Nieznany
6 33 id 43161 Nieznany (2)
33 1 id 35788 Nieznany (2)
33 3 id 35675 Nieznany (2)
Jezyk polski 33 id 222209 Nieznany
33 8 id 35683 Nieznany (2)
4 33 id 37006 Nieznany (2)
II 33 id 209765 Nieznany
26 33 id 31365 Nieznany (2)
laoboratorium skory 33 id 26334 Nieznany
III CZP 33 11 id 210275 Nieznany
33 stereoautografy id 35775 Nieznany (2)
III CZP 33 70 id 210276 Nieznany
III CZP 33 11 id 210275 Nieznany
Abolicja podatkowa id 50334 Nieznany (2)
więcej podobnych podstron