
2. Interpretacja probabilistyczna mechaniki kwantowej, zasada nieoznaczoności
Heisenberga i ich ilustracja na przykładzie cząstki uwięzionej w studni potencjału.
INTERPRETACJA PROBABILISTYCZNA.
Na przykładzie elektronu chcemy zilustrować jak można zjednoczyć opis korpuskularny i
falowy.
Przeprowadzamy eksperyment:
Wiązkę elektronów przepuszczamy przez szczelinę o
szerokości Δx. Elektron przechodzi przez szczelinę i
zostaje ugięty przez szczelinę. Na ekranie powstaje
obraz
dyfrakcyjny,
którego
natężenie
jest
proporcjonalne do kwadratu amplitudy.
Jeśli potraktujemy elektron jak falę i przyjmiemy, że
jego amplituda wynosi Ψ, wtedy dla położenia x na
ekranie w chwili t natężenie będzie wynosiło:
𝐼 = |𝛹(𝑥, 𝑡)|
2
.
Ekran może być traktowany jako przyrząd służący do detekcji pojedynczych elektronów jako
cząstek. Ekran fluorescencyjny rozbłyskuje za każdym razem w punkcie, w którym uderza w
niego elektron. Tym samym elektron jest silnie zlokalizowany i nie powstaje obraz dyfrakcyjny.
Powtarzając doświadczenie obserwujemy rozbłyski w różnych punktach na ekranie. Jedynie,
gdy przeprowadzimy wiele doświadczeń z jednym elektronem lub pozwolimy przejść przez
szczelinę wielu elektronom, zaobserwujemy obraz dyfrakcyjny. Odgrywa to główną rolę w
zjawisku dualizmu korpuskularno-falowego. Z jednej strony natężenie na obrazie
dyfrakcyjnym w objętości ΔV jest proporcjonalne do kwadratu wartości bezwzględnej
amplitudy, a z drugiej jest proporcjonalne do prawdopodobieństwa znalezienia elektronu w
objętości ΔV. Zgodnie z podstawowym postulatem teorii prawdopodobieństwa suma
wszystkich prawdopodobieństw musi być równa 1. Ponieważ trafienie elektronu w dowolny
punkt ekranu jest tak samo prawdopodobne, wszystkie prawdopodobieństwa muszą być takie
same. Jeśli wykonany całkowanie po wszystkich punktach przestrzeni to cząstka musi gdzieś
zostać odnaleziona, a więc całkowite prawdopodobieństwo musi wynosić 1.
Interpretacja probabilistyczna funkcji falowej jest niezbędna, gdyż jeżeli uderzenie elektronu
w ekran wywołałoby jego rozbłysk to oznaczałoby to, że elektron się podzielił, a elektron jest
NIEPODZIELNY. Jeśli znajdziemy elektron w jednym miejscu, to jesteśmy pewni, że nie ma
go jednocześnie w innym miejscu.
ZASADA NIEOZNACZONOŚCI HEISENBERGA.
Zasada nieoznaczoności Heisenberga jest konsekwencją faktu, że elektron czasami zachowuje
się jak cząstka, a czasem jak fala.
„Niemożliwe jest równoczesne dokładne określenie pewnych par wielkości fizycznych układu,
do opisu którego stosuje się mechanikę kwantową.”
Zasada nieoznaczoności opisuje jedną z podstawowych własności przyrody. Pojawia się ona
wtedy, gdy opis zachowania cząstek w mikroświecie chcemy przeprowadzić używając pojęć
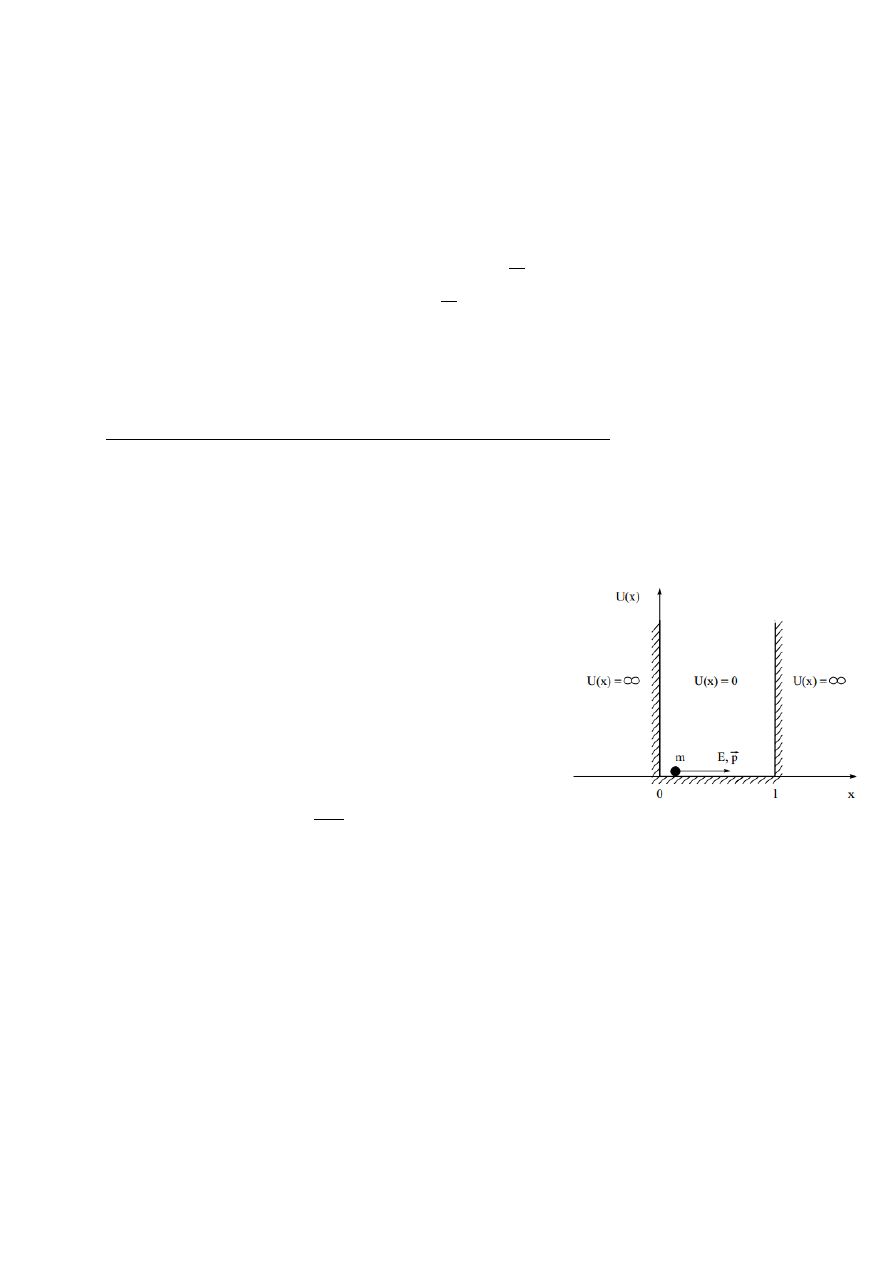
wziętych z makroświata. Zasada nieoznaczoności mówi o tym, że pewnych wielkości
fizycznych nie można zmierzyć jednocześnie z dowolną dokładnością. O wielkościach tych
mówi się, że nie komutują. Taką własność mają położenie i pęd oraz energia i czas. Z im
większą dokładnością znamy pęd cząstki, tym mniejsza jest dokładność określenia położenia.
Najczęściej zasadę nieoznaczoności Heisenberga przedstawiamy w postaci dwóch
nierówności:
jednej dla pędu i położenia cząstki:
𝛥𝑝
𝑥
∗ 𝛥𝑥 ≥
ℎ
4𝜋
drugą – dla energii i czasu:
𝛥𝐸 ∗ 𝛥𝑡 ≥
ℎ
2𝜋
,
gdzie: h=6,63*10
-34
J*s – stała Plancka.
Zasady nieoznaczoności nie warto stosować dla obiektów makroskopowych – niepewności są
nieosiągalne. Inaczej wygląda to natomiast w świecie atomów.
PRZYKŁAD CZĄSTKI UWIĘZIONEJ W STUDNI POTENCJAŁU.
Umieszczamy cząstkę w polu sił o energii potencjalnej określonej wzorem:
𝑈(𝑥) = { 0 𝑑𝑙𝑎 0 ≤ 𝑥 ≤ 𝑙
∞ 𝑑𝑙𝑎 𝑥 < 0 𝑖 𝑥 > 𝑙
,
czyli w tzw. studni potencjału o nieskończonej głębokości.
Z klasycznego punktu widzenia cząstka porusza się w
studni potencjału ruchem jednostajnym, odbijając się
kolejno od jej ścianek. Jeśli weźmiemy pod uwagę odbicia
fal de Broglie’a od ścian studni rozwiązanie równania
Schrodingera jest sumą fal poruszających się w kierunku
osi x. Funkcję falową wewnątrz studni określa wzór:
𝛹(𝑥) = 𝐴𝑒
𝑖𝑘𝑥
+ 𝐵𝑒
−𝑖𝑘𝑥
dla
0 ≤ 𝑥 ≤ 𝑙. Prawdopodobieństwo znalezienia cząstki na
zewnątrz studni powinno wynosić 0. Energia cząstki
określona jest wzorem:
𝐸 =
ℎ
2
𝑘
2
2𝑚
i w studni potencjału jest
skwantowana. Minimalna energia cząstki w studni potencjału musi być większa od zera.
Zgodnie z klasyczną mechaniką można stwierdzić, że cząstka w studni potencjału nie może
znajdować się w spoczynku, lecz porusza się swobodnie. Jest to ogólna własność rozwiązania
R.S., opisującego ruch cząstki w ograniczonym obszarze (minimalną energię nazywamy
energią zerową). Konieczność występowania zerowej energii można wytłumaczyć posługując
się zasadą nieoznaczoności. Jeżeli cząstka jest zamknięta w studni potencjału o szerokości l,
nieoznaczoność jej położenia ma skończoną wartość
𝛥𝑥 = 𝑙. Gdyby energia kinetyczna cząstki,
a co za tym idzie także pęd cząstki były równe 0, nieoznaczoność jej pędu wyniosłaby 0. Ale
wtedy iloczyn
𝛥𝑥 ∗ 𝛥𝑝 = 0 byłby sprzeczny z zasadą nieoznaczoności. Największe
prawdopodobieństwo znalezienia cząstki jest w miejscu, gdzie funkcja gęstości
prawdopodobieństwa przyjmuje największe wartości.
Wyszukiwarka
Podobne podstrony:
KPBM P5 id 249352 Nieznany
lab2 Instrukcja P2 C P id 75048 Nieznany
arkusz p2 id 68809 Nieznany (2)
LT 43 P2 id 273477 Nieznany
KPBM P15 ok id 249349 Nieznany
P2 jednostki id 344552 Nieznany
Abolicja podatkowa id 50334 Nieznany (2)
4 LIDER MENEDZER id 37733 Nieznany (2)
katechezy MB id 233498 Nieznany
metro sciaga id 296943 Nieznany
perf id 354744 Nieznany
interbase id 92028 Nieznany
Mbaku id 289860 Nieznany
Probiotyki antybiotyki id 66316 Nieznany
miedziowanie cz 2 id 113259 Nieznany
LTC1729 id 273494 Nieznany
więcej podobnych podstron