
Metabolizm leków
Metabolizm większości leków składa się z dwóch etapów:
Reakcje I fazy
•
najczęściej procesy oksydacji, redukcji, dezaminacji, dealkilacji
lub hydrolizy
•
w ich wyniku powstaje pochodna, która może być nieaktywna,
ale czasami bywa nawet bardziej chemicznie reaktywna od
związku wyjściowego
•
służą jako przygotowanie związku do reakcji II fazy (sprzęgania)
Reakcje II fazy
•
sprzęganie z podstawnikami –OH, –NH
2
czy –SH substancji
metabolizowanej związków takich jak kwas glukuronowy,
octowy, glicyna i in.
•
prawie zawsze unieczynniają związek wyjściowy
•
wskutek podwyższenia rozpuszczalności w wodzie umożliwiają
eliminację leku przez nerki
•
reakcje I i II fazy zachodzą głównie w wątrobie, rzadko w innych
narządach (np. suksametonium – osocze; prostanoidy – płuca;
salbutamol – jelita)
•
enzymy metabolizujące leki (w tym cytochrom P-450) znajdują
głównie się wewnątrz siateczki endoplazmatycznej hepatocytów
(enzymy mikrosomalne)
•
przez błonę hepatocytów przenikają
głównie cząsteczki
niespolaryzowane, leki spolaryzowane wydalane są najczęściej z
moczem w postaci niezmienionej
1

Cytochrom P-450
Enzymy cytochromu P-450 są hemoproteinami o właściwościach
oksydoredukcyjnych. Układ ten składa się z całej rodziny pokrewnych
enzymów różniących się budową, wrażliwością na indukcję i hamowanie
oraz specyficznością. Dzięki metodzie oznaczania sekwencji
aminokwasów do chwili obecnej opisano kilkadziesiąt grup
enzymatycznych dla cytochromu P-450 (geny CYP), które
odpowiedzialne są za metabolizm leków w wątrobie. Najważniejsze dla
metabolizmu leków są trzy główne grupy – CYP1, 2 i 3:
P-450 Lek
metabolizowany
CYP1A1 teofilina
CYP1A2
kofeina, ondansetron, paracetamol, takryna, teofilina
CYP2A6 metoksyfluran
CYP2C8 taksol
CYP2C9 ibuprofen, kwas mefanemowy, fenytoina, tolbutamid,
warfaryna
CYP2C19 omeprazol
CYP2D6
klozapina, kodeina, debryzochina, metoprolol, TLPD
CYP2E1 alkohol,
enfluran,
halotan
CYP3A4/5 cyklosporyna, erytromycyna, etynyloestradiol, losartan,
lignokaina, midazolam, nifedypina, terfenadyna
(za: Pichard et al. (1995) Predictability of drug metabolism fromi in vitro studies.
W: Alvan G et al. (eds) COST B1 conference on variability and specifity in drug
metabolism. European Commission, Luxembourg, pp 45-56)
Liczne substancje mogą wpływać na metabolizm leków przez enzymy
mikrosomalne:
•
hamowanie może zachodzić wskutek antagonizmu kompetycyjnego
(chinidyna – CYP2D6) lub niekompetycyjnego (ketokonazol tworzy
silne wiązania z Fe3+ ugrupowania hemowego CYP3A4)
•
indukcja może zachodzić po wielokrotnym podaniu niektórych leków
(np. ryfampicyna, etanol, karbamazepina), które zwiększają
aktywność oksydazy mikrosomalnej i układu sprzęgającego poprzez
wzmożenie syntezy enzymów mikrosomalnych
2
Rodzina
CYP
Substancje indukujące
metabolizm
Leki, których metabolizm jest
wzmożony
1A2
benzopiren (dym
papierosowy), karbamazepina,
fenobarbital, ryfampicyna
acetaminofen, klozapina, haloperidol,
teofilina, TLPD, warfaryna
2C9
barbiturany (zwł. fenobarbital),
fenytoina, prymidon,
ryfampicyna
barbiturany, chloramfenikol, warfaryna,
doxorubicyna, ibuprofen, fentyoina,
chlorpromazyna, sterydy, tolbutamid
2C19 karbamazepina, fenobarbital,
fenytoina
TLPD, fentytoina, topiramat, warfaryna
2E1
etanol, izoniazyd
acetaminofen, etanol, halotan
3A4
barbiturany, karbamazepina,
kortykosteroidy, efawirenz,
fenytoina, ryfampicyna,
troglitazon
antyarytmiki, TLPD, ketokonazol,
benzodiazepiny, blokery Ca,
cyklosporyna, doksorubicyna, SSRI,
efawirenz, erytromycyna, estrogeny,
nefazodon, omeprazol, ryfampicyna,
sildenafil, tamoksyfen, trazodon
Rodzina
CYP
Substancje hamujące
metabolizm
Leki, których metabolizm jest
hamowany
1A2
cymetydyna, fluorochinony,
sok grapefruitowy, makrolidy,
izoniazyd, zileuton
acetaminofen, klozapina, haloperidol,
teofilina, TLPD, warfaryna
2C9
amiodaron, chloramfenikol,
cymetydyna, izoniazyd,
metronidazol, SSRI, zafirlukast
barbiturany, chloramfenikol, warfaryna,
doxorubicyna, ibuprofen, fentyoina,
chlorpromazyna, sterydy, tolbutamid
2C19 omeprazol, SSRI
fenytoina, topiramat, warfaryna
2D6
amiodaron, cymetydyna,
chinidyna, SSRI
TLPD, flekainid, lidokaina,
meksyletyna, opioidy
3A4
amiodaron, ketokonazol,
cymetydyna, klarytromycyna,
cyklosporyna, erytromycyna,
fluorochinony, sok
grapefruitowy, metronidazol,
chinina, SSRI, tacrolimus
antyarytmiki, TLPD, ketokonazol,
benzodiazepiny, blokery Ca,
cyklosporyna, doksorubicyna, SSRI,
efawirenz, erytromycyna, estrogeny,
nefazodon, omeprazol, ryfampicyna,
sildenafil, tamoksyfen, trazodon
(za: Katzung BG 2001, „Basic & Clinical Pharmacology”, 8th ed. McGraw-Hill)
3
Reakcje I fazy nie zawsze przebiegają z udziałem enzymów cytochromu
P-450 jak np.:
o Niektóre reakcje oksydacji:
•
dehydrogenaza alkoholowa rozkłada etanol (rozkładany
także przez CYP2E1)
•
oksydaza ksantynowa rozkłada 6-merkaptopurynę
•
monoaminooksydaza (MAO) rozkłada aminy katecholowe
o Reakcje hydrolizy przebiegają bez udziału enzymów
mikrosomalnych wątroby (np. w osoczu)
Reakcje II fazy:
•
jeśli lek lub jego metabolit po reakcji I fazy posiada odpowiednie
ugrupowania (hydroksylowe, tiolowe, aminowe itp.), to jest
podatny na reakcje sprzęgania
•
przy udziale odpowiednich transferaz zachodzą procesy
glukuronizacji, acetylacji, metylacji itp.
•
w większości przypadków produkt reakcji II fazy pozbawiony jest
działania farmakologicznego i mniej rozpuszczalny w tłuszczach niż
związek wyjściowy, w związku z czym może zostać wydalony z
moczem lub żółcią
OCOCH
3
COOH
OH
COOH
O
COOH
O
H
H
OH
H
O
H
OH
H
H
COOH
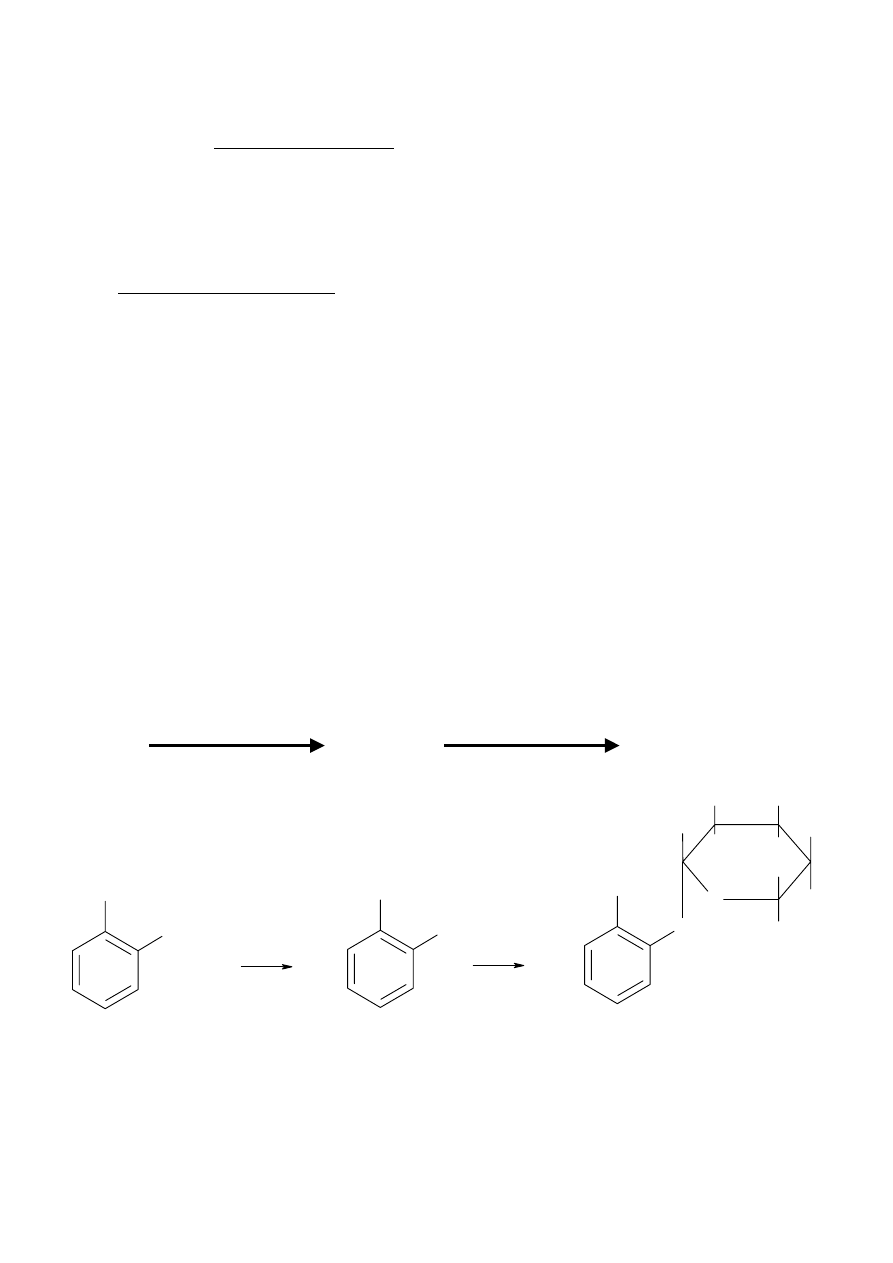
Aspiryna
Kwas salicylowy
Glukuronian
Lek Pochodna
Faza 1
Faza 2
Forma
sprzężona
4
Procesy metaboliczne zwykle prowadzą do inaktywacji leków. Niekiedy
jednak metabolity leków wykazują aktywność farmakologiczną i:
•
w dalszym ciągu działają podobnie do związku wyjściowego – np.
diazepam i jego pochodne – nordiazepam i oksazepam
•
zmieniają swoje działanie – np. aspiryna przekształcana jest w kwas
salicylowy Æ utrata działania przeciwzakrzepowego
•
proleki
stają się aktywne dopiero po zmetabolizowaniu w organizmie
– np. enalapryl, zydowudyna
•
działają toksycznie – np. paracetamol przy niedoborze glutationu
przekształcany jest w bardzo hepatotoksyczny związek – iminę
N-acetylo-p-benzochinonu
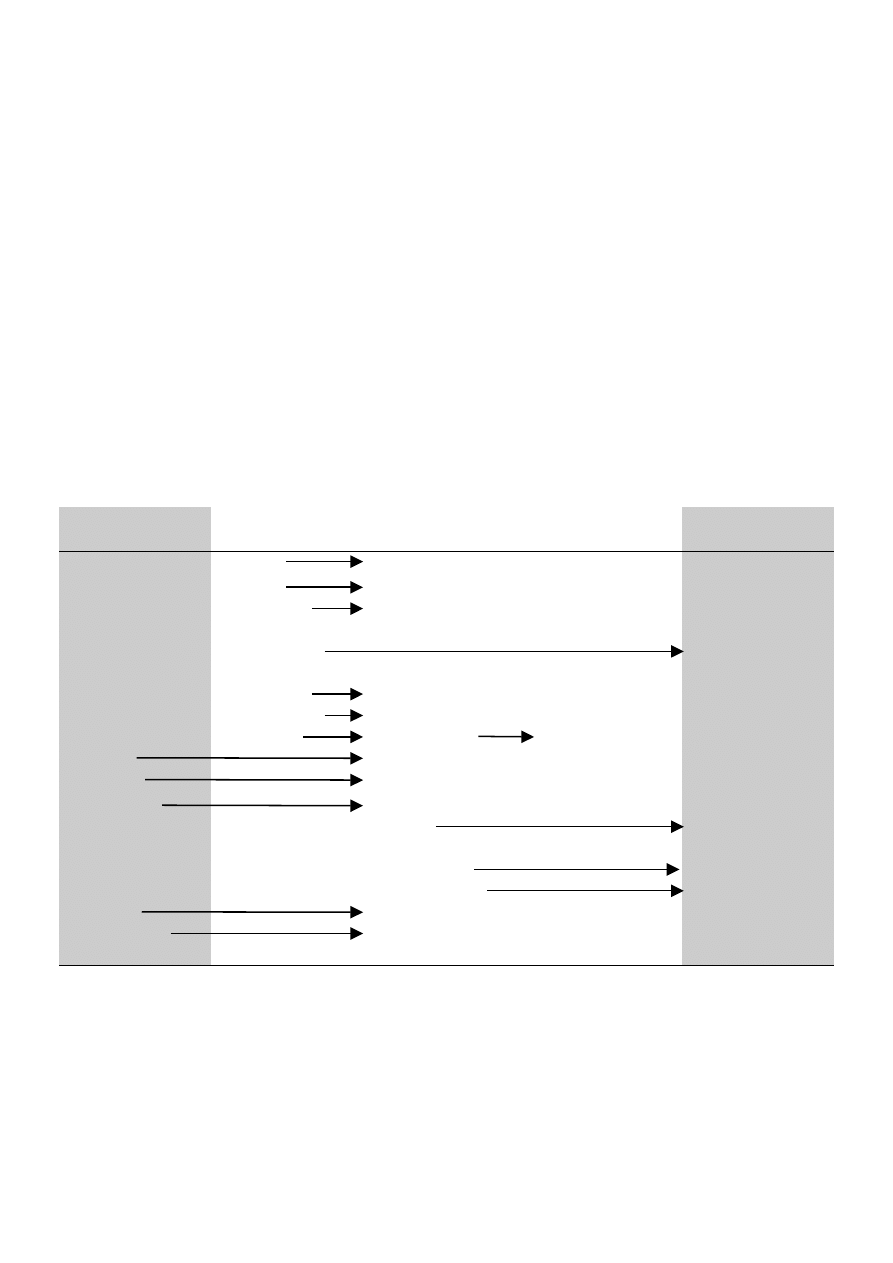
Leki ulegające przemianom do aktywnych lub toksycznych
metabolitów
Nieaktywne
(proleki)
Aktywne
Toksyczne
Heroina Morfina
Kodeina Morfina
Propranolol 4-
hydroksypropranolol
Paracetamol
Imina N-acetylo-
p-benzochinonu
Imipramina Dezmetylimipramina
Amitryptylina Nortryptylina
Diazepam Nordiazepam Oksazepam
Kortyzon
Hydrokortyzon
Prednizon
Prednizolon
Azatiopryna
Merkaptopuryna
Halotan
Kw.
trifluorooctowy
Sulfonamidy
Poch. acetylowe
Metoksyfluran
Fluor
Enalapril
Enalaprilat
Zydowudyna
Trifosforan
zydowudyny
(za: Rang 2000, „Pharmacology”, Churchil Livingstone, Edinburgh)
5
Wyszukiwarka
Podobne podstrony:
więcej podobnych podstron