
16. KWASY KARBOKSYLOWE
799. 1973/L
Wzrost długości łańcucha węglowego w cząsteczkach kwasów organicznych powoduje:
A. obniżenie temperatury topnienia kwasów
B. mniejszą reaktywność kwasów
C. wzrost stopnia dysocjacji kwasów
D. wzrost rozpuszczalności kwasów
800. 1999/L
Rozważ następujące związki chemiczne:
I. etanol;
II. etanowy kwas (octowy);
III. etanodiowy kwas (szczawiowy);
IV. fenol;
V. metanowy kwas (mrówkowy);
Charakter kwasowy wyżej wymienionych związków maleje zgodnie z uszeregowaniem:
A. V, II, IV, I, III
B. III, IV, V, I, II
C. II, V, III, IV, I
D. III, V, II, IV, I
801.
Wartości stałych dysocjacji kwasów karboksylowych wynoszą odpowiednio:
Nr
Nazwa kwasu
Stała dys. kwasu
I
kwas mrówkowy
1.7
10
-4
II
kwas octowy
1.8
10
-5
III
kwas masłowy
1.5
10
-5
IV
kwas benzoesowy
6.5
10
-5
Moc powyższych kwasów rośnie w szeregu:
A. III, II, IV, I
B. I, IV, II, III
C. III, I, II, IV
D. IV, II, I, III
E. IV, II, III, I
802.
pH 0.01 molowych wodnych roztworów kwasów, których stałe dysocjacji podane są w pytaniu nr
801, rośnie w szeregu:
A. I, II, III, IV
B. IV, III, II, I
C. I, IV, II, III
D. I,IV, III, II
E. III, II, IV, I
803. 2000/L
Na moc kwasów karboksylowych wpływa liczba obecnych w cząsteczce atomów o dużej
elektroujemności oraz ich położenie względem grupy karboksylowej. Wpływ ten jest następujący:
1. im większa liczba takich atomów, tym moc kwasu jest większa;
2. im bardziej atomy te są oddalone od grupy karboksylowej, tym moc kwasu jest mniejsza;
Na tej podstawie wybierz szereg, w którym kwasy ułożono według malejącej mocy.
A. C
3
H
7
COOH, CH
3
CHClCH
2
COOH, C
2
H
5
CHClCOOH, C
2
H
5
C(Cl)
2
COOH.
B. C
2
H
5
C(Cl)
2
COOH, C
2
H
5
CHClCOOH, CH
3
CHClCH
2
COOH, C
3
H
7
COOH.
C. C
3
H
7
COOH, C
2
H
5
CHClCOOH, C
2
H
5
C(Cl)
2
COOH, CH
3
CHClCH
2
COOH.
D. CH
3
CHClCH
2
COOH, C
2
H
5
CHClCOOH, C
2
H
5
C(Cl)
2
COOH, C
3
H
7
COOH.
804. 1974/L
Aby z acetylenu otrzymać kwas octowy, należy acetylen:
A. utlenić w obecności katalizatorów
B. poddać reakcji katalitycznego przyłączania wody i utlenić
C. uwodornić do węglowodoru nasyconego, a następnie utlenić
D. poddać reakcji przyłączania chlorowodoru, a następnie reakcji z silnymi zasadami
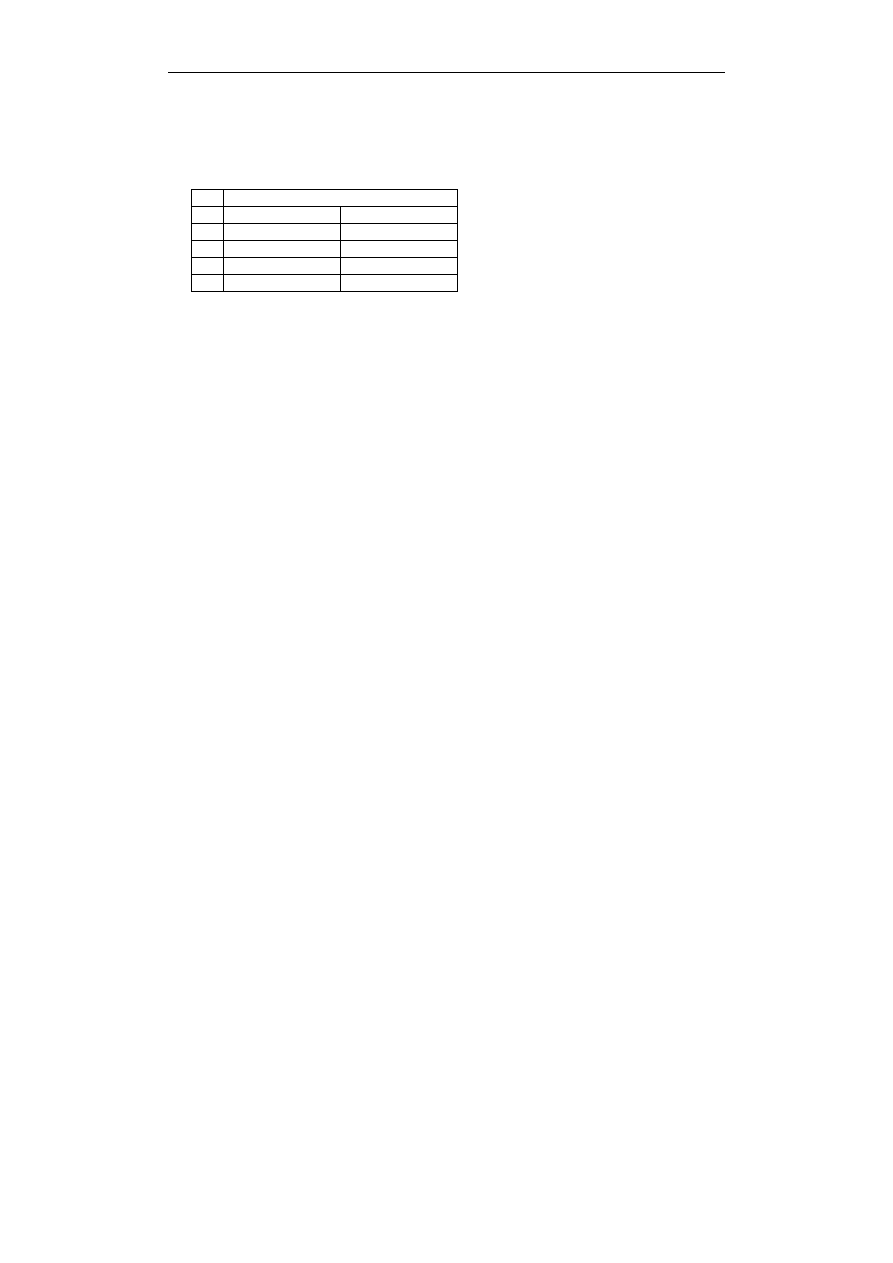
Chemia. Wybór testów...
128
805. 1995/L
Moc kwasów karboksylowych zależy od podstawników w ich strukturze. Podstawniki bardziej
elektroujemne zwiększają moc kwasu, przy czym istnieje dość prosta zależność między ich
elektroujemnością, a wzrostem mocy odpowiedniego kwasu. W oparciu o powyższe i znaną
elektroujemność pierwiastków wskaż właściwą odpowiedź:
Kwas
Mocniejszy
Słabszy
A.
CH
2
ClCOOH
CH
2
FCOOH
B.
CH
3
COOH
CH
2
BrCOOH
C.
CH
2
FCOOH
CH
2
ClCOOH
D.
CH
2
ICOOH
CH
2
BrCOOH
806. 1977/L
Stwierdzono, że badany związek ma następujące właściwości:
– jest ciekły w temperaturze 25
o
C
– rozpuszcza się w wodzie
– reaguje z wodą bromową
– reaguje z jodowodorem dając substancję o masie cząsteczkowej większej o 128 od masy cząstecz-
kowej badanego związku
– reaguje egzotermicznie z wodnym roztworem wodorotlenku sodowego
Która z wymienionych substancji jest badanym związkiem?
A. CH
3
CH = CHCHO
B. CH
3
– CH = CH – COOCH
3
C. CH
3
– CH = CH – CH
2
– OH
D. CH
3
– CH = CH – COOH
807. 1979/L
Z równania całkowitego spalania 0.5 mola kwasu palmitynowego wynika, że w reakcji tej bierze
udział:
A. 11.5 mola tlenu
B. 12 moli tlenu
C. 23 mole tlenu
D. 24 mole tlenu
808.
Ile gramów 15% roztworu NaOH potrzeba do całkowitego zobojętnienia 1 mola kwasu
cytrynowego?
A. 120g
B. 800g
C. 102g
D. 267g
E. 533g
809. 1999/F
Aby otrzymać kwas izomasłowy należy utlenić:
A. 1–butanol
B. 2–metylo–2–propanol
C. 2–metylo–1–propanol
D. 2–butanol
810. 1999/L
Kwas 2–hydroksypropanowy można otrzymać przez podstawienie atomu chloru grupą hydroksylową
w związku:
A. CH
3
CHClCOOH
B. CH
3
CH
2
CHClCOOH
C. CH
2
ClCH
2
COOH
D. CH
3
CHClCH
2
COOH
811. 1998/F
Który z podanych hydroksykwasów posiada chiralny atom węgla?
A. kwas salicylowy
B. kwas jabłkowy
C. kwas hydroksyoctowy
D. kwas 3-hydroksypropanowy

Kwasy karboksylowe
129
812.
Na próbkę, zawierającą niewielką ilość alkoholu etylowego, podziałano nadmiarem stężonego,
zakwaszonego roztworu dwuchromianu potasowego. W wyniku przebiegającej reakcji tworzy się:
A. aldehyd octowy
B. kwas octowy
C. dwutlenek węgla i woda
D. węgiel i woda
813. 1980/L
Stan skupienia jednokarboksylowych kwasów alifatycznych zależy głównie od:
A. długości łańcucha węglowego
B. liczby grup
COOH
C. tego, czy jest to kwas nasycony, czy nie
D. czynników wymienionych pod A i C
814. 1981/L
Wartości stałych dysocjacji dwóch kwasów organicznych określone w tej samej temperaturze są
następujące:
CH
3
– CH
2
– COOH
K = 1.34
10
-5
C
6
H
4
OHCOOH
K = 8.3
10
-5
Z danych wynika, że:
A. a - obydwa związki są słabymi kwasami
b - kwas propionowy jest nieco mocniejszy od kwasu hydroksybenzoesowego
B. a - obydwa związki są słabymi kwasami
b - kwas hydroksybenzoesowy jest nieco mocniejszy od kwasu propionowego
C. a - kwas propionowy można zaliczyć do kwasów mocnych
b - kwas hydroksybenzoesowy zaliczamy do kwasów słabych
D. a - kwas propionowy jest kwasem słabym
b - kwas hydroksybenzoesowy jest kwasem mocnym
815. 2000/F
Przygotowano 0,1 molowe wodne roztwory kwasów: metanowego, etanowego, etanodiowego,
aminoetanowego. Uszereguj roztwory kwasów według rosnącego pH:
A. kwas etanodiowy, kwas metanowy, kwas etanowy, kwas aminoetanowy.
B. kwas aminoetanowy, kwas etanowy, kwas metanowy, kwas etanodiowy.
C. kwas etanodiowy, kwas etanowy, kwas metanowy, kwas aminoetanowy.
D. kwas metanowy, kwas etanodiowy, kwas etanowy, kwas aminoetanowy.
816. 1982/L
Mydła sodowe i potasowe należą do anionowych środków powierzchniowo-czynnych ponieważ:
A. zawierają aniony nierozpuszczalne w wodzie
B. ich grupa hydrofobowa zawarta jest w kationie
C. ich grupa hydrofobowa zawarta jest w reszcie alkilowej
D. grupa hydrofilowa i hydrofobowa zawarte są w anionie
817. 1983/L
Do mydeł nierozpuszczalnych w wodzie należy:
A. palmitynian sodowy
B. stearynian potasowy
C. oleinian sodowy
D. palmitynian wapniowy
818. 1992-94/MIS MaP
Którym mydłem nie można się umyć?
A. stearynianem potasu
B. palmitynianem sodu
C. palmitynianem wapnia
D. oleinianem potasu
Chemia. Wybór testów...
130
819. 2000/L
Jeżeli 4,32 g kwasu szczawiowego (COOH)
2
znajduje się w 1,2 dm
3
roztworu, to stężenie tego
roztworu wynosi:
A. 0,02 mol·dm
B. 0,04 mol·dm
C. 0,002 mol·dm
D. 0,004 mol·dm
820. 1987/L
Który z niżej wymienionych związków nie ma zastosowania jako środek obniżający napięcie
powierzchniowe wody?
A. C
17
H
35
COOK
B. C
17
H
35
COO)
2
Mg
C. C
12
H
25
OSO
3
Na
C12H25
D.
SO3Na
821.
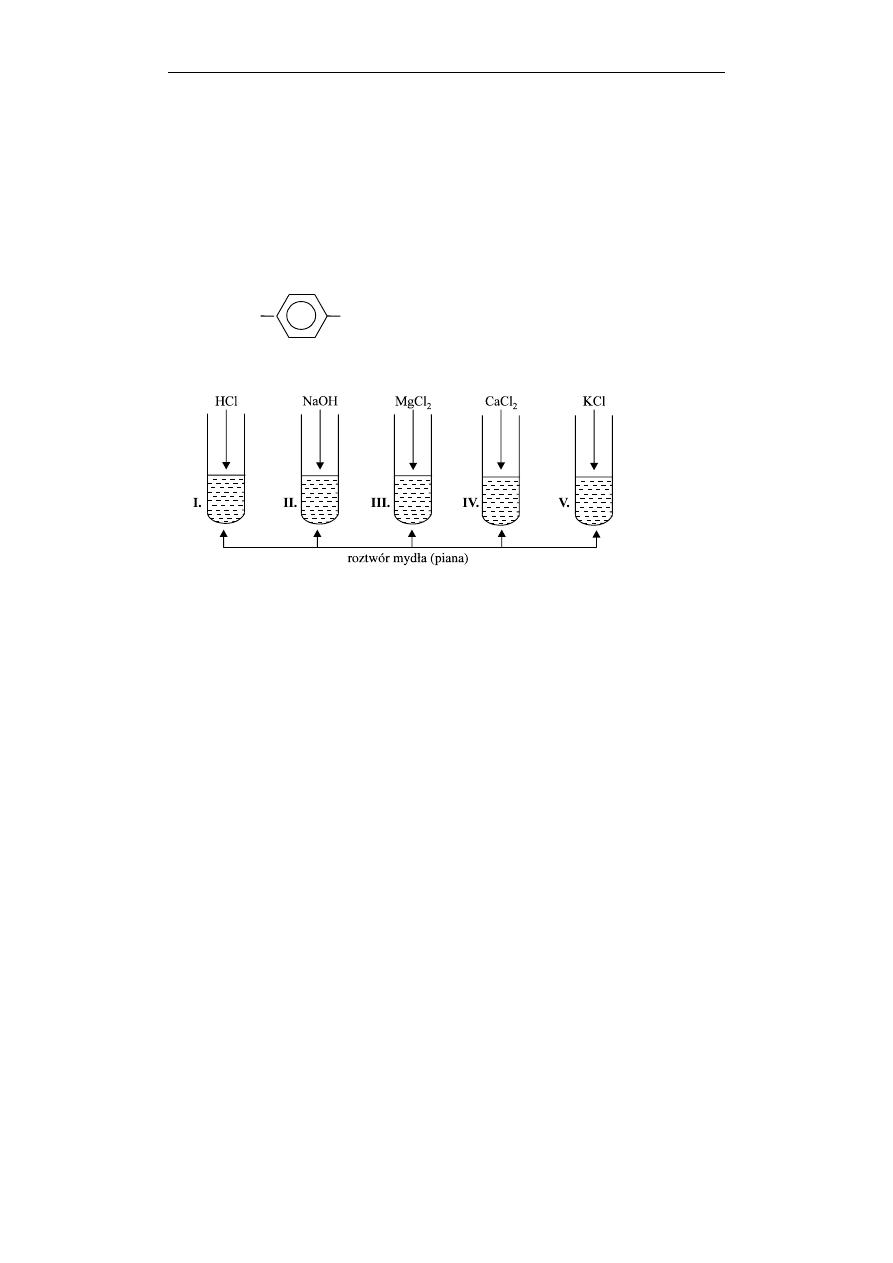
Przeprowadzono doświadczenia, które ilustruje poniższy rysunek.
W której probówce zaobserwowano znikanie piany?
A. I i II
B. III i IV
C. III, IV i V
D. tylko w IV
E. tylko w III
822. 1983/L
Który wzór przedstawia związek powstający w mięśniach podczas pracy fizycznej i powodujący
objawy zmęczenia?
A. CH
3
CH(NH
2
)COOH
B. C
6
H
4
(OH)COOH
C. C
16
H
33
COOH
D. CH
3
CH(OH)COOH
823. 1983/L
Analiza pewnego związku organicznego wykazuje, że na 2.1g węgla przypada 0.35g wodoru i 2.8g
tlenu. Gęstość pary tego związku względem wodoru wynosi 30. Jaki jest wzór cząsteczkowy tego
związku?
A. CH
2
O
B. C
2
H
4
O
2
C. C
3
H
6
O
3
D. C
4
H
8
O
4
824. 1992-94/MIS MaP
W wyniku hydrolizy produktu reakcji bromku benzylu z cyjankiem potasu otrzymano:
A. kwas benzoesowy
B. kwas p-bromobenzoesowy
C. kwas fenylooctowy
D. cyjanian benzylu
825. 1992-94/MIS MaP
Jodek metylomagnezowy po reakcji z dwutlenkiem węgla i zakwaszeniu daje:
A. kwas masłowy
B. kwas octowy
C. kwas mrówkowy
D. eten
Kwasy karboksylowe
131
826. 1986/L
Jednym z genetycznie uwarunkowanych zaburzeń metabolicznych u człowieka jest fenyloketonuria.
W swej klasycznej postaci choroba ta polega na niedoborze w komórkach enzymu utleniającego
fenyloalaninę do tyrozyny, a jednym z objawów jest wysoka zawartość w moczu kwasu
fenylopirogronowego. Budowę kwasu fenylopirogronowego przedstawia wzór:
COOH
C
CH2
HO
H
CH2
COOH
C
H2N
H
OH
CH2
COOH
C
H2N
H
A.
B.
C.
D.
CH2
COOH
C
O
827. 1986/L
Przeczytaj poprzednie zadanie, przypomnij sobie strukturę obydwu wymienionych związków
i uzupełnij tekst następującego zdania: „W przeciwieństwie do fenyloalaniny w cząsteczkach kwasu
fenylopirogronowego nie ma ... ”
A. atomów tlenu
B. grup karboksylowych
C. pierścieni aromatycznych
D. asymetrycznych atomów węgla
828. 1987/L
Stała dysocjacji kwasu octowego jest rzędu 10
-5
, a kwasu chlorooctowego rzędu 10
-3
. Oznacza to, że:
A. kwas chlorooctowy jest kwasem mocniejszym, a spowodowane jest to efektem indukcyjnym
atomu chloru
B. kwas chlorooctowy jest kwasem mocniejszym niż kwas octowy, gdyż jego masa molowa jest
większa
C. kwas chlorooctowy jest słabszy niż kwas octowy z uwagi na to, że grupa
CH
2
Cl ma większą
objętość
D. kwas octowy jest kwasem mocniejszym, a obecność chlorowca zmniejsza stopień dysocjacji
grupy karboksylowej
829. 1987/L
Zakładając, że przemiana: etanol
etanal
kwas octowy przebiega w każdym etapie
z wydajnością 90%, to z 23g etanolu otrzymano gramów kwasu octowego:
A. 12.1
B. 15.0
C. 24.3
D. 30.0
830. 1987/L
Wiele kwasów organicznych ulega reakcji dekarboksylacji, którą można przedstawić ogólnym
równaniem:
R – COOH
RH + CO
2
. Kwas acetylooctowy o wzorze: CH
3
– CO – CH
2
– COOH
ulegając dekarboksylacji obok CO
2
daje jako produkt:
A. propanol
B. propanon
C. etanal i metan
D. metan i etan
831.
Ile dm
3
dwutlenku węgla (w przeliczeniu na warunki normalne) wydzieli się podczas dekarboksylacji
61g kwasu benzoesowego?
A. 2.8 dm
3
B. 5.6 dm
3
C. 11.2 dm
3
D. 22.4 dm
3
E. 44.8 dm
3
832. 1988/L
W roztworze dwuprotonowego kwasu szczawiowego znajdują się obok niezdysocjowanych
cząsteczek kwasu H
2
C
2
O
4
jony H
+
, HC
2
O
4
i C
2
O
4
2-
, których stężenia obrazuje ciąg nierówności:
A. [C
2
O
4
2-
] > [H
+
] > [HC
2
O
4
]
B. [H
+
] > [HC
2
O
4
] > [C
2
O
4
2-
]
C. [C
2
O
4
2-
] > [HC
2
O
4
] > [H
+
]
D. [HC
2
O
4
] > [C
2
O
4
2-
] > [H
+
]
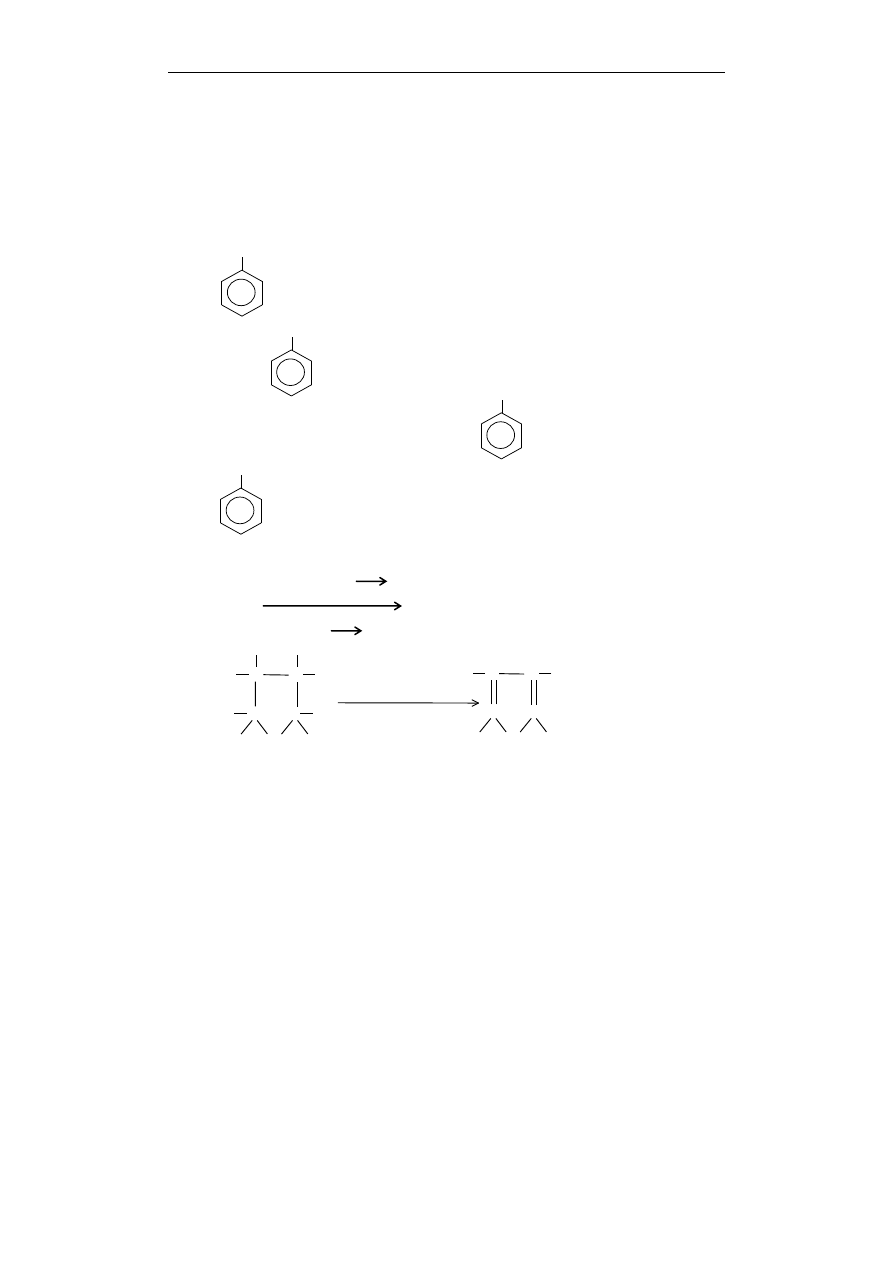
Chemia. Wybór testów...
132
833. 1988/L
W wyniku utleniania etanalu do kwasu wydzieliło się 1.08g metalicznego srebra. Otrzymany kwas
uzupełniono wodą do 200 cm
3
. Zakładając, że stopień dysocjacji wynosi 4%, pH roztworu tego kwasu
wyniesie:
A. 2
B. 3
C. 4
D. 5
834. 1988/L
W którym z przedstawionych niżej zestawów uszeregowano kwasy według rosnącego stopnia
dysocjacji w 0.1 molowych roztworach:
OH
A.
B.
OH
, H2CO3, CH3COOH, HCOOH, CHCl2COOH
, CHCl2COOH, CH3COOH, HCOOH
H2CO3,
C. HCOOH, CH3COOH, CHCl2COOH, H2CO3,
OH
D.
OH
, CCl3COOH, CH3COOH, HCOOH, H2CO3
835. 1989/L
I. CCl
3
COONa + CH
3
COOH
CH
3
COONa + CCl
3
COOH
II. HCOOH
H
2
O + CO
III. 2C
6
H
5
OH + Cu(OH)
2
C
6
H
5
O)
2
Cu + 2H
2
O
O
HO
C
CH2OH
OH
C
C
C
HO
O
C
CHO
C
C
C
+ 3 H2O
H
Z podanych reakcji najbardziej prawdopodobne są:
A. I, II
B. III, IV
C. I, III
D. II, IV
836. 1989/L
30g kwasu octowego poddano chlorowaniu otrzymując z wydajnością 80% kwas chlorooctowy,
który następnie przekształcono w odpowiedniej reakcji w kwas aminooctowy z wydajnością 70%.
W wyniku tego procesu masa otrzymanego kwasu aminooctowego w gramach wynosi:
A. 22.125
B. 26.25
C. 21.0
D. 30.0
837. 1989/L
Dane są dwa zdania:
I. Silnie elektroujemny podstawnik w sąsiedztwie grupy karboksylowej zmniejsza gęstość
elektronową przy atomie wodoru grupy hydroksylowej kwasu.
II. Kwasy
-chloropropanowy i mlekowy są mocniejsze od kwasu propanowego.
IV.
stężony kwas siarkowy
ogrzewanie w obecności
stęż. HCl

Kwasy karboksylowe
133
Z powyższych zdań prawdziwe:
A. jest tylko zdanie I
B. jest tylko zdanie II
C. są obydwa, a zdanie I jest uzasadnieniem zdania II
D. są obydwa lecz stanowią niepowiązane ze sobą stwierdzenia
838. 1991/L
W wyniku reakcji 11g kwasu jednokarboksylowego z magnezem otrzymano 1.4 dm
3
H
2
(w warunkach normalnych). Kwasem tym jest:
A. kwas mrówkowy
B. kwas octowy
C. kwas etanowy
D. kwas butanowy
E. kwas propanowy
839.
Ile cm
3
90% kwasu octowego o gęstości 1.07 g/cm
3
należy użyć aby otrzymać 1 dm
3
0.1 molowego
roztworu tego kwasu?
A. 3.13 cm
3
B. 6.23 cm
3
C. 10.7 cm
3
D. 6.9 cm
3
E. 20.1 cm
3
840. 1990/L
Do 500 cm
3
kwasu octowego o stężeniu c = 0.1 mol/dm
3
dodano 500 cm
3
wody. Stała dysocjacji
kwasu:
A. zmniejszyła się dwukrotnie
B. wzrosła dwukrotnie
C. wzrosła o 20%
D. nie zmieniła się
841. 1978/F
Jakie grupy funkcyjne posiada alifatyczny związek, jeśli wiadomo, że jedna z nich reaguje z NaOH,
a obie z metalicznym sodem?
A.
OH i =CO
B.
OH i
COOH
C.
OH i
CHO
D. =CO i
COOH
842. 1979/F
Porównując właściwości jednokarboksylowych kwasów alifatycznych można stwierdzić, że ze
wzrostem długości łańcucha węglowego w cząsteczce kwasu:
A. zwiększa się moc kwasu, wzrasta temperatura topnienia, obniża się rozpuszczalność w wodzie
B. zwiększa się moc kwasu, obniża temperatura topnienia, wzrasta rozpuszczalność w wodzie
C. zmniejsza się moc kwasu, wzrasta temperatura topnienia, obniża się rozpuszczalność w wodzie
D. zmniejsza się moc kwasu, obniża temperatura topnienia, wzrasta rozpuszczalność w wodzie
843. 1979/F
Analizując poniższe równania:
C
6
H
5
COOH + CH
3
COONa
CH
3
COOH + C
6
H
5
COONa
2CH
3
COOH + Na
2
CO
3
CH
3
COONa + CO
2
+ H
2
O
2C
6
H
5
COOH + Na
2
CO
3
2C
6
H
5
COONa + CO
2
+ H
2
O
dochodzisz do wniosku, że:
A. kwas octowy jest mocniejszy od kwasu węglowego i kwasu benzoesowego
B. kwas benzoesowy jest mocniejszy od kwasu octowego, a ten jest mocniejszy od kwasu
węglowego
C. kwas benzoesowy jest mocniejszy od kwasu węglowego, a słabszy od kwasu octowego
D. kwas octowy jest słabszy od kwasu benzoesowego i węglowego
844. 1980/F
Aby odróżnić kwas oleinowy od kwasu stearynowego wystarczy:
A. spalić oba kwasy
B. porównać stan skupienia kwasów
C. dokonać próby rozpuszczenia kwasów w wodzie
D. ogrzać kwasy z wodorotlenkiem sodowym w obecności fenoloftaleiny
Chemia. Wybór testów...
134
845. 1980/F
Kwas palmitynowy można uważać za produkt utlenienia węglowodoru o wzorze:
A. C
18
H
38
B. C
17
H
34
C. C
16
H
34
D. C
15
H
32
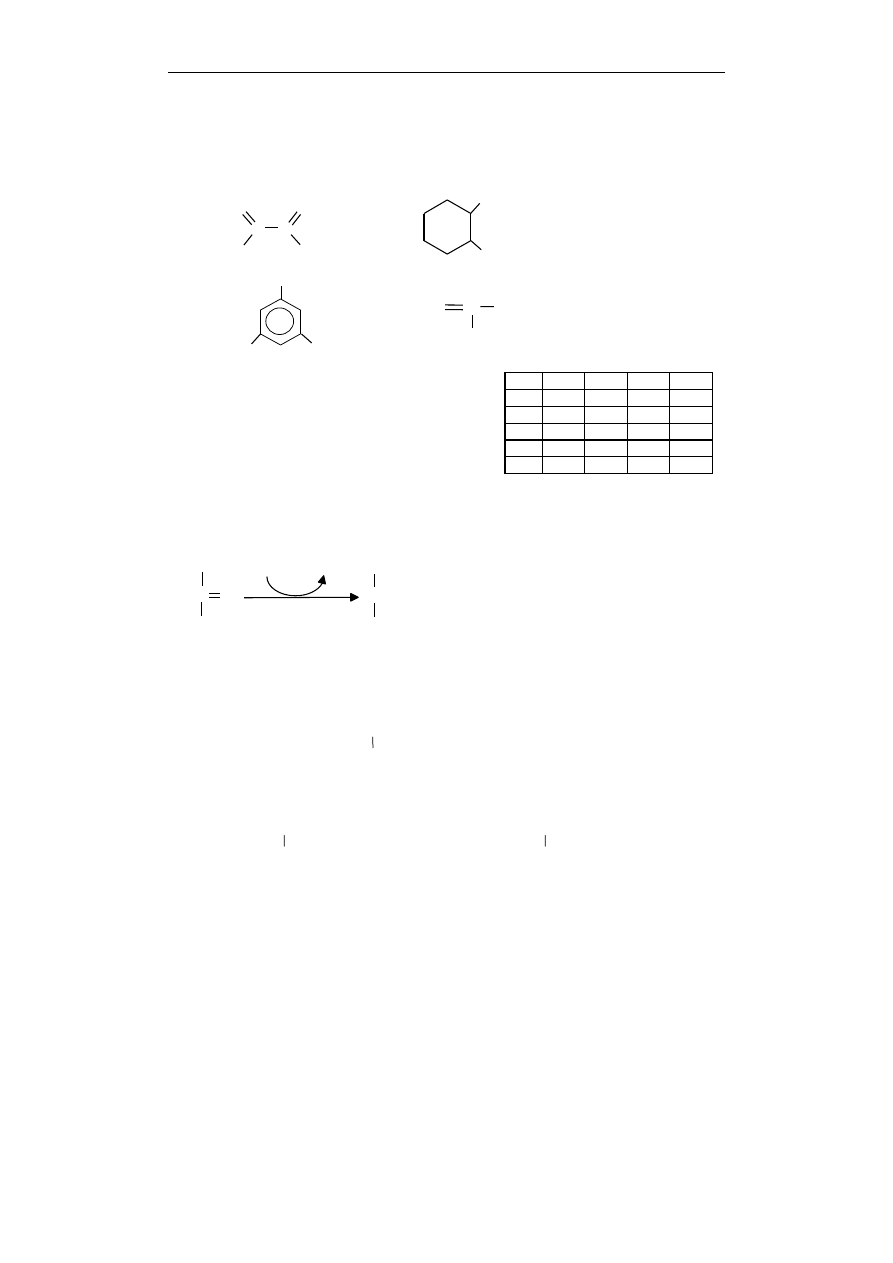
846.
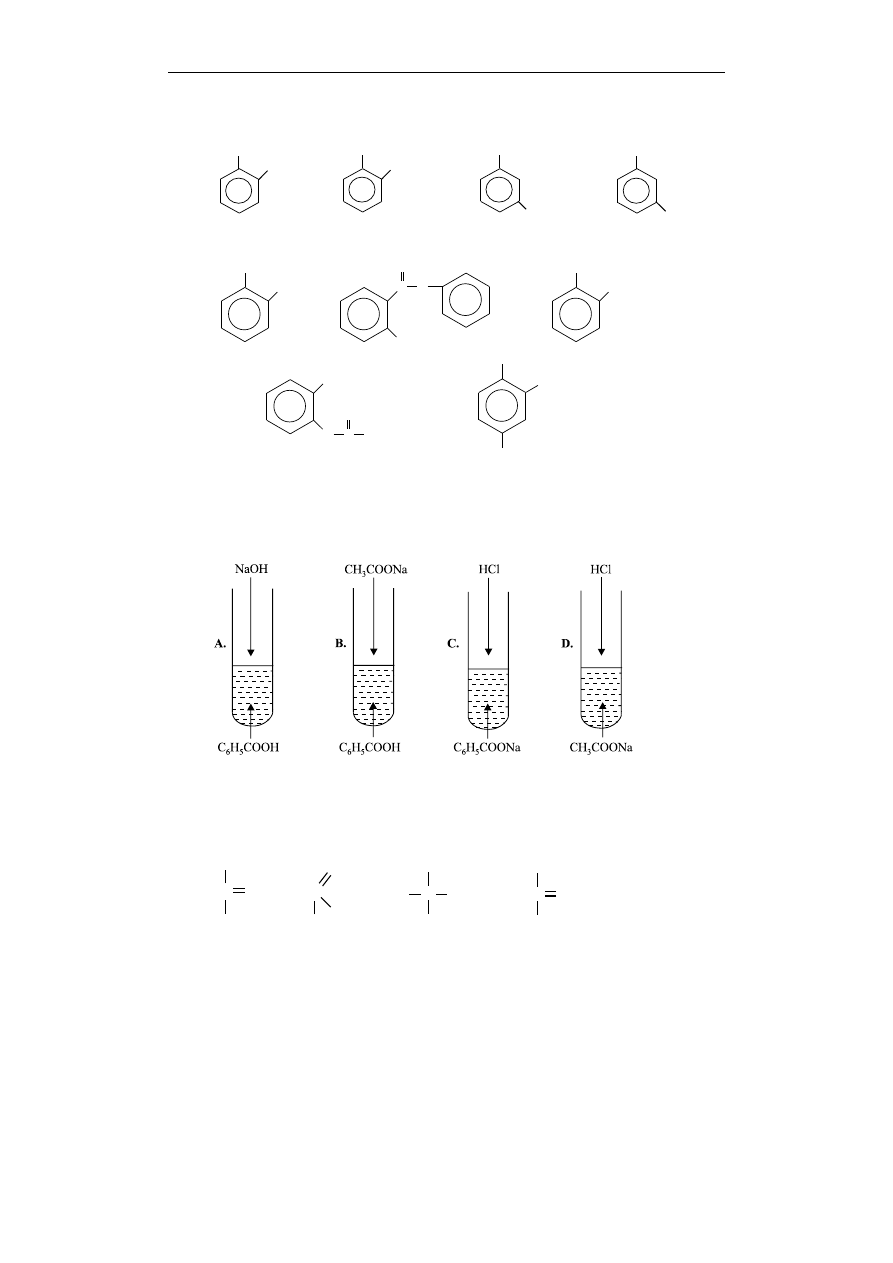
Poniżej podano wzory wybranych kwasów karboksylowych:
I.
C
O
HO
OH
C
O
III.
HOOC
COOH
COOH
IV.
C
CH3
CH2
COOH
II.
COOH
COOH
są to kwasy:
x) 1, 3, 5-benzenotrikarboksylowy
y) 1, 2-cykloheksanodikarboksylowy
z) 2-metylopropenowy
w) etanodiowy
Prawidłowe przyporządkowanie nazw podanym powyżej
wzorom kwasów jest następujące:
x
y
z
w
A.
I
II
III
IV
B.
II
IV
III
I
C.
III
II
IV
I
D.
III
II
I
IV
E.
II
III
IV
I
847. 1982/F
W organizmie zwierzęcym cząsteczka glukozy w wyniku glikolizy daje dwie cząsteczki kwasu
pirogronowego. W warunkach beztlenowych kwas pirogronowy ulega przekształceniu:
C
COOH
O
CH3
CHOH
COOH
CH3
NADH2 NAD
Reakcja ta stanowi:
A. źródło kwasu mlekowego w mięśniach
B. początek cyklu kwasu cytrynowego
C. proces utleniania kwasu pirogronowego
D. ostatni odcinek łańcucha oddechowego
848. 1984/F
Kwas o wzorze:
CH
3
CH
2
CH
CH
2
CH
3
COOH
można otrzymać przez utlenienie związku o wzorze:
A. CH
3
CH
2
CH
2
CH
2
CH
2
OH
B. CH
3
CH
2
CH
2
CH
2
CHO
C. CH
3
CH
2
CH
CH
2
CH
3
D. CH
3
CH
CH
2
CH
2
CH
3
CH
2
OH
CHO
849.
Ile moli kwasu ftalowego jest potrzebne do zobojętnienia 120g NaOH?
A. 1 mol
B. 1.5 mola
C. 2 mole
D. 2.5 mola
E. 3 mole
Kwasy karboksylowe
135
850. 1984/F
Lek przeciwgorączkowy polopirynę, otrzymuje się w wyniku acylowania związku o wzorze:
A.
B.
C.
D.
COOH
OH
COOH
NH2
COOH
COOH
COOH
OH
851.
Które z wymienionych poniżej pochodnych kwasu salicylowego zaliczysz do estrów?
COOCH
3
OH
I.
C O
O
OH
II.
OH
COONa
III.
COOH
O C CH
3
O
IV.
COOH
OH
NH
2
V.
A. I, II, IV
B. II i IV
C. I i IV
D. I, II, III, V
E. wszystkie
852. 1985/F
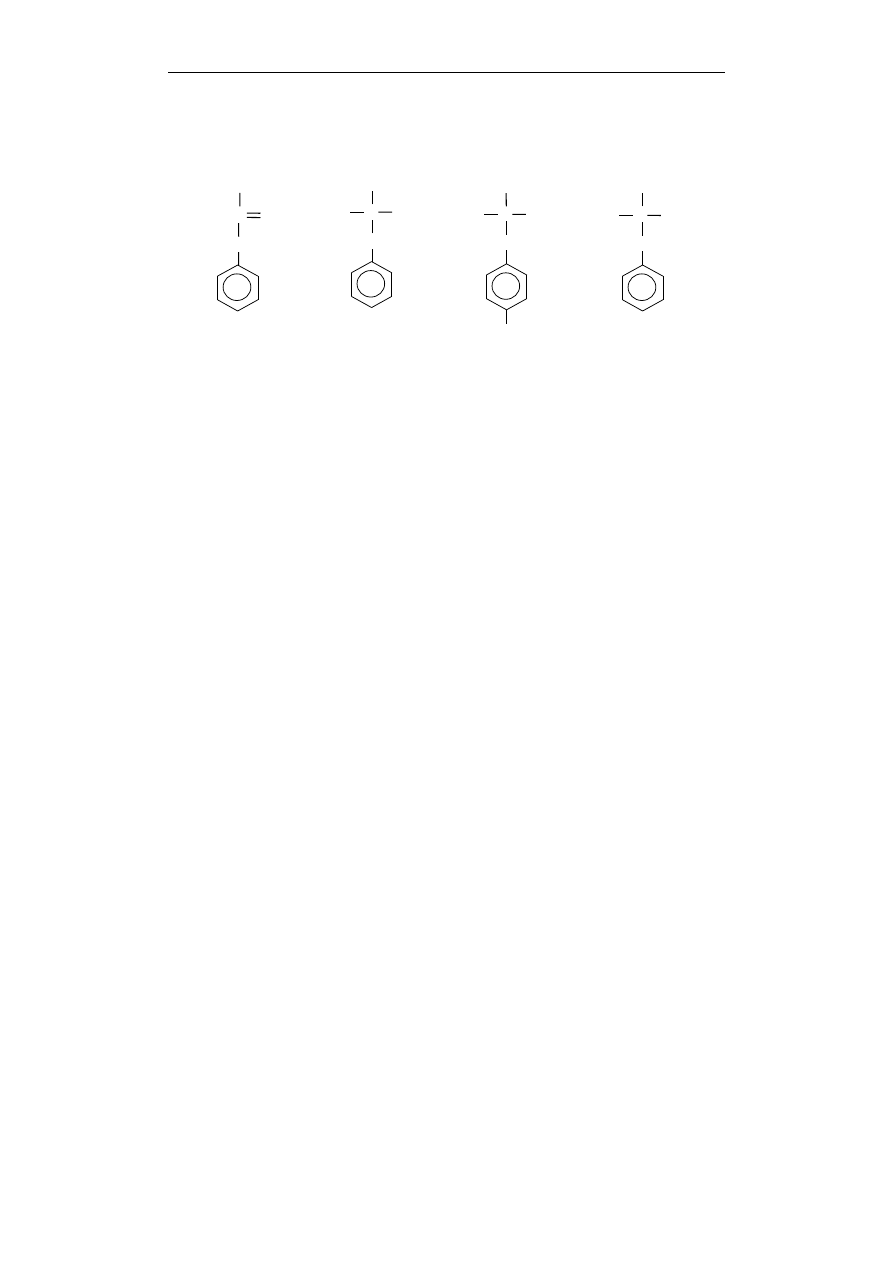
Które z niżej przedstawionych doświadczeń pozwala na porównanie mocy kwasu octowego
i benzoesowego?
853. 1985/F
W warunkach beztlenowych kwas pirogronowy kosztem NADH zostaje zredukowany w komórce
mięśniowej do produktu o podanej strukturze:
A.
B.
C.
D.
C
COOH
OH
CH3
H
C
OH
O
CH3
C
COOH
O
CH3
C
COOH
O
CH2OH

Chemia. Wybór testów...
136
854. 1986/F
Które ze zdań opisujące właściwości kwasu pirogronowego jest prawdziwe?
A. jest jednym z produktów hydrolizy kwasów dezoksyrybonukleinowych
B. zawiera w cząsteczce jeden asymetryczny atom węgla
C. w warunkach beztlenowych powstaje w komórce mięśniowej jako końcowy produkt przemiany
glikogenu
D. daje, w wyniku redukcji, hydroksykwas o tej samej liczbie atomów węgla w cząsteczce
855. 1987/F
Ile moli kwasu acetylosalicylowego powstanie w wyniku reakcji 2.5 mola kwasu salicylowego
z nadmiarem bezwodnika kwasu octowego?
A. 0.5 mola
B. 1 mol
C. 2.5 mola
D. 0.5 mola
856. 1993/L
W mięśniach ludzkich na skutek nadmiernego wysiłku fizycznego gromadzi się pewien związek
chemiczny, jest nim:
A. C
3
H
7
COOH
B. C
6
H
4
(OH)COOH
C. CH
2
(OH)
COOH
D. CH
3
CH(OH)
COOH
E. CH
3
COOH
857.
Ile gramów kwasu octowego należy użyć aby otrzymać 44g octanu etylu, jeżeli wydajność reakcji
wynosi 80%?
A. 24g
B. 30g
C. 37.5g
D. 6g
E. 48g
858. 2000/F
Wskaż w poniższym szeregu reakcje podstawienia.
octowy
kwas
etanal
etanol
bromoetan
etanol
eten
5
4
3
2
1
A. 1,2,3
B. 2, 3
C. 4, 5
D. 2, 3, 4
859. 1993/L
Na kwas mlekowy podziałano zasadą sodową w nadmiarze. W wyniku reakcji otrzymano:
A. CH
3
CH
COONa
B. CH
3
CH
COONa
C. CH
3
CH
COOH
ONa
OH
ONa
D. CH
3
CH
COOH
E. CH
3
CH
CONa
Na
OH
860. 1988/F
Przy użyciu papierka uniwersalnego uczeń stwierdził, że pH roztworu kwasu octowego o stężeniu
0.1 mol/dm
3
wynosi 3. Przybliżona wartość stałej dysocjacji kwasu octowego K
CH
COOH
(mol/dm
3
) oraz
stopień dysocjacji kwasu octowego
w badanym roztworze wynosi:
A. K = 10
-2
=10
-4
B. K = 10
-5
= 10
-1
C. K = 10
-4
= 10
-3
D. K = 10
-5
= 10
-2
861.
Ile cm
3
roztworu KOH o stężeniu 0.5 mol/dm
3
zobojętni roztwór zawierający 3.7g kwasu
propanowego?
A. 100 cm
3
B. 50 cm
3
C. 200 cm
3
D. 10 cm
3
E. 500 cm
3
862. 1989/F
Największą ilość bromu może przyłączyć 1 gram:
A. kwasu oleinowego
B. kwasu akrylowego C
3
H
4
O
2
C. chlorku winylu C
2
H
3
Cl
D. butadienu
3
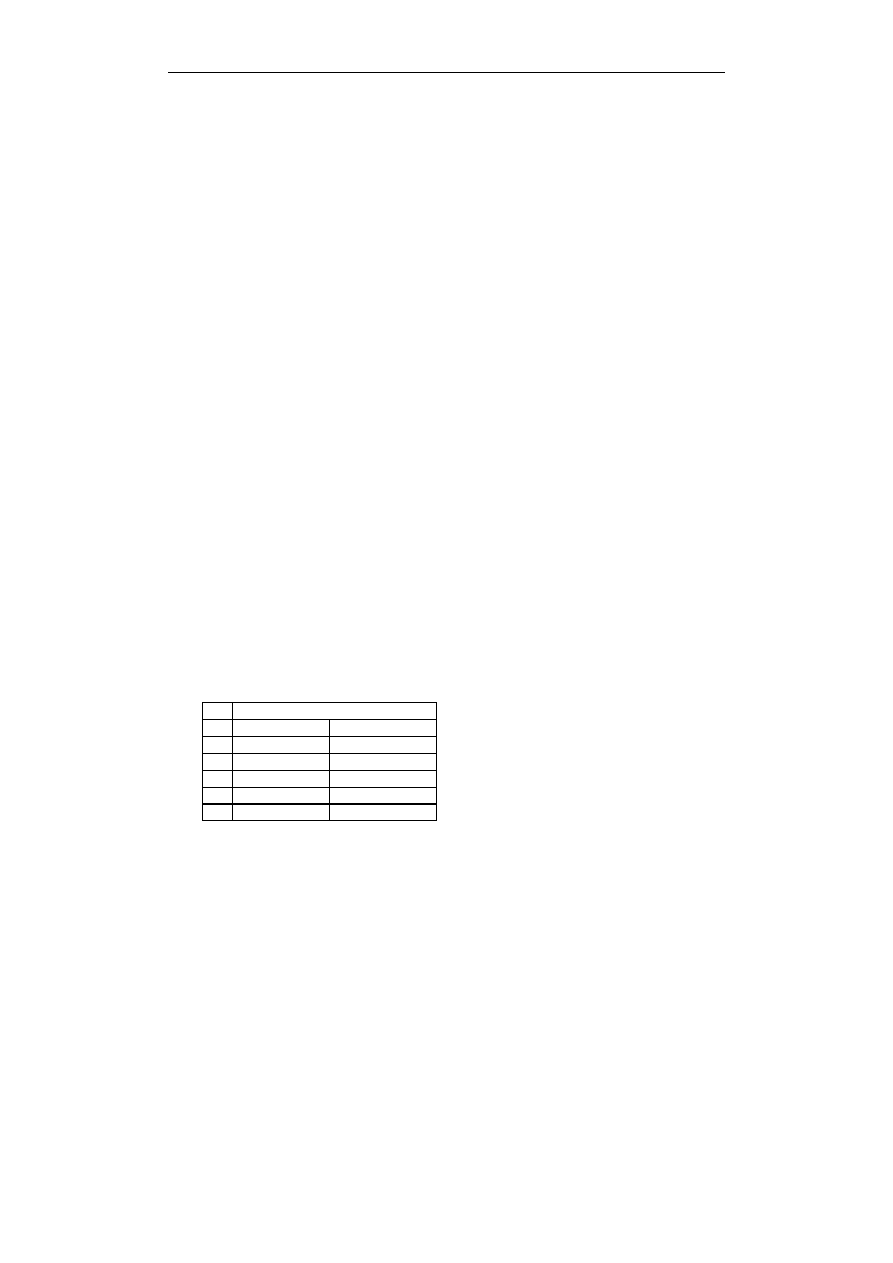
Kwasy karboksylowe
137
863. 1990/F
W wyniku rozerwania wiązania C
O w grupie karboksylowej można otrzymać:
A. amidy, estry i chlorki kwasowe
B. tylko estry
C. wyłącznie amidy
D. tylko estry i amidy kwasowe
864. 1990/F
Bardzo dobrą rozpuszczalność niskocząsteczkowych alkoholi i kwasów karboksylowych w wodzie
najlepiej wyjaśnia stwierdzenie:
A. wszystkie związki organiczne są dobrze rozpuszczalne w wodzie
B. między cząsteczkami wymienionych alkoholi, kwasów karboksylowych i wody tworzą się
wiązania wodorowe
C. małe rozmiary cząsteczek umożliwiają mieszanie się z cząsteczkami dowolnych
rozpuszczalników
D. długość łańcucha węglowego nie ma żadnego wpływu na rozpuszczalność w wodzie
865. 1981/AR
Na zobojętnienie roztworu zawierającego 0.74g kwasu organicznego jednokarboksylowego zużyto
50 cm
3
0.2 molowego NaOH. Masa cząsteczkowa tego kwasu wynosiła:
A. 46
B. 60
C. 74
D. 88
866.
Roztwór zawierający 1.15g nasyconego kwasu jednokarboksylowego zobojętniono za pomocą
roztworu zawierającego 1.4g KOH. Kwasem tym był:
A. HCOOH
B. CH
3
COOH
C. C
2
H
5
COOH
D. C
3
H
7
COOH
867.
W wyniku reakcji 110g nasyconego kwasu jednokarboksylowego z metalicznym magnezem
otrzymano 14 dm
3
wodoru (w przeliczeniu na warunki normalne). Reagującym kwasem był:
A. CH
3
COOH
B. C
2
H
5
COOH
C. C
3
H
7
COOH
D. C
4
H
9
COOH
868. 1982/AR
Jaki kwas powstanie przez utlenianie aldehydu, który ma taki sam wzór sumaryczny jak aceton?
A. kwas octowy
B. kwas propionowy
C. kwas masłowy D. kwas glicerynowy
869. 1992/L
Który z poniższych związków: etan, propan, eten, kwas octowy, alkohol metylowy i alkohol etylowy
ma najniższą, a który najwyższą temperaturę wrzenia?
temperatura wrzenia
min.
max.
A.
CH
3
OH
C
3
H
8
B.
CH
3
COOH
C
2
H
5
OH
C.
C
2
H
6
CH
3
COOH
D.
CH
3
OH
C
2
H
4
E.
C
2
H
4
CH
3
COOH
870.
I. Laktony są to estry wewnętrzne hydroksykwasów powstające w wyniku wydzielania cząsteczki
wody z hydroksykwasu.
II. Rozróżnia się
i
laktony zależnie od położenia grupy karboksylowej w stosunku do grupy
hydroksylowej w wyjściowym hydroksykwasie.
III. Laktony są cyklicznymi estrami.
Prawdziwymi są stwierdzenia:
A. I
B. II
C. III
D. I i III
E. wszystkie
Chemia. Wybór testów...
138
871.
W celu ustalenia składu mieszaniny kwasów mrówkowego i propionowego zobojętniono próbkę tej
mieszaniny o masie 1.94g przy pomocy 1 molowego roztworu KOH. Wiedząc, że na zobojętnienie tej
mieszaniny zużyto 30 cm
3
roztworu KOH obliczono jej skład. W skład mieszaniny wchodzi
(w procentach wagowych):
HCOOH
C
2
H
5
COOH
A.
25%
75%
B.
50%
50%
C.
23.7%
76.3%
D.
33.3%
66.7%
E.
19.4%
80.6%
872. 1979/F
Działanie myjące i piorące mydła jest bezpośrednio wynikiem:
A. wytrącania z wody soli wapniowych wyższych kwasów tłuszczowych
B. zmniejszania napięcia powierzchniowego wody
C. wytwarzania odczynu zasadowego wody
D. rozpuszczania tłuszczów przez mydło
873. 1982/F
Które z poniższych substancji są mydłami rozpuszczalnymi w wodzie?
I. CH
3
COONa
II. C
15
H
31
COONa
III. C
17
H
35
COOK
IV. (C
17
H
35
COO)
2
Ca
A. I i II
B. I i IV
C. II i III
D. III i IV
874. 1999/F
Podczas zmydlania 100 kg którego tłuszczu, otrzymano najwięcej moli mydła?
A. tripalmitynianu gliceryny
B. tristearynianu gliceryny
C. trioleinianu gliceryny
D. z wszystkich otrzymano tyle samo
875. 1992-94/MIS MaP
Do utworzenia bezwodnika cyklicznego nie jest zdolny kwas:
A. o-ftalowy
B. fumarowy
C. maleinowy
D. glutarowy
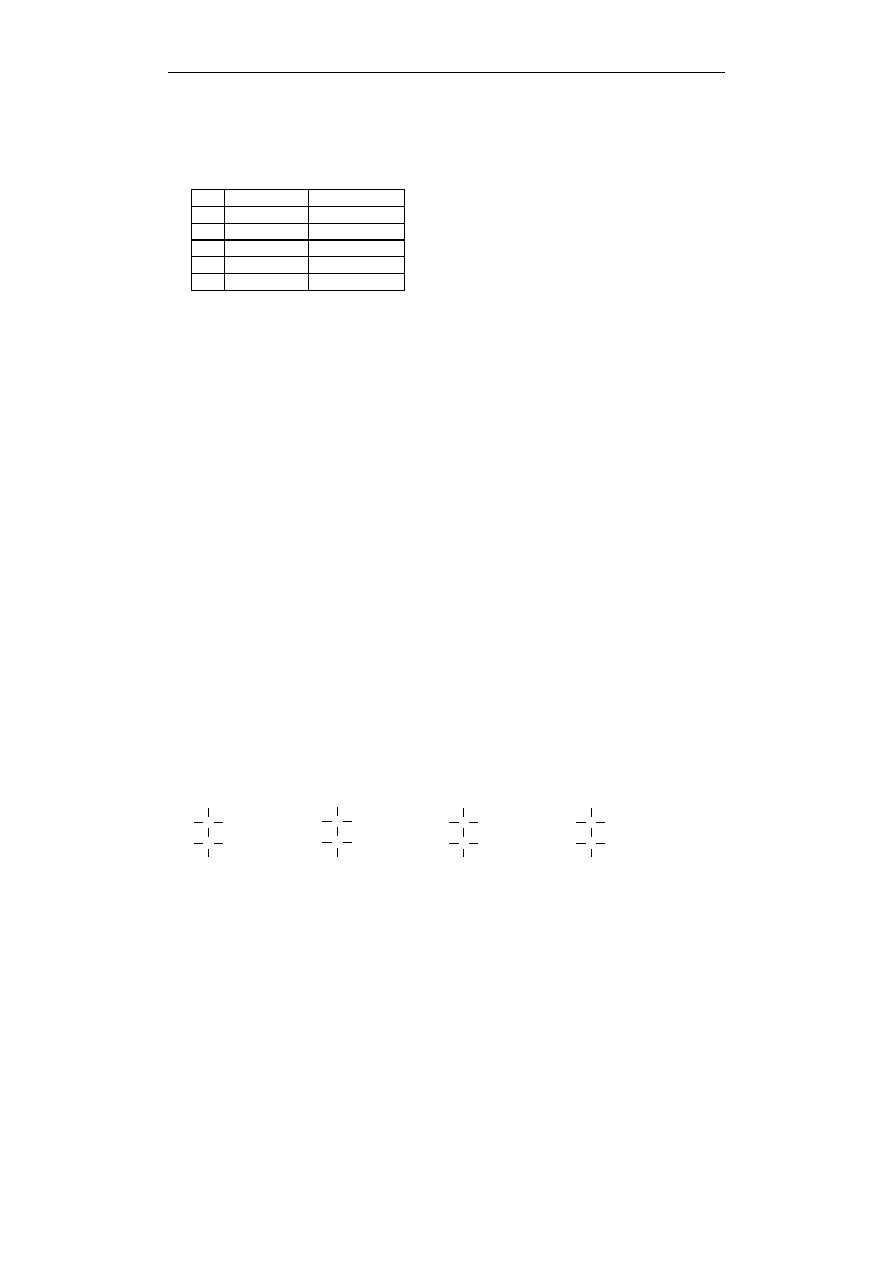
876. 2002/L
Który z podanych wzorów przedstawia cząsteczkę odmiany mezo kwasu winowego (1,2-dihydroksy-
1,2-etanodikarboksylowego):
COOH
C
C
COOH
OH
H
H
HO
COOH
C
C
COOH
H
HO
HO
H
COOH
C
C
COOH
OH
H
HO
H
COOH
C
C
COOH
OH
HO
H
H
A.
B.
C.
D.
Wyszukiwarka
Podobne podstrony:
KWASY KARBOKSYLOWE id 256009 Nieznany
kwasy karboksylowe 1 id 256027 Nieznany
BW13 KWASY NUKLEINOWE id 95709 Nieznany
3 kwasy nukleinowe id 33136 Nieznany (2)
KWASY DIKARBOKSYLOWE 2 id 25598 Nieznany
3 Kwasy nukleinowe id 33782 Nieznany
KWASY KARBOKSYLOWE 3 id 256015 Nieznany
KWASY KARBOKSYLOWE id 256009 Nieznany
kwasy karboksylowe 1 id 256027 Nieznany
BW13 KWASY NUKLEINOWE id 95709 Nieznany
kwasy id 255953 Nieznany
Abolicja podatkowa id 50334 Nieznany (2)
4 LIDER MENEDZER id 37733 Nieznany (2)
katechezy MB id 233498 Nieznany
metro sciaga id 296943 Nieznany
perf id 354744 Nieznany
interbase id 92028 Nieznany
Mbaku id 289860 Nieznany
więcej podobnych podstron