
1. a) MgO, Al
2
O
3
, SiO
2
, P
4
O
10
, SO
2
; b) Al
2
O
3
, SiO
2
, P
4
O
10
, SO
2
; c) Al
2
O
3
, SiO
2
, P
4
O
10
, MgO; d) Al
2
O
3
, SiO
2
;
e) Al
2
O
3
, MgO. Tlenek glinu.
Reakcje tlenków z:
kwasem solnym: MgO + 2 HCl
$ MgCl
2
+ H
2
O; Al
2
O
3
+ 6 HCl
$ 2 AlCl
3
+ 3 H
2
O
zasadà sodowà: SiO
2
+ 2 NaOH
$ Na
2
SiO
3
+ H
2
O; P
4
O
10
+ 12 NaOH
$ 4 Na
3
PO
4
+ 6 H
2
O
SO
2
+ 2 NaOH
$ Na
2
SO
3
+ H
2
O; Al
2
O
3
+ 2 NaOH + 3 H
2
O
$ 2 Na [Al(OH)
4
]
2. a) Mg
3
(PO
4
)
2
; b) 4 P + 5 O
2
$ P
4
O
10
; P
4
O
10
+ 6 H
2
O
$ 4 H
3
PO
4
; 2 Mg + O
2
$ 2 MgO;
Mg + 2 H
2
O
$ Mg(OH)
2
+ H
2
; MgO + H
2
O
$ Mg(OH)
2
; c) 3 Mg + 2 H
3
PO
4
$ Mg
3
(PO
4
)
2
+ 3 H
2
;
3 MgO + 2 H
3
PO
4
$ Mg
3
(PO
4
)
2
+ 3 H
2
O; 6 MgO + P
4
O
10
$ 2 Mg
3
(PO
4
)
2
;
6 Mg(OH)
2
+ P
4
O
10
$ 2 Mg
3
(PO
4
)
2
+ 6 H
2
O; 3 Mg(OH)
2
+ 2 H
3
PO
4
$ Mg
3
(PO
4
)
2
+ 6 H
2
O
3. 5,6 dm
3
dowolnego gazu (w przeliczeniu na warunki normalne) to 0,25 mola; liczb´ moli
n obli-
czamy wed∏ug wzoru:
n =
= 5,6 dm
3
: 22,4 dm
3
· mol
–1
= 0,25 mola.
O masie próbki decyduje masa molowa. Mas´ ka˝dej z próbek obliczamy ze wzoru:
m = n · M; m
NH
3
= 0,25 mola · 17 g/mol = 4,25 g;
m
N
2
O
=
m
CO
2
= 0,25 mol · 44 g/mol = 11 g. Równe obj´toÊci ga-
zów zawierajà jednakowe liczby czàsteczek.
4. a) N; b) N; c) P.
5. WartoÊci odczytujemy z wykresu, na przyk∏ad:
Masa tlenku
7 g
14 g
Masa metalu
5 g
10 g
%
metalu
=
· 100% =
· 100% = 71,428%
%
tlenu
= 100% – 71,428% = 28,572%
wzór ogólny tlenku: MeO; %Me =
: 100% = 71,428%
$ M
Me
= 4 O
$ Me to Ca;
wzór tlenku: CaO
6. 1 – c, 2 – a, 3 – d.
M
Me
––––––––––––––
M
Me
+ 16 g/mol
5 g
––––
7 g
m
metalu
–––––––
m
tlenku
V
–––
V
0
C h e m i a . P o z i o m p o d s t a w o w y
Chemia
Poziom podstawowy

O D P O W I E D Z I D O Z A D A ¡ T E S T O W Y C H . P R Ó B N A M A T U R A Z O P E R O N E M I „ G A Z E T Ñ W Y B O R C Z Ñ ”
■
7. 100 g H
2
O — 125 g NaNO
3
1000 g —
x
x = 1250 g
przyjmujemy, ˝e
d
H
2
O
= 1 g/cm
3
C
%
=
· 100% = · 100%=55,55%
8. Na
2
O + H
2
O
$ 2 NaOH
62 g — 80 g
36,5 g —
x
x = 47 g NaOH
m
s
= 47 g NaOH
m
r
= 200 g H
2
O + 36,5 g Na
2
O = 236,5 g
C
%
=
· 100% =
· 100% = 19,9%
Obj´toÊç otrzymanego roztworu:
236,5 g
V =
=
–––––––––––––
= 194 cm
3
= 0,194 dm
3
1,22 g/cm
3
Liczba moli NaOH:
n =
=
= 1,175 mola
C
mol
=
=
=6
9. a)
40
Ca, 20, 20, 40, 20, 60; b)
32
S
2–
, 16, 16, 32, 18, 50; c)
40
K
+
, 19, 21, 40, 18, 58;
d)
208
Pb
2+
, 82, 126, 208, 80, 288; e)
119
Sn
4+
, 50, 69, 119, 46, 165.
10. CH
2
=CH
2
+ Cl
2
$ CH
2
Cl—CH
2
Cl – 1,2-dichloroetan;
CH=
—
CH + 2 HCl
$ CH
3
—CHCl
2
– 1,1-dichloroetan.
11. C
2
H
5
OH + O
2
$ CH
3
COOH + H
2
O – roztwór zawiera 120 g kwasu octowego. Aby otrzy-
maç 120 g CH
3
COOH, nale˝y utleniç 92 g C
2
H
5
OH. Masa roztworu alkoholu = 500 g – masa tlenu
przy∏àczonego w procesie utleniania.
m
r
= 500 g – 64 g = 436 g;
C
%
=
· 100% = 21,1%.
12. a) 3-metylopentan-3-ol; b) np. C
5
H
11
OH, C
4
H
9
OH, C
8
H
17
OH;
c) np.
13. a)
CH
3
—CH—COO
–
—
NH
3
+
H
3
C—CH
2
—CH—CH
2
—CH
2
—CH
3
—
OH
H
3
C—CH
2
—CH—CH
CH
3
—
—
CH
3
—
OH
92 g
––––––
436 g
mol
–––––
dm
3
1,175 mola
–––––––––––
0,194 dm
3
n
––
V
47 g
–––––––––––
40 g/mol
m
––
M
m
r
–––
d
47 g
–––––––
236,5 g
m
s
––––
m
r
1250 g
–––––––
2250 g
m
s
––––––––––––
m
s
+
m
wody
C h e m i a . P o z i o m p o d s t a w o w y

b) Alanina wykazuje charakter amfoteryczny:
14. a) 2 Na + 2 H
2
O
$ 2 NaOH + H
2
– reakcja egzotermiczna; b) CH
4
+ 2 O
2
$ CO
2
+ 2 H
2
O
– reakcja egzotermiczna; c) CaCO
3
$ CaO + CO
2
– reakcja endotermiczna; d) CaO +
H
2
O
$ Ca(OH)
2
– reakcja egzotermiczna.
15. N
2
+ O
2
$ 2 NO; N
2
0
– 4 e
–
$ 2 N
II
; O
0
2
+ 4 e
–
$ 2 O
–II
; 4 NH
3
+ 5 O
2
$ 4 NO + 6 H
2
O;
N
–III
+ 5 e
–
$ N
II
| · 4; O
0
2
– 4 e
–
$ 2 O
–II
| · 5; 3 Cu + 8 HNO
3
$ 3 Cu(NO
3
)
2
+ 2 NO + 4 H
2
O;
Cu
II
– 2 e
–
$ Cu
II
| · 3; N
V
+ 3 e
–
$ N
II
| · 2
16. NH
3
+ H
2
O
#
$ NH
4
+
+ OH
–
; CH
3
NH
2
+ H
2
O
#
$ CH
3
NH
3
+
+ OH
–
; roztwory przewodzà pràd dzi´-
ki obecnym jonom, a fenoloftaleina barwi si´ pod wp∏ywem jonów wodorotlenkowych.
17. a) Ba
2+
+ SO
4
2–
$ BaSO
4
.; H
2
SO
4
+ BaCl
2
$ BaSO
4
. + 2 HCl; b) 699 g; c) czerwonà.
18.
a) 2 CO
2
; b) SO
2
; c) 2 CO
2
; d) CH
2
=CH
2
19. st´˝enie kwasu w 1. kolbie:
C
%1
= 8%
równanie reakcji: SO
3
+ H
2
O
$ H
2
SO
4
masa kwasu siarkowego(VI) = 9,8 g
st´˝enie kwasu w 2. kolbie:
C
%2
= 9,8%
20. a) 17 grupa, 2 okres
b) niemetaliczny
c) 0, –I
21. podpunkt a;
produkt reakcji z wodà bromowà: wzór CH
2
Br—CHBr—CHO
nazwa: 2,3-dibromopropanal
produkt reakcji z odczynnikiem Tollensa:
wzór: CH
2
=
CH—COOH, nazwa: kwas propenowy
22.
3
7
5
9
Br – liczba nukleonów = 79, liczba elektronów walencyjnych = 7
3
8
5
1
Br – liczba nukleonów = 81, liczba elektronów walencyjnych = 7
23. obliczenie w 1. roztworze: 0,5 mola jonów chlorkowych
obliczenie w 2. roztworze: 0,6 mola jonów chlorkowych
24.
22
8
2
6
Rn
25.
A – C
2
H
5
OH, etanol
B – CH
3
CHO, etanal
C – CH
3
COOH, kwas etanowy
1) CH
3
CHO + Ag
2
O
$ CH
3
COOH + 2 Ag
2) C
2
H
5
OH + CuO
$
CH
3
CHO + H
2
O + Cu
CH
3
—CH—COO
–
+
H
$
CH
3
—CH—COOH
—
NH
3
—
NH
3
CH
3
—CH—COO
–
+
OH
–
$
CH
3
—CH—COO
–
+
H
2
O
—
NH
3
—
NH
2
+
+
+
+
O D P O W I E D Z I D O Z A D A ¡ T E S T O W Y C H . P R Ó B N A M A T U R A Z O P E R O N E M I „ G A Z E T Ñ W Y B O R C Z Ñ ”
■
C h e m i a . P o z i o m p o d s t a w o w y

O D P O W I E D Z I D O Z A D A ¡ T E S T O W Y C H . P R Ó B N A M A T U R A Z O P E R O N E M I „ G A Z E T Ñ W Y B O R C Z Ñ ”
■
26. W∏aÊciwoÊci substancji o wiàzaniu jonowym: a, c i d; w∏aÊciwoÊci substancji o wiàzaniu kowa-
lencyjnym: b, e i f.
27. a) 28, czàsteczek, 22,4; b) 2, 8, atomów, 44,8; c) 1,2; d) 27.
28. 2 KMnO
4
$ K
2
MnO
4
+ MnO
2
+ O
2
2 · 158 g KMnO
4
— 22,4 dm
3
O
2
50 g KMnO
4
—
x
x = 3,5 dm
3
O
2
29. 1 – D; 2 – C; 3 – B; 4 – D; 5 – A.
30.
C
%
= ;
m
r
= 1,33 g;
d = 1,33 g/cm
3
;
C
m
= =
10
;
31. Reakcje utleniania i redukcji zajdà w probówkach: 1 i 3.
1) 3 Zn + 2 Fe
3+
$ 3 Zn
2+
+ 2 Fe – utleniacz: Fe
3+
, reduktor: Zn
2) Fe + 2 H
+
$ Fe
2+
+ H
2
– utleniacz: H
+
, reduktor: Fe
32.
33.
34.
A: CH=
—
C—CH
3
;
B: CH
3
—CHOH—CH
3
;
C: .
——
O
CH
3
—C—CH
3
mol
–––––
dm
3
0,4 g
–––––––––––––––––––––
40 g/mol · 0,001 dm
3
m
s
· 100%
––––––––––––
m
r
C h e m i a . P o z i o m p o d s t a w o w y
W∏aÊciwoÊç
Wzór zwiàzku
mocny kwas
H
2
SO
4
substancja higroskopijna
NaOH
tlenek o charakterze kwasowym
SO
3
tlenek o budowie jonowej
K
2
O
sól trudno rozpuszczalna w wodzie
Ca
3
(PO
4
)
2
kwas, którego wszystkie sole sà dobrze
rozpuszczalne w wodzie
HNO
3
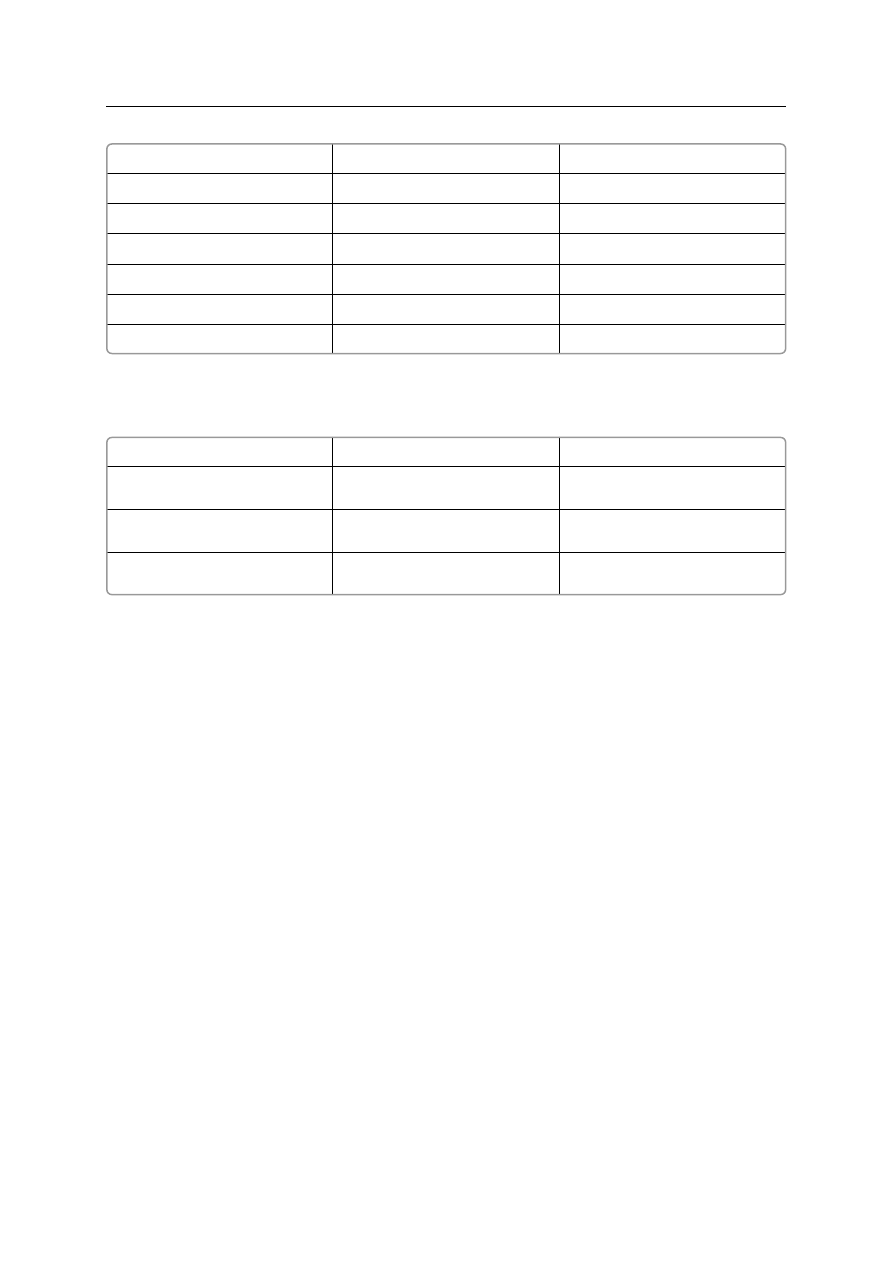
Typ zwiàzku
Wzory zwiàzków
B∏´dnie (omy∏kowo)
wpisane wzory
zwiàzków
tlenki zasadowe
MgO, Li
2
O, CaO, BeO
BeO
tlenki reagujàce z wodà
CaO, SO
2
, P
4
O
10
, SO
3
—
mocne kwasy
HNO
3
, HCl, HBr, HClO
4
—
kwasy wieloprotonowe
H
3
PO
4
, H
4
P
2
O
7
, HPO
3
, H
3
PO
3
HPO
3
zwiàzki trudno rozpuszczalne w wodzie
Mg
3
(PO
4
)
2
, Mg(OH)
2
, MgCO
3
, MgSO
4
MgSO
4
silne reduktory
Ca, Mg, CO, SO
2
, F
2
F
2
35.
36. 1 – B; 2 – E; 3 – C.
37.
38. S + O
2
$ SO
2
SO
2
+
O
2
$ SO
3
SO
3
+ Ba(OH)
2
$ BaSO
4
+ H
2
O
masa osadu:
1 mol S — 233 g BaSO
4
0,1 mola —
x
x
= 23,3 g
39. przyk∏adowa para substancji (rozpuszczalna sól wapnia i rozpuszczalny fosforan, np. Ca(NO
3
)
2
,
Na
3
PO
4
.
czàsteczkowe równanie reakcji np.: 3 Ca(NO
3
)
2
+ 2 Na
3
PO
4
$ Ca
3
(PO
4
)
2
+ 6 NaNO
3
skrócone jonowego równania reakcji: 3 Ca
2+
+ 2 PO
4
3–
$ Ca
3
(PO
4
)
2
40. 2 i 3
41. obliczenie masy molowej pierwiastka
II –II
MeO
=
=
M
Me
=
· 16 g/mol = 40 g/mol
& Ca
2 Ca + O
2
$ 2 CaO
5
––
2
5
––
2
M
Me
–––––––––––
16g/mol
5
––
2
M
Me
–––––
M
O
1
––
2
O D P O W I E D Z I D O Z A D A ¡ T E S T O W Y C H . P R Ó B N A M A T U R A Z O P E R O N E M I „ G A Z E T Ñ W Y B O R C Z Ñ ”
■
C h e m i a . P o z i o m p o d s t a w o w y
Substancja
Etanol
Fenol
Na
+
+
NaOH
–
+
HNO
3
+
+
CH
3
COOH
+
+
woda bromowa
–
+
Na
2
CO
3
–
–
Nazwa procesu
Nr probówki
Obserwacje
wysalanie
2
Powstaje bia∏y, k∏aczkowaty
osad, bia∏ko si´ „Êci´∏o”.
reakcja biuretowa
3
Roztwór w probówce zabarwia
si´ na kolor ró˝owofioletowy.
reakcja ksantoproteinowa
1
ZawartoÊç probówki przyjmuje
˝ó∏te zabarwienie.

O D P O W I E D Z I D O Z A D A ¡ T E S T O W Y C H . P R Ó B N A M A T U R A Z O P E R O N E M I „ G A Z E T Ñ W Y B O R C Z Ñ ”
■
42.
=
=
m
NH
3
=
m
HCl
·
m
NH
3
= 7,3 g ·
= 3,4 g NH
3
4 g – 3,4 g = 0,6 g NH
3
43.
zawartoÊç
X w stopie:
100% – 90,8% = 9,2%
m
X
= 0,092 · 70,5 g = 6,49 g
X + 2 HCl
$ X Cl
2
+ H
2
n
X
=
n
wodoru
=
= 0,1 mola
M
X
= =
=
64,9
g/mol
X = Zn
44. A – 1; B – 4; C – 3; D – 2
45. 1 – A, B, E; 2 – C, D
46. tlenek wapnia; tlenek zasadowy; CaO + H
2
O
$ Ca(OH)
2
tlenek siarki(VI); tlenek kwasowy; SO
3
+ H
2
O
$ H
2
SO
4
tlenek potasu; tlenek zasadowy; K
2
O + H
2
O
$ 2 KOH
47. liczba protonów: 16; liczba elektronów: 18; liczba neutronów: 16
48. przemiana
b
–
49. rozpuszczalna sól wapnia, np. CaCl
2
, Ca(NO
3
)
2
rozpuszczalny w´glan, np. Na
2
CO
3
, K
2
CO
3
, (NH
4
)
2
CO
3
kwasy, np. HCl, HNO
3
Przyk∏ad opisu:
Do roztworu CaCl
2
dodajemy roztwór Na
2
CO
3
. Wytràca si´ osad w´glanu wapnia. Do odsàczo-
nego osadu dodajemy roztwór kwasu solnego. Osad si´ roztwarza, powstaje klarowny roztwór
zawierajàcy jony wapnia.
równania czàsteczkowe
CaCl
2
+ Na
2
CO
3
$ CaCO
3
. + 2 NaCl
CaCO
3
+ 2 HCl
$ CaCl
2
+ CO
2
+ H
2
O
równania jonowe
Ca
2+
+ CO
3
2–
$ CaCO
3
.
CaCO
3
. + 2 H
+
$ Ca
2+
+ H
2
O + CO
2
50.
–II 0
S
$ S + 2
e
–
/ . 2
IV
0
S + 4
e
–
$ S / . 1
6,49 g
––––––––––
0,1 mola
m
–––
n
2,24 dm
3
–––––––––––––––––
22,4 dm
3
/mol
17 g/mol
––––––––––––––
36,5 g/mol
17
–––––
36,5
17 g/mol
––––––––––––
36,5/mol
m
NH
3
–––––
m
HCl
1
––
1
n
NH
4
–––––
n
HCl
C h e m i a . P o z i o m p o d s t a w o w y

zbilansowanie liczby elektronów w równaniach po∏ówkowych
–II 0
2 S
$ 2 S + 4
e
–
IV
0
S + 4
e
–
$ S
–II IV
0
2 S + S
$ 3 S
wspó∏czynniki w równaniu
2 H
2
S + SO
2
$ 3 S + 2 H
2
O
wskazanie utleniacza i reduktora
IV –II
utleniacz: S, reduktor: S
O D P O W I E D Z I D O Z A D A ¡ T E S T O W Y C H . P R Ó B N A M A T U R A Z O P E R O N E M I „ G A Z E T Ñ W Y B O R C Z Ñ ”
■
C h e m i a . P o z i o m p o d s t a w o w y

O D P O W I E D Z I D O Z A D A ¡ T E S T O W Y C H . P R Ó B N A M A T U R A Z O P E R O N E M I „ G A Z E T Ñ W Y B O R C Z Ñ ”
■
C h e m i a . P o z i o m p o d s t a w o w y
Numer
zadania
Punktacja czàstkowa
Maksymalna
liczba punktów
1
15–17 przyporzàdkowaƒ – 3 pkt
12–14 przyporzàdkowaƒ – 2 pkt
9–11 przyporzàdkowaƒ – 1 pkt
wskazanie tlenku glinu – 1 pkt
napisanie równania reakcji – 1 pkt
6
2
podanie wzoru soli – 1 pkt
napisanie równania reakcji z b – 5x1 pkt
napisanie równania reakcji z c – 5x1 pkt
11
3
obliczenie masy próbek – 1 pkt
porównanie liczby czàsteczek – 1 pkt
2
4
3 przyporzàdkowania – 2 pkt
2 przyporzàdkowania – 1 pkt
2
5
odczytanie danych z wykresu – 1 pkt
obliczenie sk∏adu procentowego – 1 pkt
ustalenie wzoru – 2 pkt
4
6
za ka˝de przyporzàdkowanie – po 1 pkt
3
7
obliczenie masy soli, którà nale˝y rozpuÊciç w 1 dm
3
wody – 1 pkt
obliczenie st´˝enia procentowego – 1 pkt
2
8
napisanie równania reakcji – 1 pkt
obliczenie masy NaOH – 1 pkt
obliczenie masy roztworu – 1 pkt
obliczenie
C
%
– 1 pkt
obliczenie moli NaOH – 1 pkt
obliczenie obj´toÊci roztworu – 1 pkt
obliczenie
C
m
– 1 pkt
7
9
za uzupe∏nienie ka˝dego wiersza tabeli – 1 pkt
5
10
za ka˝de równanie reakcji – po 1 pkt
podanie nazw – 1 pkt
3
11
napisanie równania reakcji – 1 pkt
obliczenie masy alkoholu – 1 pkt
obliczenie masy roztworu – 1 pkt
obliczenie st´˝enia – 1 pkt
4
12
podanie nazwy – 1 pkt
podanie wzoru homologu – 1 pkt
podanie wzorów izomerów – 2 pkt
4
13
a – 1 pkt
b – równania reakcji – 2 pkt
3
14
napisanie równania reakcji – 4x1 pkt
zaklasyfikowanie 4 reakcji do odpowiednich procesów – 2 pkt
6

O D P O W I E D Z I D O Z A D A ¡ T E S T O W Y C H . P R Ó B N A M A T U R A Z O P E R O N E M I „ G A Z E T Ñ W Y B O R C Z Ñ ”
■
C h e m i a . P o z i o m p o d s t a w o w y
Numer
zadania
Punktacja czàstkowa
Maksymalna
liczba punktów
15
dla ka˝dej przemiany:
za równanie reakcji – 1 pkt
za bilans elektronowy – 1 pkt
6
16
wskazanie roztworów przewodzàcych pràd – 1 pkt
napisanie równania reakcji – 2x1 pkt
3
17
a – równanie czàsteczkowe – 1 pkt
równanie jonowe – 1 pkt
b – 1 pkt
c – 1 pkt
4
18
za uzupe∏nienie ka˝dego równania reakcji – 1 pkt
4
19
obliczenie st´˝enia kwasu w 1. kolbie – 1 pkt
napisanie równania reakcji – 1 pkt
obliczenie masy kwasu siarkowego(VI) – 1 pkt
obliczenie st´˝enia kwasu w 2. kolbie – 1 pkt
4
20
za ka˝dy podpunkt – po 1 pkt
3
21
za wskazanie podpunktu a – 1 pkt
podanie produktu reakcji z wodà bromowà (wzór i nazwa) – 1 pkt
podanie produktu reakcji z odczynnikiem Tollensa (wzór i nazwa) – 1 pkt
3
22
podanie symboli izotopów – 1 pkt
podanie liczby nukleonów – 1 pkt
podanie liczby elektronów walencyjnych – 1 pkt
3
23
obliczenie w ka˝dym roztworze – po 1 pkt
2
24
podanie symbolu pierwiastka – 1 pkt
podanie liczby atomowej i liczby masowej – 1 pkt
2
25
za podanie wzorów i nazw – po 1 pkt
za napisanie równaƒ reakcji – po 1 pkt
5
26
podanie nazw wiàzaƒ – 1 pkt
6–5 poprawnych przyporzàdkowaƒ – 2 pkt
4–3 poprawne przyporzàdkowania – 1 pkt
3
27
9–8 poprawnych obliczeƒ – 4 pkt
7–6 poprawnych obliczeƒ – 3 pkt
5–4 poprawne obliczenia – 2 pkt
3–2 poprawne obliczenia – 1 pkt
4
28
obliczenie obj´toÊci tlenu – 2 pkt
2
29
przyporzàdkowanie równania – 5x1 pkt
5
30
obliczenie g´stoÊci roztworu – 1 pkt
obliczenie st´˝enia molowego roztworu – 1 pkt
2
31
za podanie numerów probówek – 1 pkt
za równania reakcji – 2x1 pkt
za wskazanie utleniacza i reduktora – 1 pkt
5

O D P O W I E D Z I D O Z A D A ¡ T E S T O W Y C H . P R Ó B N A M A T U R A Z O P E R O N E M I „ G A Z E T Ñ W Y B O R C Z Ñ ”
■
C h e m i a . P o z i o m p o d s t a w o w y
Numer
zadania
Punktacja czàstkowa
Maksymalna
liczba punktów
32
podanie 6 wzorów – 3 pkt
podanie 5–4 wzorów – 2 pkt
podanie 3 wzorów – 1 pkt
3
33
wpisanie 4 zwiàzków – 2 pkt
wpisanie 3 zwiàzków – 1 pkt
2
34
za ka˝dy wzór – po 1 pkt
3
35
za ka˝dy wype∏niony wiersz tabeli – po 1 pkt
6
36
za ka˝de poprawne przyporzàdkowanie – po 1 pkt
3
37
za wype∏nienie ka˝dej komórki tabeli – po 1 pkt
6
38
napisanie 2 równaƒ reakcji – 1 pkt
napisanie równania reakcji – 1 pkt
obliczenie masy osadu – 1 pkt
3
39
podanie przyk∏adowej pary substancji – 1 pkt
napisanie czàsteczkowego równania reakcji – 1 pkt
napisanie skróconego jonowego równania reakcji – 1 pkt
3
40
podanie numerów – 1 pkt
1
41
obliczenie masy molowej pierwiastka – 1 pkt
podanie symbolu Ca – 1 pkt
napisanie równania reakcji – 1 pkt
3
42
podanie stosunku molowego substratów reakcji – 1 pkt
wyliczenie masy jednego substratu – 1 pkt
wyliczenie iloÊci amoniaku – 1 pkt
3
43
rozwiàzanie zadania – 3 pkt
podanie nazwy – 1 pkt
4
44
4 prawid∏owe przyporzàdkowania – 3 pkt
3 prawid∏owe przyporzàdkowania – 2 pkt
2 prawid∏owe przyporzàdkowania – 1 pkt
3
45
podanie 5 prawid∏owych w∏aÊciwoÊci – 2 pkt
podanie 4 prawid∏owych w∏aÊciwoÊci – 1 pkt
2
46
za prawid∏owe uzupe∏nienie ka˝dego wiersza tabeli – po 1 pkt
3
47
podanie prawid∏owego zestawu wartoÊci – 1 pkt
1
48
okreÊlenie typu przemiany – 1 pkt
1
49
podanie zestawu odczynników – 1 pkt
opisanie doÊwiadczenia – 1 pkt
za napisanie równaƒ czàsteczkowych – po 1 pkt
za napisanie równaƒ jonowych – po 1 pkt
6
50
napisanie równaƒ po∏ówkowych – 1 pkt
zbilansowanie liczby elektronów w równaniach po∏ówkowych – 1 pkt
uzgodnienie wspó∏czynników w równaniu – 1 pkt
wskazanie utleniacza i reduktora – 1 pkt
4
Wyszukiwarka
Podobne podstrony:
2 Próbna matura 2008 poz rozszerz odp
1 Próbna matura 2008 poz post
3 Próbna matura 2008 poz rozszerz odp koment(1)
2 Próbna matura 2008 poz rozszerz odp
2 Próbna matura 2008 poz rozszerz
MATEMATYKA (rozszerzony) probna 2008, PROBNA MATURA GRU2007 Matematyka PR odp
MATEMATYKA (podstawowy)probna 2008 PROBNA MATURA GRU2007 Matematyka PP odp
Odpowiedzi Test przed probna matura 2008 Arkusz PR Wos
PROBNA MATURA GRU2007 Chemia PP odp
Odpowiedzi Test przed probna matura 2008 Arkusz PP Matematyka
Odpowiedzi Test przed probna matura 2008 Arkusz PR Fizyka
PROBNA MATURA GRU2007 Geografia PP odp
Matura 2008 WOS podstawowy odp
PROBNA MATURA GRU2007 Rosyjski PR odp
więcej podobnych podstron