
1
w w w. o p e r o n . p l
Modele odpowiedzi do arkusza Próbnej Matury z OPERONEM
Chemia
Poziom podstawowy
Listopad 2008
Nr
zadania
Modele odpowiedzi
Suma
punktów
1.
po praw ne uzu pe∏ nie nie ka˝ de go wier sza ta be li – po 1 pkt
3
2.
po praw ne za pi sa nie ka˝ de go rów na nia re ak cji – po 1 pkt
Ca + 2 H
2
O
$ Ca(OH)
2
+ H
2
-
Ca(OH)
2
+ SO
3
$ Ca SO
4
+ H
2
O
lub:
H
2
O + SO
3
$ H
2
SO
4
H
2
SO
4
+ Ca
$ Ca SO
4
+ H
2
-
2
3.
po da nie ob ser wa cji – 1 pkt
Wy dzie la si´ bez barw ny (i bez won ny) gaz.
za pi sa nie rów na nia re ak cji – 1 pkt
Na
2
CO
3
+ H
2
SO
4
$ Na
2
SO
4
+ H
2
O + CO
2
-
2
4.
po da nie licz by po w∏ok elek tro no wych i licz by elek tro nów wa len cyj nych – 1 pkt
Licz ba po w∏ok elek tro no wych: 5, licz ba elek tro nów wa len cyj nych: 2
1
5.
po da nie sym bo li lub nazw od po wied nich pier wiast ków – 1 pkt
K i F
po da nie wzo ru i na zwy zwiàz ku tych pier wiast ków – 1 pkt
KF, flu orek po ta su
2
6.
po da nie kon fi gu ra cji elek tro no wej – 1 pkt
1s
2
2s
2
2p
6
3s
2
3p
6
wska za nie elek tro nów wa len cyj nych – 1 pkt
3s
2
3p
6
po da nie w∏a Êci wo Êci che micz nych – 1 pkt
Bu do wa elek
tro no wa ato
mu wska
zu je na prak
tycz nie ca∏
ko wi tà bier
noÊç che
micz nà pier
-
wiast ka.
3
7.
za pi sa nie rów na nia re ak cji – 1 pkt
Zn + 2 HCl
–
" ZnC l
2
+ H
2
-
me to da ob li cze nia ob j´ to Êci wo do ru – 1 pkt
np: 65 g Zn – 22,4 dm
3
H
2
20 g Zn – x dm
3
H
2
po da nie wy ni ku wraz z jed nost kà – 1 pkt
6,89 dm
3
H
2
3
8.
ob li cze nie ma sy sub stan cji w pierw szym roz two rze – 1 pkt
m
s
=
= 40 g
ob li cze nie ma sy sub stan cji w dru gim roz two rze – 1 pkt
m
s
=
M · V · C
m
= 111,75 g
ob li cze nie st´ ˝e nia pro cen to we go pozostałego roz two ru – 1 pkt
C
p
= =
· 100% = 4,46%
m
s
m
r
40 g + 111,75 g
400 g + 3000 g
C
p
·
m
r
100%
3
Wzór tlen ku
Cha rak ter che micz ny tlen ku
Rów na nie re ak cji tlen ku z wo dà
CO
2
kwa so wy
CO
2
+ H
2
O
$ H
2
CO
3
Na
2
O
za sa do wy
Na
2
O + H
2
O
$ 2 Na OH
P
4
O
10
kwa so wy
P
4
O
10
+ 6 H
2
O
$ 4 H
3
PO
4
Chemia. Poziom podstawowy
Próbna Matura z OPERONEM i „Gazetà Wyborczà”
2
w w w. o p e r o n . p l
Nr
zadania
Modele odpowiedzi
Suma
punktów
9.
za na pi sa nie ka˝ de go ze wzo rów – po 1 pkt
Octan ety lu: CH
3
–CO OC
2
H
5
Izo mer, np: CH
3
–CH
2
–CH
2
–CO OH
2
10.
za na pi sa nie ka˝ de go rów na nia wraz z po da niem wa run ków – po 1 pkt
a) H
3
C–CH
2
–CH=CH
2
+ H
2
H
3
C–CH
2
–CH
2
–CH
3
b)
H
2
C–CH
2
=CH
2
+ H
2
O
c)
Al
2
O
3
, temp.
H
3
C – CH
2
– CH
2
OH
Pt
3
11.
na pi sa nie wzo ru po li me ru – 1 pkt
–CF
2
–CF
2
–CF
2
–CF
2
–CF
2
–CF
2
–CF
2
–CF
2
–
1
12.
za pi sa nie ob ser wa cji – 1 pkt
Bar wa osa du w pro bów ce zmie nia si´ z nie bie skiej na czer wo nà (po ma raƒ czo wà).
na pi sa nie rów na nia re ak cji – 1 pkt
2 Cu(OH)
2
+ HCHO
" Cu
2
O
. + HCO OH + 2 H
2
O
lub
2 Cu(OH)
2
+ HCHO + Na OH
" Cu
2
O + HCO ONa + 3 H
2
O
po da nie na zwy pro ce su – 1 pkt
Utle nia nie lub de ze lek tro na cja
3
13.
po da nie wszyst kich od po wie dzi – 1 pkt
a) 1 mol, b) 2 mo le, c) 3 mo le
1
14.
za pi sa nie wzo ru kwa su – 1 pkt
H
3
C – (CH
2
)
16
– COOH
1
15.
ob li cze nie ma sy 3 dm
3
t∏usz czu – 1 pkt
m
t∏usz czu
= V · d = 2790 g
ob li cze nie ma sy kwa su – 1 pkt
m = 0,52 · m
t∏usz czu
= 1450,8 g
2
16.
po da nie wzo rów jo nów – 1 pkt
Fe
3+
, SO
4
2–
, H
+
(lub H
3
O
+
), OH
–
za pi sa nie rów na nia w po sta ci czà stecz ko wej – 1 pkt
Fe
2
(SO
4
)
3
+ 6 KOH
" 2 Fe(OH)
3
. + 3 K
2
SO
4
za pi sa nie rów na nia re ak cji w po sta ci jo no wej skróconej – 1 pkt
Fe
3+
+ 3 OH
–
" Fe(OH)
3
.
3
17.
sfor mu ∏o wa nie wnio sku – 1 pkt
Szyb koÊç re ak cji che micz nej jest za le˝ na od st´ ˝eƒ sub stra tów. Im wi´k sze st´ ˝e nie sub stra -
tów, tym re ak cja prze bie ga szyb ciej.
po da nie po praw nej od po wie dzi – 1 pkt
szyb koÊç re ak cji wzro Ênie
2
18.
na pi sa nie rów na nia re ak cji dy so cja cji – 1 pkt
CH
3
CO OH
E CH
3
COO
–
+ H
+
lub CH
3
CO OH + H
2
O
E CH
3
COO
–
+ H
3
O
+
me to da ob li cze nia stop nia dy so cja cji – 1 pkt
po da nie wy ni ku – 1 pkt
α =
· 100% = 1,3%
[H
+
]
C
0
3
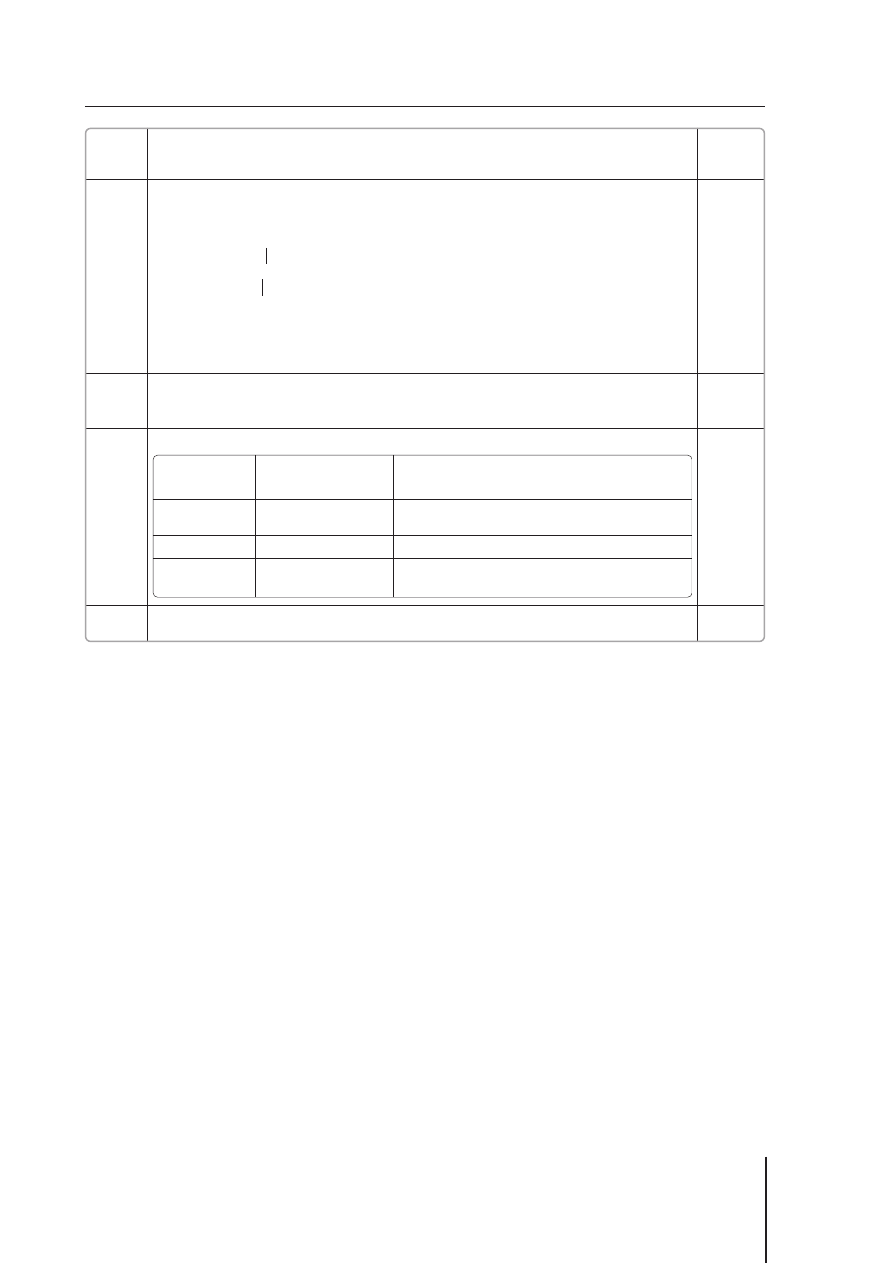
NO
2
NO
2
NO
2
+ HNO
3
+ H
2
O
H
2
SO
4
st., temp.
3
w w w. o p e r o n . p l
Chemia . Poziom podstawowy
Próbna Matura z OPERONEM i „Gazetà Wyborczà”
Nr
zadania
Modele odpowiedzi
Suma
punktów
19.
po da nie re duk to ra i utle nia cza – 1 pkt
Re duk tor:
, utle niacz:
prze pro wa dze nie bi lan su elek tro no we go – 1 pkt
+ 5e
–
"
· 2
2
"
+ 2e
–
· 5
2
+ 10
" 2
+
zbi lan so wa nie rów na nia re doks – 1 pkt
2 MnO
4
–
+ 10 Br
–
+ 16 H
+
" 2 Mn
2+
+ 5 Br
2
+ 8 H
2
O
VII
Mn
–I
Br
VII
Mn
0
Br
2
–I
Br
0
Br
2
VII
Mn
II
Mn
–I
Br
–
VII
MnO
4
–
3
20.
po da nie ob ser wa cji w ka˝ dym z do Êwiad czeƒ – po 1 pkt
Fio le to wy roz twór od bar wi∏ si´ w pro bów ce a).
W pro bów ce b) z roz two ru wy trà ci∏ si´ bru nat ny osad.
2
21.
po praw ne uzu pe∏ nie nie ka˝ de go wier sza ta be li – po 1 pkt
3
22.
po da nie ka˝ de go ze stop ni utle nie nia – po 1 pkt
N: – III, C: 0
2
Typ
roz two ru
Przy k∏ad
W∏a Êci wo Êci
roz twór
w∏a Êci wy
roz twór glu ko zy
w wo dzie
czàst ki sub stan cji roz pusz czo nej nie sà wi docz ne
go ∏ym okiem ani pod mi kro sko pem
ko lo idal ny
mg∏a
wy ka zu je efekt Tyn dal la
za wie si na
mie sza ni na pia sku
i wo dy
ule ga szyb kie mu roz dzie le niu si´ na roz pusz czal -
nik i sub stan cj´ roz pusz czo nà
Wyszukiwarka
Podobne podstrony:
2007 operon klucz chemia pp
2010 klucz chemia pp
2007 operon klucz chemia pr
2010 klucz chemia pp
biologia 2009 pp operon klucz
2010 operon chemia pp
chemia pp pr odp klucz(1) id 11 Nieznany
2007 operon chemia pp
chemia pp 2011 operon
więcej podobnych podstron