
Chemia organiczna
Instrukcje do ćwiczeń laboratoryjnych dla
Biologii (I rok)
Zakład Chemii Organicznej
Wydział Chemii
Uniwersytet Wrocławski
2005

Lista wykonywanych ćwiczeń:
wersja 2 (WWW)
2
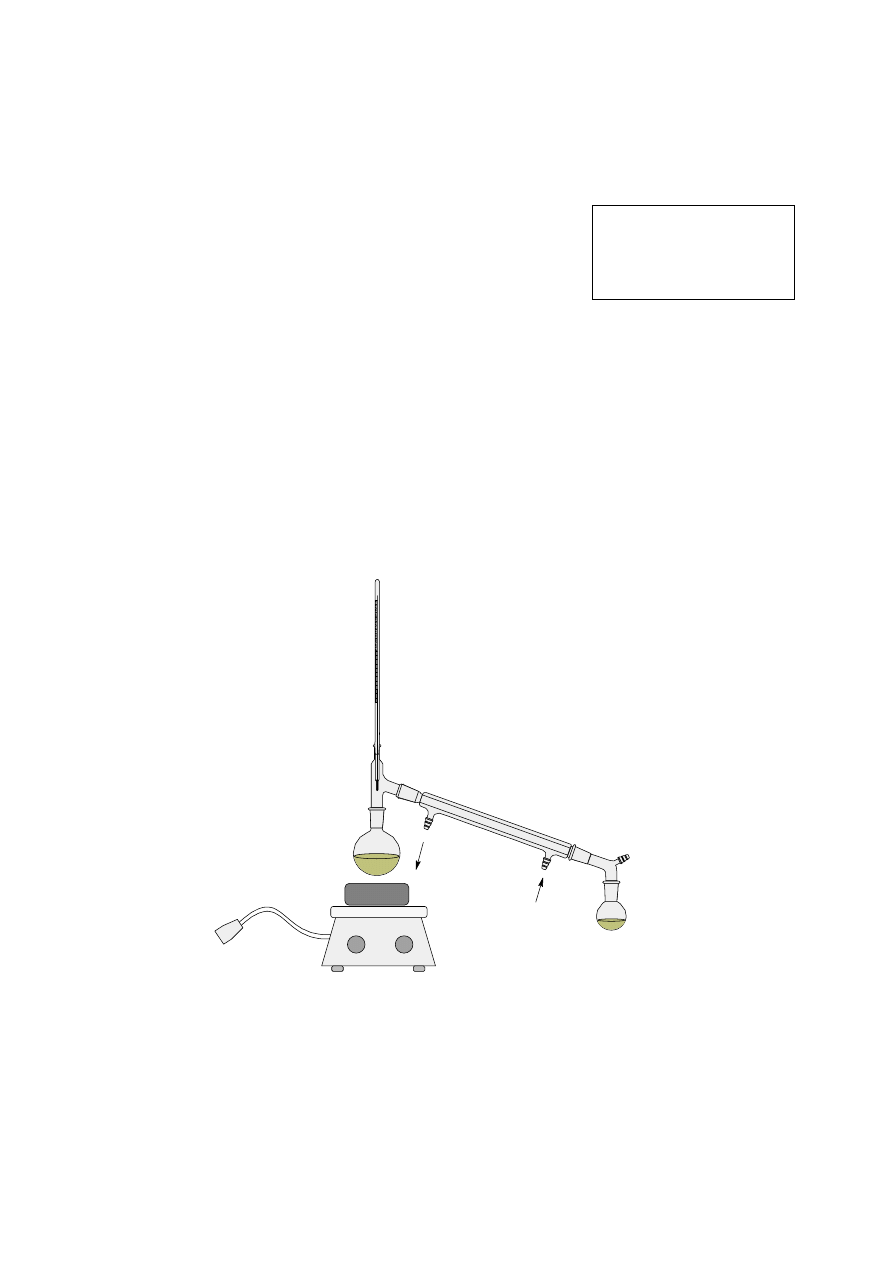
[DF] Destylacja
frakcyjna
Nalać do kolby destylacyjnej mieszaninę acetonu i toluenu
a następnie dodać kilka drobnych kamyczków wrzennych.
Przeprowadzić destylację prostą mieszaniny (bez deflegmatora).
Mierzyć objętość destylatu i co 2 ml zapisywać temperaturę. Po
zakończeniu destylat przelać z powrotem do kolby destylacyjnej i przeprowadzić destylację
frakcyjną (z deflegmatorem). Tak jak poprzednio zapisywać temperaturę co 2 ml destylatu.
Tym razem należy rozdzielić destylat na frakcje (aceton, toluen i ewentualnie frakcje
pośrednie). Dla obu destylacji sporządzić wykresy zależności temperatury od objętości
destylatu. Z wykresu dla destylacji frakcyjnej oszacować ilość acetonu i
toluenu
w mieszaninie.
Odczynniki:
• mieszanina acetonu
i toluenu
1
1 1
2
3
4
5
6
7
8
9
1
10
2
3
4
5
6
7
8
9
1
1 0
wersja 2 (WWW)
3
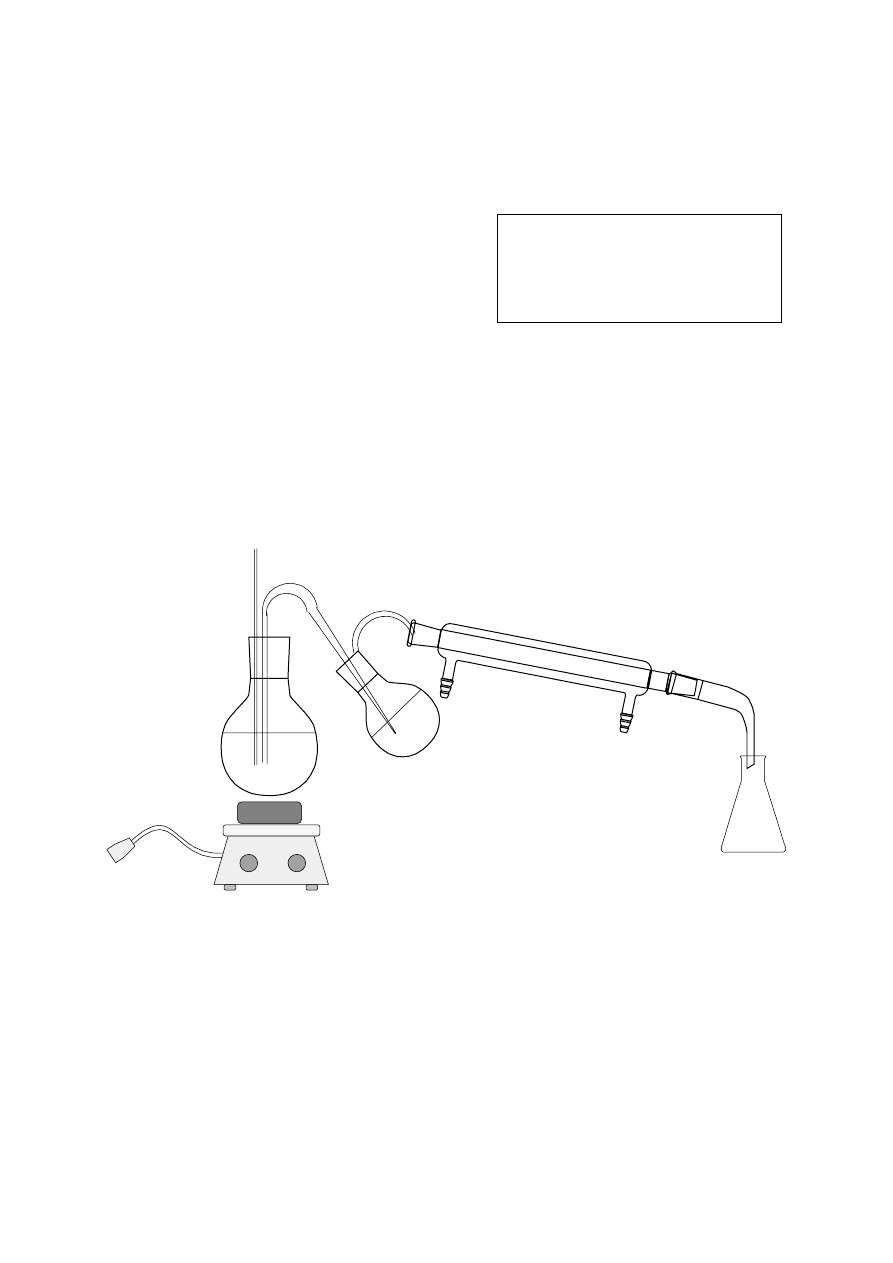
[DPW]
Destylacja z parą wodną
Zmontować zestaw do destylacji z para wodną.
W
kolbie destylacyjnej umieścić chlorowodorek
aniliny, a następnie dodać roztwór 5 g NaOH w 250
ml wody. Przedestylować uzyskaną anilinę z parą
wodną. Destylację należy prowadzić do momentu, gdy zacznie destylować sama woda. Po
zakończeniu destylacji dodać do destylatu 2 łyżki NaCl po czym wymieszać do rozpuszczenia
się soli. Następnie przelać destylat do rozdzielacza i oddzielić anilinę od wody. Zmierzyć
objętość uzyskanej aniliny. Napisać reakcję i na jej podstawie obliczyć wydajność
oczyszczania.
Odczynniki:
• chlorowodorek aniliny 15 g
• NaOH 5
g
• NaCl
1
1 1
2
3
4
5
6
7
8
9
1
10
2
3
4
5
6
7
8
9
1
1 0
H
2
O
wersja 2 (WWW)
4

[KR]
Krystalizacja z rozpuszczalnika organicznego
W kolbie umieścić 10 g 2,5-dichloroaniliny i dodać 30
ml metanolu. Ogrzać do wrzenia pod chłodnicą zwrotną
na łaźni wodnej lub płaszczu grzejnym. W razie
niecałkowitego rozpuszczenia się substancji dodawać
małymi porcjami rozpuszczalnik przez wylot chłodnicy. Po rozpuszczeniu substancji
przerwać ogrzewanie, dodać 1 g węgla aktywnego i ponownie ogrzać do wrzenia. Przesączyć
gorący roztwór przez uprzednio ogrzany lejek szklany z sączkiem fałdowanym. Przesącz
pozostawić do ostygnięcia. Wykrystalizowaną 2,5-dichloroanilinę odsączyć pod
zmniejszonym ciśnieniem, a następnie pozostawić do wysuszenia. Zważyć uzyskaną
substancję i obliczyć wydajność krystalizacji.
Odczynniki:
• 2,5-dichloroanilina 1 10
g
• metanol 1 50
ml
• węgiel aktywny
1 g
wersja 2 (WWW)
5

[KW]
Krystalizacja z wody
Kwas sulfanilowy umieścić w zlewce, dodać 100 ml wody
i ogrzać do wrzenia. W razie nierozpuszczenia się kwasu
dodawać wodę, po 25 ml, za każdym razem doprowadzając
do wrzenia i sprawdzając czy kwas uległ całkowitemu rozpuszczeniu. Po rozpuszczeniu się
kwasu przerwać na chwilę ogrzewanie, po ustaniu wrzenia wsypać ostrożnie 1 g węgla
aktywnego po czym ponownie ogrzać do wrzenia. Roztwór przesączyć na gorąco. Przesącz
pozostawić do krystalizacji. Odsączyć kryształy pod zmniejszonym ciśnieniem, przemywając
je na lejku niewielką ilością wody. Po wysuszeniu zważyć otrzymany kwas i obliczyć
wydajność krystalizacji.
Odczynniki:
• kwas sulfanilowy
10 g
• węgiel aktywny
1 g
wersja 2 (WWW)
6

[SEAR] Substytucja elektrofilowa w związkach aromatycznych
a) Do trzech probówek nalać po około 1 ml CCl
4
, a następnie
dodać do pierwszej 2 ml cykloheksenu, do drugiej kilka
kryształków fenolu, a do trzeciej 2 ml toluenu. Do każdej
z probówek dodać po kilka kropli Br
2
. Zawartość probówek
wstrząsać przez chwilę. Zaobserwować zachodzące
zmiany. Wyjaśnić różnice i napisać reakcje chemiczne.
b) Zmieszać ostrożnie 5-6 kropli węglowodoru z 5-6 kroplami
stężonego kwasu azotowego(V). Obserwować zmiany
zachodzące w probówkach. Ćwiczenie przeprowadzić
z n-heksanem, benzenem i toluenem. Napisać reakcje
chemiczne.
c) Do suchej probówki nalać około 2 ml suchego chloroformu
lub czterochlorku węgla, po czym dodać 3-4 krople lub około 0.5 g węglowodoru.
Wymieszać zawartość. Następnie dodać 0.5-1 g bezwodnego chlorku glinu, tak aby część
proszku zatrzymała się na ściankach probówki. Przechylając probówkę zwilżyć ostrożnie
chlorek glinu roztworem. Zaobserwować zachodzące zmiany, biorąc do reakcji n-heksan,
benzen, chlorobenzen, naftalen oraz antracen. Napisać reakcje chemiczne.
Odczynniki:
• brom 1
• HNO
3
stęż.
• CCl
4
• CHCl
3
• AlCl
3
bezw.
• cykloheksen
• fenol 1
• toluen
• n-heksan
• benzen 1
• chlorobezen
• naftalen
• antracen
Brom jest silnie żrący i trujący!
Fenol ma właściwości parzące, działa szkodliwie na skórę. W razie poparzenia skórę
należy umyć wodą z mydłem.
Pracować w gumowych rękawicach i okularach!
Ćwiczenie wykonywać wyłącznie pod wyciągiem!
wersja 2 (WWW)
7
[BA] Barwniki
azowe
Roztwór soli diazoniowej
Około 0.1 g badanej aminy rozpuścić w 5 ml
10% HCl, ochłodzić wodą z lodem do 0-5˚C, po
czym dodawać kroplami roztwór 1 g NaNO
2
w 5 ml H
2
O do dodatniej próby z papierkiem
jodoskrobiowym (niebieskie zabarwienie).
Odczynniki:
• anilina 1 0.1
g
• kwas p-aminobenzoesowy 0.1
g
• kwas sulfanilowy
0.1 g
• 10% HCl
5 ml
• azotan(III) sodu 1 1
g
• fenol 1 0.1
g
• 1-naftol 0.1
g
• 2-naftol 0.1
g
• 10% NaOH
5 ml
Roztwór fenolu
Około 0.1 g fenolu rozpuścić w 5 ml 10%
NaOH.
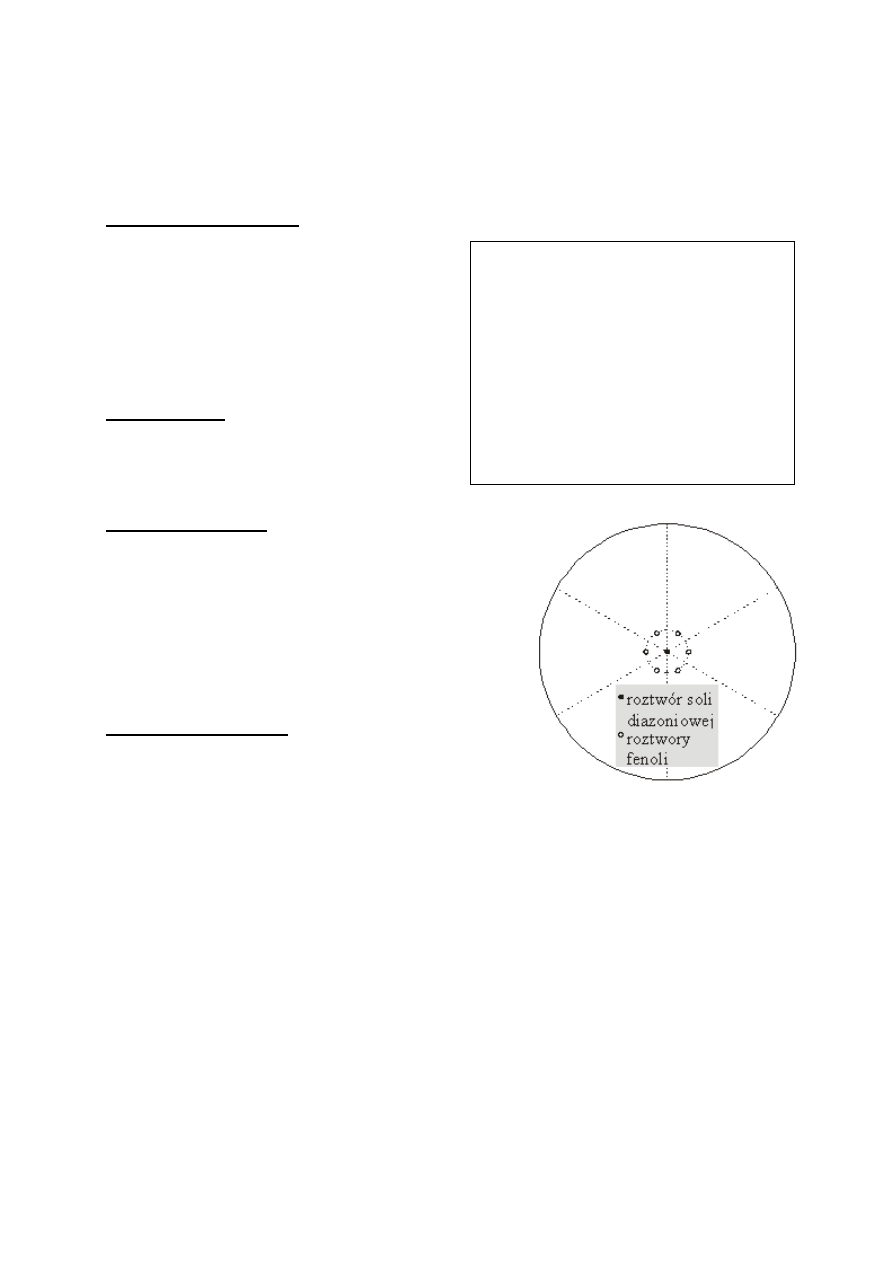
Sprzęganie na bibule
Na krążek bibuły nanieść po jednej kropli alkalicznego
roztworu każdego z fenoli. Krople nanosić na okręgu
o promieniu około 2 cm. W środek okręgu nanieść
roztwór soli diazoniowej i obserwować zjawiska na
granicy roztworu soli diazoniowej oraz fenolu.
Sprzęganie w probówce
Do trzech probówek dodać po dwie krople
alkalicznego roztworu danego fenolu. Do każdej z nich
dodać po dwie krople roztworu soli diazoniowej. Zawartość probówek rozcieńczyć 5 ml
wody. Roztwór z każdej probówki podzielić na dwie części i do jednej połowy dodać
roztworu HCl do uzyskania odczynu kwaśnego, a do drugiej roztworu NaOH do uzyskania
odczynu alkalicznego. Obserwować zmiany barwy.
Ćwiczenie należy przeprowadzić z następującymi związkami:
• fenole – 1-naftol, 2-naftol, fenol;
• aminy – anilina, kwas p-aminobenzoesowy, kwas sulfanilowy.
Napisać reakcje otrzymywania soli diazoniowych z amin oraz wszystkie reakcje sprzęgania.
Pracować w gumowych rękawicach i okularach!
Ćwiczenie wykonywać wyłącznie pod wyciągiem!
wersja 2 (WWW)
8
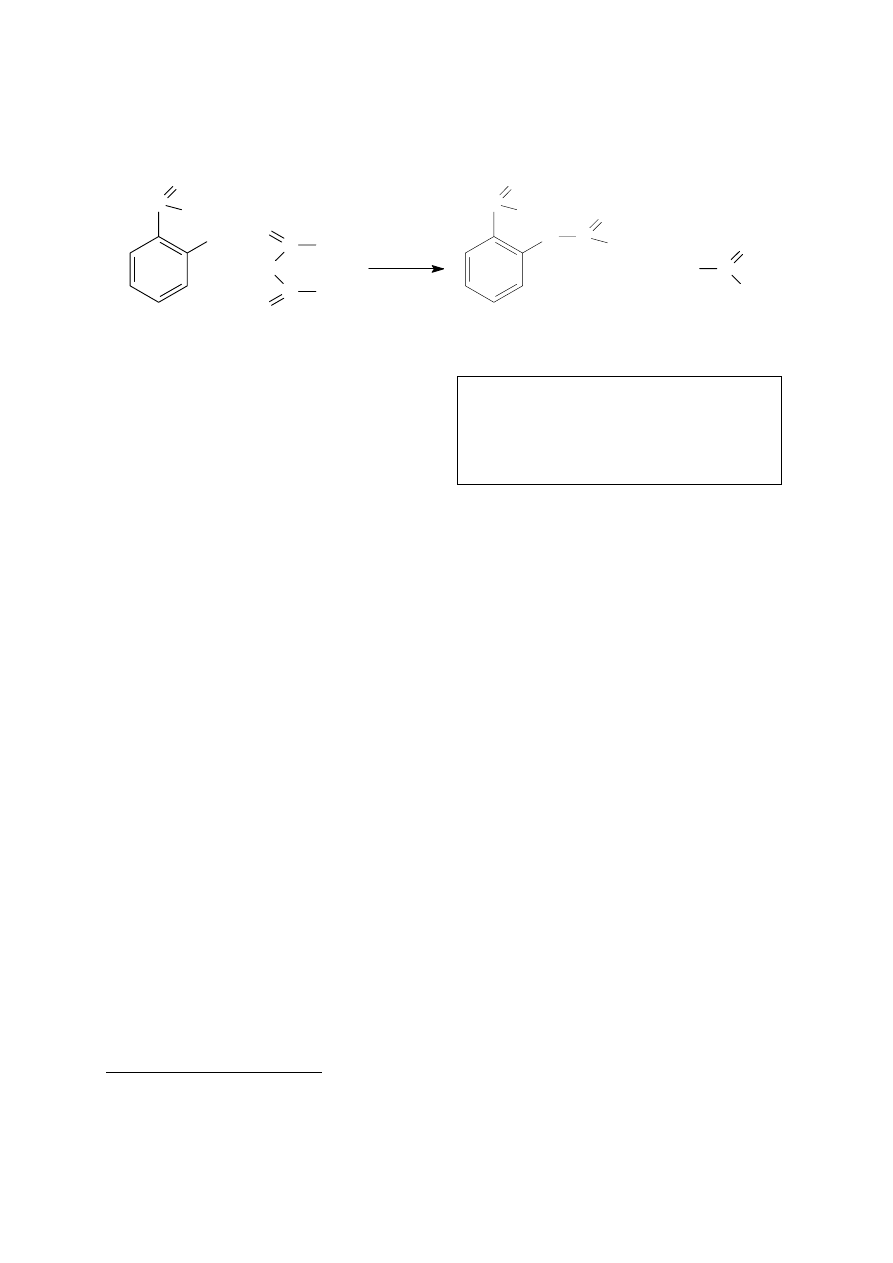
[ASP] Kwas
acetylosalicylowy
(aspiryna)
C
O
OH
OH
+
H
3
C
C
O
OH
C
CH
3
O
O
C
O
CH
3
+
C
O
OH
O
C
O
CH
3
H
2
SO
4
kwas acetylosalicylowy (aspiryna); rozkład 129–133
°C
W małej kolbie stożkowej 200–250 ml
z szeroką szyją umieszcza się 12.5 g
bezwodnego kwasu salicylowego, 17.5 ml
bezwodnika octowego i dodaje 1 ml stężonego
kwasu siarkowego, mieszając przy tym starannie zawartość kolby ruchem wirowym.
Następnie mieszaninę ogrzewa się na łaźni wodnej do około 50–60
°C w ciągu 15 minut,
mieszając ją jednocześnie za pomocą termometru (ostrożnie, termometry są dość kruche).
Mieszaninę pozostawia się do ostygnięcia, wstrząsając ją co pewien czas, dodaje 150 ml
wody, starannie miesza i sączy pod zmniejszonym ciśnieniem przez lejek Büchnera.
Odczynniki:
• kwas salicylowy
12.5 g
• bezwodnik octowy 1
19 g (17.5 ml)
• kwas siarkowy
1 ml
Otrzymany produkt powinien topić się z rozkładem w temperaturze 129–133
°C.
wysuszeniu należy zważyć i obliczyć wydajność na podstawie reakcji.
Pracować w gumowych rękawicach i okularach!
Ćwiczenie wykonywać wyłącznie pod wyciągiem!
1
A. I. Vogel, „Preparatyka organiczna, wydanie drugie całkowicie zmienione i poprawione”,
Wydawnictwa Naukowo-Techniczne, Warszawa 1984, str. 710.
2
Kwas acetylosalicylowy w czasie ogrzewania ulega rozkładowi i nie można go scharakteryzować
poprzez właściwą, ściśle określoną temperaturę topnienia. Temp. rozkładu związku waha się w zakresie
128-135
°C; oznaczana na ogrzewanej elektrycznie płytce wynosi 129-133°C.
wersja 2 (WWW)
9
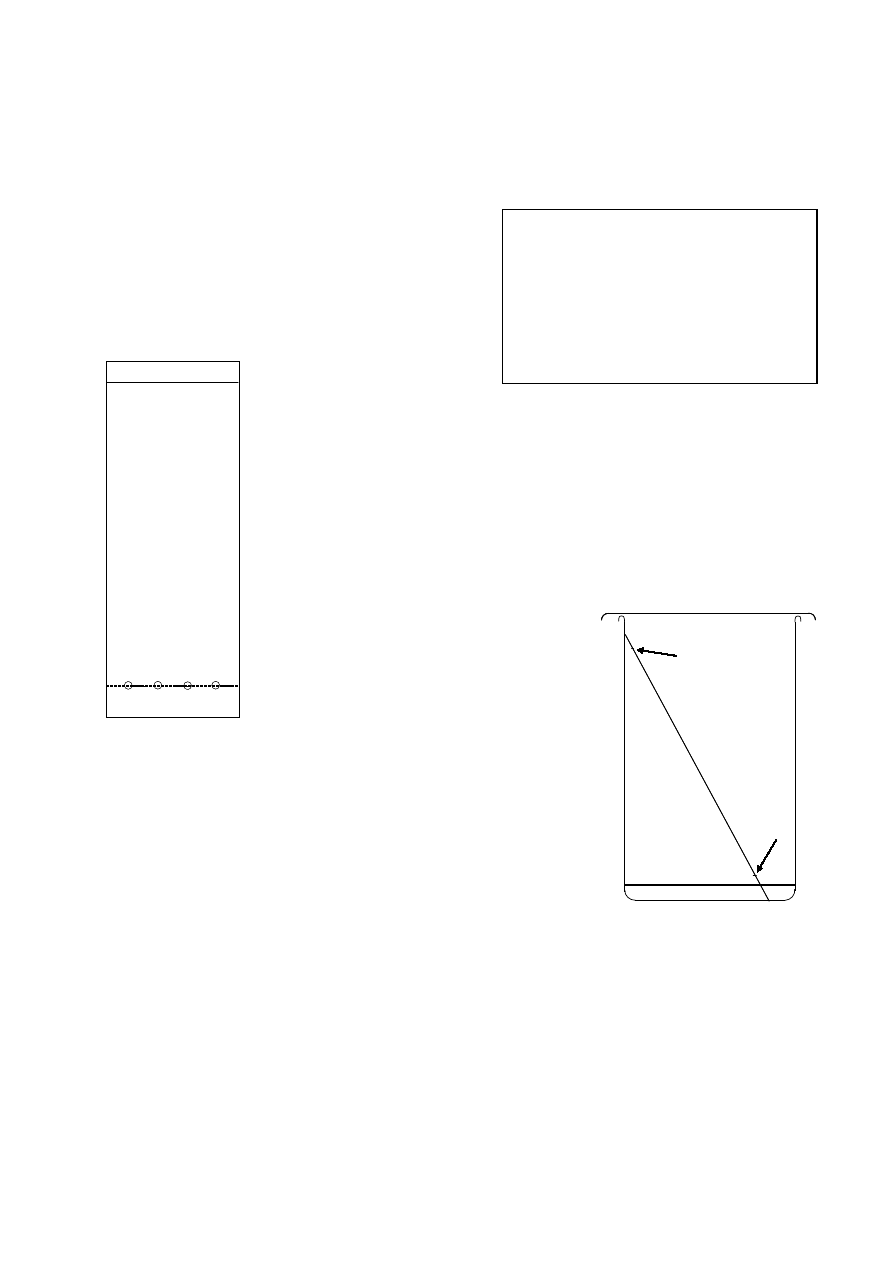
[CHR]
Chromatografia cienkowarstwowa barwników (TLC)
Na płytce do chromatografii cienkowarstwowej
(płytka aluminiowa o wymiarach 90x40 mm lub
szersza, pokryta żelem krzemionkowym,) należy
zaznaczyć delikatnie ołówkiem linię startu (ok.
8
mm od dolnej krawędzi
płytki), starając się nie
uszkodzić powierzchni żelu. Należy unikać dotykania powierzchni płytki
palcami. Na linii startu zaznacza się punkty nanoszenia roztworów w
odstępie ok. 1 cm. (cztery tory dla roztworów wzorcowych i dwa dla
mieszanin). Na przygotowaną płytkę nanosi się kapilarkami metanolowe
roztwory każdego z barwników oraz dwie mieszaniny dwóch dowolnych
barwników, tworząc plamki o średnicy nie większej niż 3 mm.
Materiały i sprzęt:
• płytka do chromatografii TLC
• linijka i ołówek
• wzorce barwników i kapilarki
• komora chromatograficzna
• eluent
(1-butanol-kwas octowy-woda 4:1:1)
Do komory chromatograficznej wlewa
się eluent tworząc warstwę o głębokości ok.
5 mm. Płytkę umieszcza się pionowo
w komorze, zwracając uwagę, by poziom
cieczy nie sięgał do linii startu. Jeżeli w tej
samej komorze mają być rozwijane dwie płytki, umieszcza się je
tyłem do siebie, zetknięte tylko górnymi krawędziami. Boczne
krawędzie płytek nie powinny dotykać ścianek komory. Komorę
nakrywa się szalką i czeka na rozwinięcie chromatogramu (ok. 40-
60 minut). Komora powinna stać w
spokojnym miejscu,
w temperaturze pokojowej.
8 mm
5 mm
start
czoło
( po rozwinięciu)
8 mm
5 mm
start
czoło
( po rozwinięciu)
start
czoło
eluent
płytka chromatograficzna
start
czoło
eluent
płytka chromatograficzna
Płytki wyjmuje się z komory, gdy poziom eluentu znajdzie się ok. 5 mm od górnej
krawędzi płytki, zaznacza ołówkiem linię czoła rozpuszczalnika i suszy płytki suszarką (pod
wyciągiem).
Po zmierzeniu odległości start-czoło i start-środek plamki należy obliczyć
współczynniki R
f
wszystkich analizowanych barwników. Na podstawie współczynników R
f
plamek należy zidentyfikować barwniki w mieszaninach.
wersja 2 (WWW)
10
Wyszukiwarka
Podobne podstrony:
prep
activity about prep
prep galenowe 3, ziółka
clad exam prep guide english
06-Zasady bezp.pracy z prep.chemicznymi przy pracach porząd~2, Instrukcje BHP, XXVIII - SPRZĄTANIE
Heat Treatment Prep Sheet
tkanka łączna- konserwacja prep, Medycyna itp
prep chemical fact sheet
aerozole 3, prep galenowe
allo prep cache 002Allophones
Dz.U.2009.152.1222 Substancje i prep. chemiczne, BHP, Akty prawne
directions, places, prep
bhp w pracach porządkowych z prep. chemią, INSTRUKCJE
bhp w pracach porządkowych z prep. chemią, INSTRUKCJE
prep galenowe 2
Abioseptyna 30ml prep + najpopularniejsze choroby, akwarium
Prep Gal
prep ied fact sheet
więcej podobnych podstron