II Ogólnopolska Próbna Matura z Chemii ODPOWIEDZI – arkusz rozszerzony
www.NowaMatura.edu.pl
1
II Ogólnopolska Próbna Matura z Chemii – KLUCZ ODPOWIEDZI – ARKUSZ ROZSZERZONY
Kolorem niebieskim naniesiono dodatkowe zmiany do klucza dokonane po godz. 18.
Zadanie/podpunkt
Odpowiedź
Uwagi/komentarze
1.1
bilans elektronowy, np.:
-II 0
S → S + 2e
+I +II x 3
2 Cu → 2 Cu + 2e
__________________________
+V +II
N + 3e → N
x 4
1 pkt
dopuszcza się KAŻDĄ poprawną formę
bilansu elektronowego
…
1.2 (bez punktu)
3 Cu
2
S + 4 NO
3
-
+ 16 H
+
→ 6 Cu
2+
+ 3 S + 4 NO + 8 H
2
O
…i prawidłowo zbilansowaną reakcję
1.3
utleniacz: NO
3
-
reduktor: Cu
2
S
1 pkt
Uwaga: nie przyznajemy pkt, jeśli uczeń poda
sam pierwiastek, który zmienił stopień a nie
poda całej drobiny.
2
(C
17
H
35
COO)
2
Ca lub (C
15
H
31
COO)
2
Ca
1 pkt
3
Pierwiastki chemiczne zapisane symbolami w kolejności:
N, P, As, Sb, Bi
należą do tej samej grupy układu okresowego
(prawda/fałsz) i charakteryzują się praktycznie jednakową
elektroujemnością (prawda/fałsz). Zostały uszeregowane
według
malejącej
zasadotwórczości
(prawda/fałsz)
a ich promienie atomowe rosną od bizmutu do azotu
(prawda/fałsz). Analizując wzrost metaliczności od azotu
do bizmutu należy stwierdzić, że metaliczność zmienia się
tak samo jak zasadotwórczość (prawda/fałsz).
za 5 poprawnych odpowiedzi – 3 pkt
za 4 poprawne odpowiedzi – 2 pkt
za 3 poprawne odpowiedzi – 1 pkt
4
Za reakcję spalania kwasu:
C
4
H
9
COOH +
13/2
O
2
→
5
CO
2
+ 5 H
2
O
1 pkt
Dopuszcza się wzięcie do reakcji każdej formy
zapisu wzoru kwasu (nawet wzoru
sumarycznego).
Uwaga: Jeżeli uczeń zapisał prawidłowo
reakcję spalania ale użył ZŁEGO wzoru kwasu
ale dalsze obliczenia prowadził prawidłowo –
odbieramy tylko 1 pkt od całości
Za prawidłowy wybór metody
1 pkt
Za wynik z jednostką:
−2515
kJ lub
−2515
kJ/mol kwasu
1 pkt
Dopuszczamy obie formy gdyż uczeń obliczał
entalpię reakcji
5.a
Papierek nad probówką I – CZERWONY
Papierek nad probówką II – niebieski (niebieskozielony)
1 pkt
Punkt przyznajemy za poprawną pełna
odpowiedź
5.b
Gaz w probówce I: CO
2
Gaz w probówce II: NH
3
1 pkt
Punkt przyznajemy za poprawną pełna
odpowiedź
Uwaga: punktu nie przyznajemy jeśli uczeń
udzielił prawidłowej odpowiedzi ale zamiast
wzorów podał NAZWY gazów
6.a
klucz elektrolityczny
1 pkt
6.b
SO
4
2-
1 pkt
7.1
2-bromopropan
1 pkt
Uwaga: nie uznajemy jeśli uczeń zamiast
słówka „bromo” użyje „chloro” lub „jodo”
Uwaga: nie przyznajemy punktu jeśli zamiast
nazwy uczeń poda, nawet prawidłowy, wzór
substancji X
7.2
OH
| H
+
CH
3
-CH-CH
3
+ CH
3
-CH(CH
3
)-COOH
CH
3
-CH(CH
3
)-O-CO-CH(CH
3
)-CH
3
+ H
2
O
1 pkt
Uznajemy każdą poprawną formę zapisu
reakcji estryfikacji.
Uwaga: nie przyznajemy punktu jeśli uczeń
pominie środowisko reakcji
8
główna liczba kwantowa 4
poboczna liczba kwantowa 0
1 pkt
1 pkt
9
bromek rubidu
chlorek potasu
2 pkt
za każdą poprawnie podaną nazwę
Uwaga: nie przyznajemy punktu, jeśli uczeń
zapisze prawidłowo odpowiedź wzorami a nie
za pomocą nazw.
Uwaga: każda błędna odpowiedź skreśla
poprawną.
10.1
Redukcja zachodzi w półogniwie X
Utlenianie zachodzi w półogniwie Y
1 pkt
10.2
2 MnO
4
-
+ 6 H
+
+ 5 SO
3
2-
→ 2 Mn
2+
+ 5 SO
4
2-
+ 3 H
2
O
1 pkt
Uznajemy również poprawnie zapisaną reakcje
II Ogólnopolska Próbna Matura z Chemii ODPOWIEDZI – arkusz rozszerzony
www.NowaMatura.edu.pl
2
będącą sumą stron reakcji połówkowych bez
dokonania skróceń jonów i wody.
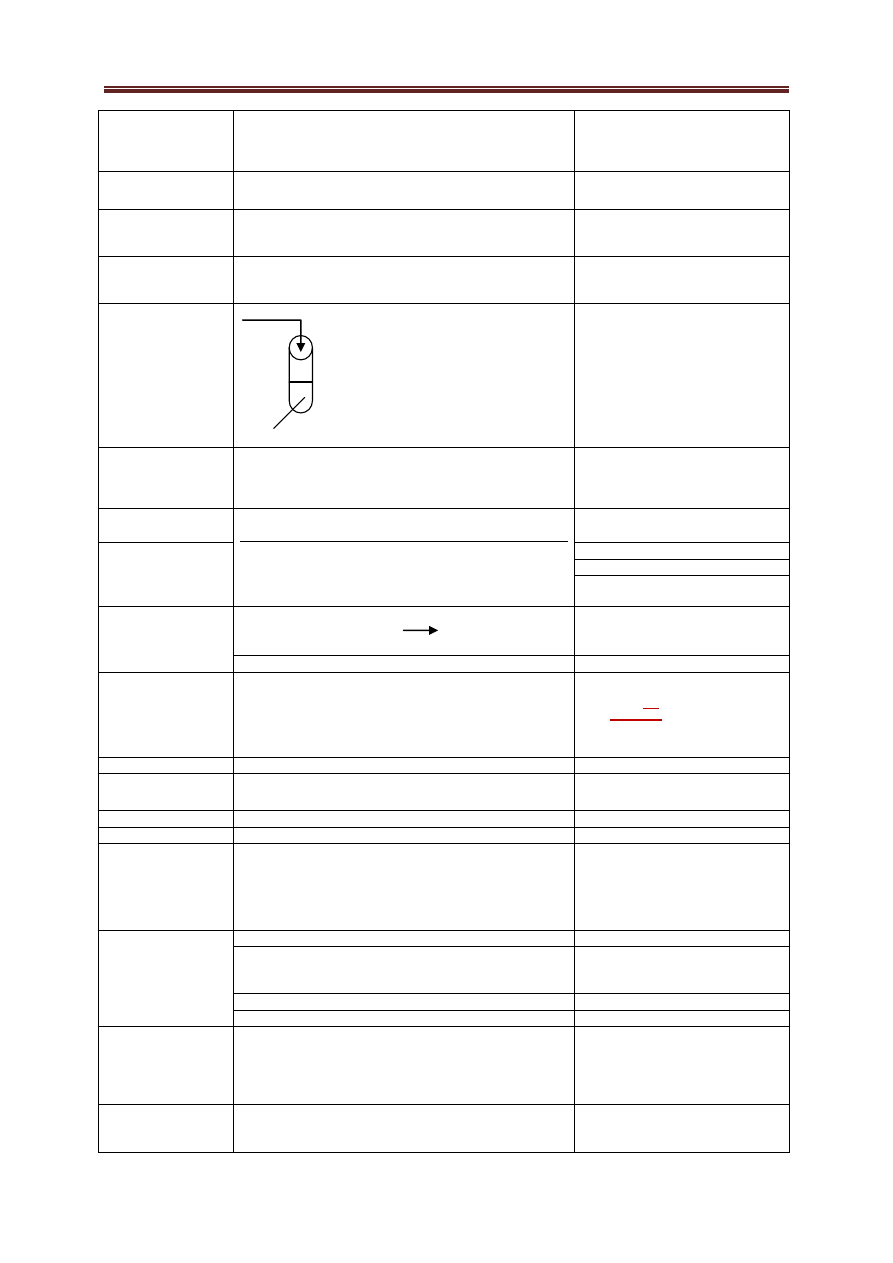
Uwaga: nie przyznajemy punktu nawet gdy
reakcje zapisano dobrze jeśli uczeń zapisze
strzałkę w formie
11
Kolejne stopnie: +I, 0, -I
3 pkt
po jednym punkcie za każdy stopień kolejnego
atomu węgla
12.a
(CH
3
)
2
C
H
─CH─COO
-
|
NH
3
+
1 pkt
12.b
(CH
3
)
2
C
H
─CH─COO
-
|
NH
2
1 pkt
13.a
CuSO
4
+ NaOH
C
5
H
12
O
5
1 pkt
13.b
Świeżo strącona zawiesina Cu(OH)
2
rozpuszcza się i
powstaje szafirowy klarowny roztwór.
1 pkt
Uwaga: odpowiedź w każdym słowie musi
być pozbawiona błędu
Uwaga: w obserwacji muszą paść słowa:
„osad rozpuszcza się”
14
FeO, FeCl
2
za 2 poprawne odp. 2 pkt
za 1 poprawną odp. 1 pkt
Za napisanie wzoru na stałą równowagi
1 pkt
15
Z obliczenie wartości stałej K =
270
1 pkt
Za podanie wartości stężeń równowagowych wraz z
jednostką: [H
2
] = 0,30 mola/dm
3
, [Br
2
] = 0,01 mola/dm
3
1 pkt
16
280
0
C
CH
2
OH─CH(OH) ─CH
2
OH 2 H
2
O +
+ CH
2
=CH─CHO
1 pkt
Punktu nie przyznajemy jeśli uczeń nie
zaznaczy (w dowolny sposób), że reakcja
wymaga wysokiej temperatury, ogrzania
H─CHO + CH
3
CHO → CH
2
=CH─CHO + H
2
O
1 pkt
17.1
Fe
2
O
3
(tlenek żelaza (III))
(i FeO – tlenek żelaza (II))
1 pkt
Uwaga:
możemy uznać odpowiedź, w której
uczeń poda oba tlenki jako amfoteryczne
ale tylko wtedy jeśli zapisze poprawnie
wszystkie reakcje w punktach 17.3 i 17.4
Nie przyznajemy punktu, gdy uczeń
wybierze TYLKO FeO!!!
17.2
KOH, HCl
1 pkt
17.3
Fe
2
O
3
+ 6 OH
-
+ 3 H
2
O →
2
Fe(OH)
6
3-
1 pkt
Dopuszcza się również sole otrzymane w
formie cząsteczkowej: FeO
3
3-
lub FeO
2
-
17.4
Fe
2
O
3
+ 6 H
+
→ 2 Fe
3+
+ 3 H
2
O
1 pkt
18
Wszystkie odpowiedzi są fałszywe
po 1 pkt za każdą prawidłową odpowiedź
19
x dm
3
O
2
---------------- 0,002 mola MnO
4
-
5 ∙ 22,4 dm
3
------------ 2 mole
--------------------------------------------
x = 0,112 dm
3
1 pkt
za metodę – prawidłowo ułożoną proporcję
wynikającą z bilansu elektronowego i
stechiometrii reakcji połówkowych
Odpowiedź: 0,112 dm
3
tlenu
1 pkt
za poprawne obliczenie i wynik z jednostką
Probówka I: odczyn kwaśny
1 pkt
20
CH
3
NH
3
+
+ H
2
O → CH
3
NH
2
+ H
3
O
+
lub
CH
3
NH
3
+
+ H
2
O → CH
3
NH
2
∙ H
2
O + H
+
1 pkt
Probówka II: odczyn zasadowy
1 pkt
NO
2
-
+ H
2
O → HNO
2
+ OH
-
1 pkt
21.a
Uczeń prowadzi obliczenia na bazie reakcji Na z wodą.
Wykonane rachunki pokazują, że otrzymany roztwór
NaOH ma stężenie 1,74%
(po drodze wyniki obliczeń: masa NaOH = 3,48 g, masa
wydzielonego wodoru = 0,08 g, masa roztworu = 199,92 g)
1 pkt
punkt przyznajemy za pełny ciąg obliczeń
prowadzący do obliczenia cp innego niż
1-procentowy
Przykładowe uzasadnienie: nie udało się otrzymać
roztworu 1% gdyż sód przereagował z wodą i stężenie
roztworu wyniosło 1,74%
1 pkt
II Ogólnopolska Próbna Matura z Chemii ODPOWIEDZI – arkusz rozszerzony
www.NowaMatura.edu.pl
3
21.b
Np. sód jest higroskopijny (chłonie wodę z powietrza)
1 pkt
uznajemy tylko wyjaśnienie odnośnie reakcji
z wodą
Uwaga: przyznajemy punkt gdy uczeń wskaże
na łatwość reakcji metalicznego sodu z tlenem
lub CO
2
z powietrza
21.c
Np. podczas reakcji sodu z wodą wydziela się dużo energii
(reakcja jest silnie egzoenergetyczna)
1 pkt
Uwaga:
zaliczamy zdanie, że powstający
wodorotlenek działa parząco na skórę
22
1.
np.
CH
3
-C(CH
3
)
2
-CH(CH
3
)-CH
2
-CH
3
2. np. CH
3
-CH
2
-CH
3
3. np.
CH
3
CH
3
4. np. HC≡CH
4 pkt
Punkt przyznajemy za każdy prawidłowo
narysowany półstrukturalne wzór związku
organicznego spełniające podane właściwości
23.a
Ba
2+
+ SO
4
2-
→ BaSO
4
↓
1 pkt
23.b
Na
+
, NO
3
-
1 pkt
23.c
obojętny
1 pkt
Wyszukiwarka
Podobne podstrony:
2009 p podst próbna NowaMatura rozw
2010 p rozsz próbna NowaMatura rozw
2009 p rozsz próbna NowaMatura
2008 p rozsz próbna NowaMatura rozw
2009 p podst próbna NowaMatura
2008 p podst próbna NowaMatura rozw
2010 p podst próbna NowaMatura rozw
2008 p podst próbna NowaMatura rozw
2008 p rozsz próbna NowaMatura
2009 czerwiec praktyka bez rozw
arkusz Jezyk polski poziom r rok 2009 3136 próbna
2010 p podst próbna NowaMatura
więcej podobnych podstron