Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
11/IV
b
3. Sieci metaliczne
Metale mają budowę krystaliczną.
W węzłach sieciowych występują rdzenie atomowe; są one dodatnio naładowane.
W przestrzeniach międzywęzłowych istnieją swobodne, nie związane
z pojedynczymi atomami, elektrony (elektrony walencyjne)
Cechy wspólne metali:
- dobre przewodnictwo elektryczne,
- dobre przewodnictwo cieplne,
- połysk metaliczny,
- plastyczność,
- niskie ciepło właściwe.
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
12/IV
b
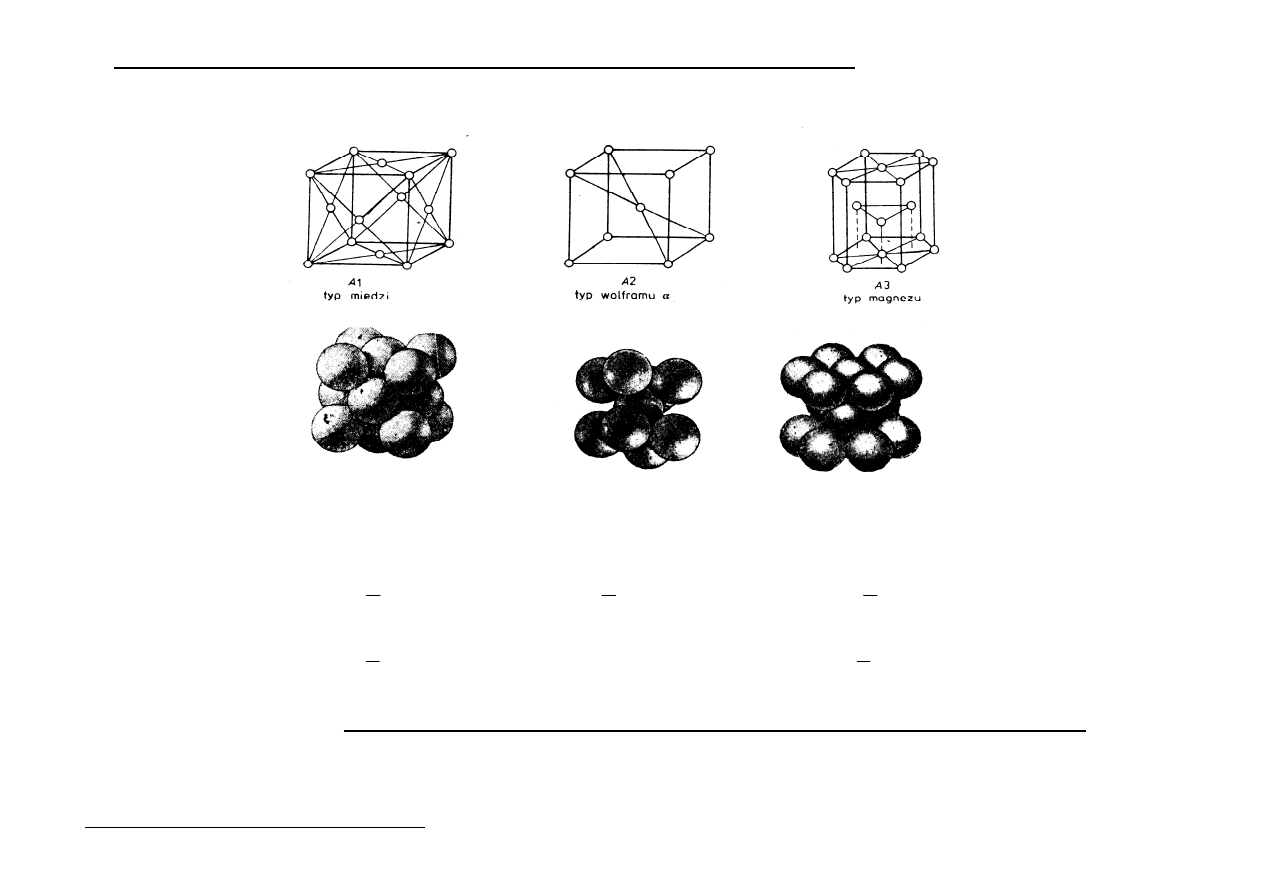
Metale krystalizują w jednej z 3 typów sieci, tj.:
A
1
A
2
A
3
Sieci te są bardzo gęsto upakowane.
Najbardziej zapełnione komórki sieciowe można osiągnąć na dwa sposoby:
- regularne najgęstsze upakowanie (A
1
)
-
heksagonalne najgęstsze upakowanie (A
3
)
1
o
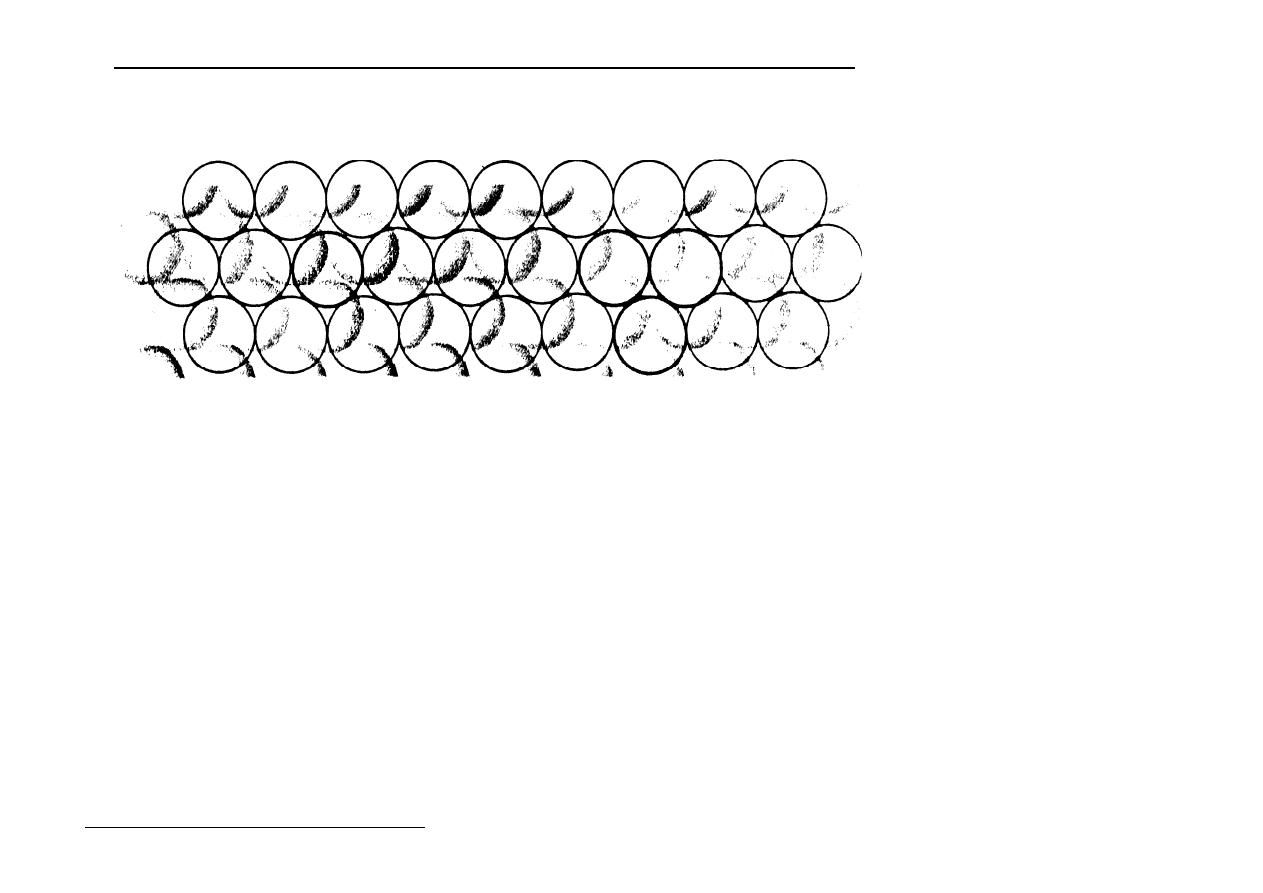
Umieścić kulę na powierzchni
2
o
Otoczyć ją 6-ma takimi samymi kulami
3
o
Teraz utwórzmy 2-gą warstwę 7 kul, tak aby je "zagnieździć" w stosunku do pierwszej
warstwy (warstwa b)
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
13/IV
b
Mamy więc ułożenie typu ab
4
o
Trzecią warstwę można ułożyć na dwa sposoby :
a) ta warstwa jest tak samo ułożona jak warstwa
a
→
→
→
→
ułożenie
ababab
....
→
→
→
→
jest prześwit
→
→
→
→
komórka
typu A
3
b) warstwa trzecia nie jest ani nad
a
ani nad
b
.
Jest to warstwa c
→
→
→
→
ułożenie
abcabc
....
→
→
→
→
nie ma prześwitu
→
→
→
→
komórka typu A
1
Stopień upakowania w obu typach sieci jest taki sam i wynosi 74 %
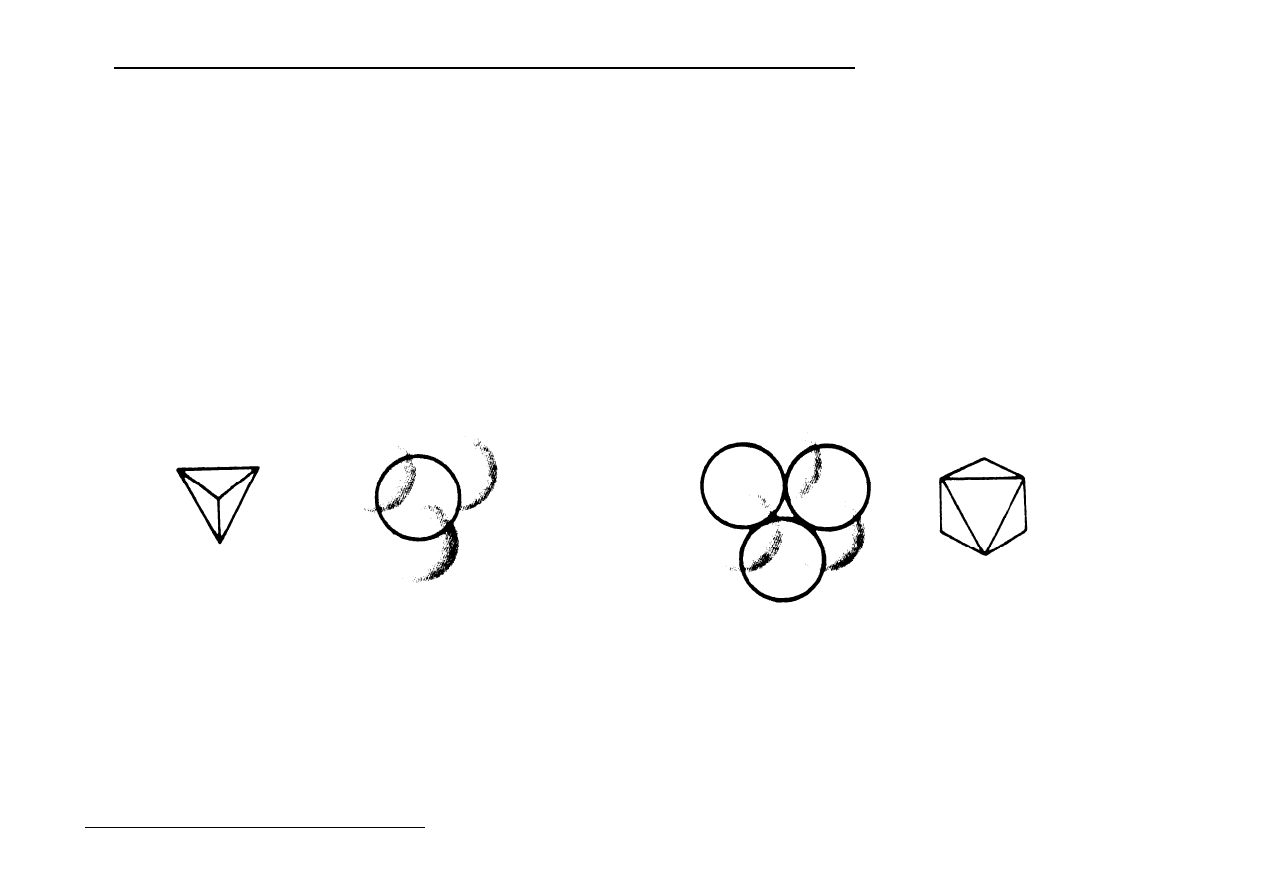
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
14/IV
b
Luki w przestrzeniach międzywęzłowych dla sieci typu A
1
i A
3
- tetraedryczne
r = 0,21 r
kuli
2N - luk
- oktaedryczne
r = 0,41 r
kuli
N - luk
N - liczba kul, r- promień kuli
Trzeci typ sieci (A
2
) jest mniej upakowany - 68 %
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
15/IV
b
Pokażmy te 3 komórki elementarne:
Liczba koord.
12
8
12
liczba atomów
8 x
1
8
= 1
8 x
1
8
= 1
12 x
1
6
= 2
w kom. elem. :
6 x
1
2
= 3
1 x 1 = 1
2 x
1
2
= 1
3 x 1 = 3
ΣΣΣΣ
= 4
ΣΣΣΣ
= 2
ΣΣΣΣ
= 6
6 : 3 = 2
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
16/IV
b
A
1
- sieć regularna zewnętrznie centrowana
Cu, Ag, Ca, Sr, Pd, Ir, Pt,
γγγγ
-Fe,
ββββ
-Co,
ββββ
-Ni
A
2
- sieć regularna wewnętrznie centrowana
αααα
-W, V, Nb, Ta, Mo,
αααα
-Fe
A
3
- sieć heksagonalna
Mg, Zn, Cd, Ti, Zr, a-Co
Znając parametry komórki elementarnej, np. stałą sieciową (a), można obliczyć promień tego
atomu metalu (rdzenia atomowego).
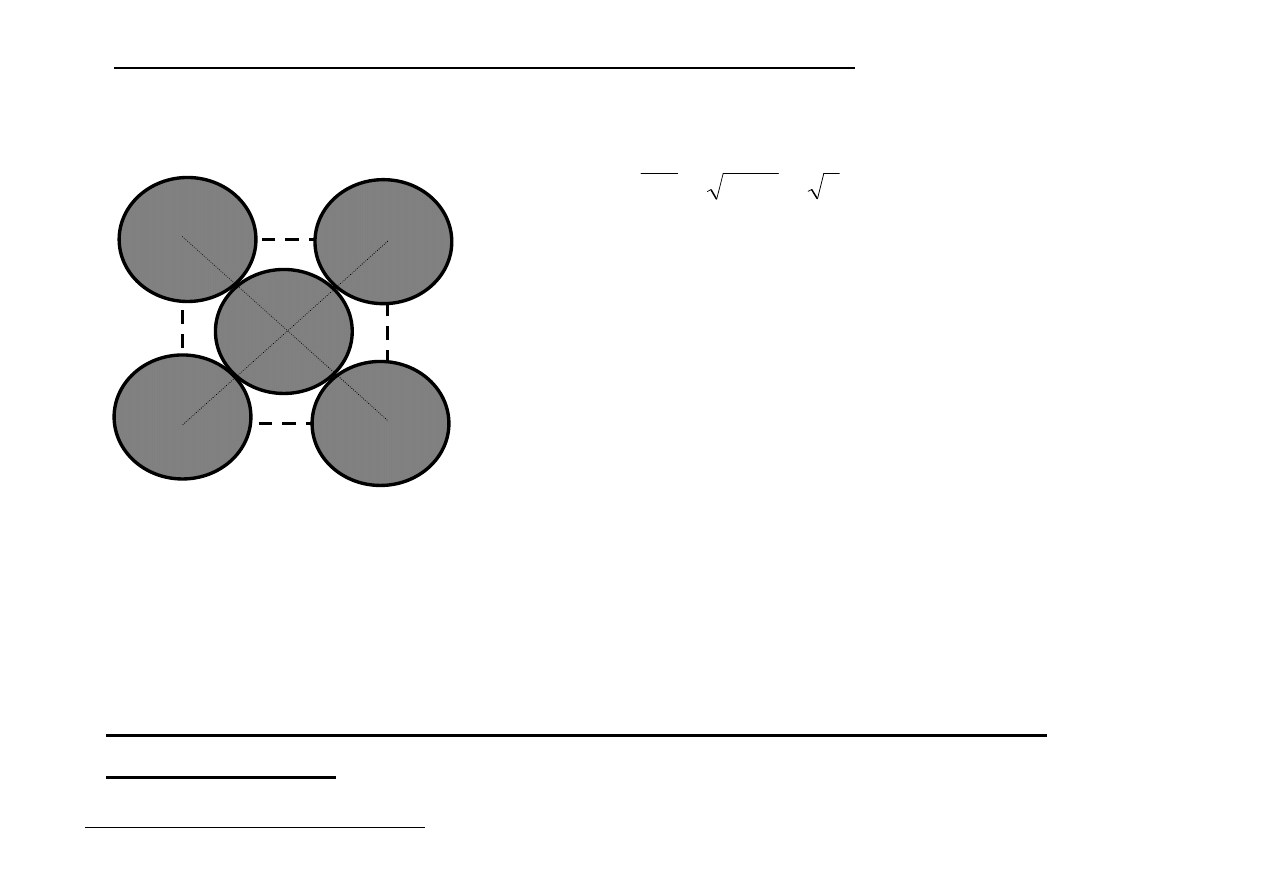
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
17/IV
b
Dla sieci typu A
1
w przypadku miedzi a = 362 pm.
Komórka sieciowa złota (też A
1
) ma a = 407 pm.
Obliczyć promień atomu złota.
Metoda badania struktury kryształów - rentgenografia -prześwietlanie promieniami
rentgenowskimi (X)
B
A
C
)
A
28
,
1
(
pm
128
r
pm
512
r
4
pm
512
pm
362
2
AC
2
AB
••••
====
====
====
⋅⋅⋅⋅
====
====
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
18/IV
b
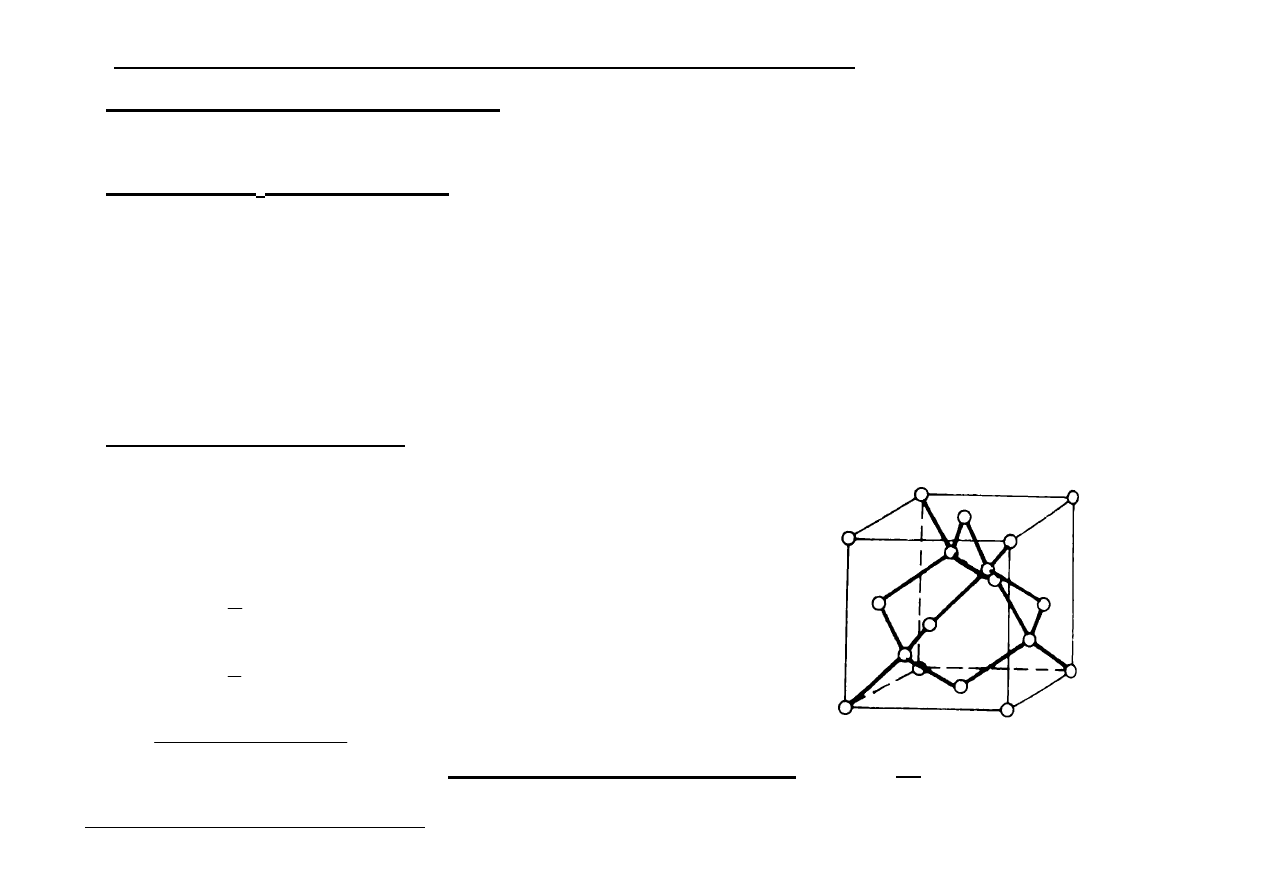
4. Sieci kowalencyjne (atomowe)
Sieć typu - A
4
(sieć diamentu)
Sieć w której krystalizuje diament - sieć regularna zewnętrznie centrowana z dodatkowymi
atomami węgla, które są na przemian w środku co drugiej kostki (komórkę dzielimy na 8
równych kostek). W węzłach sieci występują atomy między którymi są silne wiązania
kowalencyjne. W komórce jest 8 luk tetraedrycznych i połowę z nich zajmują atomy węgla a
druga połowa jest pusta.
Tutaj w węzłach są atomy a nie zręby atomowe - nie ma więc swobodnych elektronów - jest
do dielektryk (słabo przewodzi prąd elektryczny).
Liczba koordynacyjna - 4 (hybrydyzacja typu sp
3
)
Liczba atomów w komórce elementarnej:
8 x
1
8
= 1
6 x
1
2
= 3
4 x 1 = 4
ΣΣΣΣ
8 atomów C
Przykład sieci typu diamentu : Si, Ge,
αααα
-Sn
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
19/IV
b
5. Sieci jonowe
W węzłach sieciowych są dodatnie i ujemne jony, tj. kationy i aniony.
Trwałość zawdzięczają siłom elektrostatycznym tj. siłom Coulomba.
Zasada ułożenia jonów w sieci - zapewnić minimum energii
→
→
→
→
każdy jon dąży do największej liczby koordynacji.
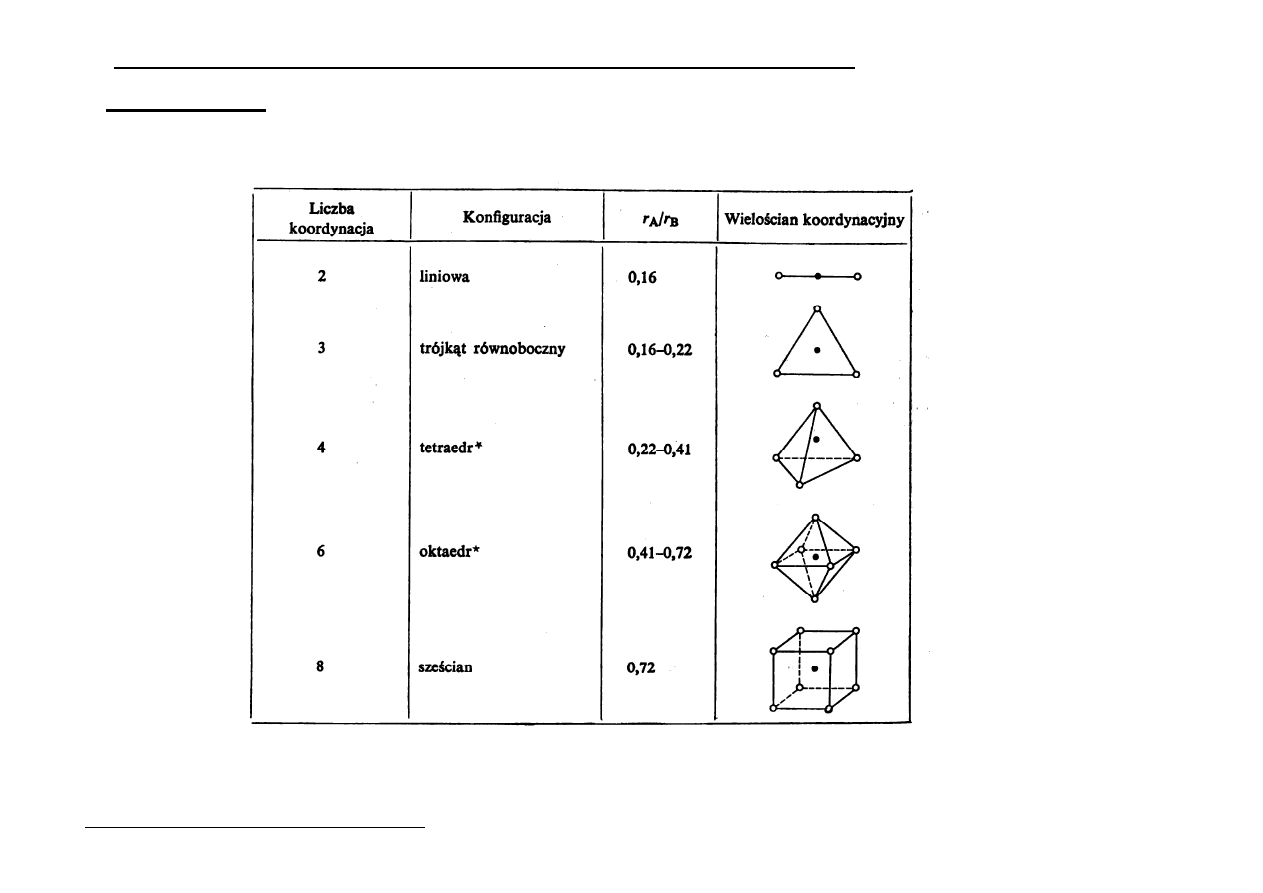
Tutaj nie można osiągnąć liczby koordynacji 12 lecz liczby mniejsze to jest : od 8 do 3
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
20/IV
b
Wg. Magnusa liczba koordynacyjna kationu jest tym większa im stosunek r
k
/r
A
jest bliższy
jedności.
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
21/IV
b
Najbardziej typowe sieci jonowe:
AB
NaCl
→
→
→
→
B
1
CsCl
→
→
→
→
B
2
αααα
-ZnS (blenda cynkowa)
→
→
→
→
B
3
AB
2
CaF
2
→
→
→
→
C
1
TiO
2
→
→
→
→
C
4
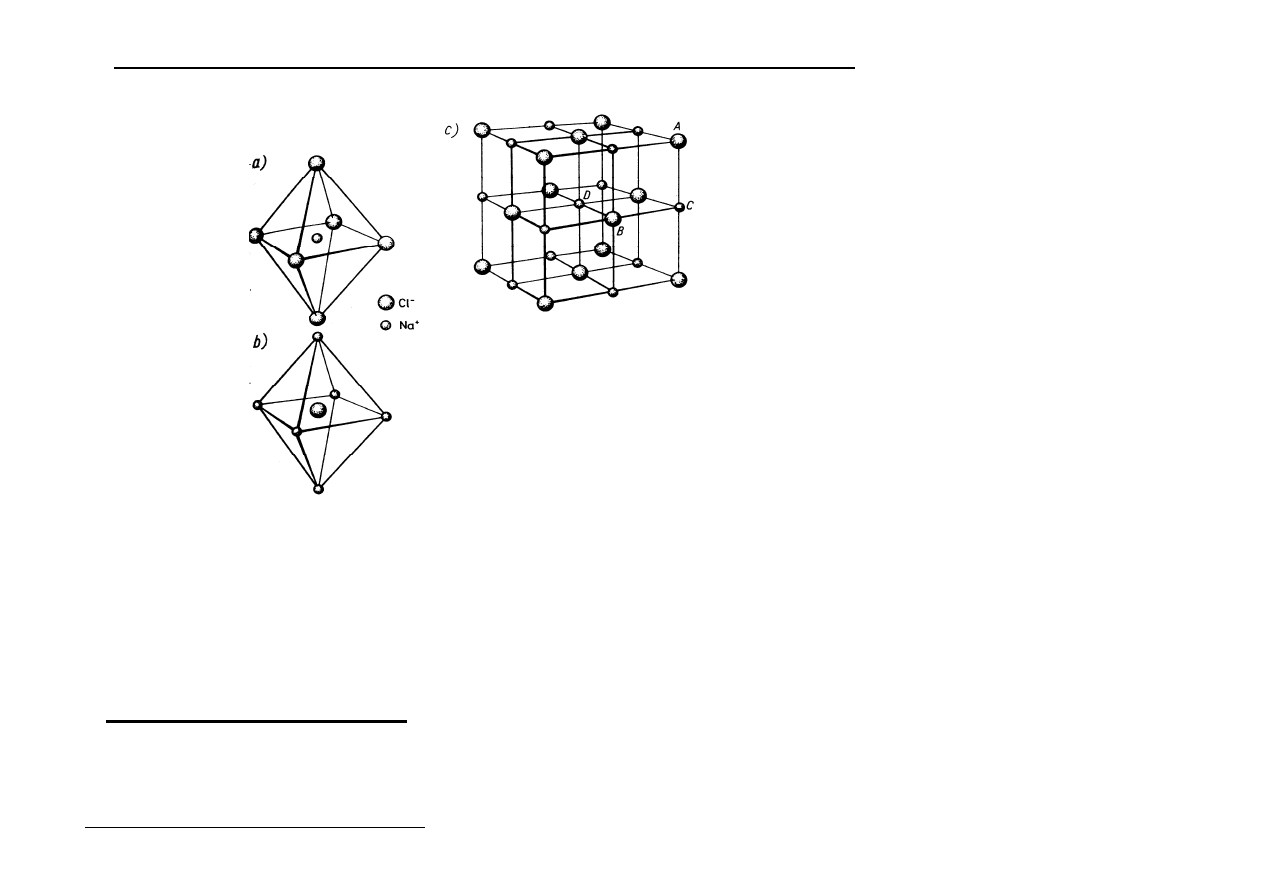
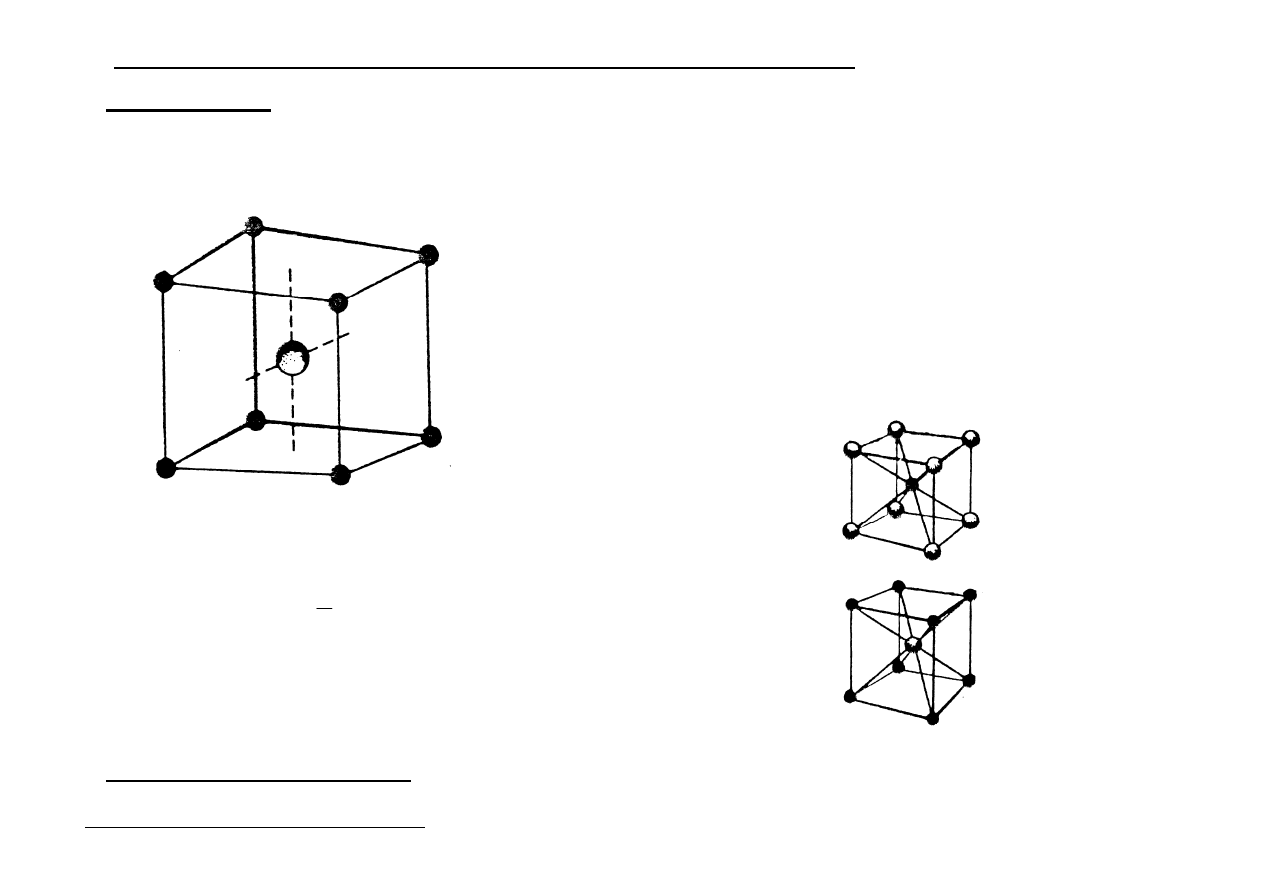
Sieć typu NaCl - regularna zewnętrznie centrowana
Wyprowadzić można z sieci A
1
→
→
→
→
w lukach oktaedrycznych tej sieci złożonej z anionów Cl
-
są kationy Na
+
, są to więc dwie sieci typu A
1
zbudowane z różnych indywiduów tj.
Na
+
i Cl
-
.
{
{
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
22/IV
b
a)
koordynacja kationów Na
+
,
b)
koordynacja anionów Cl
-
,
c)
wycinek sieci przestrzennej – komórka elementarna
Przykłady sieci typu NaCl: AgCl, AgBr, PbS
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
23/IV
b
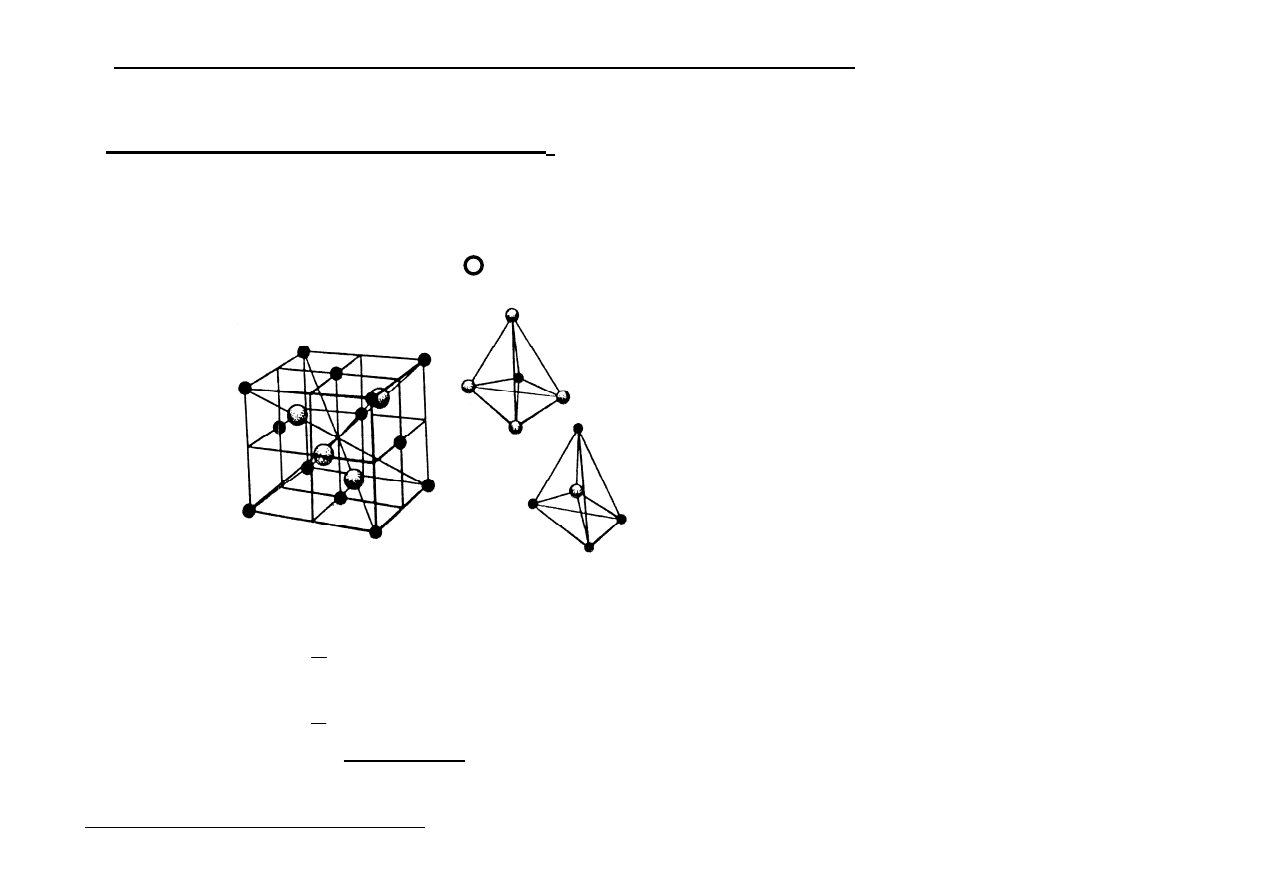
Sieć typu CsCl - regularna wewnętrznie centrowana.
Można ją wyprowadzić z sieci A
2
→
→
→
→
w środku komórki jest kation Cs
+
a w narożach aniony
Cl
-
(może być odwrotnie)
Liczba jonów w komórce elementarnej :
kationy Cs
+
1 x 1 = 1
aniony Cl
-
8 x
1
8
= 1
Liczby koordynacji
Cs
+
→
→
→
→
8 Cl
-
→
→
→
→
8
Przykłady sieci typu CsCl : TlCl, NH
4
Cl, NH
4
Br
Ta sieć przestaje być
wewnętrznie centrowana
→
→
→
→
powstają 2 komórki
prymitywne przesunięte
względem siebie.
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
24/IV
b
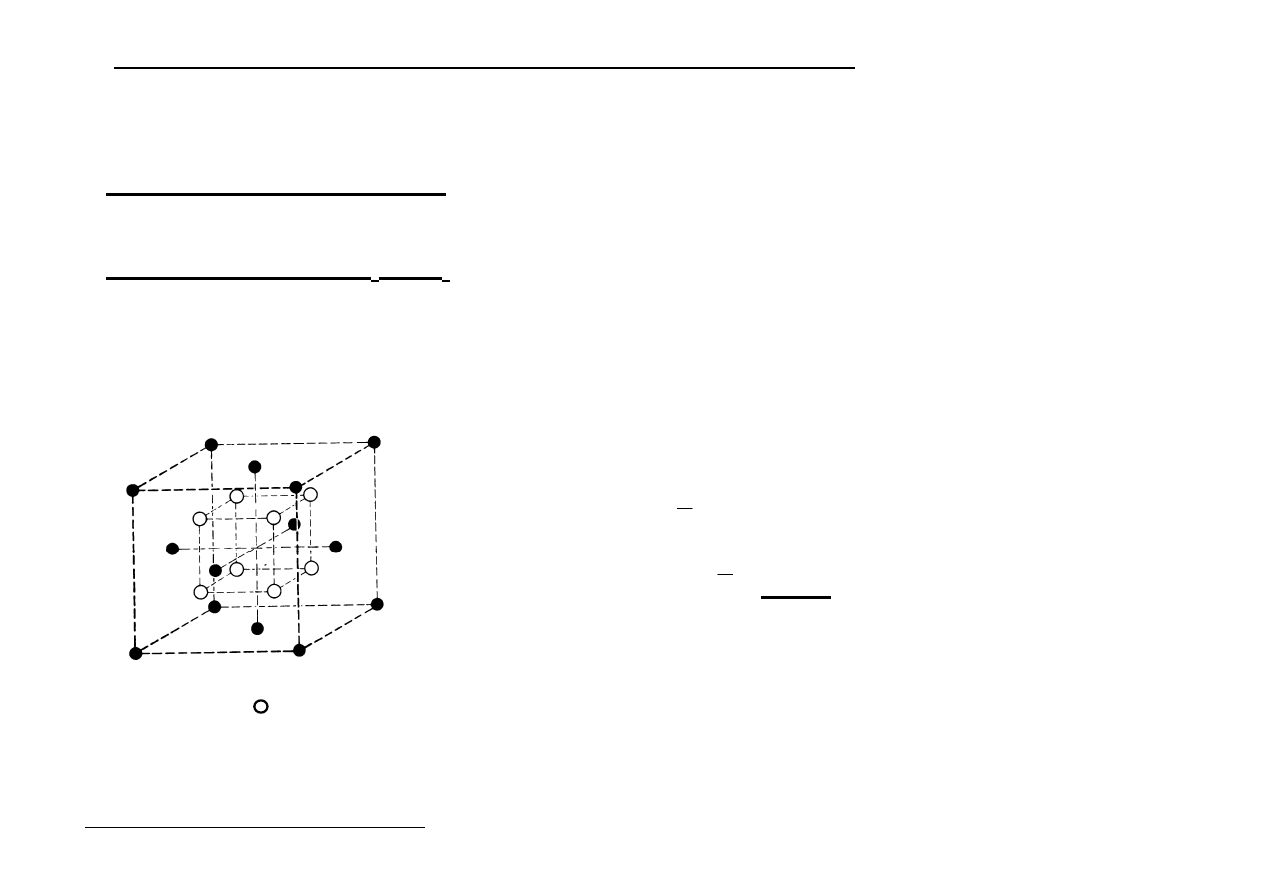
Sieć typu
αααα
-ZnS (blendy cynkowej) - B
3
Jest to sieć typu diamentu. W komórce regularnej zewnętrznie centrowanej złożonej z
kationów Zn
2+
są 4 aniony S
2-
w środkach co drugiej 1/8 części komórki.
••••
Zn
2+
, S
2-
Liczebność komórki:
Zn
2+
→
→
→
→
8 x
1
8
= 1
S
2-
→
→
→
→
4 x 1 = 4
6 x
1
2
= 3
4
⇐
⇐
⇐
⇐
liczba koordynacji
Zn
2+
→
→
→
→
4
⇐
⇐
⇐
⇐
liczba koordynacji
S
2-
→
→
→
→
4
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
25/IV
b
Jest to sieć tworzona gdy różnica elektroujemności anionu i kationu jest niewielka
→
→
→
→
oprócz
wiązania jonowego jest pewien procent wiązania kowalencyjnego
Przykłady sieci typu
αααα
-ZnS : CuCl, CuBr, AgI, HgS, ZnSe, HgSe
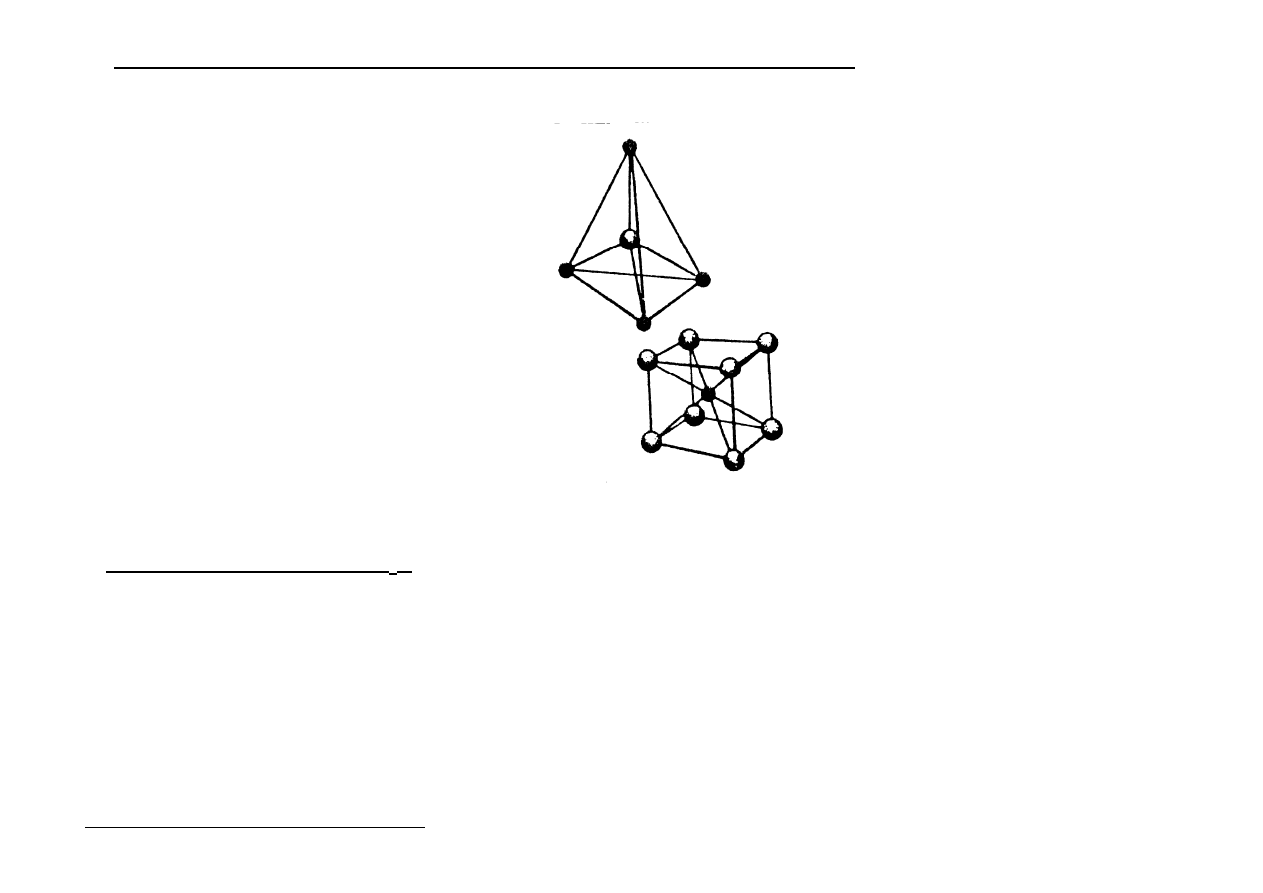
Sieć typu fluorytu (CaF
2
) - C
1
Tą sieć można wyprowadzić z sieci A
1
. W tej sieci naroża i środki ścian są wypełnione
kationami Ca
2+
. Wszystkie luki tetraderyczne w sieci są zapełnione anionami F
-
.
Komórka ulega znacznemu rozepchnięciu.
F
-
→
→
→
→
8 x 1 = 8
••••
Ca
2+
F
-
Liczebność komórki
Ca
2+
→
→
→
→
8 x
1
8
= 1
6 x
1
2
= 3
4
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
26/IV
b
Liczby koordynacji :
4 dla F
-
⇒
⇒
⇒
⇒
8 dla Ca
2+
⇒
⇒
⇒
⇒
Przykłady sieci typu CaF
2
: SrF
2
, BaF
2
, PbF
2
, LiO
2
Może też wystąpić sieć odwrotna, tj. kationy będą na miejscu anionów, a aniony na miejscu
kationów - jest to struktura antyfluorytu. Przykłady takiej sieci:
Li
2
S, Na
2
S, Cu
2
S
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
27/IV
b
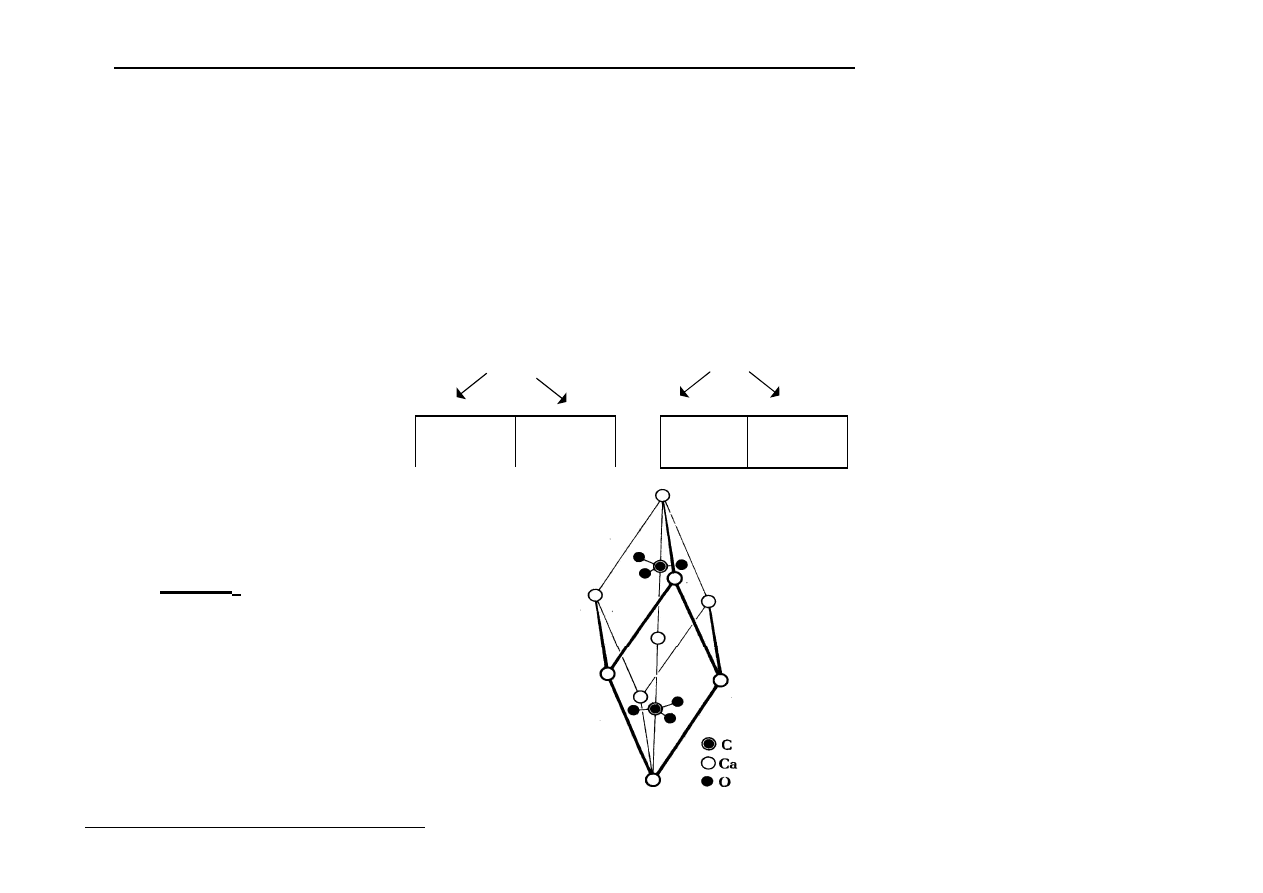
5. Inne sieci jonowe (struktury bardziej złożone)
a) sole kwasów tlenowych zawierają w sieci :
- kationy metali
- aniony kwasów tlenowych
Np.:
CaCO
3
KNO
3
Ca
2+
CO
3
2-
K
+
NO
3
-
CaCO
3
:
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
28/IV
b
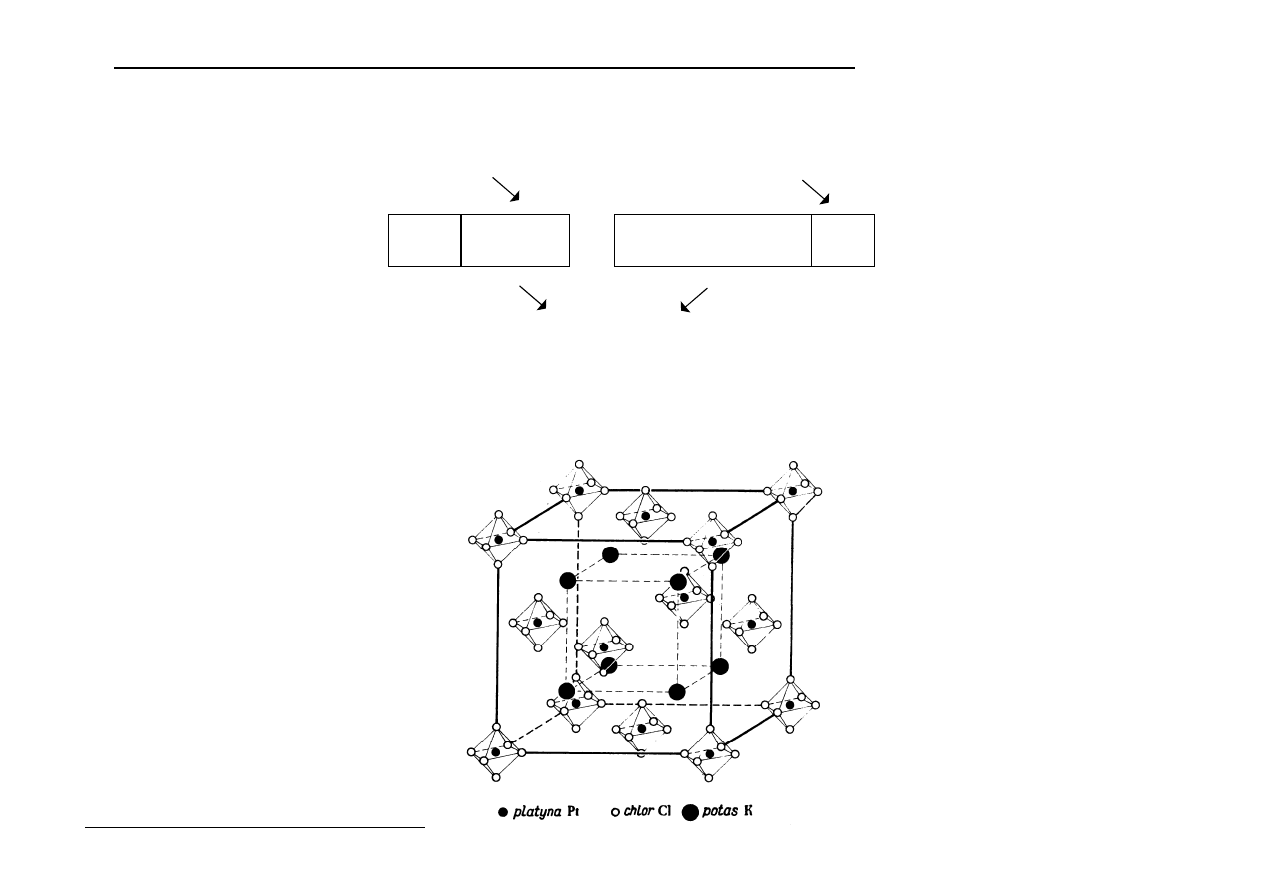
b) związki kompleksowe:
K
2
PtCl
6
[Ni(NH
3
)
6
]Cl
2
↓↓↓↓
↓↓↓↓
K
+
PtCl
6
2-
[Ni(NH
3
)
6
]
2+
Cl
-
struktura oktaedryczna
Na rysunku poniżej przedstawiono komórkę elementarną K
2
PtCl
6
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
29/IV
b
Uwaga: Oprócz soli bezwodnych (NaCl, CaF
2
) mamy jeszcze tzw. -hydraty (wodziany),
np.CuSO
4
·5H
2
O (5-cio wodny siarczan miedzi).
6. Sieci molekularne (cząsteczkowe)
W węzłach sieciowych występują cząsteczki.
Przykładem sieci cząsteczkowej jest sieć stałego chloru, jodu, azotu, wodoru czy tlenu.
Cząsteczki X
2
(X= Cl, Br, N, H, O). W węzłach sieciowych mogą też występować
wieloatomowe, np.: P
4
, S
8
, B
12
lub C
60
.
Również gazy szlachetne krystalizują w sieciach molekularnych z tym, że w węzłach są
pojedyncze atomy. Wreszcie w sieciach molekularnych występują takie związki nieorganiczne
jak dwutlenek węgla, amoniak czy woda.
Tutaj w węzłach są cząsteczki a oddziaływania między nimi to słabe oddziaływania typu
van der Waalsa lub wiązania wodorowe.
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
30/IV
b
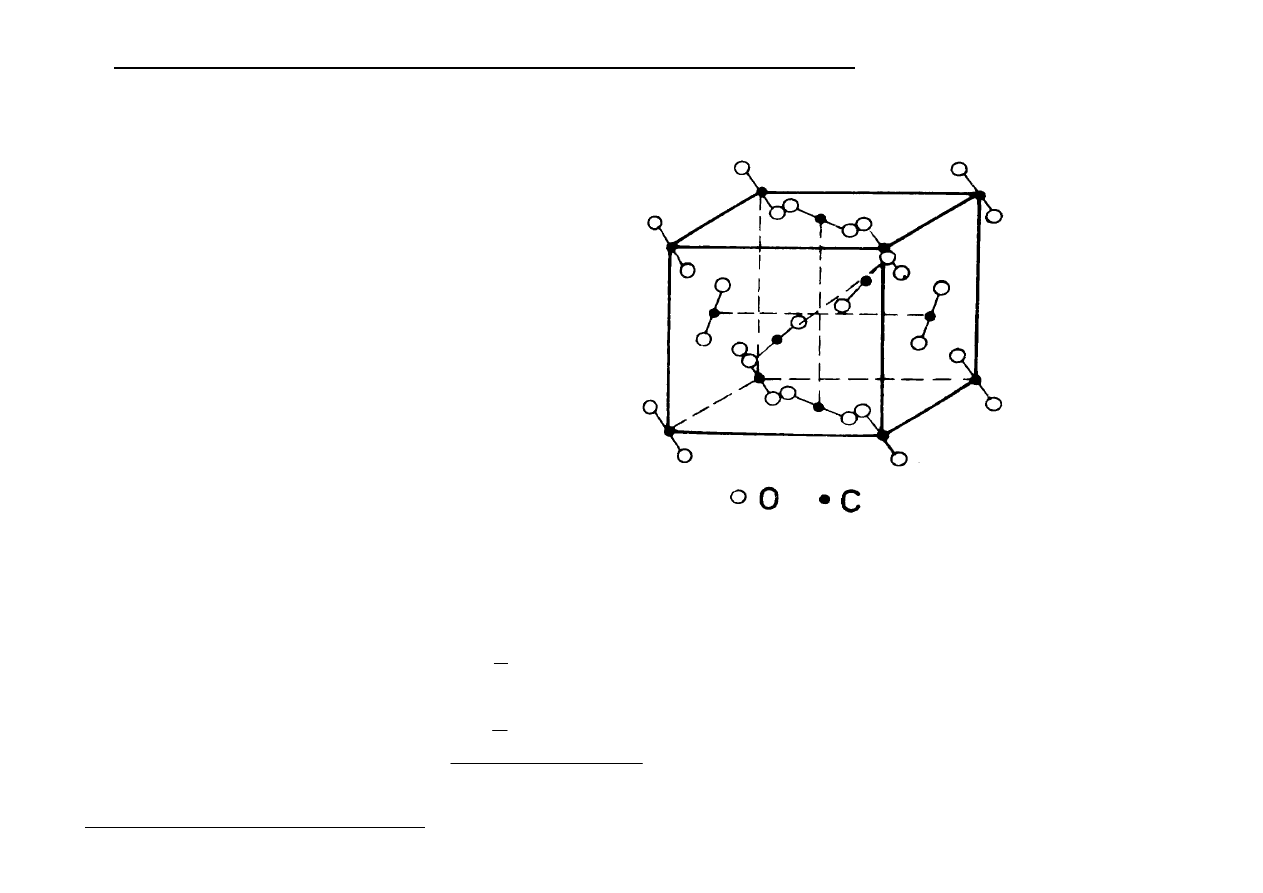
Struktura
krystaliczna
stałego CO
2
- sieć typu A
1
Cząsteczki CO
2
występują :
a) w narożach sześcianu
1
=
8
1
x
8
b) w środkach ścian
3
2
1
x
6
====
Razem 4 cz. CO
2
Władysław Walkowiak - Chemia Nieorganiczna II – CHC1041w- (PWr)
Budowa Ciała Stałego IVb
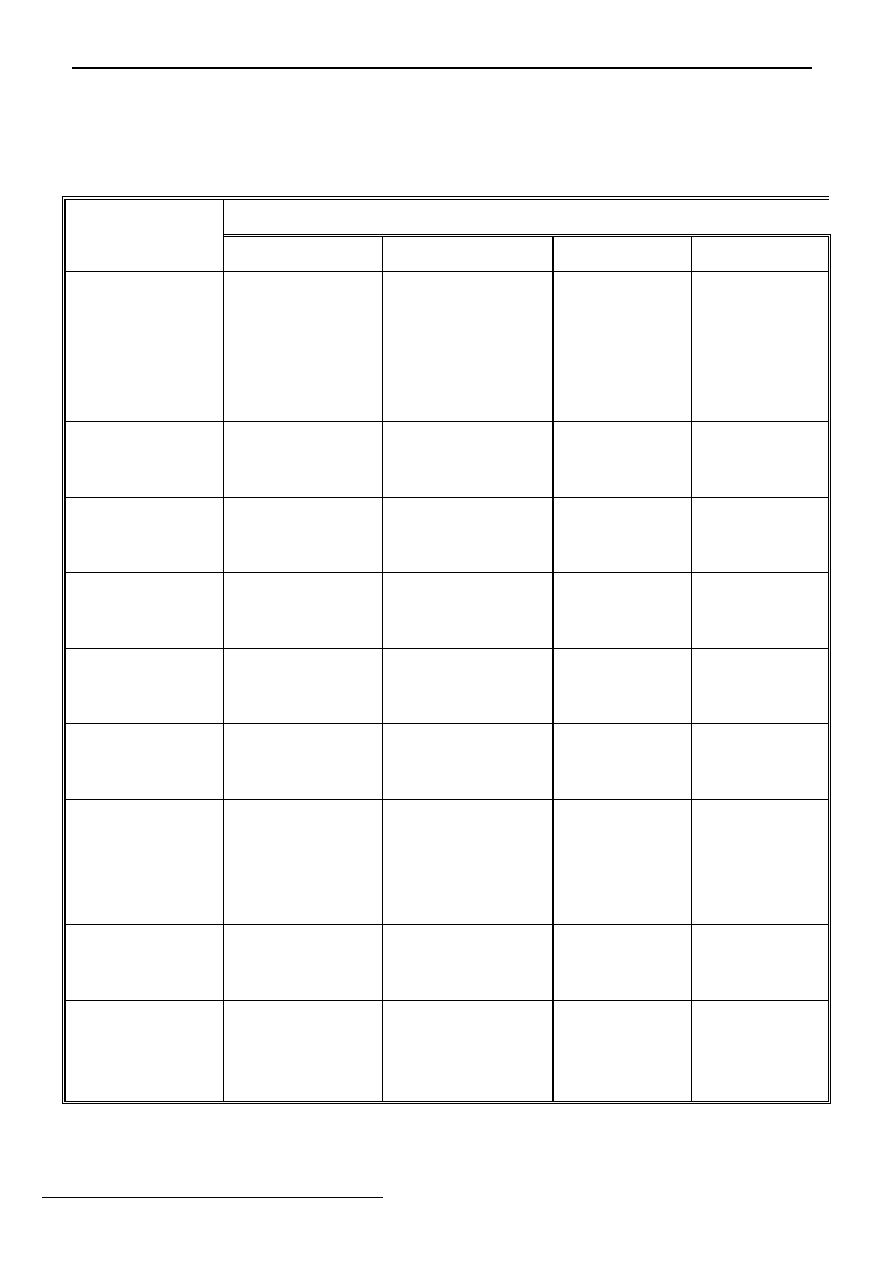
7. Zestawienie typów sieci
Właściwości fizykochemiczne kryształów a rodzaj sieci
Kryształy
molekularne
kowalencyjne
jonowe
metaliczne
Jednostki
cząsteczki
atomy
kationy i
aniony
dodatkowo
naładowane
rdzenie
atomowe
i swobodne
elektrony
Siły wiążące
Van der
Waalsa
wiązania
kowalencyjne
wiązania
jonowe
oddz. rdzeni
atomowych z
elektronami
Energia
sieciowa,
kJ/mol
He: 2,5
CO
2
: 23,5
H
2
O: 53,5
C (diament): 710
SiO
2
: 1720
NaCl: 770
CaF
2
: 2610
W: 840
Na: 105
Wytrzymałość
mechaniczna
i twardość
mała,
miękkie
duża,
twarde
duża
zazwyczaj
duża,
ciągliwe
Temperatura
topnienia
niska
wysoka
wysoka
zmienia się w
szerokich
granicach
Współczynnik
rozszerzalności
cieplnej
duży
mały
mały
duży
Przewodnictwo
elektryczne w
stanie stałym
małe (izolatory) bardzo małe
nie
przewodzą
prądu w
stanie
stałym
(x)
duże
Przewodnictwo
w stanie
stopionym
bardzo
małe
bardzo małe
duże
duże
Przykłady
helowce,
H
2
, O
2
, N
2
, I
2
,
P
4
, C
60
,
CO
2
, H
2
O
C (diament),
Si,
αααα
-Sn, SiC,
SiO
2
NaCl,
CsCl,
KNO
3
,
Na
2
SO
4
Cu, Ag, Au,
W, Mo, Mg
(x)
Przewodzą prąd elektryczny po roztworzeniu w rozpuszczalnikach polarnych,
np. w wodzie.
Wyszukiwarka
Podobne podstrony:
4 Budowa ciala stalego id 3714 Nieznany
4 Budowa ciala stalego id 3714 Nieznany
Budowa ciała stałego
wykład 8 budowa ciała stałego
WYK-4c.Budowa ciala stalego
Budowa ciała stałego 3
4. Budowa ciala stałego, pwr biotechnologia(I stopień), II semestr, Chemia nieorganiczna, Wykłady Ap
Budowa ciała stałego 2
Budowa ciała stałego 2
5 Teoria pasmowa ciala stalego Nieznany (2)
Fizyka Ciala Stalego II id 1766 Nieznany
5 Teoria pasmowa ciala stalego Nieznany (2)
28 Zjawiska towarzyszące bombardowaniu ciała stałego elektro
więcej podobnych podstron