
Acetylocholina
Acetylocholina
Histamina
Histamina
Bradykinina
Bradykinina
Substancja P
Substancja P
NO
ET1
ET2
ET3
PGI
2
Angiotensyna I
Angiotensyna I
Angiotensyna II
Angiotensyna II
Konwertaza
Konwertaza
KOMPLEKSY AKTYNA
KOMPLEKSY AKTYNA
-
-
MIOZYNA
MIOZYNA
CIA
CIA
Ł
Ł
KA WEIBELA
KA WEIBELA
-
-
PALADE
PALADE
’
’
A (
A (
czynnik VIII krzepni
czynnik VIII krzepni
ę
ę
cia)
cia)
Ć
WICZENIE 22(7). 31 marca i 1, 2 kwietnia 2010 r.
Temat: Układ kr
ąż
enia.
1. Serce (preparat nr 33).
2. Aorta barwiona rezorcyn
ą
fuksyn
ą
(preparat nr 31).
3.Aorta barwiona hematoksylin
ą
– eozyn
ą
(preparat nr 30).
4.
ś
yła i t
ę
tnica
ś
redniego kalibru (preparat nr 29).
5. Naczynia włosowate krezka (preparat nr 28).
6.
ś
yła nasienna, komórki epitelioidalne (preparat nr 24).
7. Regulacja rozwoju i regeneracji naczy
ń
krwiono
ś
nych (tekst z rycinami 22/1).
8. Schemat naczynia włosowatego (schemat 22/2).
9. Naczynie włosowate siatkówki (EM 22/3 - powi
ę
kszenie 10 tys. razy).
10. Model reologiczny aorty (schemat 22/4).
11. Schemat budowy
ś
cian t
ę
tnic typu spr
ęż
ystego (schemat 22/5).
12. Model reologiczny t
ę
tnic typu mi
ęś
niowego (schemat 22/6).
13. Schemat budowy
ś
cian t
ę
tnic typu mi
ęś
niowego (schemat 22/7).
14. Udział komórek
ś
ródbłonka w regulacji skurczu mi
ęś
niówki gładkiej naczy
ń
krwiono
ś
nych (schemat 22/8).
15. Ciałka Weibel Palade'a (EM 22/9).
16. Komórki epitelioidalne w anastomozach t
ę
tniczo-
ż
ylnych (Tekst 22/10).
17. Czynnik wzrostu
ś
ródbłonka (tekst 22/11).
Tekst z rycinami 22/1.
REGULACJA ROZWOJU I REGENERACJI NACZY
Ń
KRWIONO
Ś
NYCH
Układ krwiono
ś
ny stanowi wa
ż
ny element spajaj
ą
cy poszczególne tkanki i narz
ą
dy w jeden organizm.
Cały
układ
krwiono
ś
ny
podobnie
jak
układ
limfatyczny
jest
wysłany
nabłonkiem
pochodzenia
mezenchymatycznego (
ś
ródbłonkiem). Komórki
ś
ródbłonka, ogl
ą
dane od strony
ś
wiatła naczynia, maj
ą
kształt
wydłu
ż
onych wielok
ą
tów (najcz
ęś
ciej sze
ś
ciok
ą
tów) o wymiarach ok. 10 x 30
µ
m, z osi
ą
dług
ą
równoległ
ą
do osi
naczynia. Grubo
ść
cytoplazmy wynosi ok. 0,2
µ
m, a cytoplazmy i j
ą
dra ok. 3
µ
m.
Ś
rednica naczy
ń
włosowatych jest
porównywalna z wielko
ś
ci
ą
erytrocytów, co zapewnia efektywn
ą
wymian
ę
gazów (rycina 1 i 2 w materiałach). Niektóre
komórki
ś
ródbłonka
ż
ył, t
ę
tnic i kapilar (np. w mózgu, grasicy) tworz
ą
poł
ą
czenia typu occludens i neksus, które sprawiaj
ą
,
ż
e jest on szczelny (wymiana substancji odbywa si
ę
poprzez transcytoz
ę
). Przechodzenie jonów mi
ę
dzy komórkami
zapewniaj
ą
poł
ą
czenia typu neksus. Poł
ą
czenia te ulegaj
ą
czasem zerwaniu, zwłaszcza podczas migracji komórek
macierzystych zwi
ą
zanej z tworzeniem nowych naczy
ń
, prawidłowych oraz patologicznych nowotworu (w tych ostatnich
zwykle nie ulegaj
ą
ponownemu odtworzeniu). Tak
ż
e VEGF oraz działaj
ą
ca z nim synergistycznie Ang-2 powoduj
ą
rozszerzenie tych poł
ą
cze
ń
natomiast Ang-1 działa przeciwnie. W przypadku braku tej kostymulacji mo
ż
e doj
ść
do
obumarcia komórek
ś
ródbłonka.
Ś
ródbłonek, szczególnie kapilar i małych t
ę
tnic zawiera liczne pory, powstałe przez fuzj
ę
p
ę
cherzyków, słu
żą
ce do
transportu makrocz
ą
steczek. Swoistymi strukturami cytoplazmy endotelium
wsierdzia, t
ę
tnic i
ż
ył s
ą
pałeczkowate twory o wymiarze 0,2 x 0,4
µ
m,
otoczone błon
ą
– ciałka Weibela-Palade’a. Zawieraj
ą
białko von
Willebranda oraz mikrotubule.
Ś
ródbłonek, dzi
ę
ki obecno
ś
ci kompleksów
aktyny i miozyny, ma zdolno
ść
kurczenia si
ę
. Dzi
ę
ki temu zwi
ę
ksza si
ę
jego przepuszczalno
ść
. Na wolnej powierzchni komórek, szczególnie nad
j
ą
drami, znajduj
ą
si
ę
grupy mikrokosmków, a w błonie komórkowej liczne
glikoproteiny.
Ś
ródbłonek bierze udział w transporcie gazów i substancji
chemicznych, w sposób bierny – zgodny z gradientem st
ęż
e
ń
(np. O
2
,
CO
2
) lub czynny – głównie przez transcytoz
ę
. Przez pory oraz przestrzenie mi
ę
dzykomórkowe mog
ą
przechodzi
ć
leukocyty i erytrocyty – diapedeza.
Komórki syntetyzuj
ą
i uwalniaj
ą
hormony miejscowe: prostacyklin
ę
PGI
2
(przeciwdziała agregacji płytek i rozszerza naczynia), inne prostaglandyny oraz
endoteliny ET-1, ET-2, ET-3 (21-aminokwasowe peptydy powstaj
ą
ce z 200-
aminokwasowych proendotelin, kurcz
ą
ce mi
ęś
niówk
ę
naczy
ń
oraz b
ę
d
ą
ce
mitogenami).
Ś
ródbłonek wytwarza równie
ż
tlenek azotu NO, przez który działaj
ą
rozkurczaj
ą
co na naczynia takie substancje jak: acetylocholina, histamina,
bradykinina, substancja P i inne.
Endotelium wydziela tak
ż
e Ang1 i Ang2 oraz konwertaz
ę
powoduj
ą
c
ą
przej
ś
cie
angiotensyny-1 w angiotensyn
ę
-2.
PDGFB, uwalniany z ECs po stymulacji VEGF, wpływa głównie na tworzenie
si
ę
i dojrzewanie
ś
ciany naczy
ń
.
Wzajemna interakcja pomi
ę
dzy otaczaj
ą
cymi tkankami a komórkami
ś
ródbłonka jest jednym z podstawowych procesów odpowiedzialnym za ró
ż
nicowanie oraz prawidłowe funkcje organów
ludzkiego ciała.
Najwa
ż
niejszym czynnikiem wpływaj
ą
cym na angiogenez
ę
jest VEGF (czynnik wzrostu
ś
ródbłonka naczy
ń
–
vascular endothelial growth factor). Pierwsze wzmianki o istnieniu substancji stymuluj
ą
cej angiogenez
ę
pojawiły si
ę
w
1948 roku, po badaniach Michaelsona nad powstawaniem naczy
ń
siatkówki. W latach osiemdziesi
ą
tych, po wyizolowaniu
jej przez Sengera i współpracownicy, z tkanek nowotworowych w 1983 roku, substancja ta znana była jako czynnik
przepuszczalno
ś
ci naczy
ń
(VPF – vascular permeability factor – ze wzgl
ę
du na wyst
ę
puj
ą
ce rozszczelnienie
ś
ródbłonka

po zadziałaniu nim na naczynia). Natomiast za dat
ę
odkrycia funkcji angiogenetycznych VPF oraz nadania mu obecnej
nazwy przyjmuje si
ę
rok 1989 (badania prowadzone w laboratoriach Uniwersytetu San Francisco i firmy Genentech).
VEGF jest wydzielany przez liczne komórki, m.in. przez włókna obwodowych nerwów czuciowych w skórze płodu,
p
ę
cherzyki płucne czy poddane działaniu hipoksji astrocyty w czasie tworzenia si
ę
naczy
ń
siatkówki. Receptory dla niego
znajduj
ą
si
ę
głównie na komórkach
ś
ródbłonka. Stanowi on czynnik toruj
ą
cy dla tworz
ą
cych si
ę
naczy
ń
Poza VEGF, który jest ogólnoustrojowym czynnikiem angiogenetycznym, istniej
ą
tak
ż
e tkankowo-specyficzne
czynniki wzrostu, takie jak EG-VEGF (endocrine gland VEGF) wydzielany tylko przez gruczoły produkuj
ą
ce hormony
sterydowe (np. kora nadnerczy) oraz działaj
ą
cy proliferacyjnie głównie na naczynia tych narz
ą
dów (ale nie na
ś
ródbłonek
aorty, naczy
ń
p
ę
powinowych czy skóry). By
ć
mo
ż
e zostan
ą
wkrótce odkryte tak
ż
e czynniki specyficzne dla innych
narz
ą
dów.
Regulacja rozwoju naczy
ń
na przykładzie tkanki nerwowej.
Przykładem wzajemnego oddziaływania
ś
ródbłonka i tkanki nerwowej mog
ą
by
ć
do
ś
wiadczenia z
przeszczepianiem tkanki mózgowej z naczyniami do innych tkanek oraz naczy
ń
obwodowych do mózgu. W pierwszym
przypadku zmniejszała si
ę
liczba poł
ą
cze
ń
ś
cisłych mi
ę
dzy ECs (endothelial cells, komórki
ś
ródbłonka) oraz zwi
ę
kszała
przepuszczalno
ść
naczy
ń
, w drugim - nabierały charakteru naczy
ń
mózgowych (obwódki zamykaj
ą
ce occludens i
przylegania adherens miedzy komórkami
ś
ródbłonka, ci
ą
gła i dobrze rozwini
ę
ta błona podstawna) wraz z wytworzeniem
bariery krew-mózg.
Równie
ż
w dojrzałym hipokampie istnieje współdziałanie
ś
ródbłonka oraz neuronów. W miejscach podziału
naczy
ń
oraz na ko
ń
cach kapilar istniej
ą
konglomeraty neuroblastów, gleju i angioblastów, mog
ą
ce by
ć
ź
ródłem nowych
neuronów w dorosłym organizmie.
Wydaje si
ę
,
ż
e czynniki wydzielane przez ECs, jak np. BDNF (brain-derived neurotrophic factor, mózgowy czynnik
neurotroficzny), s
ą
konieczne do prze
ż
ycia, migracji, wzrostu oraz dojrzewania neuronów. Wytwarzanie BDNF przez
ś
ródbłonek stymulowane jest przez VEGF.
Nerwy i naczynia pokonuj
ą
cz
ę
sto te same szlaki w trakcie embriogenezy. Przykładem mog
ą
by
ć
ko
ń
czyny gdzie
t
ę
tnice i nerwy tworz
ą
wspólne p
ę
czki zaopatruj
ą
ce mi
ę
snie i ko
ś
ci. Spowodowane jest to prawdopodobnie
wykorzystywaniem przez oba te układy wspólnych mechanizmów przeka
ź
nikowych, składaj
ą
cych si
ę
z semaforyn i VEGF
oraz receptorów dla nich – neuropilin, wyst
ę
puj
ą
cych na komórkach
ś
ródbłonka i aksonach neuronów.
Rozwój naczy
ń
w siatkówce oka.
W trakcie rozwoju embrionalnego, pierwsz
ą
sieci
ą
naczy
ń
siatkówki s
ą
te wychodz
ą
ce ze szczytu nerwu
wzrokowego i rozpostarte na wewn
ę
trznej powierzchni tej cz
ęś
ci oka. Towarzyszy im bli
ź
niacza sie
ć
astrocytów
pochodz
ą
cych równie
ż
z tego nerwu – uwa
ż
a si
ę
,
ż
e naczynia pod
ąż
aj
ą
za powstaj
ą
cymi wypustkami komórek
glejowych. Po wytworzeniu si
ę
pierwotnej, jednopoziomowej sieci, naczynia zaczynaj
ą
wnika
ć
gł
ę
biej w siatkówk
ę
, a
ż
do
warstwy splotowatej wewn
ę
trznej, formuj
ą
c drug
ą
, równoległ
ą
sie
ć
naczyniow
ą
(niezale
ż
n
ą
od astrocytów). Pierwotna
sie
ć
powstaje w mechanizmie waskulogenezy (formowanie si
ę
naczy
ń
de novo z komórek prekursowych, migruj
ą
cych i
ró
ż
nicuj
ą
cych w komórki
ś
ródbłonka), natomiast wtórna – angiogenezy (powstawanie nowych naczy
ń
w wyniku
rozrastania si
ę
istniej
ą
cej sieci naczyniowej).
Wa
ż
n
ą
rol
ę
w rozwoju siatkówki odgrywa VEGF. Poza
ś
ródbłonkiem, receptory dla tego czynnika wzrostu
znajduj
ą
si
ę
na komórkach glejowych oraz komórkach barwnikowych siatkówki. Poł
ą
czenie VEGF z receptorem powoduje
migracj
ę
tych komórek (bez proliferacji). VEGF wydzielany jest zarówno przez astrocyty jak i komórki
ś
ródbłonka – jest to
wi
ę
c zarówno oddziaływanie autokrynne jak i parakrynne.
Brak wła
ś
ciwej kontroli procesów formowania si
ę
naczy
ń
w siatkówce mo
ż
e prowadzi
ć
do wielu schorze
ń
, takich
jak: retinopatia cukrzycowa, starcze zwyrodnienie plamki, retinopatia wcze
ś
niaków.
Angiogeneza w procesie ko
ś
ciotworzenia.
Dosy
ć
dobrze poznane jest wzajemne oddziaływanie chrz
ą
stki i ko
ś
ci z naczyniami (zwłaszcza podczas
osteogenezy na podło
ż
u chrz
ę
stnym). Prawidłowa, spoczynkowa chrz
ą
stka wydziela silne czynniki antyangiogenetyczne i
w zwi
ą
zku z tym pozbawiona jest naczy
ń
. Jednak w pocz
ą
tkowym okresie osteogenezy, kiedy nast
ę
puje proliferacja
chondrocytów, wyst
ę
puje równie
ż
zwi
ę
kszenie ekspresji czynników wzrostu naczy
ń
w chondrocytach. W chrz
ą
stk
ę
zaczynaj
ą
wnika
ć
naczynia, chondrocyty wchodz
ą
w apoptoz
ę
a w ich miejsce zaczynaj
ą
migrowa
ć
osteoblasty i
osteoklasty.
Eksperymenty ze wspóln
ą
hodowl
ą
chondrocytów i komórek
ś
ródbłonka wykazały,
ż
e te ostatnie wydzielaj
ą
czynniki powoduj
ą
ce hipertrofi
ę
chondrocytów oraz opó
ź
niaj
ą
ich ró
ż
nicowanie. Hipertroficzne chondrocyty wydzielaj
ą
VEGF, który dodatkowo pobudza wnikanie naczy
ń
. Tworzy si
ę
wi
ę
c p
ę
tla dodatniego sprz
ęż
enia zwrotnego.
Badania in vitro z u
ż
yciem HUVEC (human umbilical vein endothelial cells, komórki
ś
ródbłonka pochodz
ą
ce z
ż
yły
p
ę
powinowej) i komórek prekursorowych osteoblastów umo
ż
liwiły potwierdzenie komunikowanie si
ę
tych dwóch rodzajów
komórek (przez koneksyn
ę
-43), co jest konieczne do ró
ż
nicowania si
ę
komórek prekursorowych w osteoblasty.
Regeneracja
ś
ródbłonka
Ś
redni czas
ż
ycia komórek
ś
ródbłonka wynosi ok. 100 dni, w zwi
ą
zku z tym konieczne jest ich ci
ą
głe odtwarzanie
w celu utrzymania ci
ą
gło
ś
ci tej warstwy
ś
ciany naczynia.
Jednym ze spostrze
ż
e
ń
poczynionych w badaniach in vivo jest obserwacja dotycz
ą
ca szybszego skracania si
ę
telomerów w komórkach
ś
ródbłonka naczy
ń
, które najcz
ęś
ciej s
ą
dotkni
ę
te zmianami mia
ż
d
ż
ycowymi (takie jak np.
t
ę
tnice wie
ń
cowe). Istniej
ą
miejsca, np. t
ę
tnice biodrowe, gdzie
ś
ródbłonek jest szczególnie nara
ż
ony na działanie sił
hemodynamicznych. Wyst
ę
puje w nich znaczna proliferacja komórek, a w jej nast
ę
pstwie szybsze skracanie telomerów i
zwi
ę
kszone ryzyko wyst
ą
pienia mia
ż
d
ż
ycy. W hodowlach in vitro, ECs z zaburzon
ą
funkcj
ą
telomerów (wył
ą
czonym
genem dla białka TRF2) maj
ą
zahamowan
ą
proliferacje oraz zmieniony fenotyp. S
ą
powi
ę
kszone, zwi
ę
ksza si
ę
ekspresja
inhibitorów kinaz zale
ż
nych od cyklin (cyclin-dependent kinase, CDK), ICAM-1, spada natomiast produkcja tlenku azotu
przez
ś
ródbłonkow
ą
syntetaz
ę
tlenku azotu. Podobne zmiany wyst
ę
puj
ą
tak
ż
e w replikacyjnym starzeniu si
ę

niezmienionych komórek (po około 50 podziałach). Komórki te maj
ą
równie
ż
wi
ę
ksz
ą
aktywno
ść
ß-galaktozydazy,
enzymu charakterystycznego dla “starych” komórek.
W niekorzystnych warunkach, takich jak: zmniejszenie przepływu czy st
ęż
enia ró
ż
nych substancji (np. VEGF,
bFGF, MMPs, PDGF czy NO), mo
ż
e nast
ą
pi
ć
regresja naczy
ń
. Przykładem mo
ż
e by
ć
zanik kł
ę
buszków nerkowych w
przypadku braku VEGF.
Komórki
ś
ródbłonka pochodz
ą
z angioblastów płodu (podobne pochodzenie jak komórek krwi) oraz z komórek
prekursorowych
ś
ródbłonka (mog
ą
tak
ż
e wydziela
ć
czynniki wzrostu naczy
ń
) i komórek macierzystych szpiku u dorosłych.
Wszystkie te rodzaje komórek maj
ą
podobne antygeny, receptory dla podobnych cytokin (np. VEGF, PlGF, angiopoetyny
(Ang)-1, ID)) oraz mog
ą
przekształca
ć
si
ę
jedne w drugie (np. HSCs) mog
ą
powstawa
ć
w
ż
yciu płodowym z komórek
ś
ródbłonka a leukocyty i HSCs mog
ą
zarówno przekształca
ć
si
ę
w EC jak i stymulowa
ć
formowanie naczy
ń
), ró
ż
ni
ą
si
ę
natomiast czasem i miejscem wyst
ę
powania.
Tak
ż
e w pó
ź
niejszych etapach
ż
ycia istnieje grupa komórek, kr
ążą
ce
ś
ródbłonkowe komórki prekursorowe,
wywodz
ą
ca si
ę
głównie ze szpiku i maj
ą
ce znaczenie w naprawie uszkodzonych naczy
ń
oraz wzro
ś
cie guzów. Ludzkie
EPCs charakteryzuj
ą
si
ę
obecno
ś
ci
ą
antygenów powierzchniowych takich jak np.: CD31,CD34, CD133, CD146, CXCR4,
c-Kit, VE-cadherin, VEGFR2, vWF. W stanie spoczynku CEPs VEGFR
+
stanowi
ą
tylko 0,01% j
ą
drzastych komórek krwi.
Je
ż
eli konieczny jest wzrost
ś
ródbłonka, nast
ę
puje mobilizacja tych komórek (ich liczba we krwi wci
ą
gu 24 godzin wzrasta
do 12%), po czym osiadaj
ą
one w miejscach gdzie został odsłoni
ę
ty kolagen i fibronektyna, a nast
ę
pnie, w zale
ż
no
ś
ci od
działaj
ą
cych na nie czynników, przekształcaj
ą
si
ę
w
ś
ródbłonek (pod wpływem VEGF-A) lub mi
ęś
niówk
ę
gładk
ą
(dzi
ę
ki
obecno
ś
ci PDGF). Uwa
ż
a si
ę
,
ż
e VEGF-A, metaloproteinazy oraz PlGF s
ą
odpowiedzialne za uwalnianie komórek
prekursorowych ze szpiku. Komórki prekursorowe maj
ą
zdecydowanie wi
ę
ksze zdolno
ś
ci proliferacyjne ni
ż
dojrzałe ECs.
Regeneracja
ś
ródbłonka naczy
ń
przy udziale EPCs (endothelial progenitor (precursor) cells – komórek
prekursorowych
ś
ródbłonka).
Angiogeneza w gojeniu ran.
Do szybkiej i efektywnej naprawy uszkodzonych tkanek konieczne jest dostarczenie do nich odpowiedniej ilo
ś
ci
tlenu, substancji od
ż
ywczych, czynników wzrostu oraz komórek „naprawczych” (usuwaj
ą
cych zniszczon
ą
tkank
ę
,
drobnoustroje, odbudowuj
ą
cych struktur
ę
narz
ą
du). Ju
ż
w pocz
ą
tkowym okresie gojenia (faza proliferacyjna) mo
ż
na
stwierdzi
ć
wysokie st
ęż
enie jednego z czynników angiogenetycznych – zasadowego czynnika wzrostu fibroblastów (bFGF
– basic fibroblasts growth factor). Powoduje on migracje i proliferacje komórek
ś
ródbłonka. Pochodzi prawdopodobnie z
zapasów nagromadzonych w płytkach krwi i uszkodzonej tkance gdy
ż
jego maksymalne st
ęż
enie obserwuje si
ę
w ci
ą
gu
pierwszych 24 godzin po urazie a nast
ę
pnie spada. W przeciwie
ń
stwie do bFGF, poziom VEGF nie wzrasta bezpo
ś
rednio
po uszkodzeniu, ale dopiero w kilka dni po nim (ze szczytem w siódmym dniu). Z tego wzgl
ę
du VEGF wydaje si
ę
by
ć
w
tym przypadku czynnikiem podtrzymuj
ą
cym a nie inicjuj
ą
cym wzrost naczy
ń
. Mo
ż
e by
ć
wydzielany przez wiele ró
ż
nych
rodzajów komórek, np. przez: makrofagi, neutrofile, keratynocyty, fibroblasty czy
ś
ródbłonek, zwłaszcza w warunkach
hipoksji, cz
ę
sto wyst
ę
puj
ą
cej w okolicach rany.
Wa
ż
ny wpływ na angiogenez
ę
maj
ą
makrofagi. Zwłaszcza po stymulacji hipoksj
ą
, wysokim st
ęż
eniem mleczanów
lub cytokinami produkowanymi przez
ś
ródbłonek, mog
ą
one wydziela
ć
czynniki bezpo
ś
rednio indukuj
ą
ce wzrost naczy
ń
.
Makrofagi powoduj
ą
równie
ż
degradacj
ę
macierzy pozakomórkowej, co ma kluczowe znaczenie dla powstawania nowych
naczy
ń
i regeneracji tkanek. Oddziaływaj
ą
one równie
ż
na inne komórki pobudzaj
ą
c je do produkcji substancji
proangiogenetycznych.
Powy
ż
szy tekst powstał na podstawie prac:
Lipski KM, Ostrowski K, Komender J,
Ś
ladowski D: Udział
ś
ródbłonka w formowaniu si
ę
naczy
ń
. Post
ę
py Biologii
Komórki, 33 (2006): 59-70
Lipski KM, Ostrowski K, Komender J,
Ś
ladowski D: Rola
ś
ródbłonka w trakcie rozwoju oraz dojrzewania tkanek i
narz
ą
dów. Post
ę
py Biologii Komórki, 33 (2006): 95-102
Opracowali K. Lipski & D.
Ś
ladowski
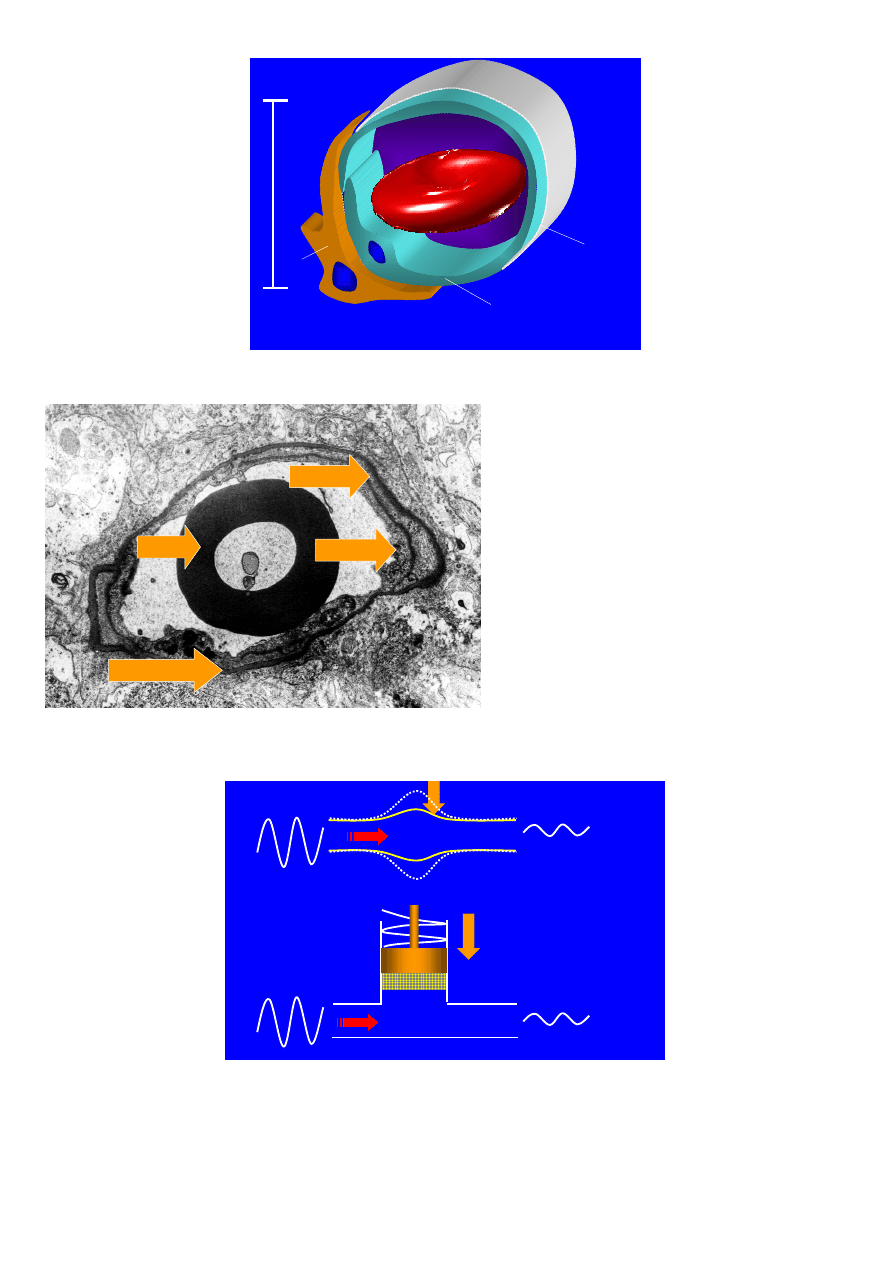
erytrocyt
ś
ródbłonek
perycyt
błona podstawna
erytrocyt
ś
ródbłonek
perycyt
błona podstawna
Schemat nr 22/2
perycyt
Komórka śródbłonka
Błona podstawna
erytrocyt
10 µm
Schemat naczynia włosowatego
EM nr 22/3
Naczynie włosowate siatkówki (EM powi
ę
kszenie 10 tys. razy)
Schemat nr 22/4
F
F
ciśnienie
ciśnienie
ciśnienie
ciśnienie
Model reologiczny aorty. Du
ż
e skoki ci
ś
nienia wyst
ę
puj
ą
ce w aorcie w czasie pracy serca s
ą
„buforowane”
poprzez błony spr
ęż
yste b
ę
d
ą
ce charakterystycznym elementem błony
ś
rodkowej t
ę
tnic typu spr
ęż
ystego.
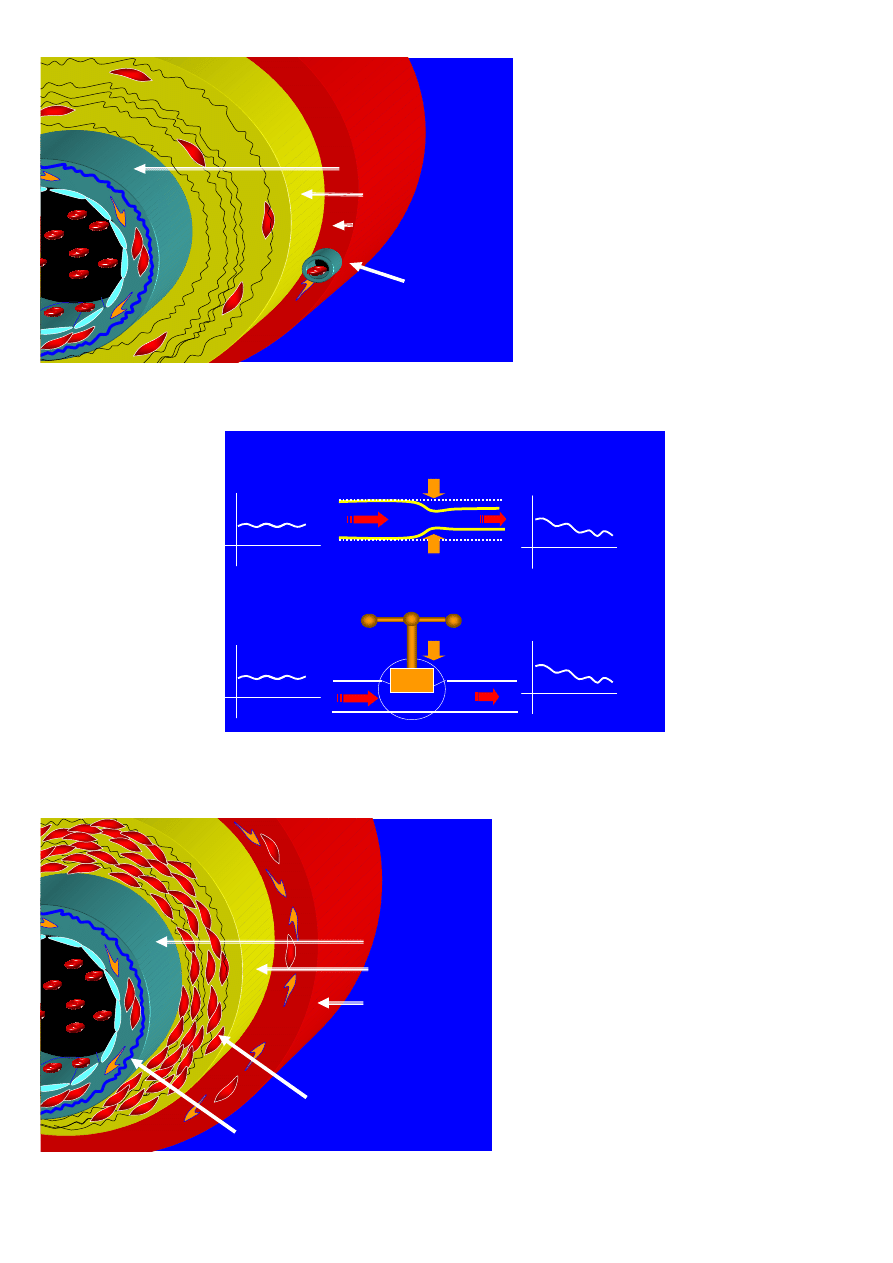
Schemat nr 22/5
NACZYNIA NACZY
NACZYNIA NACZY
Ń
Ń
(
(
vasa
vasa
vasorum
vasorum
)
)
B
B
ł
ł
ona wewn
ona wewn
ę
ę
trzna
trzna
B
B
ł
ł
ona dodatkowa
ona dodatkowa
B
B
ł
ł
ona
ona
ś
ś
rodkowa
rodkowa
T
T
Ę
Ę
TNICE TYPU SPR
TNICE TYPU SPR
Ęś
Ęś
YSTEGO
YSTEGO
(du
(du
ż
ż
ego kalibru)
ego kalibru)
Schemat budowy
ś
cian t
ę
tnic typu spr
ęż
ystego
Schemat nr 22/6
F
T
T
Ę
Ę
TNICE TYPU MI
TNICE TYPU MI
ĘŚ
ĘŚ
NIOWEGO
NIOWEGO
(
(
ś
ś
redniego kalibru)
redniego kalibru)
przepływ
przepływ
F
przepływ
przepływ
Model reologiczny t
ę
tnic typu mi
ęś
niowego. Regulacja przepływu krwi nast
ę
puje dzi
ę
ki skurczowi komórek
mi
ęś
niówki gładkiej, której nagromadzenie w błonie
ś
rodkowej jest charakterystyczne dla t
ę
tnic
ś
redniego
kalibru.
Schemat nr 22/7
B
B
ł
ł
ona wewn
ona wewn
ę
ę
trzna
trzna
B
B
ł
ł
ona dodatkowa
ona dodatkowa
B
B
ł
ł
ona
ona
ś
ś
rodkowa
rodkowa
30-40 warstw
miocytów
T
T
Ę
Ę
TNICE TYPU MI
TNICE TYPU MI
ĘŚ
ĘŚ
NIOWEGO
NIOWEGO
(
(
ś
ś
redniego kalibru)
redniego kalibru)
Błona sprężysta wewnętrzna
Schemat budowy
ś
cian t
ę
tnic typu mi
ęś
niowego.

Schemat nr 22/8
Acetylocholina
Acetylocholina
Histamina
Histamina
Bradykinina
Bradykinina
Substancja P
Substancja P
NO
ET1
ET2
ET3
PGI
2
Angiotensyna I
Angiotensyna I
Angiotensyna II
Angiotensyna II
Konwertaza
Konwertaza
Udział komórek
ś
ródbłonka regulacji skurczu mi
ęś
niówki gładkiej naczy
ń
krwiono
ś
nych
Wyszukiwarka
Podobne podstrony:
więcej podobnych podstron