1. Wydzielanie kwasu 6-aminopenicylanowego.
Zawiesina poreakcyjna
↓ Oddzielenie biokatalizatora
Roztwór wyjściowy
↓ Schłodzenie, Zakwaszenie (pH 1.5-2.5); Ekstrakcja penicyliny kw. fenylooctowego
Faza wodna
↓ Neutralizacja (pH 7.8, NaOH); Zatężanie (<30
o
C)
Roztwór kwasu 6-AP
↓ Wytrącanie (pH 4.2 - 4.3 HCl lub H
2
SO
4
); Odsączanie; Przemywanie wodą i acetonem ,Suszenie
Kryształy kwasu 6-AP
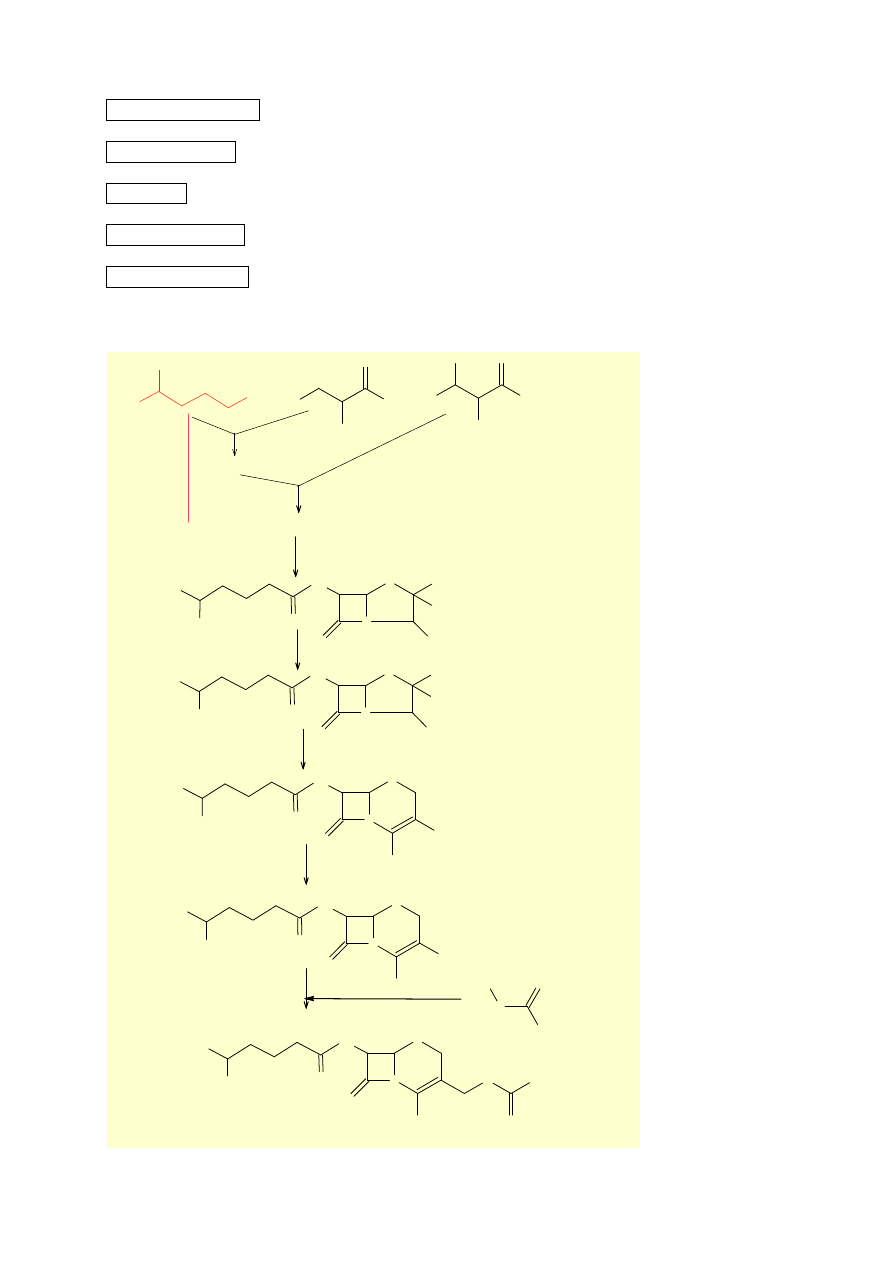
2. Biogeneza cefalosporyny C.
COOH
HOOC
NH
2
O
NH
2
S
H
OH
O
NH
2
CH
3
C
H
3
OH
L-Cys
L-Val
L-AA-L-Cys
SYNTETAZA
TRIPEPTYDU
ACV
L-AA-L-Cys-D-Val (DLL-ACV)
N
S
O
CH
3
CH
3
COOH
NH
O
N
H
2
COOH
cyklaza
L
N
S
O
CH
3
CH
3
COOH
NH
O
N
H
2
COOH
epimeraza
D
N
O
NH
O
N
H
2
COOH
S
CH
3
COOH
ekspandaza
N
O
NH
O
N
H
2
COOH
S
CH
2
OH
COOH
oksygenaza
N
O
NH
O
N
H
2
COOH
S
COOH
O
CH
3
O
izopenicylina N
(LLD)
penicylina N
(DLD)
deacetoksycefalosporyna C
deacetylocefalosporyna C
cefalosporyna C
acetylotransferaza
S
CH
3
CH
2
CoA
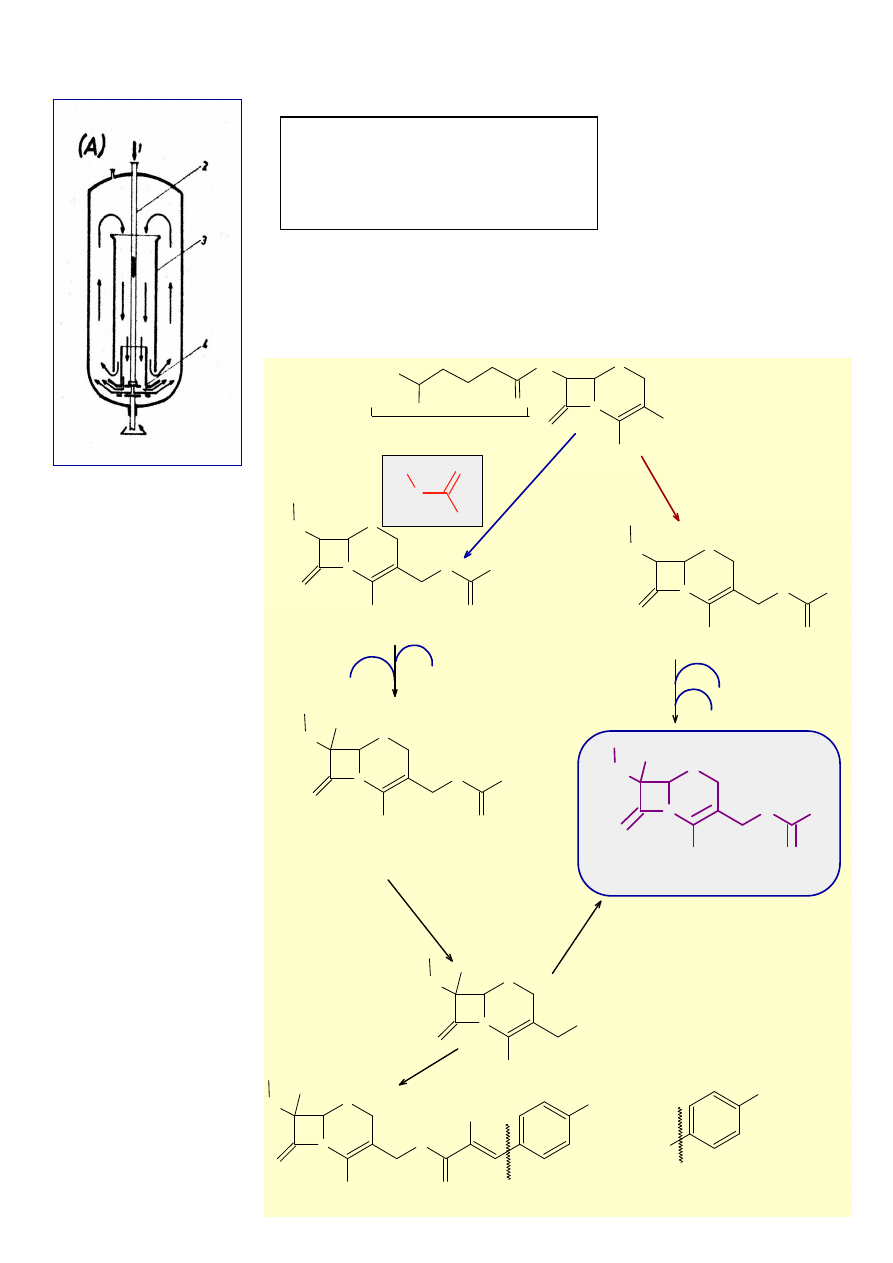
3. Rozpoznać na rysunku: bioreaktor Frings i opisać.
4. Cefamycyny u
promieniowców.
1. Zasysane powietrze
2. Wydrążony wał mieszadła
3. Rura cyrkulacyjna
4. Wirujące urządzenie mieszająco-
napowietrzające
CEFAMYCYNA C
N
O
NH
O
N
H
2
COOH
S
CH
2
OH
COOH
deacetylocefalosporyna C
cefalosporyna C
S
CH
3
CH
2
CoA
R
N
O
NH
S
COOH
O
CH
3
O
R
N
O
NH
S
COOH
O
NH
2
O
R
O-karbamoilodeacetylocefalosporyna C
O
2
S-adenozylometionina
N
O
NH
S
COOH
O
NH
2
O
R
OCH
3
O
2
S-adenozylometionina
N
O
NH
S
COOH
O
CH
3
O
R
OCH
3
7-a-metoksycefalosporyna C
N
O
NH
S
COOH
OH
R
OCH
3
karbamoilofosforan
N
O
NH
S
COOH
O
R
OCH
3
O
OCH
3
OH
O
H
OH
cefamycyna C
cefamycyna B
OSO
3
H
C
H
3
O
H
OH
cefamycyna A
karbamoilofosforan
CH
2
CO NH
N
S
O
CH
3
COOH
CH
3
CH
2
Cl
CH
3
COSiMe
3
CH
3
O
S
N
N
C
Me
3
SiCl/PCl
5
CH
2
C N
N
S
O
CH
3
COSiMe
3
CH
3
OEt
EtOH
N
S
O
CH
3
COOH
CH
3
H
2
N
CH
2
COOH
Acylaza
penicylinowa
H+
H
2
O
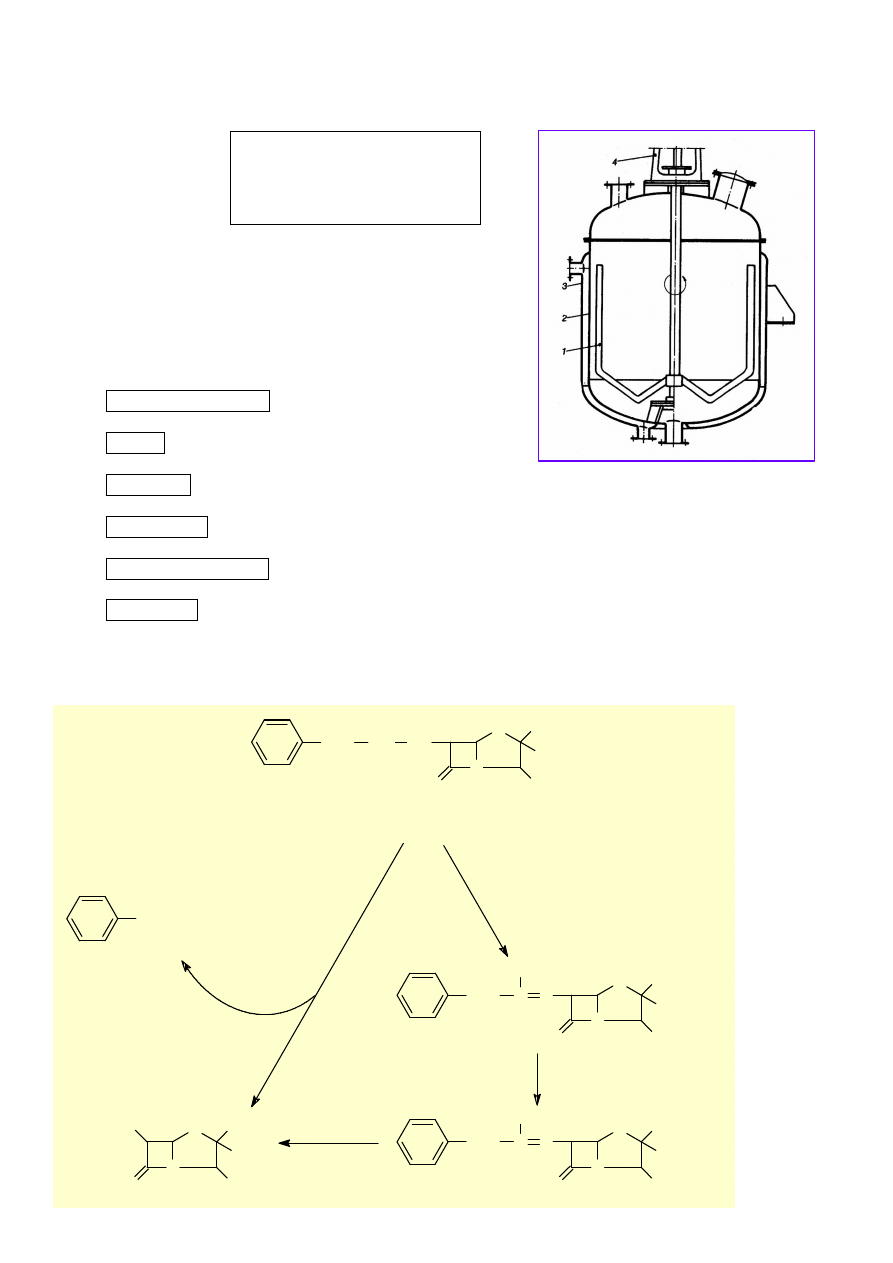
5. Reaktor z mieszadłem kotwicowym rozpoznać i opisać.
6. Wyodrębnianie acylazy z E. Coli.
Zawiesina pohodowlana
↓ Wirowanie lub filtracja
Biomasa
↓ Dezintegracja komórek; Wirowanie
Supernatant
↓ Wytrącanie białek (NH
4
)
2
SO
4
lub PEG; Rozpuszczanie w wodzie
Roztwór białek
↓ Chromatografia adsorpcyjna lub jonowymienna; Dializa; Ultrafiltracja
Stężony roztwór acylazy
↓ Wytrącanie; Krystalizacja; Wirowanie
Czysty enzym
7. Enzymatyczna i chemiczna hydroliza penicyliny G.
1. Mieszadło kotwicowe
2. Zbiornik
3. Płaszcz grzejny
4. Stojak napędu mieszadła
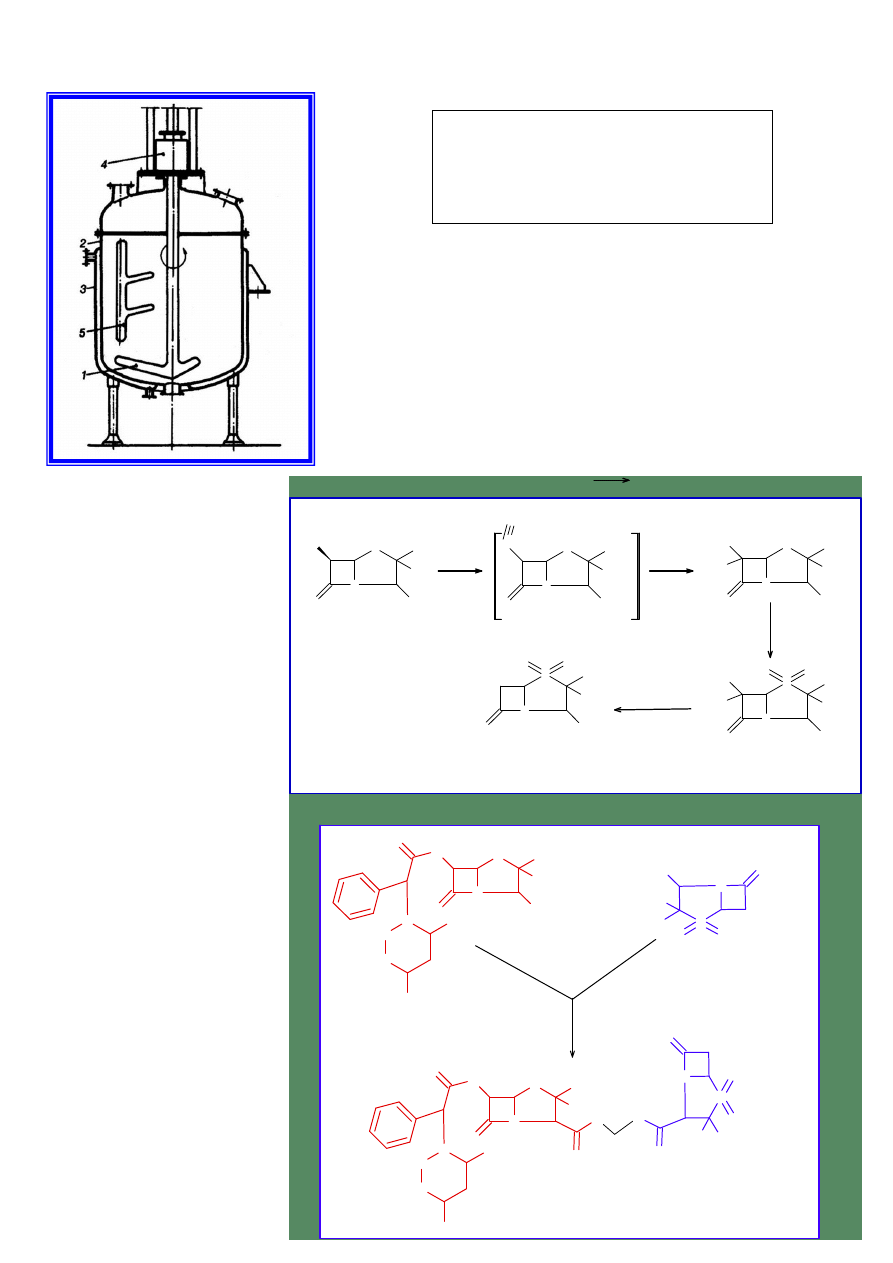
8. Mieszalnik z mieszadłem kotwicowym nierównoramiennym – opisać.
8. Biogeneza cafamycyn. (patrz pkt. 4)
9. Synteza sulbaktamu i
sultamycyliny.
1. Mieszadło kotwicowe nierównoramienne
2. Zbiornik
3. Płaszcz grzejny
4. Stojak napędu mieszadła
5. Mieszadło nieruchome
N
S
N
H
2
CH
3
CH
3
COOH
O
HNO
2
N
S
N
+
CH
3
CH
3
COOH
O
N
Br
2
N
S
Br
CH
3
CH
3
COOH
O
Br
N
S
Br
CH
3
CH
3
COOH
O
Br
O
O
KMnO
4
/H
3
PO
4
H
2
, Pd/C
N
S
CH
3
CH
3
COOH
O
O
O
sulbaktam
N
S
NH
CH
3
CH
3
COOH
O
O
N
O
O
CH
3
OCH
3
N
S
C
H
3
C
H
3
HOOC
O
O
O
+
N
S
NH
CH
3
CH
3
O
O
N
O
O
CH
3
OCH
3
O
O
O
O
N
S
CH
3
C
H
3
O
O
O
sultamycylina
10. Interdyscyplinarne zastosowanie biotechnologii.
Biotechnologia jest interdyscyplinarną dziedziną nauki, obejmującą różne kierunki technicznego wykorzystania
materiałów i procesów biologicznych. Biotechnologia korzysta ze zdobyć wielu dziedzin nauki, np.: ekologii,
mikrobiologii, biologii komórki, genetyki, biochemii, biologii molekularnej, chemii, inżynierii, informatyki, matematyki,
fizyki czy ekonomii. Jest natomiast wykorzystywana m.in. w ochronie zdrowia, ochronie środowiska, rolnictwie,
przemyśle spożywczym, przemyśle chemicznym, do otrzymywania surowców, nośników energii, w analityce oraz wielu
innych dziedzinach życia...
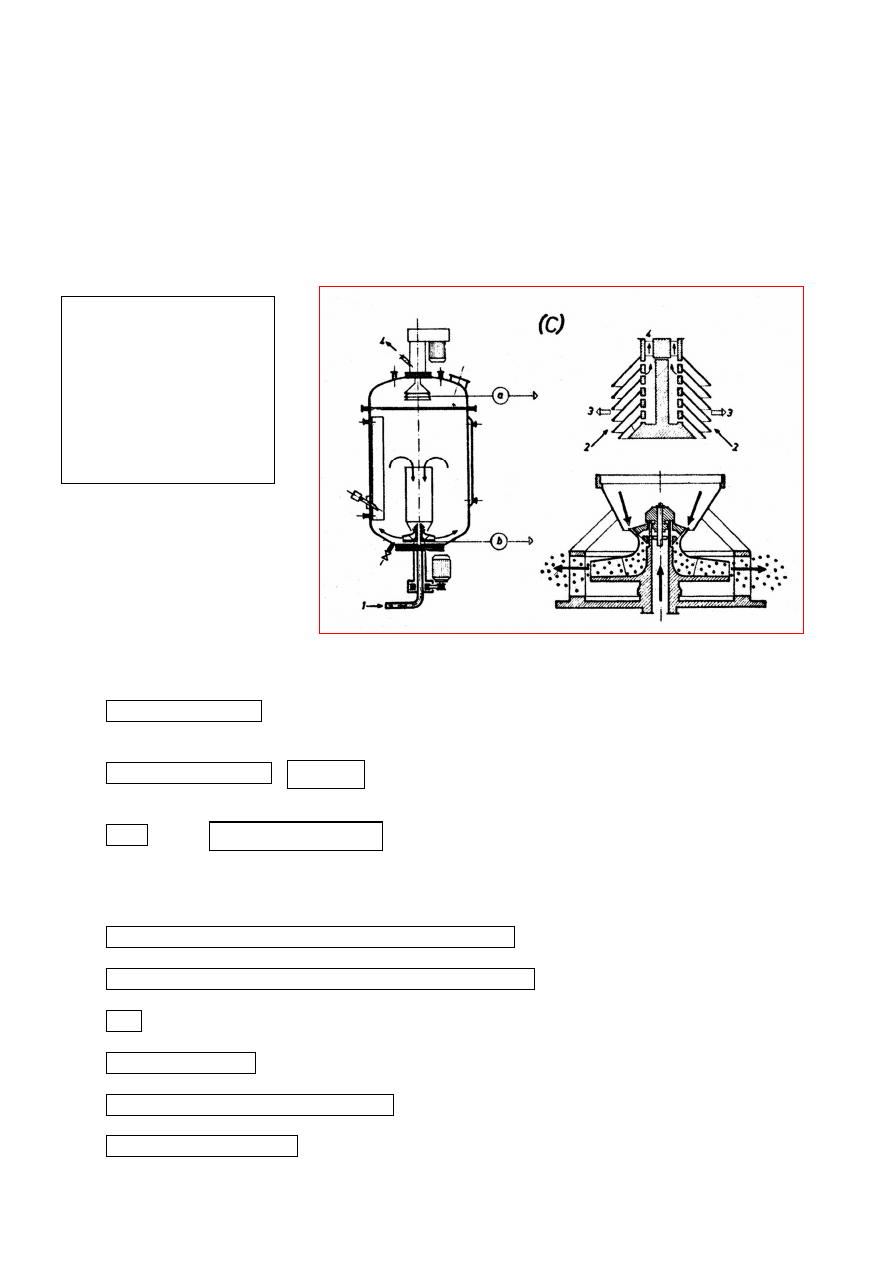
11. Bioreaktor CHEMAP.
13. Wydzielanie i oczyszczanie cefalosporyny C.
Zawiesina pofiltracyjna
↓ Schłodzenie do +10 st.C; zakwaszenie do pH 5,5 (kwas octowy); dodatek ziemi okrzemkowej
Bębnowy filtr próżniowy
↓
↓
Filtrat
↓ 1. zakwaszenie do pH 2,8 – 3,0 (kationit); 2.ogrzewanie w 37
o
C – następuje rozkład penicyliny N;
3. schłodzenie do 0
o
C
Kolumna z anionitem silnie zasadowym (eliminacja anionów)
↓
Kolumna z anionitem słabo zasadowym (elucja cefalosporyny C)
↓ Elucja kwasem octowym i pirydyną (pH 5,0 – 5,5, temp. 0
o
C)
Eluat
↓ 1. Zatężanie; 2. Wytrącanie bezw. acetonem 3. Filtracja; 4. Suszenie pod zmniejszonym ciśń.
Surowa cefalosporyna
↓ Rozpuszczenie w wodzie; Neutralizacja rozc. NaOH
Kolumna z kationitem (usuwanie pirydyny)
↓ 1. Zatężanie (próżnia); 2. Krystalizacja; 3. Wirowanie; 4. Przemywanie etanolem, suszenie
Sól sodowa cefalosporyny C
1. Doprowadzenie
powietrza
a) Urządzenie odpieniające:
2. Wlot piany
3. Wylot cieczy
4. Wylot gazu
b) Urządzenie mieszająco -
napowietrzające
+ H2O
Grzybnia odpadowa
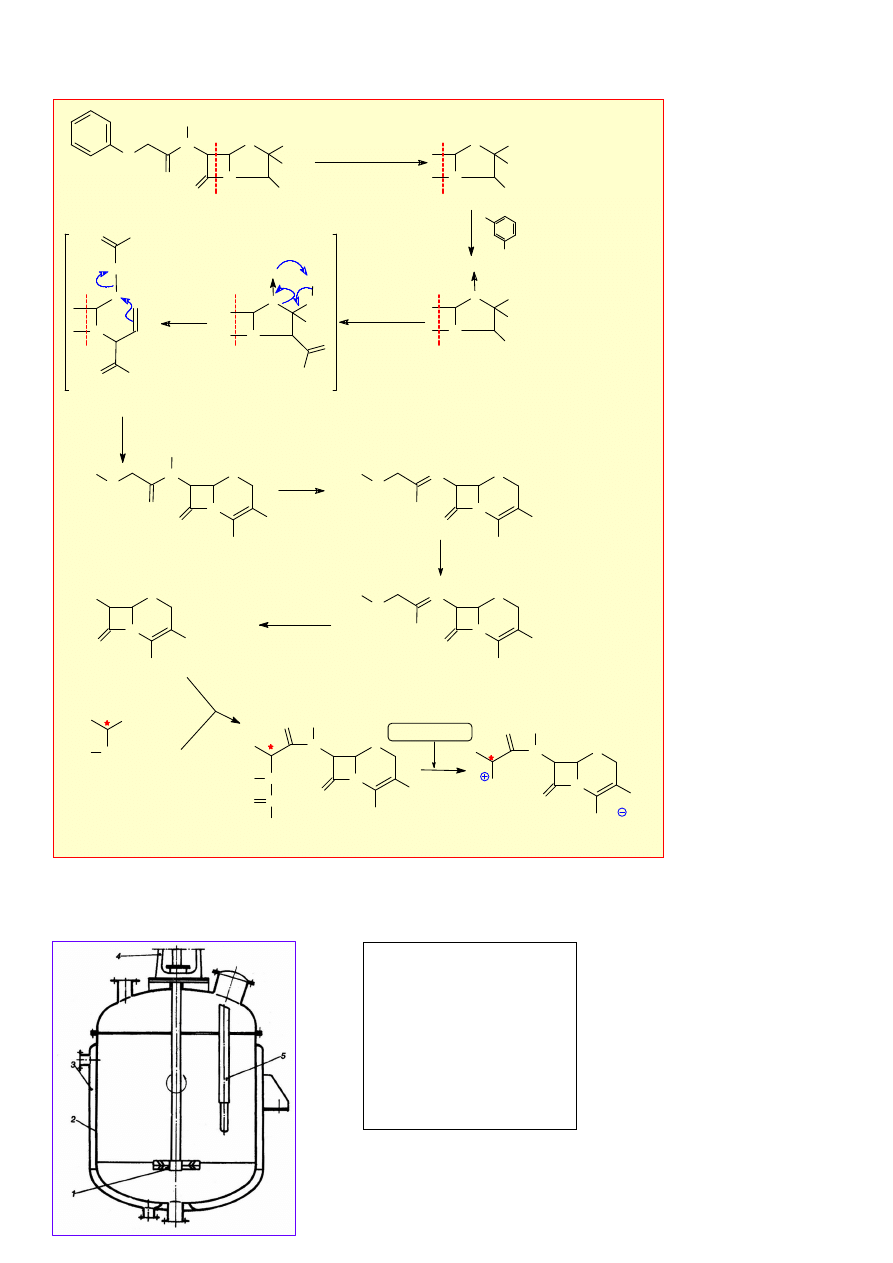
12. Synteza cefaleksyny (na forum było, że cefalotyny, ale to chyba błąd) z penicyliny V.
O
O
N
O
CH
3
COOK
CH
3
S
N
H
CH
3
COOCH
2
CCL
3
CH
3
S
N
ClCOOCH
2
CCl
3
-CO
2
CH
3
COOCH
2
CCL
3
CH
3
S
N
O
COOOH
Cl
(CH
3
CO)
2
O
DMF
O
H
N
S
CH
2
CH
3
Cl
3
CCH
2
O
O
H
S
N
CH
3
O
O
OCH
2
CCl
3
O
N
S
COOCH
2
CCl
3
CH
3
O
N
O
C
6
H
5
H
O
PCl
5
pirydyna
benzen
N
S
COOCH
2
CCl
3
CH
3
O
N
O
C
6
H
5
Cl
CH
3
OH
N
S
COOCH
2
CCl
3
CH
3
O
N
O
C
6
H
5
OCH
3
H
2
O
N
S
COOCH
2
CCl
3
CH
3
O
H
2
N
C
6
H
5
COOH
NCOOC(CH
3
)
3
H
D
C
6
H
5
N
H
C
N
O
CH
3
COOCH
2
CCl
3
S
N
O
H
OC(CH
3
)
3
O
C
6
H
5
NH
3
N
O
CH
3
COO
S
N
O
H
CEFALEKSYNA
odblokowanie
13. Mieszalnik z mieszadłem turbinowym.
1. Mieszalnik turbinowy
2. Zbiornik
3. Płaszcz grzejny
4. Stojak napędu mieszadła
5. Mieszadło nieruchome
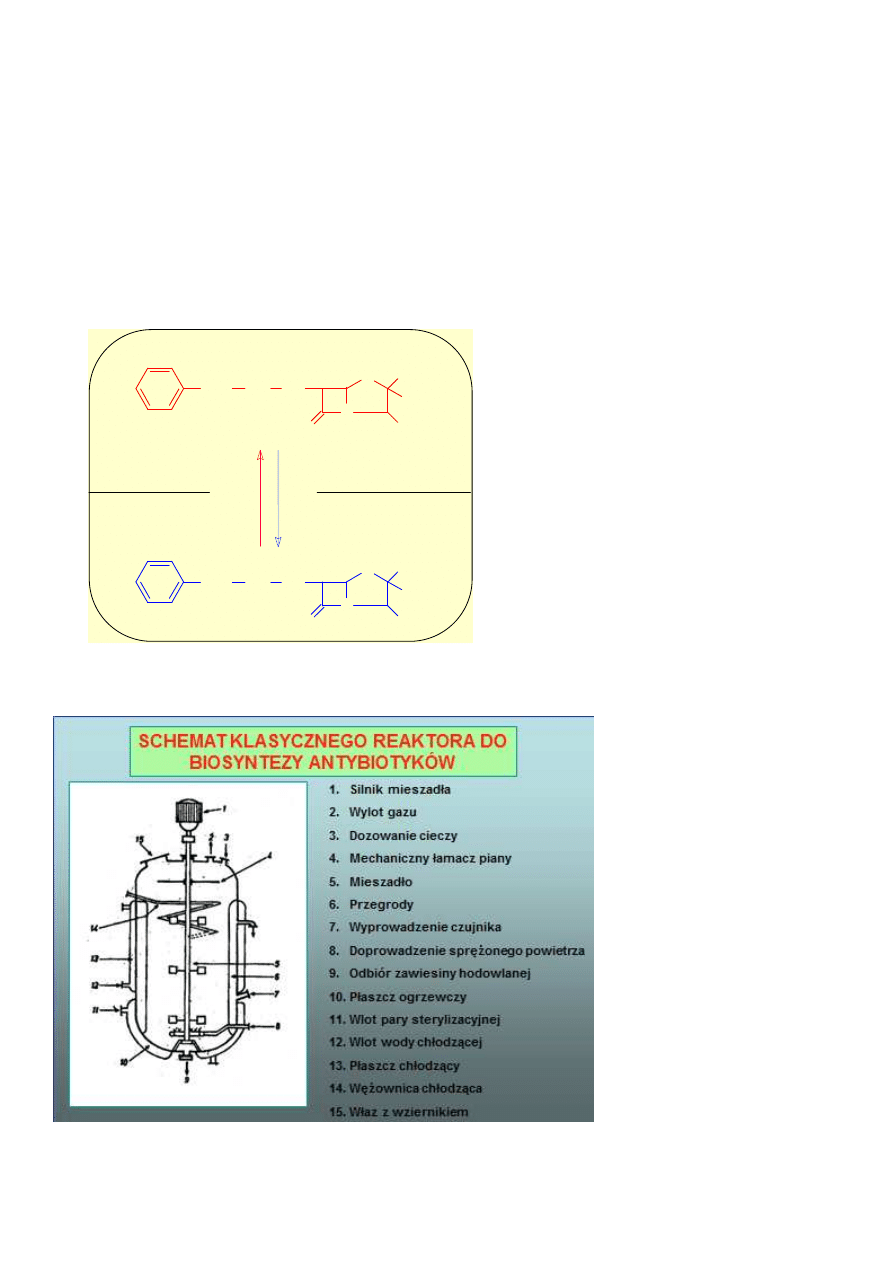
CH
2
CO NH
N
S
O
CH
3
COOH
C H
3
CH
2
CO NH
N
S
O
CH
3
COOH
CH
3
pH 2.5
pH 7
faza organiczna
faza wodna
14. Mechanizmy obronne producentów .
•
Brak miejsca uchwytu – enzymu, procesu, struktury subkomórkowej.
•
Miejsca uchwytu niewrażliwe lub zablokowane (osłonięte).
•
Zwielokrotnienie (nadprodukcja) liczby miejsc uchwytu dla antybiotyku.
•
Wytworzenie zastępczych procesów metabolicznych (by-pass).
•
Bariera transportu antybiotyku do miejsca uchwytu.
•
Transport antybiotyku poza komórkę.
•
Unieczynnienie antybiotyku przez wiązanie ze strukturami komórkowymi.
•
Enzymatyczna inaktywacja antybiotyku.
•
Biosynteza antybiotyku dopiero po fazie namnożenia komórek.
15. Reguła ekstrakcji penicyliny G.
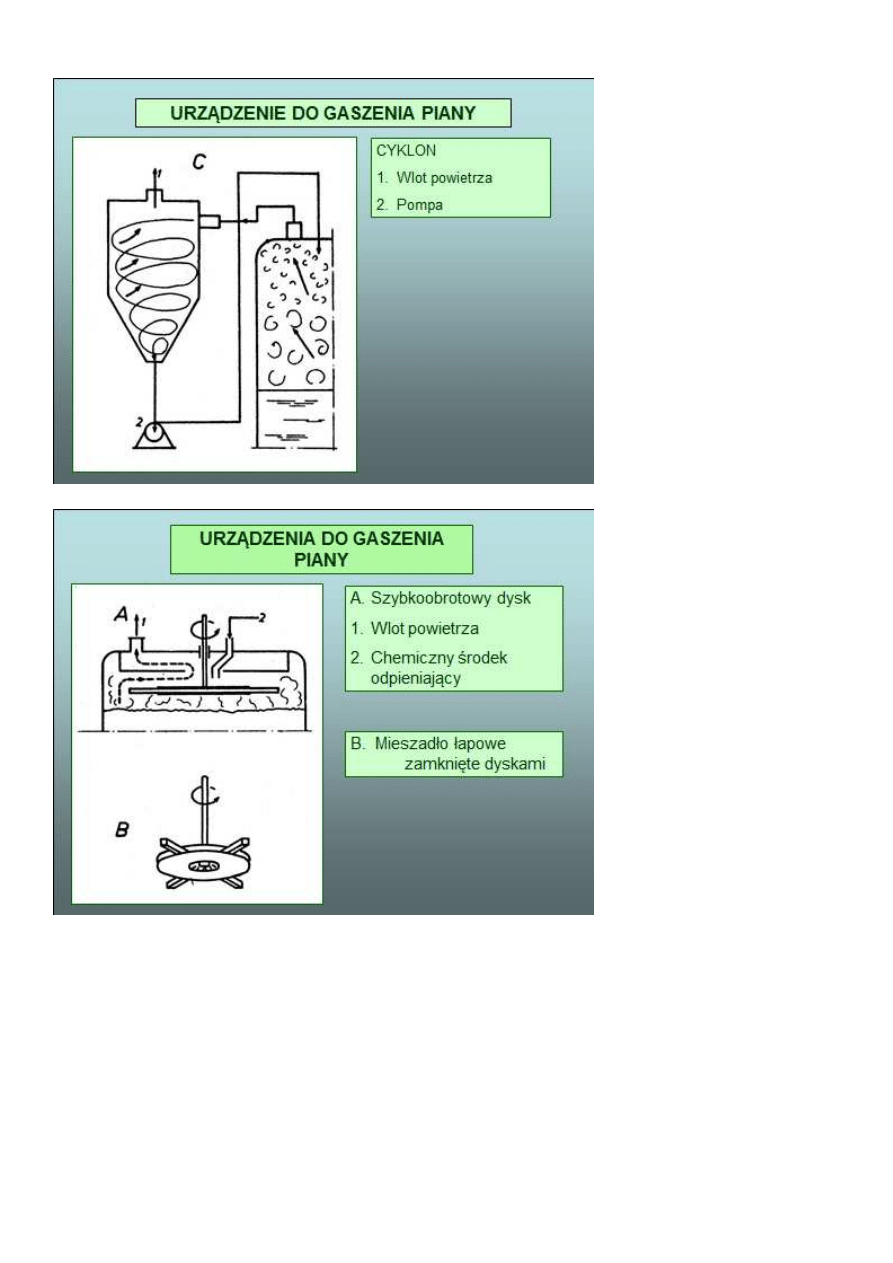
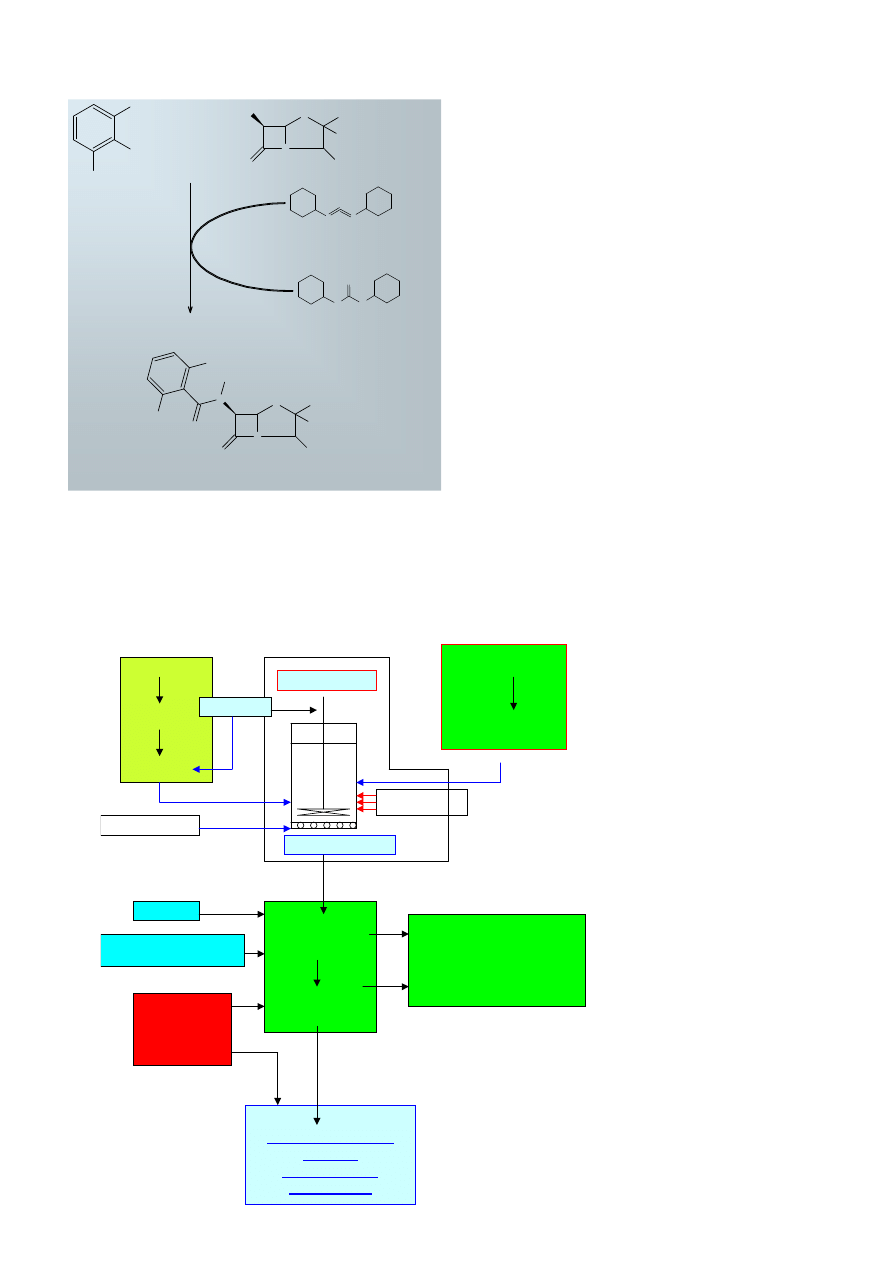
Synteza metycyliny
16. Ogólny schemat procesu biotechnologicznego.
SUROWCE
PODLO
ŻE
STERYLIZA
CJA
SZCZEP
NAMNO
ŻENIE
INOKULUM
ODDZIELENIE
BIOMASY
IZOLACJA
PRODUKTU
ZAGOSPODAROWANIE
PRODUKTÓW
ODPADOWYCH
KONTROLA
LABOR.
OTRZYMYWANIE
FORMY
HANDLOWEJ
PRODUKTU
BIOREAKTOR
KONTROLA
BIOSYNTEZA
POWIETRZE
ENERGIA
ENERGIA
MATERIAŁY I
SUROWCE
N
S
N
H
2
CH
3
CH
3
COOH
O
COOH
OCH
3
OCH
3
+
N
N
NH
NH
O
DCCI
(N,N'-dicykloheksylokarbodiimid)
DCC
(N,N'-dicykloheksylomocznik)
N
S
N
CH
3
CH
3
COOH
O
CH
3
O
H
3
CO
OCH
3
metycylina
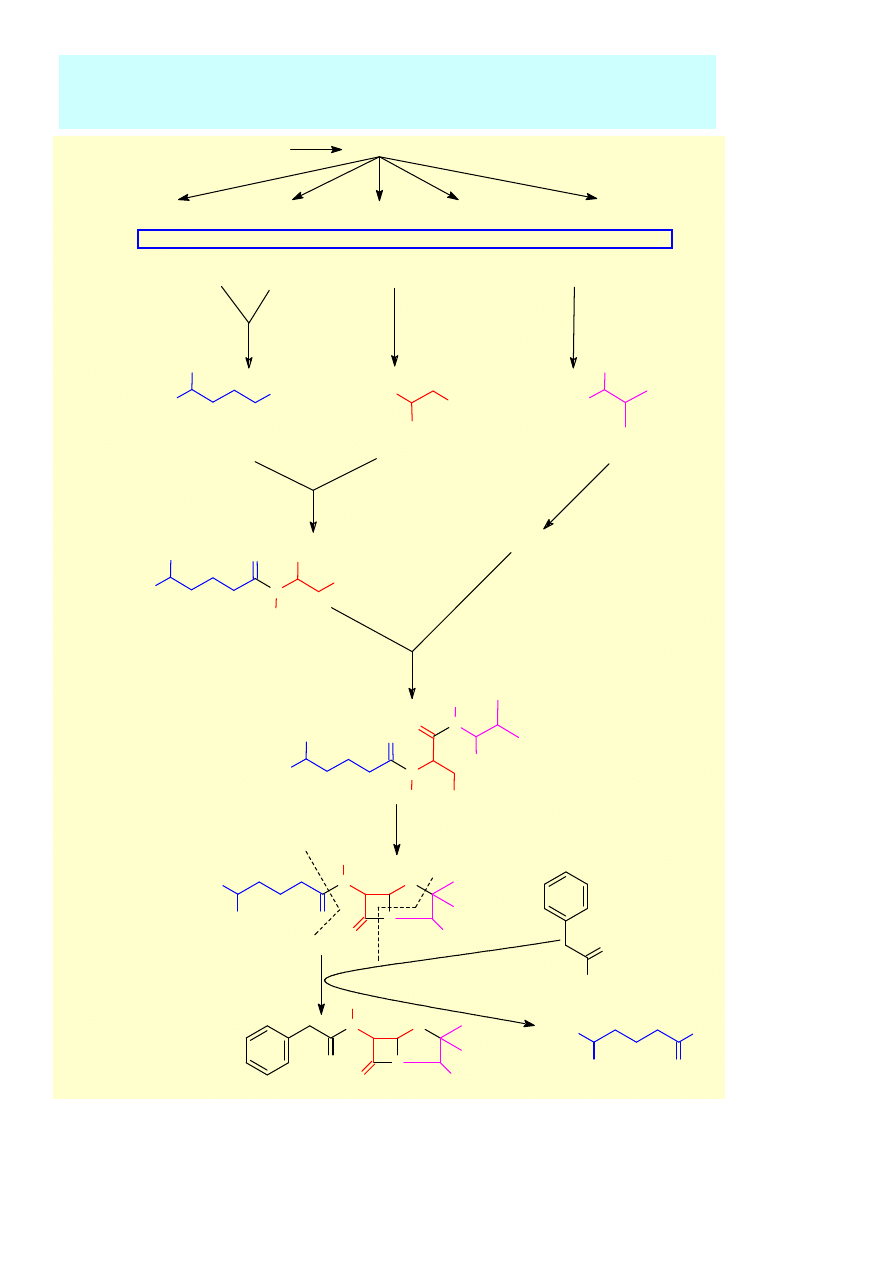
CUKRY
GLIKOZA
HOOC
COOH
NH
2
H
2
N
SH
HOOC
HOOC
H
2
N
L-
α
-AA
(Kwas
α
-aminoadypinowy) L-Cys L-Val
HOOC
NH
2
N
O
H
COOH
SH
L-a-AA-L-Cys
(L-
α
-aminoadypinoilo)-L-
α
-cysteina)
HOOC
NH
2
N
O
H
N
O
H
SH
COOH
D-Val
N
S
COOH
N
O
H
O
H
2
N
COOH
L
L
D
N
S
COOH
N
O
H
O
SCoA
O
L-
α
-AA
O
H
2
N
COOH
OH
2-oksoglutaran acetylo-CoA acetylo-Ser L-Met pirogronian
m e t a b o l i t y p o s r e d n i e p r z e m i a n p o d s t a w o w y c h
syntetaza ACV
syntetaza ACV
syntaza IPN(cyklaza)
izopenicylina N
cylaza/amidaza
+ acylotransferaza
BIOGENEZA PENICYLINY G
D
O
OCH
CH
3
N
N
N
N
S
H
N
COONa
O
S
N
O
N
S
O
COOh
H
2
N
O
CH
3
O
OH
COOH
D
HCOOH
Ac
2
O
O
COOH
O
CH
D
SOCl
2
O
COCl
O
CH
D
N
N
N
N
CH
3
S
H
2
N
COOH
O
S
N
+
BSA(
SPRAWDZIæ
STRUKTURE ZE STR 164)
N
N
N
N
CH
3
S
N
COOSi(CH
3
)
3
O
S
N
(CH
3
)
3
SI
H
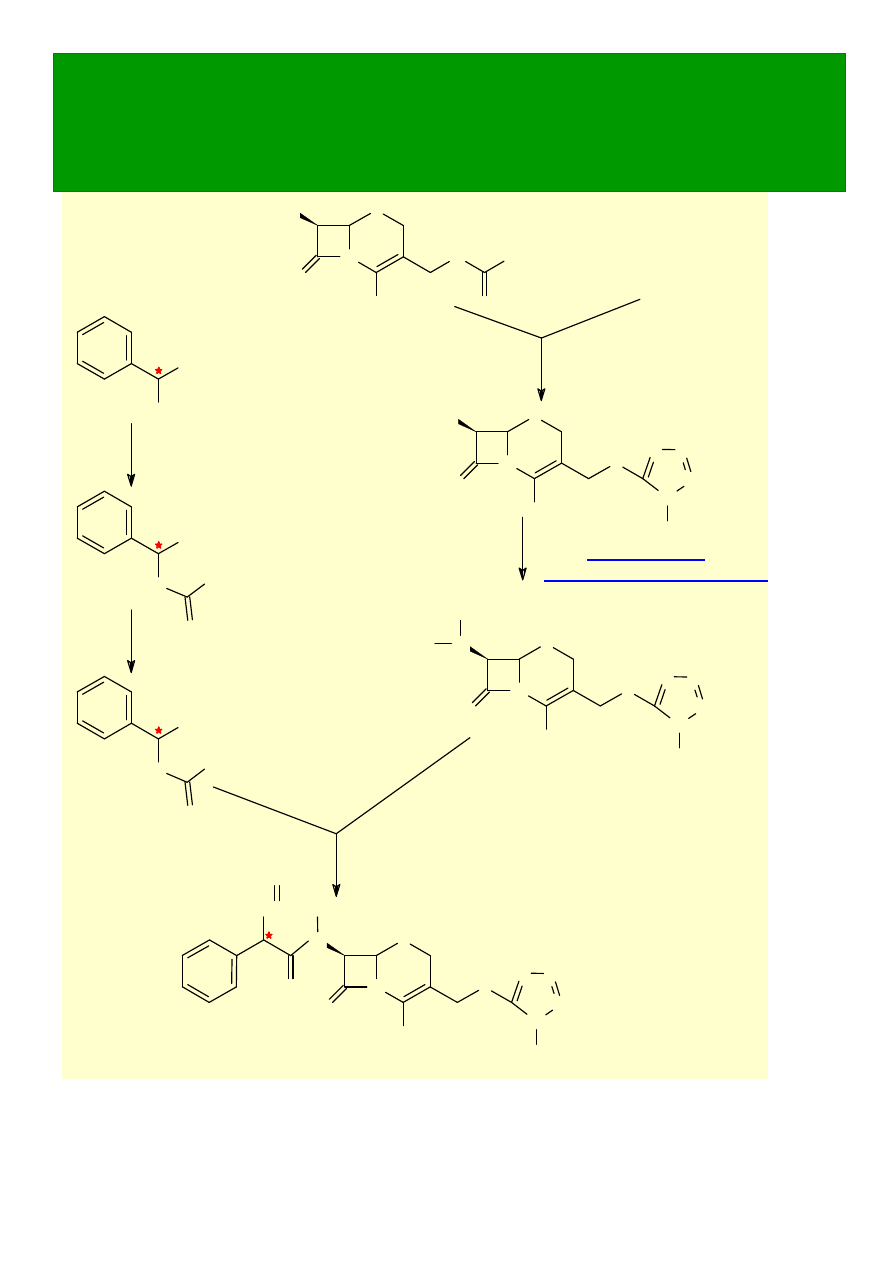
CEFAMANDOL NAFAT
SYNTEZA CEFAMANDOLU
Z KWASU 7-AC I KWASU MIGDAŁOWEGO
Wyszukiwarka
Podobne podstrony:
opracowanie2 id 338681 Nieznany
Opracowanie07v2 id 338680 Nieznany
chemia opracowanie id 112613 Nieznany
edema biotech materialy id 1501 Nieznany
ginexy opracowanie id 191652 Nieznany
Najlepsze opracowanie id 313141 Nieznany
Biotechnologia egzamin id 89038 Nieznany
Promethidion Opracowanie id 40 Nieznany
Immunologia opracowanie id 2121 Nieznany
Filozofia opracowanie id 170613 Nieznany
ZFHi tech Opracowanie id 932670 Nieznany
Opracowanie 3 id 338046 Nieznany
PE opracowanie id 353179 Nieznany
zmk opracowanie id 591480 Nieznany
Opracowanie1 id 338664 Nieznany
lab2 Opracowanie02 id 750512 Nieznany
opracowanie 7 id 338056 Nieznany
Opracowanie 6 id 338054 Nieznany
Inne opracowanie id 214648 Nieznany
więcej podobnych podstron