
ZAKŁAD OPAKOWALNICTWA I BIOPOLIMERÓW
CHEMIA ŻYWNOŚCI
Ćwiczenia laboratoryjne nr 2
Wyodrębnianie, badanie właściwości i analiza jakościowa sacharydów
Artur Bartkowiak, Szczecin 2003
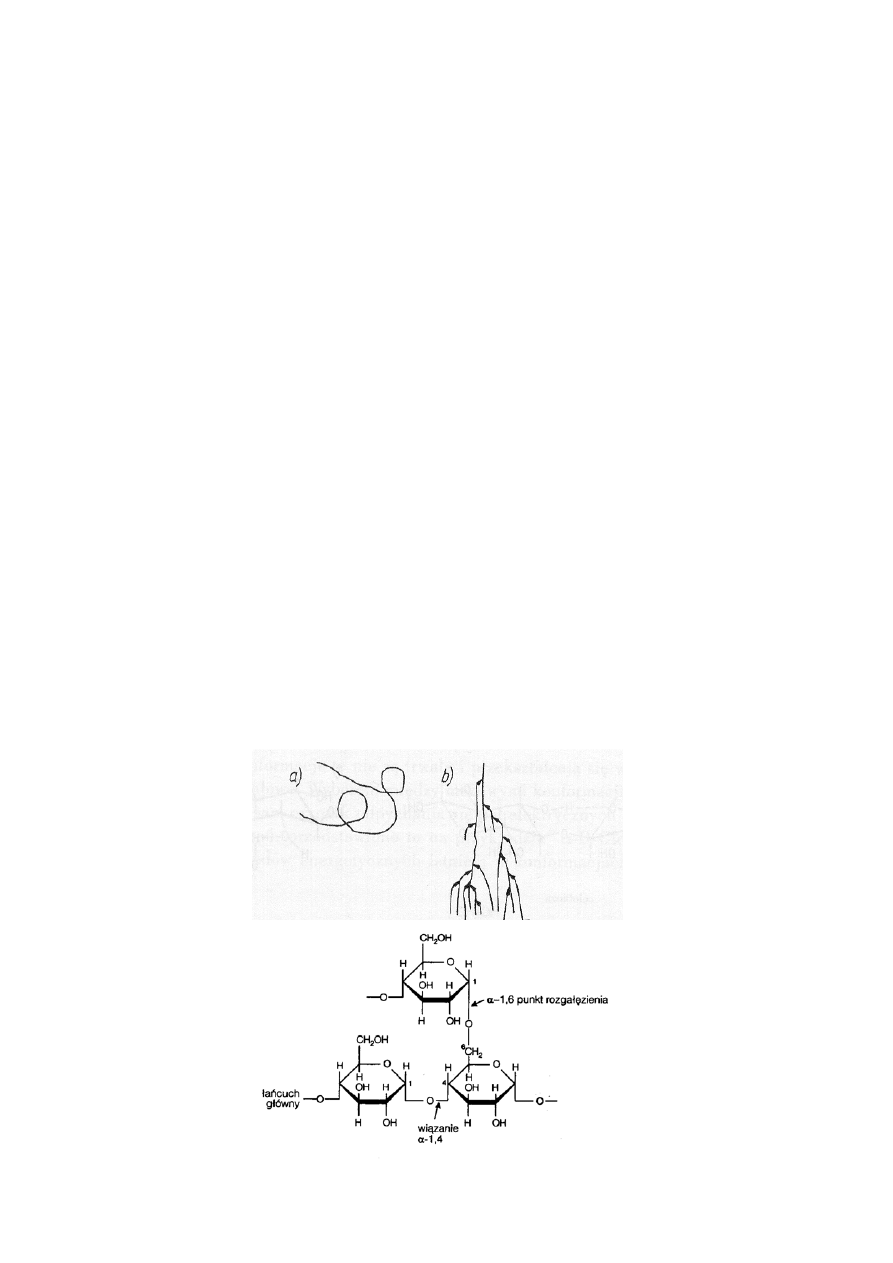
Wydzielanie i identyfikacja homoglikanów
Do homoglikanów należą takie wielocukry, jak skrobia (A), a w niej amyloza i amylopektyna,
glikogen, celuloza (B), galaktogen, mannan, inulina i inne. Homoglikany charakteryzują się in-
nymi właściwościami chemicznymi i fizycznymi niż jednocukry. Po pierwsze, praktycznie nie
wykazują właściwości redukcyjnych z powodu znikomej ilości grup redukujących w porównaniu
z ilością cząsteczek cukru prostego wchodzącego w skład homog1ikanu. W wodzie rozpuszczają
się z trudnością lub wcale.
Skrobia. Składa się z dwóch wielocukrów - amylozy i amylopektyny - zbudowanych odmiennie
z
α-D-glukopiranozy. Amyloza tworzy łańcuchy proste, zbudowane z cząsteczek glukozy sprzę-
żonych ze sobą wiązaniem
α-l → 4. Natomiast amylopektyna charakteryzuje się budową roz-
gałęzioną; zasadniczym połączeniem cząsteczek glukozy jest również wiązanie
α-l → 4, lecz co
25-30 reszt glukozylowych występują wiązania
α-l → 6, tworzące rozgałęzienia. Stąd wynikają
nieco inne właściwości fizyczne obu wielocukrów. Roztwory wodne amylopektyny bardziej opa-
lizują, a w reakcji z jodem wykazują zabarwienie fioletowe, podczas gdy amyloza barwi się z
jodem na kolor ciemnoniebieski.
SKROBIA (poliglukoza)
Amyloza Amylopektyna
(krystaliczna) (amorficzna)
α-1→6
α-1→4
α-1→4
2

Ćwiczenie 1. Otrzymywanie skrobi
Obrane i umyte ziemniaki (uprzednio zważone) utrzeć na miazgę i po dodaniu równej objętości
wody, zmieszać i przesączyć przez kilka warstw gazy. Przesącz rozcieńczyć 2-3-krotnie wodą i
pozostawić do dekantacji. Zlać ciecz znad osadu (pozostawić i obserwować zachodzące zmiany),
a skrobię zawiesić w metanolu i przesączyć na lejku Büchnera. Po przemyciu metanolem wysu-
szyć na powietrzu i zważyć (obliczyć zawartość skrobi w ziemniakach).
Rozpuszczalność skrobi
a) Do około 1 g skrobi dodać kilka cm
3
H
2
O, dobrze wymieszać i przesączyć przez bibułę. Do
przesączu wprowadzić kroplę roztworu jodu w KI. Ciecz pozostaje bezbarwna. Świadczy to o
nierozpuszczalności skrobi w zimnej wodzie.
b) Otrzymywanie kleiku skrobiowego: Zagotować ok. 75 cm
3
wody. W drugim naczyniu spo-
rządzić jednolitą zawiesinę 1 g skrobi w 15 cm
3
zimnej wody, którą wlewa się do wrzącej wody
ciągle mieszając. Naczynie po skrobi popłukać 10 cm
3
wody i dodać do wrzącego roztworu. Go-
tować do rozpuszczenia się. Otrzymuje się jednolity, opalizujący roztwór skrobi, który posłuży
do dalszych ćwiczeń.
Reakcje skrobi z jodem
Amyloza daje z jodem zabarwienie niebieskie, zaś amylopektyna fioletowe. Amyloza o konfigu-
racji liniowej nie jest zdolna do tworzenia kompleksu z jodem. Musi istnieć konfiguracja heliksu,
aby cząsteczki jodu mogły się w niej regularnie ułożyć. Jedna cząsteczka jodu przypada na sześć
reszt glukozylowych, czyli na jeden skręt heliksu. Ogrzewanie powoduje rozkręcanie się heliksu,
co jest przyczyną znikania zabarwienia z jodem.
a) Do 2 cm
3
kleiku skrobiowego dodać kroplę roztworu jodu w jodku potasu (KI). Kleik skro-
biowy nie może oddziaływać zasadowo. Powstaje niebieskie zabarwienie.
b) Probówkę w której powstała niebieska barwa, ogrzać w łaźni wodnej. Niebieskie zabarwienie
znika. Po ochłodzeniu pod bieżącą wodą zabarwienie powraca.
c) Wpływ zasad na zabarwienie z jodem. W środowisku zasadowym zabarwienie nie powstaje,
ponieważ jod reaguje z zasadą według równania:
I
2
+ 2NaOH
→ NaIO + NaI + H
2
O
w środowisku kwasowym reakcja przebiega w kierunku odwrotnym:
NaIO + Nal + 2HCl
→ 2NaCl + I
2
+ H
2
O
Do 2 cm
3
kleiku skrobiowego dodać kilka kropli 1 M roztworu NaOH i kroplę roztworu jodu w
KI. Zabarwienie nie powstaje. Po zakwaszeniu kwasem solnym barwa pojawia się.
3
Właściwości redukujące skrobi przed hydrolizą i po niej
a) Wykonać próbę Benedicta (patrz opis poniżej) z roztworem glukozy, sacharozy, skrobi .
b) Roztwór skrobi gotować z HCl lub H
2
SO
4
przez kilka minut, ostudzić, zobojętnić za pomocą
NaOH i wykonać próbę Benedicta.
Próba Benedicta
Zasada: Próba Benedicta należy do najbardziej swoistych i czułych prób redukcyjnych na cukry.
Odczynnik zawiera zamiast wodorotlenku sodowego - węglan sodu, a zamiast winianu -
cytrynian sodu. Powstaje więc nie wodorotlenek miedziowy, lecz węglan. Czułość próby jest
dość duża. Już 0,1% stężenie cukru redukującego powoduje zmianę barwy z niebieskiej na zie-
loną. Zielone zabarwienie jest wynikiem zmieszania pomarańczowej zawiesiny Cu
2
0 z niebie-
skim odczynnikiem.
Przygotowanie odczynnika:
Do 20 cm
3
1% roztworu CuSO
4
dodać 80 cm
3
10% cytrynianu sodu a następnie 20 cm
3
10%
Na
2
CO
3
.
Wykonanie: Do 5 cm
3
odczynnika dodać 0,5 cm
3
badanego roztworu i wstawić do wrzącej łaźni
wodnej na 5 min. Zależnie od ilości sacharydu powstaje albo tylko zielone zabarwianie, albo
osad żółty, pomarańczowy czy czerwony.
Hydroliza skrobi
Zasada: Skrobia pod wpływem kwasów ulega stopniowej hydrolizie przez stadium dekstryn do
maltozy i małej ilości glukozy. Pośrednimi produktami są: amylodekstryny (zabarwienie z jodem
fioletowe), erytrodekstryny (czerwone), achro- i maltodekstryny oraz maltoza (zabarwienie z
jodem nie powstaje). W miarę hydrolizy wzrastają również stopniowo właściwości redukujące.
Wykonanie: Do 10 cm
3
roztworu skrobi dodać 1 cm
3
stężonego roztworu HCl lub H
2
SO
4
(koń-
cowe stężenie kwasu powinno być 1-2 M) i ogrzewać we wrzącej łaźni wodnej. W statywie
ustawić 2 szeregi probówek po 10 sztuk ( napełnić je 1 cm
3
bardzo rozcieńczonego roztworu
jodu w KI (ok. 0,002%)) i co chwilę przenosić po kilka kropli z ogrzewanej probówki do probó-
wek pierwszego i drugiego szeregu. W pierwszym szeregu probówek zawierającym zabarwienie
zmienia się kolejno z niebieskiego, przez fioletowe, czerwone, brunatne na bezbarwne. Drugi
szereg probówek zobojętnić wodorotlenkiem sodowym i wykonać próbę Benedicta (patrz powy-
żej). Obserwować coraz wyraźniejszą redukcję w miarę trwania hydrolizy.
4

Ćwiczenie2. Celuloza (błonnik).
Celuloza jest najbardziej rozpowszechnioną substancją organiczną. Stanowi ona główny skład-
nik ścian komórkowych roślin. Przykładem prawie czystego błonnika jest włókno bawełniane,
bibuła lub wata. Wielocukier ten jest liniowym polimerem
β-D-glukopiranozy; podstawową jed-
nostkę strukturalną: celulozy jest celobioza. Szereg reszt celobiozowych (ok. 1500) tworzy dłu-
gie łańcuchy, które są złączone siłami międzycząsteczkowymi i wiązaniami wodorowymi w
równolegle przebiegające pęczki - micele. Tego rodzaju budowa zapewnia celulozie dużą wy-
trzymałość mechaniczną. Masa cząsteczkowa celulozy mieści się w granicach 4,6
⋅10
5
-1,7
⋅10
6
(w
zależności od pochodzenia).
Celuloza jest nierozpuszczalna w wodzie i rozpuszczalnikach organicznych. Należy podkreślić
jej szczególną odporność na działanie różnych odczynników, m.in. rozcieńczonych kwasów.
Dopiero bardziej stężone roztwory kwasów hydrolizują celulozę. Rozpuszcza się ona również w
odczynniku Schweitzera lub Cross-Bewana. Wiele gatunków bakterii, grzybów oraz niektóre
zwierzęta, np. ślimaki, wskutek posiadania enzymu
β-celulazy są zdolne do rozkładania celulozy
i korzystania z niej jako pożywienia.
Rozpuszczalność celulozy
a) Zbadać rozpuszczalność bibuły lub waty w wodzie.
c) Rozpuszczalność w odczynniku Cross-Bewana. Odczynnik: Rozpuścić 1 g ZnCl
2
w 2,5 cm
3
stężonego (37%) roztworu HCl. Rozpuścić bibułę w tym odczynniku i ponownie wytrącić, doda-
jąc równą objętość wody.
Hydroliza celulozy
Parę skrawków bibuły zalać 10 cm
3
H
2
O i dodać 1 cm
3
stężonego roztworu H
2
SO
4
. Wstawić do
wrzącej łaźni wodnej na kilkanaście minut. Po zobojętnieniu wykonać próbę redukcyjną na cu-
kry proste - próba Benedicta (patrz ćw. 2A.4). Opisać wyniki próby.
5

IMIĘ I NAZWISKO GRUPA DATA
SPRAWOZDANIE Z ĆWICZENIA NR 2
Wyodrębnianie, badanie właściwości i analiza jakościowa sacharydów
Ćwiczenie1. Skrobia
Otrzymywanie skrobi
1. Jakie podstawowe grupy zw. chemicznych występują w ziemniakach i na którym eta-
pie zostają one rozdzielone?
2. Jakie zmiany obserwuje się w pozostawionej cieczy znad osadu, (czym to jest spowo-
dowane i do jakiej grupy reakcji zaliczamy takie procesy - w jakich innych produktach
można zaobserwować takie zmiany)?
3. Otrzymane wyniki skomentować/porównać z zawartością teoretyczną skrobi w ziem-
niakach (Z.Sikorski, Chemia Żywności, WNT 2000 lub inne poz. literaturowe). Obli-
czyć wydajność procesu.
6
IMIĘ I NAZWISKO GRUPA DATA
Właściwości redukujące skrobi przed hydrolizą i po niej
1. Dlaczego niektóre składniki żywności wykazują wł. redukujące a inne nie?
2. Kiedy i dlaczego obserwuje się wł. redukujące preparatów skrobiowych?
Próba Benedicta
1. Cukrem redukującym w próbie okazał(y) się……………………………..
Cukier redukujący −.
Hydroliza skrobi
Produktami hydrolizy skrobi są
7

IMIĘ I NAZWISKO GRUPA DATA
Ćwiczenie2. Celuloza (błonnik)
1. Który z polisacharydów, skrobia czy celuloza, wykazuje wyższą odporność na reakcję
hydrolizy kwasowej?
2. W jaki inny sposób można przeprowadzić reakcję hydrolizy polisacharydów (samo-
dzielna praca w czytelni)?
Suma punktów ………
8
Wyszukiwarka
Podobne podstrony:
Sprawozdanie 2 Badanie właściwości i analiza jakościowa anionów, Politechika Białostocka, budownictw
Sprawozdanie 2 Badanie właściwości i analiza jakościowa kationów, Politechika Białostocka, budownict
Badanie wlasciwosci i analiza jakosciowa anionow(2), Studia, Chemia, chemia od Ines(1)
Badanie właściwości i analiza jakościowa tłuszczów
TEMAT 2, TEMAT: BADANIE WŁAŚCIWOŚCI I ANALIZA JAKOŚCIOWA ANIONÓW
Badanie właściwości i analiza jakościowa kationów(2), Badanie właściwości i analiza jakościowa katio
Chemia żywnosci Cwiczenie laboratoryjne nr 1 wyodrebnianie i badanie własciwosci fizykochemicznych b
chemia żywności ćwiczenie 1
Analiza zywnosci sciaga, Dietetyka 2012,2013, Analiza jakosci zywnosci, egzamin
Chemia żywnosci Cwiczenie 3 Reakcje nieemzymatycznego brunatnienia zywnosci
Tok jakościowej analizy organicznej, Farmacja ŚUM, II ROK, Chemia organiczna, Chemia organiczna, Ćwi
SPRAWOZDANIE Z CWICZENIA NR 4, Technologia zywnosci, semestr III, chemia zywnosci
1 ćwiczenie (Analiza jakościowa wody) OZNACZANIE CHLORKÓW I SIARCZANÓW
1 ćwiczenie (Analiza jakościowa wody) OZNACZANIE ZWIĄZKÓW AZOTU
więcej podobnych podstron