16. PEPTYDY, BIAŁKA
Peptydy są to produkty kondensacji aminokwasów. Aminokwasy w peptydach są połączone
wiązaniem amidowym (peptydowym) pomiędzy grupą karboksylową jednego aminokwasu a grupą
aminową drugiego.
Zapis struktury peptydów:
aminokwas mający wolna grupę –NH
3
+
zapisuje się z lewej strony cząsteczki peptydu, a
aminokwas z wolna grupą –COO
-
z prawej. Aminokwasy te nazywa się odpowiednio:
N-końcowym i C-końcowym.
strukturę peptydu („sekwencję aminokwasów”) możemy podawać stosując odpowiednie skróty
trzyliterowe każdego aminokwasu poczynając od aminokwasu N-końcowego po lewej stronie
np. H
2
N-Ala-Gly .... - ….Cys – Glu - COOH
Szczególnym typem peptydów są białka. Charakterystyczną cechą białek, z punktu widzenia ich
budowy jest występowanie w nich charakterystycznych struktur: pierwszo-, drugo-, trzecio-
i czwartorzędowych (nie wszystkie białka wykazują tę strukturę).
STRUKTURA I-RZĘDOWA BIAŁEK
Określa kolejność występowania reszt aminokwasowych w łańcuchu peptydowym czyli sekwens
aminokwasów. Wiązania łączące poszczególne elementy łańcucha peptydowego to wiązania
peptydowe.
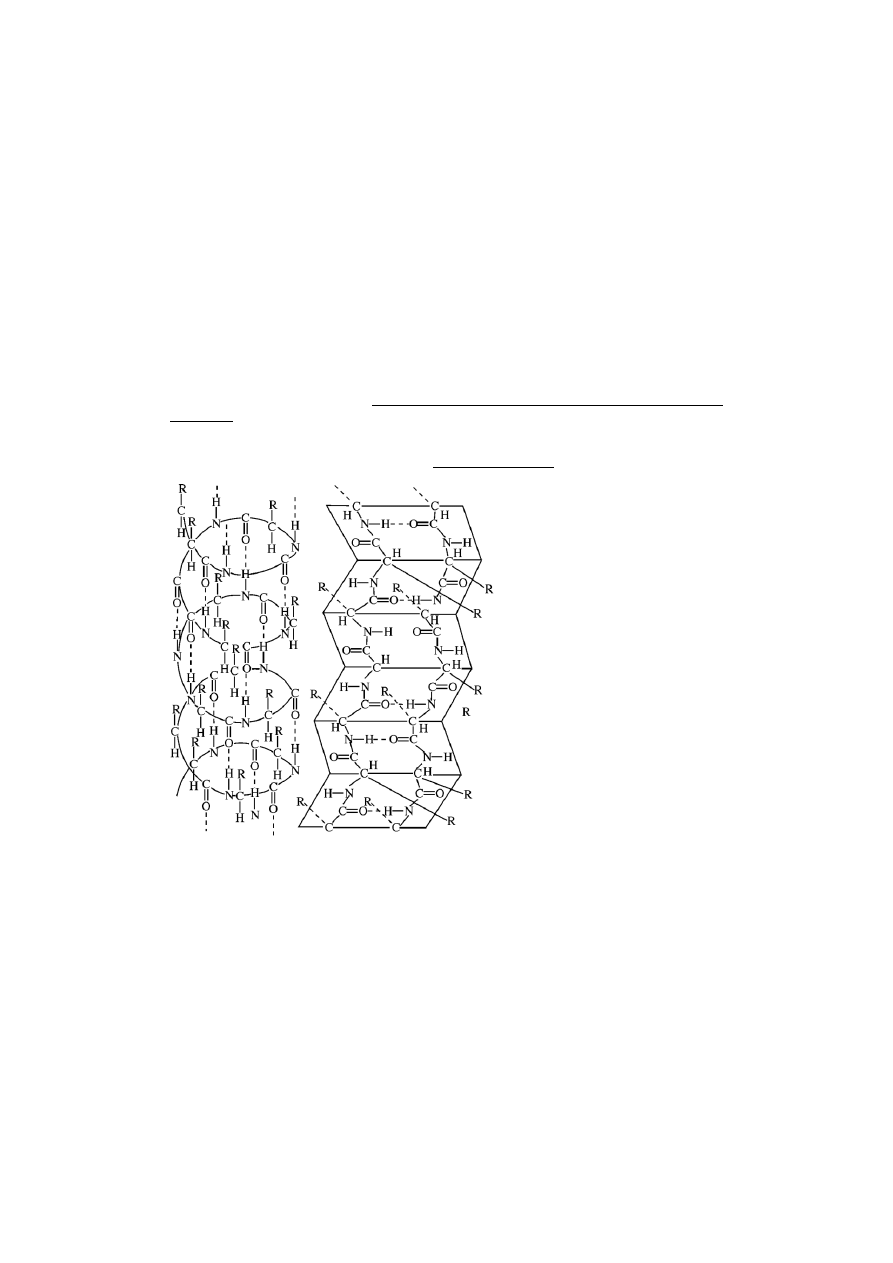
STRUKTURA
II-RZĘDOWA
określa
rodzaj przestrzennego
usytuowania
łańcuchów
polipetydowych, wynikający z obecności wiązań wodorowych między składnikami reszt
aminokwasowych polipeptydu.
α-heliks
struktura harmonijkowa
STRUKTURA III-RZĘDOWA
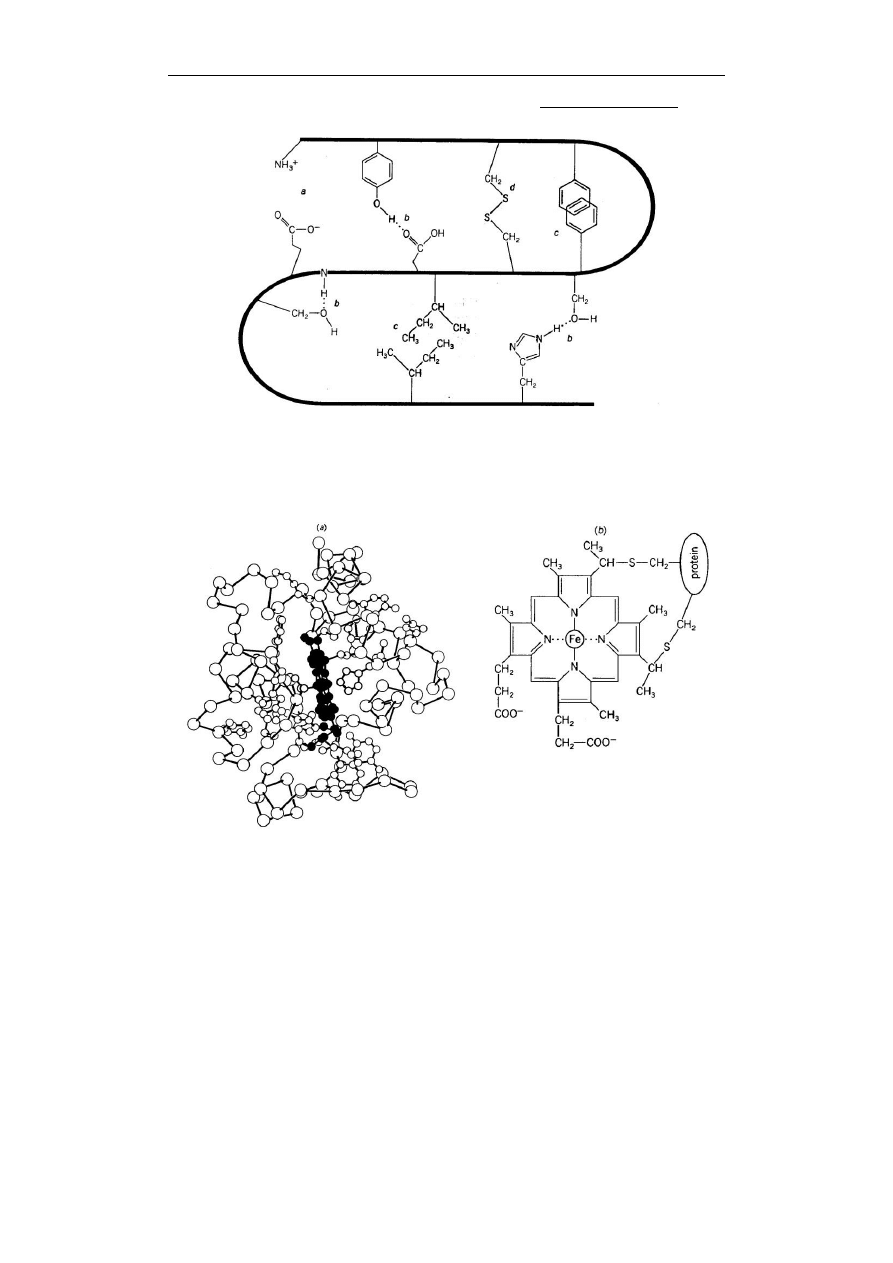
Trzeciorzędowa struktura białka, to ułożenie poszczególnych fragmentów łańcucha polipetydowego
względem siebie w przestrzeni (patrz rysunek) stabilizowanych między innymi oddziaływaniami
elektrostatycznymi (a), wiązaniami wodorowymi(b) oddziaływaniami hydrofilowymi pomiędzy
niepolarnymi częściami łańcucha (c) oraz wiązaniami dwusiarczkowymi (d).
132
Repetytorium z chemii
Spośród wymienionych najsilniejszymi elementami wiązania są wiązania dwusiarczkowe (-S-S-)
dlatego często wiązanie to czyni się głównie odpowiedzialnym za strukturę trzeciorzędową białka.
CZWARTORZĘDOWA STRUKTURA BIAŁKA
Czwartorzędowa struktura białek dotyczy cząsteczek białek zbudowanych z większej ilości
łańcuchów polipetydowych tworzących odpowiedni układ przestrzenny za pomocą różnego typu
wiązań i oddziaływań (rys.). Struktura ta określa stopień asocjacji lub polimeryzacji poszczególnych
cząsteczek białka lub łańcuchów polipetydowych w większe agregaty (jak włókienek w niciach).
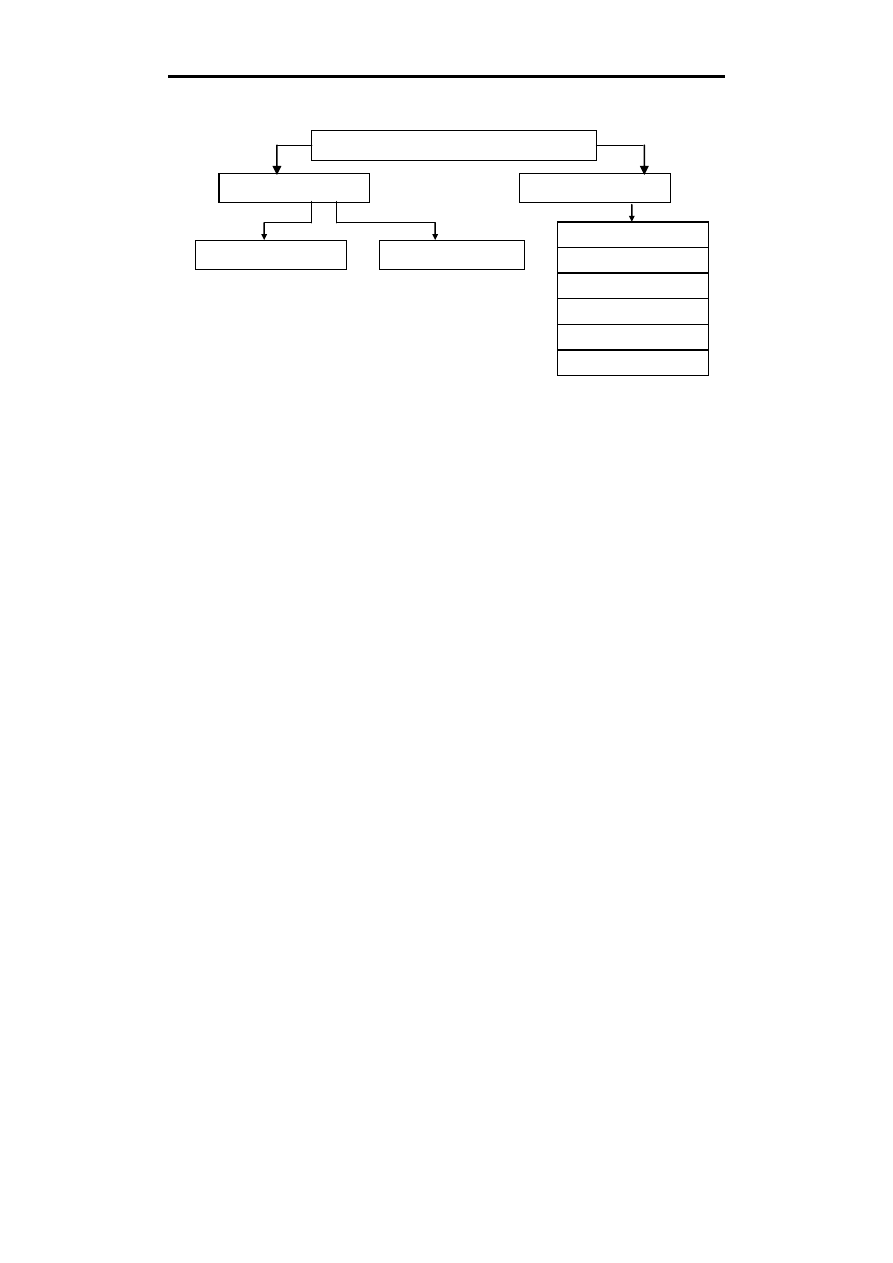
Struktura hemoglobiny (zaczerniony fragment przedstawiony na rysunku obok)
Białko hemoglobiny złożone jest z czterech podjednostek hemu (tetramer jest zdolny do przenoszenia
tlenu z płuc do komórek, pojedyncza jednostka – nie)
a
Peptydy, białka
133
BIAŁKA PROSTE (PROTEINY)
dają w wyniku hydrolizy wyłącznie aminokwasy i ich pochodne
BIAŁKA FIBRYLARNE (SKLEROPROTEINY) – są to łańcuchy włókniste o strukturze
spiralnej lub pofałdowanej. Białka te zazwyczaj są nierozpuszczalne w wodzie np. kreatyny
(włosy, skóra), miozyna (mięśnie), kolageny (tkanka łączna, skóra) i elastyny (ściana aorty,
tkanka łączna)
BIAŁKA GLOBULARNE (SFEROPROTEINY) – są to łańcuchy polipeptydowe zwinięte w
postać kłębka. Białka te są zazwyczaj rozpuszczalne w wodzie. Do białek globularnych
należą np. albuminy (surowica krwi, żółtko jaja), globuliny (nierozpuszczalne w wodzie np.
fibrynogen – w krwi, aktyna i miozyna w mięśniach); histony (w jądrze komórkowym),
gluteiny (gluteina – pszenica), prolaminy (zeiny – kukurydza)
BIAŁKA ZŁOŻONE (PROTEIDY)
Są to białka, w których cząsteczki białka prostego połączone są z inną niebiałkową cząsteczką
organiczną (grupą prostetyczną) lub nieorganiczną.
Do proteidów należą:
FOSFOPROTEIDY – zawierające reszty kwasu fosforowego(V), np. kazeina, pepsyna
LIPOPROTEIDY – zawierające glicerydy, cholesterol i jego estry, fosfolipidy, kwasy
tłuszczowe; występują w błonach komórkowych, osoczu krwi
GLUKOPROTEIDY – zawierają reszty węglowodanowe np. fibrynogen, tereotropina
NUKLEOPROTEIDY – zawierają kwasy nukleinowe; białka zasadowe (protaminy i
histony) – występują w jądrach komórkowych
METALOPROTEIDY – zawierają jony metali np. Fe
2+
, Mg
2+
, Cu
2+
, Zn
2+
, Mo
2+
, np.
ceruloplazmina zawiera Cu
2+
, ksantynooksydaza zawiera Mo
2+
CHROMOPROTEIDY – składnikiem niebiałkowym jest substancja barwna np.
hemoglobina, mioglobina, chlorofil
16.1.
WŁAŚCIWOŚCI FIZYCZNE BIAŁEK
wodne roztwory białek to roztwory liofilowe
nie przenikają przez błony półprzepuszczalne
wykazują efekt Tyndalla (rozpraszanie światła)
ulegają wysalaniu (koagulacji odwracalnej) pod wpływem stężonych roztworów soli metali
alkalicznych i amonowych
ulegają denaturacji (koagulacji nieodwracalnej)
o
zniszczeniu ulega przestrzenna struktura białek (niszczenie struktur białkowych i
zanik aktywności biologicznej) pod wpływem soli metali ciężkich, podwyższonej
temperatury, niższych alkoholi i aldehydów oraz rozpuszczalników organicznych
PODZIAŁ BIAŁEK
PROSTE
ZŁOŻONE
FIBRYLARNE
GLOBULARNE
metaloproteidy
chromoproteidy
nukleoproteidy
glikoproteidy
lipoproteidy
fosfoproteidy
134
Repetytorium z chemii
16.2.
WŁAŚCIWOŚCI CHEMICZNE BIAŁEK
wykazują właściwości kwasowo-zasadowe, ich ładunek jest wypadkową wszystkich
dysocjujących grup kwasowych i zasadowych w łańcuchach składowych aminokwasów. Forma
występowania białka zależy od pH roztworu. W punkcie izoelektrycznym (wartość pH
charakterystyczna dla każdego białka) występują w postaci cząstek obojętnych (mają
sumaryczny ładunek zerowy); przy wartości pH > pI występują w postaci makroanionów; przy
pH < pI makrokationów. Zjawisko to jest wykorzystywane przy rozdziale białek na drodze
elektroforezy (elektroforeza migracja naładowanych cząsteczek w zewnętrznym polu
elektrycznym)
reakcja ksantoproteinowa – pod wpływem stężonego roztworu HNO
3
białko przyjmuje żółte
zabarwienie, zmieniające się na pomarańczowe pod wpływem zasad. Zachodzi wtedy reakcja
nitrowania pierścieni aromatycznych w resztach aminokwasów aromatycznych (np. tyrozyny,
fenyloalaniny). Reakcja ta służy do wykrywania reszt aminokwasów aromatycznych w
cząsteczkach białek
(stęż)
fenyloalanina
żółty
sól sodowa formy aci (pomarańczowa)
reakcja biuretowa – po dodaniu roztworu CuSO
4
do alkalicznego roztworu białka pojawia się
fioletowe zabarwienie. reakcja charakterystyczna dla związków posiadających w swojej budowie
blisko położone względem siebie grupy amidowe (peptydowe)
CuSO
4
+ 2NaOH → Cu(OH)
2
+ Na
2
SO
4
R
C
H
NH
2
COOH
+ Cu(OH)
2
R
C
H
C
O
O
Cu
O
O
C
NH
2
H
C
R
H
2
N
+ 2H
2
O
fioletowy
hydroliza – proces prowadzący do rozpadu białek na prostsze składniki, finalnie do
aminokwasów. Hydroliza może być kwasowa, zasadowa lub enzymatyczna.
białko
O
H
2
białko proste
O
H
2
pepton
O
H
2
pepton prosty ——→
–––→ aminokwasy i inne związki (cukry, lipidy, zasady heterocykliczne)
CH
2
CH COOH
NH
2
HNO
3
CH
2
CH COOH
NH
2
O
2
N
KOH (NaOH)
CH
2
CH COOH
NH
2
N
Na
+
O
-
N
2
O
Wyszukiwarka
Podobne podstrony:
aminokwasy i peptydy id 59133 Nieznany
Abolicja podatkowa id 50334 Nieznany (2)
4 LIDER MENEDZER id 37733 Nieznany (2)
katechezy MB id 233498 Nieznany
metro sciaga id 296943 Nieznany
perf id 354744 Nieznany
interbase id 92028 Nieznany
Mbaku id 289860 Nieznany
Probiotyki antybiotyki id 66316 Nieznany
miedziowanie cz 2 id 113259 Nieznany
LTC1729 id 273494 Nieznany
D11B7AOver0400 id 130434 Nieznany
analiza ryzyka bio id 61320 Nieznany
pedagogika ogolna id 353595 Nieznany
Misc3 id 302777 Nieznany
cw med 5 id 122239 Nieznany
D20031152Lj id 130579 Nieznany
więcej podobnych podstron