
• procesy odwracalne i
nieodwracalne
Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ
TERMODYNAMIKA
TERMODYNAMIKA
• entropia
• druga i trzecia zasada
termodynamiki
• połączenie pierwszej i drugiej zasady
termodynamiki

PROCES NIEODWRACALNY
PROCES NIEODWRACALNY
( SAMORZUTNY )
( SAMORZUTNY )
różnica
temperatur
różnica ciśnień
różnica stężeń
Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ
stan początkowy stan końcowy
procesy samorzutne, aby zajść, nie wymagają wykonania
pracy,
np.

Przykłady
•
przepływ ciepła pomiędzy dwiema częściami układu
o rożnych
temperaturach
•
rozprężanie gazu przeciwko stałemu ciśnieniu lub do
próżni
•
przepływ masy pomiędzy dwoma obszarami, w
których stężenia
są różne
Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ

PROCES NIESAMORZUTNY
PROCES NIESAMORZUTNY
nie zachodzi w sposób naturalny w danych
warunkach
Przykłady
•
wybicie piłki na skutek ruchu termicznego atomów i
cząstek podłoża
•
uniesienie się wody z niższego poziomu na wyższy
Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ

PROCES
PROCES
ODWRACALNY
ODWRACALNY
stan początkowy stan końcowy
nieskończony ciąg stanów równowagi
Przykłady
•
topnienie lodu lub krzepnięcie wody w temperaturze
273,15 K pod
ciśnieniem 1013 hPa
•
graniczny proces sprężania ( rozprężania ) gazu
realizowany poprzez
nieskończenie wiele kroków z nieskończenie małą różnicą
ciśnień po
obu stronach tłoka
Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ

W toku przemiany odwracalnej układ pozostaje w stanie
równowagi termodynamicznej i zmienne określające
stan układu są równocześnie współrzędnymi opisującymi
przemianę.
Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ

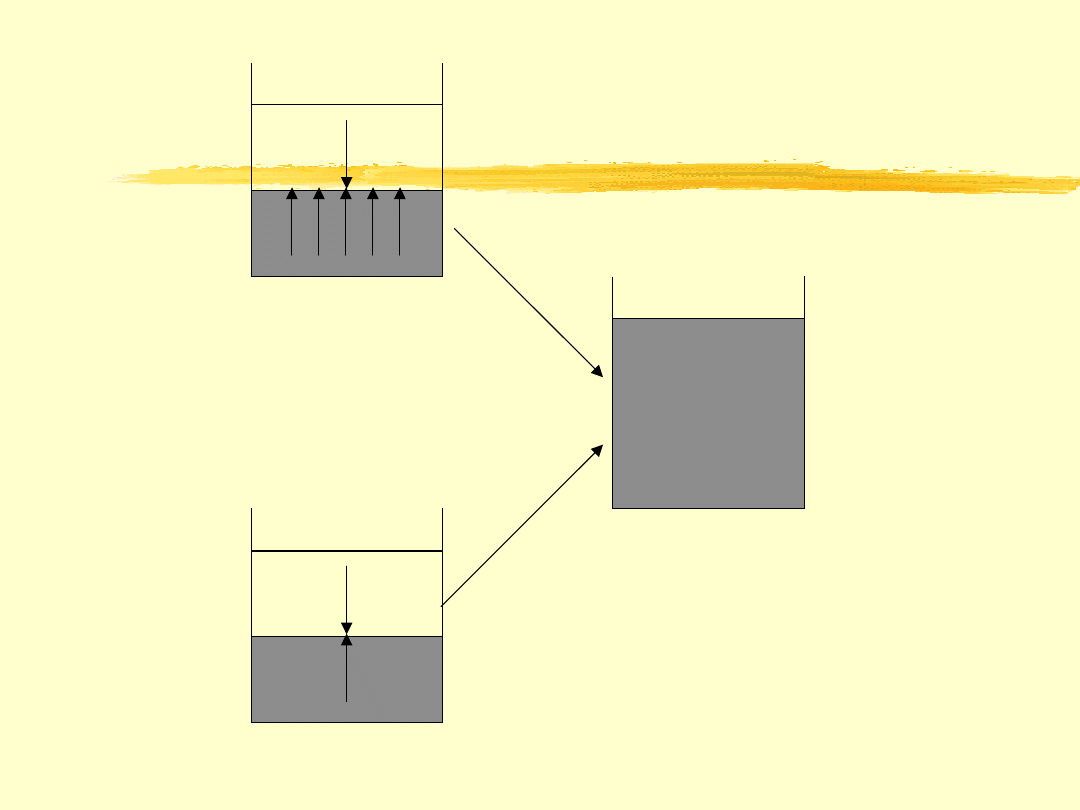
Rozprężanie 1 mola gazu doskonałego od tego
samego stanu początkowego do tego samego stanu
końcowego w sposób:
a )
a )
nieodwracalny
b)
b)
odwracalny
Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ
1
2
.
obj
V
V
ln
T
R
-
W
1
2
z
z
.
obj
V
-
V
p
-
V
p
-
W
p
z
< p
w ,
p
z
= const
.
(a)
stan początkowy
V
2
V
2
V
1
W
N
p
z
= p
w
const
stan końcowy
(b)
V
2
W
O
V
1
W
O
W
N
stan początkowy
Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ

ENTROPIA – S
ENTROPIA – S
[ J K
[ J K
-1
-1
] , [ J mol
] , [ J mol
-1
-1
K
K
-1
-1
]
]
TERMODYNAMICZNA FUNKCJA STANU
TERMODYNAMICZNA FUNKCJA STANU
dS = S
2
– S
1
S = S
2
– S
1
ZMIANA ENTROPII W PROCESIE ODWRACALNYM,
izotermicznym ( zachodzącym w układzie zamkniętym )
wynosi:
T
Q
dS
(odwr.)
el.
T
Q
S
(odwr.)
Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ

ZMIANA ENTROPII W PROCESIE NIEODWRACALNYM:
T
Q
dS
el.
T
Q
S
Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ
NIERÓWNOŚĆ CLAUSIUSA
NIERÓWNOŚĆ CLAUSIUSA

Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ
Zmiana entropii układu izolowanego
określa kierunek samorzutności procesu
DRUGA ZASADA TERMODYNAMIKI
DRUGA ZASADA TERMODYNAMIKI
( kryterium samorzutności procesów )
( kryterium samorzutności procesów )
S
S
u. iz.
u. iz.
0
0
S
S
ukł. iz.
ukł. iz.
=
=
S
S
ukł. z.
ukł. z.
+
+
S
S
otocz
otocz
.
.
Zmiana entropii układu izolowanego w procesie odwracalnym
jest równa zero, a w procesie nieodwracalnym
( samorzutnym ) jest większa od zera.
S
S
u. Iż.
u. Iż.
= 0
= 0 proces odwracalny
S
S
u. Iż.
u. Iż.
> 0
> 0 proces samorzutny
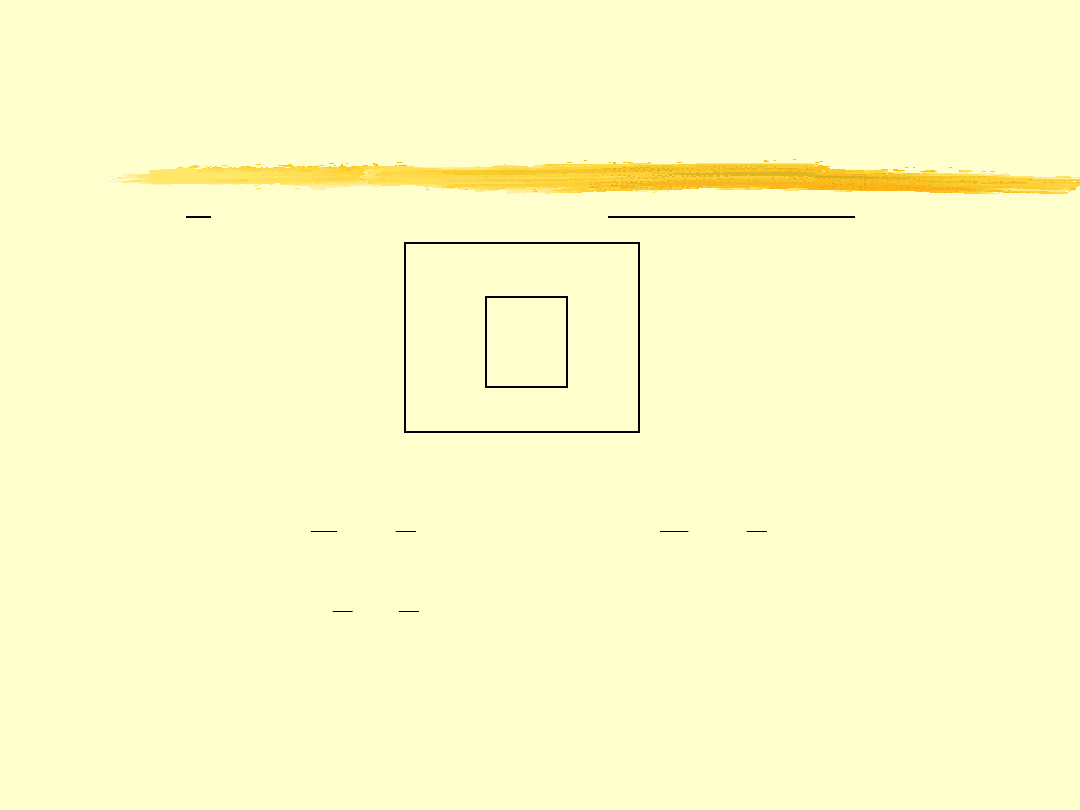
Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ
( a )
Z m i a n a e n t r o p i i u kł a d u i z o l o w a n e g o w p r o c e s i e o d w r a c a l n y m
o t o c z .
T
2
u kł .
T
1
T
1
= T
2
= T
S
u kł . i z .
= S
u kł .
+ S
o t o c z .
T
Q
T
Q
S
1
.
ukl
,
T
Q
T
Q
S
2
.
otocz
0
T
Q
T
Q
S
iz.
.
ukl

Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ
b ) Z m i a n a e n t r o p i i u kł a d u i z o l o w a n e g o w p r o c e s i e n i e o d w r a c a l n y m
( s a m o r z u t n y m )
o t o c z .
T
2
u kł .
T
1
T
1
< T
2
S
u kł . i z .
= S
u kł .
+ S
o t o c z .
T
Q
S
1
.
ukl
,
T
Q
S
2
.
otocz
0
T
T
T
-
T
Q
T
T
T
Q
-
T
Q
T
Q
T
Q
S
2
1
1
2
2
1
1
2
2
1
iz. .
ukl

Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ
TRZECIA ZASADA TERMODYNAMIKI
TRZECIA ZASADA TERMODYNAMIKI
TEOREMAT NERNSTA
TEOREMAT NERNSTA
S
S
T = 0 K
T = 0 K
= 0
= 0
Jeśli entropię każdego pierwiastka w jego najbardziej
trwałej postaci
w T = 0 K przyjmiemy za równą zero, to każda substancja
ma entropię
dodatnią, która dla T = 0 K może przyjmować wartość
zero i która
przyjmuje wartość zero dla wszystkich doskonale
krystalicznych
substancji, ze związkami chemicznymi włącznie.
Entropia
regularnie
ułożonych
cząsteczek
(
ciał
krystalicznych )
w temperaturze zera bezwzględnego ( T = 0 K ) wynosi
zero.

Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ
ENTROPIA
ENTROPIA
miara nieuporządkowania materii i
miara nieuporządkowania materii i
energii
energii
nieuporządkowanie entropia
S
ciało stałe
< S
ciecz
< S
gaz
temperatura nieuporządkowanie
Jedyna funkcja termodynamiczna, dla której można podać wartość bezwzględną:
S

Przykłady
S tan d ard o w e w artoś c i en tro p ii m o lo w yc h
d la w yb ran yc h s u b s tan c ji
S u b s tan c ja
K
298
S
[J /m o lK ]
S u b s tan c ja
K
298
S
[J /m o lK ]
C
(g r)
5.69
S O 2
(g )
248.52
O 2
(g )
205.03
S O 3
(g )
256.23
C O 2
(g )
213.64
A g 2 C O 3
(s )
167.40
H 2
(g )
130.60
C 2H2
(g )
200.80
H 2O
(c )
69.96
C H 4
(g )
186.10
H 2O
(g )
188.7
C 2H4
(g )
219.40
C O
(g )
197.99
C 6H 6
(c )
175.30
H B r
(g )
198.60
C H 3C O O H
(c )
160.00
A g B r
(s )
107.10
C 6H 5-NO 2
(c )
224.00
A g 2O
(s )
121.70
C 6H 5-N H 2
(c )
192.00
Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ

Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ
OBLICZANIE ZMIAN ENTROPII
OBLICZANIE ZMIAN ENTROPII
p.f.
p.f.
T
H
n
S
•
PRZEMIANY FAZOWE ( T, p = const. )
PRZEMIANY FAZOWE ( T, p = const. )
•
REAKCJE CHEMICZNE
REAKCJE CHEMICZNE
.
substr
i
i
i
.
prod
i
i
i
S
n
-
S
n
S

Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ
•
PROCESY OGRZEWANIA I OZIĘBIANIA
PROCESY OGRZEWANIA I OZIĘBIANIA
SUBSTANCJI
SUBSTANCJI
p
=
c
o
n
s
t.
C
p
=
c
o
n
st. :
1
2
p
T
T
ln
C
n
S
v
=
c
o
n
s
t
.
C
v
=
c
o
n
s
t
. :
1
2
v
T
T
ln
C
n
S
T
1
- temperatura początkowa
T
2
- temperatura końcowa
C
p (V)
= const.

Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ
•
PROCESY OGRZEWANIA I OZIĘBIANIA
PROCESY OGRZEWANIA I OZIĘBIANIA
SUBSTANCJI
SUBSTANCJI
T
1
- temperatura początkowa
T
2
- temperatura końcowa
p
=
c
o
n
s
t
.
C
p
c
o
n
s
t
. :
dT
T
C
n
S
2
1
T
T
p
v
=
c
o
n
s
t
.
C
v
c
o
n
s
t
. :
dT
T
C
n
S
2
1
T
T
V
C
p (V)
const. , C
p (V)
=
f (T)

POŁĄCZENIE PIERWSZEJ I DRUGIEJ ZASADY
POŁĄCZENIE PIERWSZEJ I DRUGIEJ ZASADY
TERMODYNAMIKI
TERMODYNAMIKI
dU = Q
el.
+ W
Dla dowolnej przemiany - odwracalnej lub nieodwracalnej -
w układzie zamkniętym, który nie wykonuje pracy nieobjętościowej.
W = W
obj. odwr.
= - p dV
T
Q
dS
odwr.
Q
odwr.
= T dS
dU = T dS - p dV
Dla przemiany odwracalnej w układzie zamkniętym o stałym składzie
i przy braku pracy nieobjętościowej:
RÓWNANIE FUNDAMENTALNE
Mgr Beata Mycek -
Zakład Farmakokinetyki i Farmacji Fizycznej
CM UJ
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
Wyszukiwarka
Podobne podstrony:
chfwyklad 2
chfwyklad 8
chfwyklad 4
chfwyklad 7
chfwyklad 2
więcej podobnych podstron