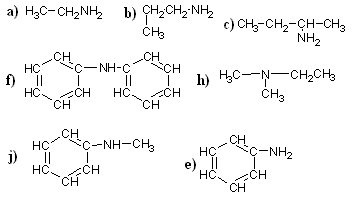
Aminy i amidy
Przykładowe zadania na kartkówkę
1. Podaj wzory półstrukturalne związków: zidentyfikować te roztwory, dysponując roztworami lakmusu a) aniliny,
b) butyloaminy, c) etylodimetyloaminy i fenoloftaleiny?
d) o-chloroaniliny
e) mocznika
Odp.: Etanol nie zmienia barwy wskaźników, etyloamina powoduje zabarwienie r-ru fenoloftaleiny na różowy, kwas 2. Podaj nazwy związków:
octowy powoduje zmianę barwy lakmusu na pomarańczowo-czerwony.
13. Do trzech probówek zawierających substancje praktycznie nierozpuszczalne w wodzie: nitrobenzen, anilinę oraz chlorobenzen dodano roztworu kwasu solnego? Podaj równania ewentualnych reakcji.
Podpowiedź.: Tylko anilina ulega reakcji z HCl tworząc rozpuszczalny w wodzie chlorowodorek aniliny.
14. Wstaw w miejsce liter A, B, C itd. wzory półstrukturalne odpowiednich związków:
a) CaC2
H O
trimeryza j
c a
HNO
H
,
SO
2
→ A
→ B
32 4→ C
3. Podaj wzory półstrukturalne i nazwy wszystkich C
Zn ,
HCl → D
Na
OH
,
H O
2
→ E
izomerycznych amin o wzorze sumarycznym C3H9N.
b) A
HCl → B N
H3→ CH
Na
OH
, H
O
2
→ C
4. Narysuj wzory strukturalne i elektronowe wszystkich amin 3CH2NH+Cl¯
Cl
ś
, wiatło
NH
NaOH
, H
O
o składzie chemicznym C
c) toluen
2
→ A
3→ B
2 → C
4H11N? Podaj ich nazwy oraz
rzędowość.
d) benzen
Cl2
F
, e
Cl3 → B N
H3→ C
Na
OH
,
H O
2
→ D
5. Zapisz poniższe równania reakcji:
D
HCl → C
a) CH3CH2Cl + NH3 ;b) CH3–CH2–NH2 + H2O
e) A Al2
O3→ etylen
HCl → B N
H3→ C
c) 1-fenylometyloamina + CH
temp.
3Cl
; j) mocznik
→
NaOH
, H
O
HCl
d) nitrobenzen + Zn +HCl
;e) 2-metyloanilina + HCl
C
2 → D
→ E
HCl
NH
NaOH
, H
O
HCl
f) anilina + HNO
H
SO
2
4 →
f) propen
→ B
3→ C
2 → D
→ E
3
;g) anilina + CH3Cl
HCl
NH
NaOH
, H
O
h) acetamid + NaOH
H O
2
→ ;i) acetamid + HCl + H
g) 1,3-butadien
→ B
3→ C
2 → D
2O
6. Wodny roztwór metyloaminy ma odczyn zasadowy. Wyja HCl
śnij
D
→ E
dlaczego, oraz podaj odpowiednie równanie reakcji.
15. Napisz równania następujących przemian chemicznych: Odp.: Ponieważ aminy reagują z wodą zabierając jej kation a) toluen
p-nitrotoluen
p-aminotoluen,
wodorowy, co powoduje wzrost stężenia jonów b) R–CH2OH R–CHO
R–COOH
R–COONH4
OH¯ w roztworze: CH
+
3NH2 + H2O
CH3NH3 + OH¯
R–CONH2
7. Omów zmianę właściwości fizycznych amin alifatycznych 16. W reakcji mocznika ze stężonym kwasem azotowym(V) wraz
ze
wzrostem
długości
łańcucha
węglowego?
wykrystalizowuje się osad azotanu(V) mocznika.
Odp.: Aminy o krótkich łańcuchach węglowych są gazami, Mocznik reaguje z kwasem w stosunku molowym 1:1. Podaj wyższe są cieczami i ciałami stałymi. Podobnie jak równanie tej reakcji wzorami półstrukturalnymi.
w przypadku alkoholi, w miarę wzrostu długości łańcucha Odp.: NH2CONH2 + HNO3
[NH2CONH3]+NO3¯
węglowodorowego maleje rozpuszczalność amin w wodzie.
17. Zapisz równania reakcji hydrolizy kwasowej i zasadowej Aminy mają zapach przypominający ryby, nasila się on w mocznika.
miarę wzrostu długości łańcucha węglowego.
Odp.:a) NH2CONH2 + H2SO4 + H2O (NH4)2SO4 + CO2
8. Wyjaśnij przyczynę różnic temperatur wrzenia etanolu b) NH2CONH2 + 2NaOH 2NH3 + Na2CO2
(78°C), i etyloaminy (17°C)
18. Ogrzewając bezwodny mocznik powodujemy wydzielanie się Odp.: Pomiędzy cząsteczkami etyloaminy występują amoniaku i powstanie biuretu, którego obecność możemy znacznie słabsze wiązania wodorowe.
wykryć w reakcji z Cu(OH)2. Zapisz równanie reakcji 9. Temperatury wrzenia amin alifatycznych są niższe od otrzymywania biuretu oraz zmiany barw, jakie obserwuje się temperatur wrzenia alkoholi o takich samych łańcuchach podczas tej reakcji.
węglowodorowych. Wyjaśnij przyczynę tych różnic.
te
mperatura →
Odp.: Pomiędzy cząsteczkami alkoholi występują znacznie Odp.: 2NH2CONH2
NH2-CO-NH-CO-NH2
silniejsze wiązania wodorowe.
19. W laboratoriach fotograficznych stosuje p-hydroksyanilinę.
10. Napisz wzory półstrukturalnych wszystkich związków, jakie Podaj równania reakcji p-hydroksyaniliny z: mogą znajdować się w zbiorniku, po reakcji mieszaniny a) kwasem solnym,
1-chloropropylu, chloroetylu i amoniaku.
b) wodorotlenkiem sodu.
11. Zapisz równania reakcji wzorami półstrukturalnymi: 20. Zaproponuj doświadczenie pozwalające wykazać, że w a) anilina + kwas solnym
moczniku znajduje się grupa aminowa. Podaj schemat b) anilina + kwas siarkowy (stosunek molowy 1 : 1) doświadczenia, obserwacje, oraz zapisz równania c) anilina + kwas siarkowy (stosunek molowy 2 : 1) zachodzących reakcji wzorami półstrukturalnymi.
Odp.:
a) C
+
21. Podaj nazwisko chemika, którego prace doświadczalne stały 6H5NH2 + HCl
C6H5NH3 Cl¯
b) C
+
się końcem tzw. teorii witalistycznej.
6H5NH2 + H2SO4
C6H5NH3 HSO4¯
c) C
+
2–
Odp.: Fryderyk Wöhler w 1828 r. otrzymał mocznik z 6H5NH2 + 2H2SO4
(C6H5NH3 )2SO4
12. W trzech probówkach znajdują się wodne roztwory etanolu, cyjanianu amonu.
etyloaminy i kwasu octowego. W jaki sposób można
- 1 -