UNIWERSYTET PRZYRODNICZY
Wydział Medycyny Weterynaryjnej
KATEDRA BIOCHEMII I FIZJOLOGII ZWIERZĄT
Zakład Biochemii
20-033 Lublin, ul. Akademicka 12
tel. 081 445 69 73
Analiza miareczkowa
część praktyczna ćwiczenia
Zadanie 1
Celem zadania jest oznaczanie stęŜenia kwasu solnego przy pomocy mianowanego roztworu zasady sodowej.
Zasada oznaczania
Oznaczanie opiera się na zobojętnieniu kwasu solnego roztworem wodorotlenku sodu wobec fenoloftaleiny. Nadmiar wodorotlenku sodu, po zobojętnieniu całego miareczkowanego kwasu, zmienia środowisko roztworu na alkaliczne, w którym fenoloftaleina przybiera barwę róŜowo-malinową.
HCl + NaOH ⇒ NaCl + H2O
Wykonanie
Do dwóch kolb stoŜkowych odmierzyć dokładnie po 10 cm3 roztworu HCl o nieznanym stęŜeniu, dodać 3 krople roztworu fenoloftaleiny jako wskaźnika.
Biuretę napełnić mianowanym roztworem NaOH o stęŜeniu 0,1 mol/dm3.
Miareczkować, intensywnie mieszając do czasu odbarwienia roztworu.
Za punkt końcowy miareczkowania przyjmujemy moment gdy po dodaniu kro-pli NaOH roztwór nie zmienia barwy.
Obliczyć stęŜenie molowe nieznanego roztworu HCl.
Analogicznie postępować z druga kolbą. Jako wynik końcowy podać średnią z dwóch oznaczeń.
Zadanie 2
Celem zadania jest oznaczenie stęŜenie molowego i procentowego kwasu salicylowego w spirytusie salicylowym.
Zasada oznaczania
Oznaczanie opiera się na zobojętnieniu kwasu salicylowego roztworem wodorotlenku sodu wobec fenoloftaleiny. Nadmiar wodorotlenku sodu, po zobojętnieniu całego miareczkowanego kwasu, zmienia środowisko roztworu na alkaliczne, w którym fenoloftaleina przybiera barwę róŜowo-malinową.
HO-C6H4COOH + NaOH ⇒ HO-C6H4COONa + H2O
Wykonanie
10-10-18 www.biochfiz.up.lublin.pl Wersja 2.18.10.10
CHEMIA 4, Analiza miareczkowa
- 1 z 4 -

UNIWERSYTET PRZYRODNICZY
Wydział Medycyny Weterynaryjnej
KATEDRA BIOCHEMII I FIZJOLOGII ZWIERZĄT
Zakład Biochemii
20-033 Lublin, ul. Akademicka 12
tel. 081 445 69 73
Do dwóch kolb stoŜkowych odmierzyć dokładnie po 10 cm3 roztworu kwasu salicylowego o nieznanym stęŜeniu, dodać 3 krople roztworu fenoloftaleiny jako wskaźnika.
Biuretę napełnić mianowanym roztworem NaOH o stęŜeniu 0,1 mol/dm3.
Miareczkować, intensywnie mieszając do czasu odbarwienia roztworu.
Za punkt końcowy miareczkowania przyjmujemy moment gdy po dodaniu kro-pli NaOH roztwór nie zmienia barwy.
Obliczyć stęŜenie molowe i procentowe nieznanego roztworu kwasu salicylowego.
Analogicznie postępować z druga kolbą. Jako wynik końcowy podać średnią z dwóch oznaczeń.
Zadanie 3
Celem zadania jest określenie właściwości nadmanganianu potasu w zaleŜności od środowiska reakcji.
Zasada oznaczania
W zaleŜności od środowiska reakcji moŜemy obserwować zmianę stopnia utlenienia KMnO4:
− w środowisku kwaśnym redukcja do bezbarwnego jonu Mn2+:
2 KMnO4 + 5 Na2SO3 + 3 H2SO4 ⇒ 2 MnSO4 + 5 Na2SO4 + K2SO4 + 3 H2O
− w środowisku obojętnym redukcja do brunatnego tlenku MnO2:
2 KMnO4 + 3 Na2SO3 + 3 H2O ⇒ 2 ↓MnO2 + 3 Na2SO4 + 2 KOH
− w środowisku alkalicznym redukcja do zielonego jonu MnO 2-
4
:
2 KMnO4 + Na2SO3 + 2 KOH ⇒ 2 K2MnO4 + 5 Na2SO4 + H2O
Wykonanie
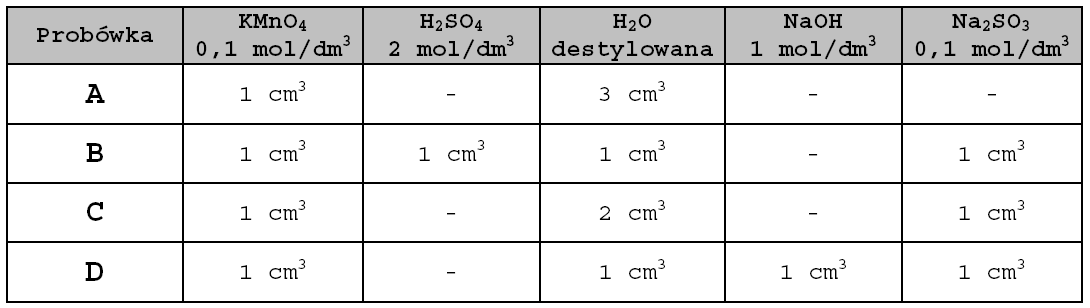
Do czterech probówek (A, B, C, D) odmierzyć odczynniki zgodnie z tabelą. Przed dodaniem roztworu Na2SO3 zawartość probówek dokładnie wy-mieszać.
Obserwować przebieg reakcji. Zapisać jonowo równania reakcji prze-biegających w probówkach, wskazać stopnie utlenienia manganu.
10-10-18 www.biochfiz.up.lublin.pl Wersja 2.18.10.10
CHEMIA 4, Analiza miareczkowa
- 2 z 4 -

UNIWERSYTET PRZYRODNICZY
Wydział Medycyny Weterynaryjnej
KATEDRA BIOCHEMII I FIZJOLOGII ZWIERZĄT
Zakład Biochemii
20-033 Lublin, ul. Akademicka 12
tel. 081 445 69 73
Zadanie 4
Celem zadania jest manganometryczne oznaczenie stęŜenie nadtlenku wodoru w roztworze wodnym (wodzie utlenionej).
Zasada oznaczania
Oznaczenie nadtlenku wodoru opiera się na jego redukcyjnych właści-wościach w reakcji z manganianem(VII). Podawany z biurety manganian(VII) do roztworu oznaczanego nadtlenku ulega redukcji i odbarwie-niu. Po utlenieniu całości nadtlenku, nadmiar KMnO
4 zabarwia miareczko-
wany roztwór na róŜowo, co świadczy o osiągnięciu punktu końcowego miareczkowania.
2 MnO -
↑
4 + 5 H2O2 + 6 H3O+ ⇒ 5 O2
+ 2 Mn+2 + 14 H2O
Wykonanie
Do dwóch kolb stoŜkowych odmierzyć dokładnie po 2 cm3 roztworu nadtlenku wodoru o nieznanym stęŜeniu, 10 cm3 wody destylowanej oraz 5
cm3 2 mol/dm3 H2SO4. Wymieszać.
Biuretę
napełnić
mianowanym
roztworem
KMnO4
o
stęŜeniu
0,1 mol/dm3.
Miareczkować, intensywnie mieszając do czasu odbarwienia roztworu.
Za punkt końcowy miareczkowania przyjmujemy moment gdy po dodaniu kro-pli KMnO4 roztwór zabarwi się na róŜowo i zabarwienie to będzie się utrzymywać przez minutę.
Obliczyć stęŜenie procentowe nieznanego roztworu nadtlenku wodoru.
Przyjąć, Ŝe 1 cm3 0,1 mol/dm3 roztworu KMnO4 odpowiada 1,7008 mg H2O2.
Analogicznie postępować z druga kolbą. Jako wynik końcowy podać średnią z dwóch oznaczeń.
10-10-18 www.biochfiz.up.lublin.pl Wersja 2.18.10.10
CHEMIA 4, Analiza miareczkowa
- 3 z 4 -

UNIWERSYTET PRZYRODNICZY
Wydział Medycyny Weterynaryjnej
KATEDRA BIOCHEMII I FIZJOLOGII ZWIERZĄT
Zakład Biochemii
20-033 Lublin, ul. Akademicka 12
tel. 081 445 69 73
Notatki:
10-10-18 www.biochfiz.up.lublin.pl Wersja 2.18.10.10
CHEMIA 4, Analiza miareczkowa
- 4 z 4 -