Układ okresowy pierwiastków
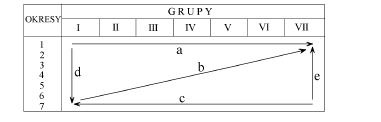
Zad.1 Rysunek przedstawia schemat układu okresowego. Wskaż jakie zmiany wielkości mogą podawać narysowane linie (a-e).
Zad.2 Pierwiastek jest metalem i tworzy wodorek, który zawiera w cząsteczce dwa atomy wodoru. Podaj grupę układu okresowego w której powinien on się znajdować .
Zad.3 Podaj symbol powłoki walencyjnej cyny.
Zad.4 Podaj liczbę elektronów walencyjnych kadmu.
Zad.5 Który pierwiastek jest aktywniejszy: a) lit czy bor b) fosfor czy arsen c) rubid czy cez d) tellur czy jod Zad.6 Podaj nazwę niemetalu i metalu o największej aktywności.
Zad.7 W którym związku tworzące go jony mają taką sama konfigurację elektronową. Uzasadnij swoją odpowiedź pisząc te konfiguracje: A. LiCl B. KBr C. CaCl2 D. MgI2
Zad.8 Pierwiastek X tworzy związek, który zawiera trzy atomy wodoru w cząsteczce. Podaj, w której grupie układu okresowego może znajdować się pierwiastek X.
Zad.9 Podaj nazwy poniższych związków: a) AsH3 b) KH c) HBr d) CH4 e) SiH4 f) PH3 g) MgH2
Zad.10 Podaj a) jedną cechę wspólną i b) jedną różnicę w 1) konfiguracjach elektronowych fluoru, chloru i bromu. Podaj różnice w ich właściwościach fizycznych.
Zad.11 Podaj nazwę(-y) pierwiastka(-ów) czwartego okresu, który posiada 7 elektronów walencyjnych.
Zad.12 Które pierwiastki posiadające trzy powłoki w atomie tworzą związek, który zawiera trzy atomy wodoru w cząsteczce?
Zad.13 Ile powłok zajmują elektrony w atomie żelaza?
Zad.14 Dane są dwa pierwiastki: X i Y. W atomie pierwiastka X elektrony zajmują trzy powłoki , a na ostatniej powłoce znajduje się sześć elektronów. Pierwiastek Y leży o jeden okres niżej w układzie okresowym , ale na ostatniej powłoce ma jeden elektron walencyjny.
a) podaj nazwę pierwiastka X i Y
b) napisz wzór najwyższego tlenku pierwiastka X
c) napisz wzór związku pierwiastka Y wodorem
Zad.15 Które pierwiastki spełniają jednocześnie następujące warunki: atom ma pięć powłoki i tworzy związek z wodorem, zawierający jeden atom wodoru w cząsteczce
Zad.16 Które z poniższych drobin mają taką samą liczbę elektronów: S2-, Kr, Ba2+, K+, Br-, Rb+, Ca2+, Ar
Zad. 17 Uszereguj podane pierwiastki według rosnącej odległości elektronów walencyjnych od jądra:
a) cez, potas, lit, sód, rubid b) siarka, glin, fosfor, krzem, chlor
Zad.18 Uszereguj podane metale według malejącej ich reaktywności: magnez, potas, glin.
Zad.19 Przyporządkuj pierwiastki do odpowiednich bloków energetycznych : rubid, cyna, srebro, hel, uran, tlen, tor, żelazo, fosfor, selen. magnez.
Zad.20 Podaj nazwy i symbole pierwiastków, które spełniają następujące warunki:
I pierwiastek: atom posiada trzy elektrony walencyjne na czwartej powłoce
II pierwiastek: leży w trzecim okresie, tworzy związki typu: E2O5 i EH3
III pierwiastek: leży w 17 grupie układu okresowego i ma pięć powłok elektronowych
Zad.21 Dany jest szereg pierwiastków: Na, Mg, Al., Si, P, S. Podaj jak zmieniają się w tym szeregu następujące wielkości: elektroujemność, promień atomu, liczba powłok elektronowych, liczba protonów w jądrze, charakter kwasowy, charakter zasadowy.
Zad.22 Jak zmienia się a) aktywność, b) elektroujemność, c) promień atomu, d) promień jonu pierwiastków w grupie 1 i 17 układu okresowego.
Zad.23 Dane są dwa pierwiastki X i Y. W atomie pierwiastka X elektrony zajmują cztery powłoki, a na ostatniej znajduje się siedem elektronów walencyjnych. Skrócona konfiguracja elektronowa pierwiastka Y to [Ar]4s2.
a) podaj wzory tlenków pierwiastka X i Y na typowym (najtrwalszym) stopniu utlenienia
b) podaj wzory i nazwy związków pierwiastków X i Y z wodorem
c) napisz wzór związku X z Y
Zad.24 Która cząstka ma większy promień: a) Na+ czy K+ b) Br- czy I- c) K+ czy Ca2+ d) S2- czy Cl-, e) Li czy Be f) O czy F
g) Mg czy Mg2+ h) Br czy Br-
Zad.25 Podaj ile powłok elektronowych zawierają następujące jony: Na+ , H+, Se2-, Cl-
Zad.26 Podaj liczbę elektronów na zewnętrznej powłoce dla jonów: Ca2+, I-, H+, N3-, Al3+, Be2+, H-
Zad.27 Wymień typowe stopnie utlenienia(wynikające z konfiguracji elektronowej) pierwiastków o liczbie atomowej: 5,15, 35, 55
Zad.28 Określ charakter chemiczny tlenków: radu, węgla(II), siarki(IV), węgla(IV), wapnia, glinu.
Zad.29 Uszereguj dane tlenki według rosnącej kwasowości: Cl2O7, Na2O, P4O10, MgO, SiO2, SO3, Al2O3