Imię i nazwisko: Łukasz Chłopczyński
Wydział : Biotechnologii i nauk o żywności
Kierunek : Biotechnologia
Grupa : IV
Ćwiczenie nr 12
Tytuł ćwiczenia: Wyznaczanie ciepła zobojętniania
Data wykonania ćwiczenia....................
Data oddania sprawozdania..................
Data zwrotu sprawozdania....................
Data ponownego oddania sprawozdania..............
Wstęp teoretyczny:
Energia wewnętrzna U [ J] – całkowita ilość energii w układzie, jest sumą energii kinetycznej i potencjalnej wszystkich atomów, jonów, cząsteczek w układzie. Całkowitą ilość energii w układzie można można scharakteryzować za pomocą entalpii H.
H = U + pV
Nie można zmierzyć bezwzględnej wartości entalpii, można natomiast zmierzyć różnice entalpii układu ΔH, w różnych satanach.
Ciepło q [ J] – jeden ze sposobów przeniesienia energii miedzy układem, a otoczeniem. Wymiana ciepła jest spowodowana różnicą temperatur pomiędzy układem i otoczeniem.
Praca w [ J] – inny sposób wymiany energii pomiędzy układem a otoczeniem. Pracę wykonaną przez układ na otoczeniu oznaczamy jako dodatnią. Pracę wykonaną przez otoczenie na układzie oznaczamy jako ujemną.
Pierwsza zasada termodynamiki jest specyficznym sformułowaniem zasady zachowania energii, która mówi, że zmiana energii wewnętrznej układu jest skutkiem wymiany ciepła i/lub pracy z otoczeniem.
ΔU = q – w
Jeśli w układzie możliwa jest jedynie praca zmiany objętości, zwana pracą objętościową pierwsza zasada termodynamiki przyjmuje postać:
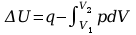
Widać stąd, że przemianie izochorycznej ( V = const) zmiana energii wewnętrznej układu jest równa ciepłu wymienionemu z otoczeniem:
ΔU = qV
Pierwszą zasadę termodynamiki można zapisać za pomocą entalpii:
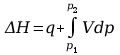
Pojemność
cieplna
– jest to ilość ciepła niezbędna do ogrzania układu o jeden
stopień
pod stałym ciśnieniem
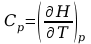
lub
w stałej objętości
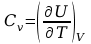 . Ilość ciepła niezbędna do
ogrzania
1 mola składnika pod stałym ciśnieniem nazywamy
molową
pojemnością cieplną pod stałym ciśnieniem
. Ilość ciepła niezbędna do
ogrzania
1 mola składnika pod stałym ciśnieniem nazywamy
molową
pojemnością cieplną pod stałym ciśnieniem
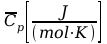 ,
lub stałej objętości
,
lub stałej objętości
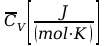 .
.
Reakcja spalania – W termochemii przez reakcje spalania rozumie się reakcję łączenia pierwiastka lub związku chemicznego z tlenem, w wyniku czego powstają produkty nie mogące ulec dalszemu spaleniu.
Reakcje zobojętniania:
Reakcje pomiędzy kwasem siarkowym a zasadą sodową możemy zapisać tak:
H2SO4 + 2NaOH = 2H2O + Na2SO4
Lub w postaci jonowej:
2H+ + 2OH- = 2H2O
Zatem reakcja ta przebiega między jonami wodorowymi a jonami hydroksylowymi z utworzeniem 2 cząsteczek wody.
Reakcja zobojętniania mocnej zasady mocnym kwasem polega na reakcji uwodnionych jonów wodorowych i hydroksylowych z utworzeniem cząsteczki wody:
H+(aq) + OH-(aq) = H2O
Ciepło tej reakcji nie zależy od rodzaju kwasu i zasady biorących udział w reakcji i wynosi -56,61 kJ w przeliczeniu na jeden mol utworzonej wody.
Cel ćwiczenia:
Celem ćwiczenia jest wyznaczenie ciepła zobojętniania.
Eksperyment przeprowadza się w naczyniu Dewara (termosie), który pełni rolę kalorymetru. Ćwiczenie obejmuje następujące etapy, które należy przeprowadzić w tym samym kalorymetrze.
Wyznaczenie pojemności cieplnej kalorymetru (kalibracja) w oparciu o ciepło rozpuszczania kwasu siarkowego wodzie.
Wyznaczanie ciepła towarzyszącego procesowi rozpuszczania kwasu siarkowego w wodzie zawierającej nadmiar stechiometryczny wodorotlenku sodu.
Wykonanie ćwiczenia:
Wyznaczanie pojemności cieplnej kalorymetru
Wyznaczanie ciepła zobojętniania
Wyszukiwarka