ANALIZA INSTRUMENTALNA
ĆWICZENIE NR 9
ILOŚCIOWE OZNACZANIE ZAWARTOŚCI WITAMINY C METODĄ WOLTAMPEROMETRII CYKLICZNEJ
Celem ćwiczenia jest ilościowe oznaczenie witaminy C w sokach owoców i warzyw. Zapoznanie się z techniką woltamperometrii cyklicznej.
Kwas askorbinowy (witamina C) można elektrochemicznie utleniać do kwasu dehydroaskorbinowego:
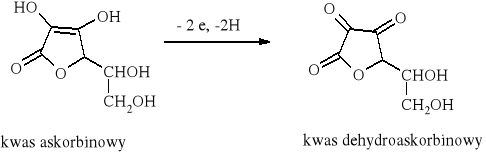
Elektrolitem podstawowym jest 0.1M bufor octanowy o pH = 4.7, ze względu na stosunkowo wolno zachodzące utlenianie witaminy C tlenem cząsteczkowym w tym roztworze.
Odczynniki i aparatura:
wielofunkcyjny analizator elektrochemiczny Pine,
bufor octanowy o stężeniu 1M i 0.1 M,
soki firmowe (np. jabłkowy, pomarańczowy, grejpfrutowy) lub świeżo wyciśnięte z cytryny, pomarańczy, grejpfruta, sok z kiszonej kapusty
Wykonanie ćwiczenia:
Sporządzić roztwory buforowe: 100 cm3 0.1M - odważyć 0,3854g octanu sodu i odmierzyć 0,306 cm3 99% kwasu octowego, uzupełnić do kreski wodą destylowaną; 100cm3 1M - odważyć 3,854g octanu sodu i odmierzyć 3,06 cm3 99% kwasu octowego, uzupełnić do kreski wodą destylowaną.
Sporządzić roztwór wzorcowy witaminy C, w tym celu zważyć tabletkę witaminy C, następnie odważyć około 0.04g tabletki witaminy C, do kolbki 25 cm3 przenieść odważoną tabletkę, dodać 2.5 cm3 1M roztworu buforowego buforowego uzupełnić do kreski wodą destylowaną, mieszać aż do rozpuszczenia tabletki. Obliczyć stężenie otrzymanego roztworu, wiedząc, że w jednej tabletce jest 0.2 mg witaminy C.
Uruchomić analizator woltamperometryczny, do naczyńka pomiarowego wlać 25cm3 odtlenionego roztworu elektrolitu podstawowego, wrzucić mieszadełko i podłączyć elektordy: referencyjna ( R)- chlorosrebrowa, odniesienia (C ) - platynowa, pracująca (W) - węglowa.
Uruchomic program AfterMatch, pojawia się okienko AfterMatch Login dac ok., następnie wybrać Cyclic Voltammerty , w okienku powinno pisać PineWaveNow(SN1910009) - jeżeli nie to wybrac ten instrument, następnie 06 ustawić parametry pomiaru:
W górnym pasku przycisnąć Perform, w tym momencie rusza pomiar. Na górze okna pomiarowego będzie pisać numer cyklowoltamogramu, np. CVExperyment (0003) - zapisać ten numer! Po zakończeniu pomiaru przycisnąć File - Save Archive as - (zapisujemy Pulpit - analiza).
W celu wykonania kolejnego pomiaru kliknąć CV Parametr(0002), jeżeli jest taka potrzeba to zmienić ustawienia parametrów pomiaru, jeżeli nie to kliknąć Perform. Dalej postąpić jak w punkcie wyżej.
Pamiętać, aby przed każdym pomiarem wyczyścić elektrodę węglową!
W celu odczytania potencjału piku i wartości prądu, najechac myszką na wykres, kliknąc prawym klawiszem i wybrać AddTool → CrossHair. Pojawi się zielony punkt, który można przesuwać po wykresie wykresie odczytywać wartość potencjału i prądu dla danego punktu.
Po zarejestrowaniu krzywej woltamperometrycznej dla elektrolitu podstawowego do roztworu dodać 2,5 cm3 badanego soku, zamieszać, wyczyścić elektrodę pracującą, wyłączyć mieszanie i zarejestrować cyklowoltamogram. Odczytać wartość natężenia prądu dla piku. Następnie do tego samego roztworu dodać 1 cm3 wzorcowego roztworu witaminy C, zamieszać, wyczyścić elektrodę, wyłączyć mieszanie i zarejestrować cyklowoltamogram. Odczytać wartość natężenia prądu dla piku.
Postępując jak opisano powyżej zarejestrować cyklowoltamogramy, dla co najmniej dwóch różnych soków.
Wyniki przedstawić w tabelce:
A. Cygański „ Podstawy metod elektroanalitycznych”, WNT 1999.
W. Szczepaniak „Metody instrumentalne w analizie chemicznej”, PWN 2005.
J. Minczewski, Z. Marzenko „Chemia Analityczna, t.3. Analiza Instrumentalna”, PWN 1998.
G.W. Swing „Metody instrumentalne w analizie chemicznej”, PWN 1980.
Liczba segmentów |
3 |
Initial potential |
0 V |
Rasing |
zaznaczyć |
Upper potential |
0.9 V |
Lower potential |
-0.1V |
Final potential |
0 V |
Scan rate |
0.1 V/s |
|
Ip [μA] |
Roztwór soku 1 |
|
Roztwór soku 1 po dodaniu witaminy C |
|
Roztwór soku 2 |
|
Roztwór soku 2 po dodaniu witaminy C |
|
Opracowanie wyników:
Obliczyć stężenie witaminy C w badanym soku. Do obliczeń należy zastosować metodę dodatku wzorca. Korzystamy z zależności:
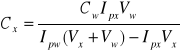
gdzie: Cx - stężenie witaminy C w badanym roztworze soku, Cw - stężenie witaminy C w roztworze wzorcowym, Ipx - natężenie prądu wyznaczone z woltamogramu próbki, Ipw - natężenie prądu wyznaczone z woltamogramu próbki z wzorcem, Vx - objętość próbki, Vw - objętość dodanego roztworu wzorcowego.
Uwaga! Jako wynik końcowy należy podać stężenie witaminy C w badanym soku.
Literatura:
Wyszukiwarka