![]()
27.04.2005
I zasada termodynamiki
Układ izolowany nie zmienia energii wewnętrznej.
Energia wewnętrzna układu zamkniętego może zmieniać się (ΔU=WO + WN + Q)
Gdy układ jest otwarty, jego energia wewnętrzna zmienia się również na sposób masy (ΔU=WO + WN + Q + EM)
Dla procesów izobarycznych (p=const), najwygodniejszą funkcją jest entalpia.
1. II zasada termodynamiki opisuje kierunki procesów.
Procesy nieodwracalne są najpospolitsze, nie ma rzeczywistych, idealnie odwracalnych procesów, ale można w przybliżeniu nazwać tak procesy zachodzące bardzo powoli (quasi statyczne)
Procesy odwracalne to takie procesy, po zajściu których układ i otoczenie mogą powrócić do stanu pierwotnego.
Proces quasi statyczny to proces, w którym nieskończenie mała zmiana wartości parametrów wystarcza do odwrócenia jego kierunku.
Realne procesy przebiegające bardzo powoli można nazywać procesami quasi statycznymi.
Rozprężanie gazu doskonałego może być procesem odwracalnym (gdy rozprężamy wolno) lub nieodwracalnym (gdy rozprężamy gwałtownie). Stopniowe obniżanie ciśnienia: T=const, V1 V2, p1 p2
2. II zasada termodyanmiki
a) w układach izolowanych,
dla procesów odwracalnych
entropia nie zmienia się (S=const; ΔS=0)
ΔFT,V = 0 (warunki izotermiczne, izohoryczne)
ΔGT,P = 0 (warunki izotermiczne, izobaryczne)
dla procesów nieodwracalnych
entropia rośnie (ΔS > 0)
ΔFT,V < 0 (warunki izotermiczne, izohoryczne)
ΔGT,P < 0 (warunki izotermiczne, izobaryczne)
b) w układach nieizolowanych całkowita zmiana entropii jest sumą zmiany entropii wewnętrznej i zewnętrznej (ΔSC = ΔSE + ΔSI). Zmiana entropii wewnętrznej (internal) jest zawsze dodatnia (ΔSI > 0), zmiana entropii zewnętrznej (external) może być większa lub mniejsza od zera (ΔSE > lub < 0)
dla procesów odwracalnych ΔSC = 0
dla procesów nieodwracalnych ΔSC > 0; im większa nieodwracalność, tym ΔSI większe.
3. Statystyczna interpretacja entropii (wg termodynamiki statystycznej, posługującej się zbiorami):
Entropia jest miarą nieporządku.
Prawdopodobieństwo termodynamiczne (W) to ilość mikrostanów realizujących dany stan termodynamiczny układu (stan makroskopowy). Im większe prawdopodobieństwo termodynamiczne, tym mniejsze jego uporządkowanie (1 < W < 0)
Dygresja wytłumaczenie prawdopodobieństwa termodynamicznego na przykładzie kostki Rubika; kostka ułożona (wszystkie pola na swoim miejscu) jest tylko jeden taki stan; kostka rozwalona bardzo dużo mikrostanów.
Jeśli występuje mała ilość mikrostanów, układ jest bardziej uporządkowany, entropia jest mniejsza.
Entropia w ujęciu termodynamiki statystycznej jest miarą nieuporządkowania, gdyż
S = klnW (k - stała Boltzmana), zatem:
![]()
Stan natywny - stan zdegenerowany - entropia rośnie.
4. Samorzutność procesu (spontaniczność)
Reakcje zachodzące w przyrodzie można podzielić na:
samorzutne (spontanicze)
niesamorzutne (wymuszone)
Samorzutności procesu nie należy mylić z realnością procesu; procesy obydwu typów zachodzą realnie w przyrodzie i podlegają ściśle regułom termodynamiki.
Dygresja Wyobraźmy sobie wahadło, wprawienie go w ruch, poprzez podniesienie go jest procesem niesamorzutnym, natomiast ruch wahadła w dół jest już procesem samorzutnym.
Procesy samorzutne.
W procesach samorzutnych - układ jest źródłem energii; proces biegnie kosztem energii wewnętrznej układu.
Procesy samorzutne przebiegają wtedy, gdy występują bodźce termodynamiczne (gradienty parametrów) i ustają po osiągnięciu przez układ i otoczenie stanu równowagi termodynamicznej (brak bodźców).
Przykładowo nieodwracalne rozprężenie gazu lub przechodzenie ciepła pomiędzy ciałami o różnych temperaturach.
Procesy niesamorzutne.
Przebiegają w wyniku dostarczenia energii do rozpatrywanego układu z otoczenia, dzięki sprzężeniu z procesami dostarczającymi energii (egzotermicznymi).
Są to wszystkie procesy porządkujące (obniżające entropię).
Przykładowo synteza biopolimerów, transport aktywny, skurcz mięśni (pompy jonowe)
Kryteria samorzutności procesu
Energetyczne udziały entalpowe i entropowe w procesach; ΔG ruchy uporządkowane,
TΔS ruchy nieuporządkowane
![]()
ENTALPIA |
ENTROPIA |
SAMORZUTNOŚĆ |
ΔH < 0 (egzo) |
ΔS > 0 |
Tak, ΔG < 0 |
ΔH < 0 (egzo) |
ΔS < 0 |
Tak, gdy |TΔS| < |ΔH| |
ΔH > 0 (endo) |
ΔS > 0 |
Tak, gdy TΔS > ΔH |
ΔH > 0 (endo) |
ΔS < 0 |
Nie, ΔG > 0 |
Stan równowagi układu
W stanie równowagi wartości parametrów w każdym punkcie tego układu (punkt rozważamy makroskopowo) są takie same i nie zmieniają się w czasie.
Nie ma gradientów i związanych z tym przepływów (strumieni)
W przebiegu procesu samorzutnego rośnie entropia; gdy proces ustaje w wyniku wyrównania się wartości parametrów, układ zbliża się do stanu równowagi, a entropia osiąga maksimum i przestaje się zmieniać.
W równowadze Smax(t) = const, ΔS = 0, produkcja entropii (ΔS/Δt = 0)
Stan stacjonarny.
Charakteryzuje się niezmiennością parametrów termodynamicznych (T, p, ni) w czasie (tak jak w stanie równowagi), ale w wyniku zerowania się strumieni:
![]()
; Ii - strumienie zdefiniowane wektorowo
Suma wpływów masy lub energii do układu jest kompensowana sumą wypływów.
W stanach stacjonarnych biegną procesy nieodwracalna, produkujące entropię (ΔSC ≠ 0 ), ale w miarę, jak dochodzimy do stanu stacjonarnego ΔSC maleje i osiąga minimum.
ΔSU(t) = 0 (z powodu kompensacji strumieni)
ΔSC(t) ≠ 0, ΔSC/Δt = min = const
Stan stacjonarny może powstawać tylko w układach otwartych (np. żywa komórka)
5. Transport masy w układach wieloskładnikowych
W układach wieloskładnikowych możemy mieć do czynienia ze strumieniami jednych składników względem nieruchomej fazy innych.
Transport masy to zjawisko występowania strumieni cząsteczek > 0.
Pojęcie strumienia ilościowo można opisać wzorem:
![]()
[mol/m2s]
Im większy strumień, tym substancja dyfunduje szybciej.
Klasyfikacja transportu substancji
transport bierny - samorzutny, na koszt energii swobodnej układu, prowadzący do stanu równowagi
dyfuzja
osmoza
dyfuzja ułatwiona
elektrodyfuzja
transport aktywny - niesamorzutny, na koszt energii uwalnianej w procesach sprzężonych z transportem; oddalający układ od stanu równowagi, realizowany przez wyspecjalizowane białka w błonie (enzymy o aktywności ATP-azowej).
Transport masy - potencjał chemiczny, z punktu widzenia termodynamiki zmiana ilości jakiegokolwiek składnika musi wywołać zmianę funkcji termodynamicznych tego układu (zmiana stanu układu).
Wielkość określająca zmianę entalpii swobodnej (ΔG) dla p = const lub zmianę energii swobodnej (ΔF) dla V = const nazywamy potencjałem chemicznym dla cząsteczek elektrycznie obojętnych lub potencjałem elektrochemicznym dla jonów.
![]()
dla p = const ![]()
dla V = const
Wielkośc ta jest funkcją parametrów T, p, Ci, Cj≠i, a dla jonów także funkcją potencjału elektrycznego φ. Potencjały chemiczne i elektrochemiczne są funkcjami parametrów układu.
![]()
dla nielelektrolitów
![]()
dla jonów
Jeśli w różnych częściach układu mamy różne μ, to samorzutnym procesem będzie proces podwyższający entropię lub obniżający G (dla procesów izobarycznych) bądź też F (dla procesów izohorycznych). Procesami takimi są strumienie dążące do wyrównania potencjałów chemicznych lub potencjałów elekektrochemicznych (dla jonów).
6. Postulaty termodynamiczne:
Strumień masy będzie tym większy (szybszy transport), im większe będzie zróżnicowanie wartości μ w różnych punktach układu (większy gradient μ).
Gradient potencjału chemicznego lub elektrochemicznego nazywamy bodźcem termodynamicznym (lub siłą termodynamiczną) - X.
Gradienty takich parametrów jak temperatura, ciśnienie, stężenie, potencjał elektryczny, wywołują gradienty μ, czyli bodźce termodynamiczne.
Postulat termodynamiki liniowej:
Zależność pomiędzy bodźcem, a strumieniem jest wprostproporcjonalna
![]()
(równanie fenomenologiczne)
Liniowość tylko dla niektórych odchyleń od równowagi.
Transport prosty i sprzężenia między strumieniami:
Strumień masy (Im) zależy od bodźców XT i Xm
![]()
L - współczynniki fenomenologiczne
![]()
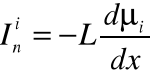
7. Dyfuzja
![]()
strumień* gradient*
*strumień i gradient są wektorami
![]()
(dla roztworów idealnych)
Dyfuzja to przypadek transportu substancji, gdy gradient potencjału chemicznego realizowany jest przez gradient stężenia (jednakowa temperatura i ciśnienie w całym układzie).
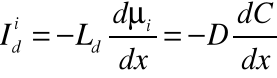
prawo Ficka
D - to funkcja temperatury, ciśnienia i rodzaju substancji
Uproszczenia idealność roztworu, jednokierunkowość dyfuzji.
1
chemia fizyczna wykład z 27.04.2005
![]()
![]()
![]()