Paweł Jagiełło
wydział chemiczny
kierunek chemia
semestr IV
Laboratorium z chemii fizycznej
Ćwiczenie Nr 29
Temat:
„Badanie kinetyki przegrupowania wewnątrzcząsteczkowego metodą fotolizy błyskowej”
Data wykonania ćwiczenia:
|
Ocena: |
Podpis: |
Data oddania sprawozdania:
|
Ocena: |
Podpis: |
I. Wstęp :
Fotoliza błyskowa jest jedną z metod, które pozwalają badać kinetykę
i mechanizm szybkich reakcji chemicznych. Metoda ta polega na dostarczeniu do układu reakcyjnego energii promienistej w postaci krótkotrwałego błysku światła widzialnego lub ultrafioletowego. Impuls świetlny trwa w zależności od konstrukcji lampy i energii emitowanej, od 10-9s do 10-2s. W rezultacie pochłonięcia przez badany układ pewnej liczby kwantów światła zachodzić
w nim mogą różnorodne procesy fizyczne i chemiczne, takie jak: wzbudzenie, jonizacja, dysocjacja cząsteczek, przegrupowanie wewnątrzcząsteczkowe itp.
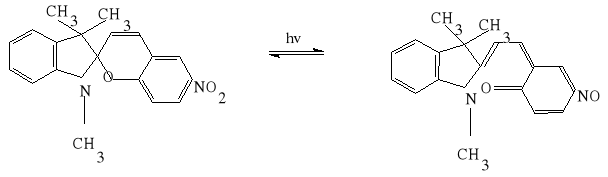
W ćwiczeniu wykorzystano własności roztworu 1,3,3-trzymetyloindolino-6-nitrobenzospiranu (TMINBS). Związek ten występuje w roztworze w postaci bezbarwnej, trwałej formy A (tzw. leukoformy), która pod wpływem światła przechodzi w niebieską formę B.

Odmiana A - trwała Odmiana B - nietrwała
leukoforma (bezbarwna) forma niebieska
Forma B jest nietrwała i ulega przemianie w odmianę A, przy czym proces ten jest I rzędu:
niebieska bezbarwna
Ponieważ jednocześnie zachodzi zmiana barwy, postęp reakcji można śledzić mierzą absorbancję roztworu. Zgodnie ze wzorem Lamberta - Beera:
![]()
A - absorbancja molowa
l - grubość warstwy absorbującej kuwety
c - stężenie substancji barwnej
Stałą szybkości reakcji nazywamy współczynnik proporcjonalności k w jej równaniu kinetycznym. W klasycznej kinetyce przyjmuje się, że stała k jest niezależna od stężenia reagentów i czasu reakcji, natomiast zmienia się z temperaturą i zależy od rodzaju i stężenia katalizatorów. Stała szybkości wyraża liczbowo szybkość reakcji, gdy stężenie każdego z substratów wynosi 1 mol/dm3. Wymiar stałej zależy od postaci równania kinetycznego i wyraża się ogólnym wzorem:
II. Obliczenia
• Szacuję wartość stałej szybkości reakcji I rzędu
k=ln2/t(1/2)= ln2/t'(1/2)= ln2/t''(1/2)
• Przybliżone wartości k wynoszą ( rozbieżności będą wynikać z niedokładności pomiaru)
k(1/2)=ln2/13s=0,0533 s-1
k(1/2')=ln2/18s=0,0385 s-1
k(1/2'')=ln2/23s=0,0301 s-1
Co daje średnią k=0,0406 s-1
• Dokładniejszy wynik daje sporządzenie wykresu ln S od czasu i obliczenie współczynnika kierunkowego ( b) krzywej.
![]()
równanie kinetyczne :
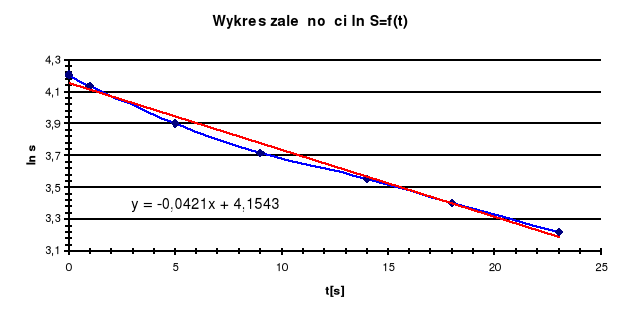
Odczytany z wykresu współczynnik kierunkowy ma wartość -0,0421 mol. Oznacza to, że wartość stałej szybkości reakcji wynosi 0,0421s-1.
III. Wnioski
Rozbieżność wartości kolejnych czasów połowicznych świadczy o niedokładności wykonanego pomiaru . Wszelkie błędy jakie zostały popełnione zostały zapewne spowodowane docieraniem do detektora światła zewnętrznego (o różnym chwilowym natężeniu) i światłem rozproszonym przez aparaturę.
W obliczeniach i przy sporządzaniu wykresu pominęłam końcową fazę doświadczenia ze względu na malejącą różnicę wychyleń pisaka (absorbancji) od czasu.
![]()