ANNA BRACIKOWSKA
EWA CYRANKIEWICZ
OCHRONA ŚRODOWISKA
GRUPA A
ZESPÓŁ IV
ĆWICZENIE NR 11
TEMAT: KOLORTMETRYCZNE OZNACZANIE BARWNYCH ZWIĄZKÓW OBOK SIEBIE.
Część teoretyczna
Natężenie wiązki światła padającego na środek materialny ulega zmniejszeniu na skutek absorbcji światła przez ten ośrodek, rozpraszania i odbicia na granicy dwóch ośrodków.
Pomiędzy tymi wielkościami istnieje zależność:
Io = Iod + Iroz + Iabs + I
gdzie:
Io - natężenie światła padającego,
Iod - natężenie światła odbitego,
Iroz - natężenie światła rozproszonego,
Iabs - natężenie światła absorbowanego,
I - natężenie światła przechodzącego.
Pomiary natężenia światła należy prowadzić w takich warunkach, aby obniżyć do minimum wielkość Iod i Iroz , wówczas w celu uproszczenia obliczeń wielkości te można pominąć. Powyższy wzór przyjmuje postać: Io = Iabs + I
Iabs = Io - I
Niech przez dany ośrodek optycznie jednorodny (np. roztwór), przechodzi równoległa wiązka światła monochromatycznego. W miarę przenikania światła w głąb ośrodka, natężenie jego maleje wskutek pochłaniania (absorpcji) promieniowania. Jeżeli przez l oznaczymy grubość warstwy próbki badanej, to natężenie światła I, po przejściu przez tą warstwę, jest pewną funkcją jej grubości I = f(l).
Dla cienkiej warstwy próbki o grubości dl zmniejszenie natężenia promieniowania dI równe jest: dI = -![]()
Icdl.
gdzie:
![]()
- wielkość charakterystyczna dla danej substancji,
c - stężenie roztworu.
Po scałkowaniu powyższego równania otrzymujemy:
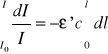
![]()
![]()
/1/
W praktyce znacznie łatwiej jest operować logarytmami, stąd poniższe przekształcenia:
![]()
/2/
Łącząc wzory /1/ i /2/ otrzymujemy podstawowe prawo kolorymetrii, które jest połączonym prawem Lamberta-Beera.
![]()
gdzie:
![]()
- jest tzw. molowym współczynnikiem absorpcji,
A - absorpcja.
Prawo Lamberta jest prawem dokładnym; ewentualne niezgodności z doświadczeniem mogą występować wówczas gdy nie spełnione są założenia przyjęte przy jego wyprowadzeniu, a mianowicie jeśli ośrodek jest niejednorodny lub też występują straty światła na skutek odbicia od powierzchni granicznych ośrodków.
Prawo Beera jest natomiast prawem granicznym, tzn spełnionym dokładnie tylko w zakresie niskich stężeń roztworów. W zakresie wyższych stężeń (gdzie zmiana stężenia powoduje zmianę absorpcji), występują odchylenia od prawa.
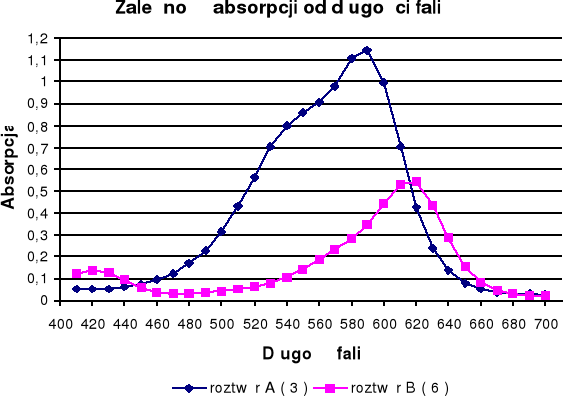
Dość istotne znaczenie ma zależność absorpcji od długości fali światła /![]()
/. Wykres tej zależności określa się mianem krzywej absorpcji lub elektronowym widmem absorpcyjnym.
Absorpcja roztworu jest wielkością addytywną, czyli równa się sumie absorpcji wszystkich składników w nim zawartych.
![]()
lub ![]()
gdzie:
A - absorpcja roztworu,
![]()
- absorpcja składnika,
![]()
- współczynniki absorpcji poszczególnych rodzajów cząsteczek lub jonów absorbujących,
![]()
- stężenia roztworów,
l - grubość warstwy roztworu.
Czynniki powodujące odchylenia od praw absorpcji:
czynniki chemiczne są związane z reakcjami chemicznymi zachodzącymi w analizowanym roztworze. Przy zmianie pH roztworu i zmianie jego stężenia mogą zachodzić takie reakcje jak: dysocjacja, asocjacja, różne reakcje kompleksowania: polimeryzacja; powodują one zmiany właściwości optycznych analizowanych substancji.
Czynniki aparaturowe powodujące odchylenia są najczęściej związane z brakiem monochromatyczności promieniowania oraz występowaniem promieniowania rozproszonego. Brak monochromatyczności promieniowania stanowi główną przyczynę odchyleń odpraw absorpcji.
Niedostateczna monochromatyczność występuje w przypadku pomiarów przy użyciu kolorymetrów i fotokolorymetrów, w których czynnikami monochromatyzującymi są filtry barwne i interferencyjne.
Aparatura
Najbardziej rozpowszechnionym jest spektrokolorymetr SPEKOL. Jest to absorpcjometr jednowiązkowy, wychyleniowy, o niewielkich rozmiarach i prostej obsłudze. Umożliwia on pomiary absorbancji w zakresie 365 - 750 nm. Zasadniczy przyrząd jest zaopatrzony w różne przystawki, pozwalające przeprowadzić miareczkowanie spektrofotometryczne, turbidymetryczne, fluorescencyjne oraz pomiary stopnia zmętnienia i natężenia fluorescencji. Światło emitowane jest przez źródło którym jest lampa wolframowa na zakres 420 - 750 nm, lub lampa rtęciowa na zakres 365 - 750 nm
Światło, emitowane przez żródło , którym jest żarówka wolframowa, przechodzi przez kondensor i po odbiciu od zwierciadła wchodzi przez szczelinę wejściową do kolimatora. Po przejściu przez układ achromatyczny pada na monochromator, którym jest siatka dyfrakcyjna. Za pomocą odpowiedniego układu dżwigni, poruszanych bębnem można obracać siatkę dyfrakcyjną i dzięki temu przepuszczać przez szczelinę wyjściową monochromatora wiązkę o żądanej długości fali. Wybrana długość widma, po przejściu przez soczewkę achromatyczną, trafia na szczelinę wyjściową i po przejściu przez kiuwetę z roztworem badanym i filtr barwny do pochłaniania promieniowania cieplnego pada na detektor. W standardowym przyrządzie detektorem jest fotoogniwo selenowe. Powstały w fotoogniwie fotoprąd ulega wzmocnieniu we wzmacniaczu tranzystorowym i dostaje się do urządzenia pomiarowego.
Wyniki
![]()
⇒ ![]()
gdzie: l = 1
![]()
![]()
Po przekształceniu ![]()
![]()
Zestawienie wyników
|
c |
A1 |
A2 |
a1 |
a2 |
cA |
cB |
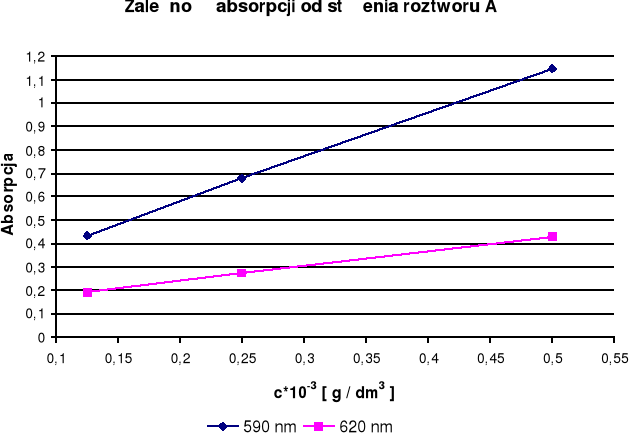
Związek A |
|
|
|
|
|
|
|
Kolba 1 |
0,000125 |
0,432 |
0,193 |
3456 |
1544 |
|
|
Kolba 2 |
0,00025 |
0,678 |
0,276 |
2712 |
1104 |
|
|
Kolba 3 |
0,0005 |
1,145 |
0,427 |
2290 |
854 |
|
|
aśrA |
|
|
|
2819,33 |
1167,33 |
|
|
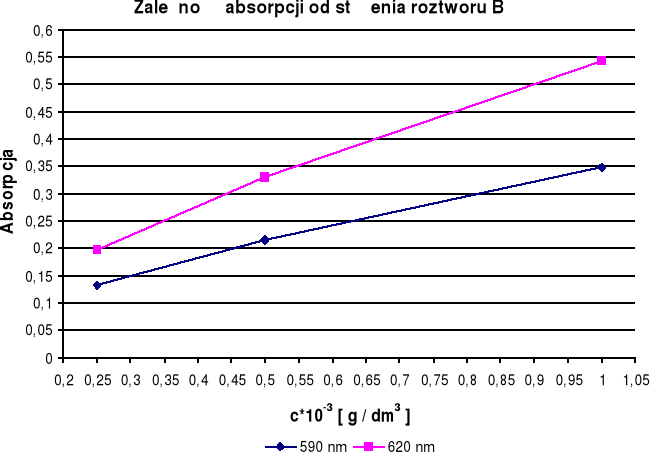
Związek B |
|
|
|
|
|
|
|
Kolba 4 |
0,00025 |
0,132 |
0,198 |
528 |
792 |
|
|
Kolba 5 |
0,0005 |
0,215 |
0,333 |
430 |
660 |
|
|
Kolba 6 |
0,001 |
0,348 |
0,544 |
348 |
544 |
|
|
aśrB |
|
|
|
435,33 |
667,33 |
|
|
R. badany |
|
0,288 |
0,332 |
|
|
3,47⋅10-5 |
4,37⋅10-4 |
cA = 3,47⋅10-5 g / dm3
cB = 4,37⋅10-4 g / dm3
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Wyszukiwarka