ĆWICZENIE 9-1
Oznaczanie grubości osadzonej powłoki miedzianej i wydajności prądowej elektrolizy
CEL ĆWICZENIA:
Celem ćwiczenia było wykonanie powłoki miedzianej na płytce metalowej wykonanej z innego metalu a następnie wyznaczenie jej grubości:
Miejscowej - metodą kroplową
Średniej - na podstawie przyrostu masy płytki
Naszym celem było również obliczenie wydajności prądowej elektrolizy.
WSTĘP TEORETYCZNY
Elektroliza jest to proces rozkładu elektrolitu, mający miejsce podczas przepływu prądu elektrycznego przez zdysocujowany elektrolit. Elektrolit ten może być zdysocjowany rozpuszczeniem w rozpuszczalniku, lub roztopieniem pod wpływem temperatury (wtedy mamy do czynienia z termoelektrolizą). Proces elektrolizy polega na wędrówce jonów do elektrod: do dodatniej elektrody (anody) ujemnych jonów (anionów), a do ujemnej elektrody (katody) jonów dodatnich (kationów), czego efektem są dwie reakcje chemiczne odbywające się równolegle i bilansujące się: w otoczeniu anody jest to reakcja utleniania, a w otoczeniu katody reakcja redukcji. W naszym doświadczeniu anodę stanowiły dwie blaszki miedziane, na których zachodzi proces utleniania miedzi do jonów miedzi Cu2+. Natomiast katodę stanowiła blaszka wykonana z mosiądzu, który chcieliśmy pokryć miedzią.
WYKONANIE ĆWICZENIA:
Układ doświadczalny składał się z: zasilacza prądu stałego, wagi analitycznej, 2 płytek miedzianych, płytki mosiężnej, stopera, elektrolizera wypełnionego wodnym roztworem CuSO4.
Przygotowanie płytki - płytka mosiężna została dokładnie oczyszczona za pomocą papieru ściernego ściernego, następnie wypłukana kolejno w ciepłej wodzie, zimnej wodzie, acetonie oraz została osuszona na powietrzu. Została także zważona na wadze analitycznej (m1)
Anody i katoda zostały zanurzone w elektrolizerze wypełnionym elektrolitem. Anody oraz katoda podłączone zostały kabelkami do zasilacza prądu stałego.
Elektroliza - po włączeniu zasilacza oraz stopera rozpoczęliśmy miedziowanie. Proces ten trwał 20minut prądem o natężeniu 0,5A, w temperaturze otoczenia
Po zakończeniu elektrolizy wyłączono zasilacz, płytkę mosiężną wyjęto wypłukano w wodzie destylowanej oraz acetonie i ponownie zważono na wadze analitycznej (m2).
Określono także wymiary powłoki galwanicznej za pomocą linijki oraz wyznaczono pole dowierzchni tej powłoki ze wzoru na pole prostokąta.
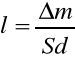
Średnia grubość powłoki galwanicznej - średnią grubość powłoki galwanicznej obliczyliśmy stosując wzór:
Gdzie, l - jest średnią grubością osadzonej powłoki miedzianej [cm]
S - jest całkowitą powierzchnią powłoki galwanicznej [cm2]
∆m - przyrost masy płytki powstały w wyniku elektrolizy [g] ∆m=m2-m1
d - gęstość powłoki miedzianej [g∙cm-3] (dcu = 8,92g∙cm-3)
Miejscowa grubość powłoki miedzianej
Stosując 0,2588 molowy roztwór AgNO3 rozpuszczaliśmy powłokę miedzianą powstałą podczas elektrolizy w dwóch miejscach ( na środku oraz na krawędzi płytki). Na czystą płytkę pokrytą miedzią nanosiliśmy po 1 kropli roztworu na każde z wyznaczonych miejsc, po czym za pomocą stopera odmierzaliśmy każdorazowo 60 sek. I zaraz potem wycieraliśmy miejsca delikatnie za pomocą papieru tak, aby nie ścierać powłoki miedzianej mechanicznie, lecz aby usunąć powstający osad. Czynności te prowadziliśmy do momentu pojawienia się warstwy mosiężnej. Miejscowa grubość powłoki została obliczona ze wzoru:
![]()
Gdzie, l - jest grubością powłoki w danym miejscu (na środku płytki lub krawędzi) [μm]
n - jest ilością kropel roztworu zużytego do rozpuszczenia powłoki
k - jest stałą podajacą grubość powłoki rozpuszczanej przez 1 kroplę roztworu w danym czasie (60s) w danej temperaturze.
Obliczyliśmy wydajność prądową elektrolizy stosując następujący wzór:
![]()
Gdzie, md=∆m - przyrost masy płytki [g]
mt - masa miedzi osadzona na płytce w wyniku elektrolizy (zgodnie z prawem Faradaya: masa substancji przekształconej na elektrodzie podczas elektrolizy jest proporcjonalna do natężenia prądu i czasu trwania elektrolizy)
I - natężenie prądu [A]
![]()
t - czas elektrolizy [s]
k - równoważnik elektrochemiczny miedzi [g∙C-1] obliczony ze wzoru:
(z-liczba moli wymienianych elektronów; F - stała Faradaya, M - masa molowa miedzi)
OPRACOWANIE WYNIKÓW
SPOSTRZEŻENIA i WNIOSKI
Cel doświadczenia został w pełni zrealizowany. Poprzez zastosowanie elektrolizy udało nam się pokryć blaszkę mosiężną warstwą miedzi oraz zmierzyć grubość tej powłoki (zarówno średniej dla całej płytki jak i w określonych punktach). Wynoszą one kolejno:
Wyniki świadczą, że grubości powłoki w różnych miejscach płytki nie są jednakowe. Co więcej średnia grubość powłoki miedzianej w dużym stopniu odbiega od grubości punktowej. Wobec tego możemy wysnuć wniosek, że w pewnych miejscach płytka ma znaczne braki a grubość powłoki osadzonej miedzi jest nierównomierna. Należy także mieć świadomość, że błąd pomiaru grubości powłoki metodą kroplową jest dosyć wysoki i wynosi 15%.
Zastosowana przez nas metoda pokrywania przedmiotu warstą porządanego metalu nosi miano galwanostegii. W metodzie tej przedmiot pokrywany włączamy właśnie w obwód prądu jako katodę a metal, który ma się osadzić (posiada cechy bardziej porządane) pełni rolę anody. Powłoką poza miedzią może być również: nikiel, srebro, chrom, lub złoto. Chronią one w ten sposób materiał konstrukcyjny przed korozją. Ochrona ta jest tym lepsza im grubsza jest dana powłoka. Dzięki zastosowaniu wzoru m=k I t, oraz uwzględnieniu wymiarów przedmiotu który ma być pokryty jesteśmy w stanie dobrać odpowiednie warunki procesu ( czas, natężenie prądu) aby uzyskać powłokę o porządanej grubości.
![]()
![]()
![]()
![]()
Wyszukiwarka