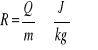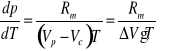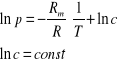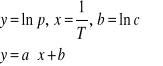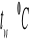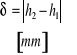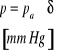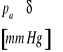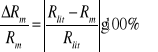Ćwiczenie nr 26
Badanie zależności temperatury wrzenia wody od ciśnienia. Wyznaczanie molowego ciepła parowania wody
Cel ćwiczenia
Celem ćwiczenia jest wyznaczenie zależności temperatury wrzenia wody od ciśnienia oraz obliczenie molowego ciepła parowania wody Rm.
Wprowadzenie
Parowaniem nazywamy proces zamiany cieczy w parę. Proces ten zachodzi w każdej temperaturze, ale tylko na powierzchni cieczy. Cząsteczka może oderwać się od powierzchni cieczy, gdy energia kinetyczna cząsteczki jest większa od energii potencjalnej przyciągania międzycząsteczkowego. W trakcie parowania temperatura cieczy obniża się. Jeżeli do cieczy nie dostarczymy ciepła to energia kinetyczna cząsteczek cieczy maleje i obniża się temperatura cieczy. Ilość energii odbieranej od cieczy w procesie parowania nazywamy ciepłem parowania R.
Ciepło parowania R definiujemy jako ilość ciepła Q jaką należy dostarczyć do cieczy, aby nastąpiło przejście 1 kg cieczy z fazy ciekłej do gazowej bez zmiany temperatury tej cieczy:
|
(26.1) |
Jednostką ciepła parowania jest J/kg, a ciepło parowania wyznaczamy standardowo w temperaturze wrzenia. Jeżeli ciepło odniesiemy nie do jednostki masy ,a 1 mola substancji to nazywamy je molowym ciepłem parowania Rm:
|
(26.2) |
Istotne czynniki mające wpływ na prędkość parowania to: ciśnienie pary nad powierzchnią cieczy, temperatura cieczy, powierzchnia czynna parującej cieczy, ruch powietrza nad cieczą, ruch samej cieczy.
Rozważmy zamknięte naczynie wypełnione częściowo cieczą. Ciecz paruje do części naczynia nad poziomem cieczy. Jej poziom w naczyniu opada. Po pewnym czasie ustala się stan równowagi termodynamicznej. Ilość cząsteczek opuszczających powierzchnię cieczy jest równa ilości cząsteczek wchodzących do niej. Parę , która znajduje się w równowadze z cieczą z której, powstała nazywamy parą nasyconą W danej temperaturze ma ona największą gęstość i wywiera największe ciśnienie na ścianki naczynia. Ciśnienie pary nasyconej zależy tylko od temperatury, a nie zależy od objętości naczynia. Wzrost temperatury cieczy powoduje intensywniejsze parowanie. Po osiągnięciu pewnej charakterystycznej wartości temperatury i ciśnienia rozpoczyna się proces parowania w całej objętości cieczy. Proces burzliwego parowania nazywamy wrzeniem , a temperaturę w której to zachodzi nazywamy temperaturą wrzenia. Podczas zjawiska wrzenia cząsteczki tworzą pęcherzyki pary wewnątrz cieczy. Jest to para nasycona a jej ciśnienie pn wewnątrz pęcherzyka zależy ciśnienia atmosferycznego pa , ciśnienia hydrostatycznego ph oraz ciśnienia związanego z napięciem powierzchniowym pσ .
|
(26.3) |
Wrzenie następuje wówczas, gdy w określonej temperaturze ciśnienie pary nasyconej może przekroczyć choćby minimalnie, ciśnienie zewnętrzne. Pęcherzyk rozrasta się i pod wpływem siły wyporu wypychany jest na powierzchnię cieczy. Ponieważ ciśnienie pary nasyconej zależy tylko od temperatury, zmiana ciśnienia zewnętrznego powoduje zmianę temperatury wrzenia.
Proces wrzenia zachodzi cały czas w stałej temperaturze, jest więc tzw. przejściem fazowym pierwszego rodzaju. Dopóki cała ciecz nie zamieni się w parę temperatura tej cieczy nie ulega zmianie.
Temperatura wrzenia cieczy zależy od panującego na zewnątrz cieczy ciśnienia można wyznaczyć z równania Clausiusa-Clapeyrona:
|
(26.4) |
gdzie: Rm jest molowym ciepłem parowania [J/mol], ΔV oznacza różnicę molowych objętości pary Vp i cieczy Vc w temperaturze bezwzględnej T -[m3].Jeżeli założymy, że Vc << Vp, wartość ciepła molowego Rm jest stała dla różnicy temperatur kilkudziesięciu stopni oraz, że właściwości pary wodnej można opisać równaniem gazu doskonałego, to jednego mola pary wodnej, z równania Clapeyrona dla gazów doskonałych, otrzymujemy:
|
(26.5) |
gdzie R = 8,314 J/mol*K jest uniwersalną stałą gazową
Podstawiając Vp z równania stanu gazu doskonałego do równania Clausiusa-Clapeyrona, po rozdzieleniu zmiennych otrzymujemy równanie:
|
(26.6) |
Całkując obustronnie, otrzymujemy zależność ciśnienia p od temperatury T:
|
(26.7) |
|
(26.8) |
Dokonując podstawienia zmiennych:
|
(26.9) |
|
(26.10) |
Otrzymujemy funkcję liniową:
|
(26.11) |
Analizując tę zależność liniową możemy, na podstawie wyznaczonego współczynnika kierunkowego prostej ,wyznaczyć molowe ciepło parowania wody Rm..
Opis stanowiska laboratoryjnego
Zestaw pomiarowy służący do wyznaczania zależności temperatury wrzenia od ciśnienia pokazano na rysunku 26.1. Składa się on z okrągłej kolby z termometrem T, chłodnicy B, U- rurki stanowiącej manometr różnicowy M oraz pompki wodnej. Na rurce prowadzącej do pompki wodnej znajduje się zawór K, którym można odciąć dostęp do pompki wodnej. W kolbie z wodą znajduje się porowaty materiał, aby zapobiec gwałtownemu wrzeniu cieczy. Do pomiaru ciśnienia atmosferycznego korzystamy z barometru znajdującego się w pracowni. Różnicę wysokości poziomów rtęci w U-rurce wyznaczamy przy pomocy linijki. Naczynie z wodą możemy ogrzewać za pomocą palnika gazowego lub grzałki elektrycznej. Powstająca para wodna skrapla się w chłodnicy i wraca do kolby. Pomiary można wykonać zarówno dla podciśnienia jak i nadciśnienia panującego w kolbie pomiarowej.
Uwaga : graniczne zakresy ciśnień to 560-960 mm Hg.
Rys. 26.1. Zestaw pomiarowy
Program ćwiczenia
Uwaga: podczas przeprowadzania ćwiczenia należy zachować szczególną ostrożność. Nie należy gwałtownie zmieniać strumienia wody przepływającego przez pompkę wodną. Nieostrożne manipulacje mogą spowodować zassanie rtęci do aparatury albo jej wylanie z manometru. Podczas wykonywania ćwiczenia należy sprawdzić czy termometr jest prawidłowo wycechowany. Temperatura wrzenia wody wynosi 100 0C tylko przy ciśnieniu normalnym tzn. po = 1,013·105 Pa. Jeżeli ciśnienie odbiega od tej wartości należy sprawdzić w tablicach jaka powinna być wartość temperatury wrzenia dla danego ciśnienia.
Ustawić ramiona U-rurki tak , aby rtęć w obu ramionach znajdowała się na tym samym poziomie. Różnica ciśnień w obu ramionach ,wyrażona w mm Hg ,równa się 0. Wówczas ciśnienie w kolbie pomiarowej jest równe ciśnieniu atmosferycznemu pa. Na barometrze znajdującym się w pracowni zmierzyć i zanotować wartość ciśnienia atmosferycznego pa. Ustalić i zapisać niepewność pomiaru Δpa .
Uruchomić obieg wody przepływającą przez chłodnicę.
Zawór K ustawić w pozycji umożliwiającej połączenie z pompką wodną.
Regulując strumieniem wody przepływającym przez pompkę wodną obniżyć ciśnienie w aparaturze o około 200 mm Hg poniżej ciśnienia atmosferycznego. Wartość podciśnienia wskazuje nam różnica wysokości słupków rtęci w U-rurce h2-h1. Ustalić niepewność odczytu Δh.
Podgrzewać wodę w zbiorniku aż zacznie wrzeć.
Odczytać i zanotować temperaturę wrzenia przy największym podciśnieniu. Ustalić i zanotować niepewność pomiaru temperatury Δt.
Zwiększać ciśnienie, co około 20 mm Hg poprzez zmniejszanie strumienia wody przepływającej przez pompkę wodną.
Odczytywać i zapisywać kolejne temperatury wrzenia oraz wartości podciśnienia pa- (h2-h1).Czynności te wykonać dla przynajmniej 6 wartości ciśnienia.
W celu przeprowadzenia pomiarów dla nadciśnienia należy zamknąć zawór K pomiędzy pompką wodną a kolbą i wyłączyć pompkę.
Powoli ogrzewać dalej wodę.
Odczytywać i zapisywać kolejne temperatury wrzenia oraz wartości nadciśnienia pa+(h1-h2). Dokonywać pomiarów co około 20 mm Hg.
Zakończyć pomiary przy ciśnieniu o około 200 mm Hg większego od ciśnienia atmosferycznego.
Wyłączyć ogrzewanie kolby z wodą.
Wyniki pomiarów umieścić w tabeli 26.1.
Tabela 26.1
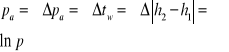
l.p. |
|
|
|
|
|
|
|
|
|
|
|
Sprawozdanie
Wykonać wykres zależności temperatury wrzenia tw od ciśnienia p tw=f(p) . Zaznaczyć niepewności pomiarowe.
W celu wyznaczenia molowego ciepła parowania wody przekształcamy dane z tabeli 26.1. i umieszczamy je w tabeli 26.2.
Tabela 26.2.
![]()
l.p. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Korzystając z programu regresja liniowa , lub korzystając z arkusza kalkulacyjnego Excel sprawdzić liniowość wykresu
Na papierze milimetrowym wykonać wykres zależności logarytmu naturalnego ciśnienia lnp od odwrotności temperatury w skali Kelvina 1/T. Nanieść niepewności pomiarowe.
Narysować prostą przechodzącą przez największa ilość prostokątów niepewności pomiarowych. Wyznaczyć współczynnik nachylenia prostej na tej podstawie obliczyć wartość molowego ciepła parowania Rm i zapisać ją wraz z jednostką.
Znaleźć w literaturze wartość molowego ciepła parowania wody Rliti porównać ją z wartością Rm otrzymaną z doświadczenia:
Pytania kontrolne
Równanie gazu doskonałego.
Kinetyczno-molekularna teoria budowy cieczy. Parowanie i wrzenie.
Przemiany fazowe.
Podstawowe równania hydrodynamiki. Zasada działania pompki wodnej.
Dlaczego temperatura wrzenia zależy od ciśnienia?
Para nienasycona i nasycona.
Wilgotność powietrza.
|
(26.12) |
gdzie T oznacza temperaturę w stopniach Kelvina. Zapisać wyliczone przez program współczynniki regresji a, b równania prostej y=ax+b oraz ich odchylenia standardowe i współczynnik korelacji. Na podstawie otrzymanej wartości współczynnika kierunkowego prostej a obliczyć wartość molowego ciepła parowania Rm i zapisać ją wraz z jednostką.
|
(26.13) |
158
Wyszukiwarka