Ćwiczenie 27: Wyznaczanie stosunku ![]()
dla powietrza.
Kamil Dobrzyń gr. 3
Ćwiczenie 27: Wyznaczanie stosunku ![]()
dla powietrza.
Gaz doskonały to fikcyjny, idealny gaz, którego cząsteczki są nieskończenie małe i nie zachodzi między nimi wzajemne przyciągania, ani nie występują w nich drgania wewnętrzne.
Dla powyższego gazu energia wewnętrzna U jest równa sumie energii kinetycznej ruchu postępowego i obrotowego cząsteczek. Aby obliczyć tą energię trzeba skorzystać z pojęcia stopni swobody, czyli liczby niezależnych współrzędnych określających położenie cząsteczki w przestrzeni. I tak dla cząsteczek jednoatomowych stopień swobody i=3 odpowiadające trzem współrzędnym przestrzennym bądź też trzem składowym prędkości. Cząsteczka dwuatomowa posiada pięć stopni swobody (i=5), ponieważ do trzech stopni swobody ruchu postępowego dochodzą dwa stopnie swobody związane z obrotem cząsteczki jako ryły sztywnej wokół dwóch prostopadłych względem siebie osi. Cząsteczki trój- lub więcej atomowa posiada sześć stopni swobody (i=6) ponieważ dla takich cząsteczek możliwe są 3 osie obrotu.
Wzór ogólny na obliczenie energii kinetycznej cząsteczek:
(1) ![]()
; gdzie:
i- stopień swobody
k- stała Boltzmanna
T- temperatura w Kelwinach
Dla jednego mola gazu jego energia wewnętrzna U jest równa:
(2) U=NE; gdzie:
N- liczba Avogardo
E- energia jednej cząstki
Więc wyprowadzając:
(3) ![]()
, gdyż: ![]()
R- stała gazowa
Ilość energii potrzebna do odniesieni temperatury jednego mola cząsteczek o jeden Kelwin nosi nazwę ciepła molowego danej substancji.
Ciepło molowe danej substancji zależy od warunków, w jakich gaz jest ogrzewany, i tak w przypadku ogrzewania izochorycznego, gdzie nie zmienia się objętość (V) dostarczone ciepło służy do zwiększenia energii wew. gazu. Ponieważ V= const. Praca sił wewnętrznych gazu równa jest zeru. W tym przypadku mamy do czynienia z ciepłem molowym przy stałej objętości Cv.
Gdy ogrzewamy gaz pod stałym ciśnieniem- przemiana izobaryczna- ciepło zostaje zużyte dodatkowo na wykonanie pracy przeciw siłom zewnętrznym- gaz rozszerza się (gdyż p=const.). Mamy wtedy doczynienia z ciepłem molowym przy stałym ciśnieniu Cp.
Cv można określić jako stosunek przyrostu energii wewnętrznej jednego mola gazu do zmiany temperatury wywołanej tym przyrostem.
(4) ![]()
; gdy ![]()
otrzymujemy:
(5) ![]()
Cp jest większe od Cv o pracę W, wykonana przez mol gazu przy rozszerzaniu się podczas wzrostu temperatury o 1 stopień.
(6) Cp=Cv+W
Praca wykonana przy zwiększaniu objętości:
(7) W= p![]()
=p(V2-V1);
Za równaniem Clapeyrona:
(8) pV1=RT; pV2=R(T+1), więc W=R(T+1)-RT=R
Wynika z tego, że stała gazowa R jest liczbowo równa pracy wykonanej przez jeden mol gazu pod stałym ciśnieniem przy podwyższaniu temperatury układu o jeden Kelwin, więc:
(9) Cp= Cv+ R; podstawiając za Cv:
(10)![]()
![]()
jest stosunkiem ciepła molowego Cp do ciepła molowego Cv:
(11)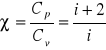
Przemiany:
Wtłoczony pod ciśnieniem gaz do balonu znajduje się pod ciśnieniem. Gaz określony jest parametrami:
1.Ciśnienie (p+ p1)- suma ciśnienia atmosferycznego i nadwyżki ciśnienia spowodowanej wtłoczeniem powietrza do balonu;
2.objętość gazu przed rozprężeniem;
3. temperaturę otoczenia.
Ciśnienie jest wprost proporcjonalne do różnicy poziomów cieczy w manometrze, ponieważ p= ρgh
Po otwarciu korka butli, w wyniku czego gaz rozpręża się adiabatycznie (oziębia się), w tym stanie parametry gazu zmieniają się:
1. ciśnienie (p) równe jest ciśnieniu adiabatycznemu
2. Objętość po rozprężeniu jest większa
3. Temperatura jest niższa
Po zamknięciu korka gaz ogrzewa się i po kilku minutach osiąga ponownie temperaturę otoczenia. W czasie zachodzącej przemiany izochorycznej powstaje nadwyżka ciśnienia, co obserwujemy na manometrze (ustala się różnica poziomów cieczy)
Stan trzeci układu określany jest przez następujące parametry:
Ciśnienie- p+p2
Objętość V2
Temperaturę otoczenia
Przejście ze stanu pierwszego w stan drugi określa równanie Poissona:
(p0+p1)V![]()
=p0V![]()
Przejście ze stanu 1 przez stan 2 w stan 3 można zastąpić przemianą izotermiczną, w której gaz przechodzi ze stanu 1 bezpośrednio w stan 3 w stałej temperaturze otoczenia.
Dla tego przejścia zastosujemy wzór Boyle'a i Mariotte'a:
(p0+p1)V1=(p0+p2)V2
Z powyższych równań obliczamy:
![]()
Pomiar:
1. Sprężyć powietrze w naczyniu i poczekać na wyrównanie temperatury między gazem i otoczeniem (ustaje wahanie cieczy w manometrze). Odczytujemy różnicę poziomów h1.
2. Wyjąć korek i po wyrównaniu ciśnienia z otoczeniem natychmiast go włożyć. Na skutek ogrzania powietrza w naczyniu powstaje nadciśnienie h2 wskazywane przez manometr.
Pomiar: |
T |
h1 |
h2 |
h1+h2 |
|
|
|
k |
mm |
mm |
mm |
- |
- |
1 |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
3 |
|
|
|
|
|
|
4 |
|
|
|
|
|
|
5 |
|
|
|
|
|
|
6 |
|
|
|
|
|
|
7 |
|
|
|
|
|
|
8 |
|
|
|
|
|
|
9 |
|
|
|
|
|
|
10 |
|
|
|
|
|
|
Obliczenia: