UNIWERSYTET ZIELONOGÓRSKI WYDZIAŁ INŻYNIERII LĄDOWEJ I ŚRODOWISKA
PRACOWNIA FIZYKI
jhgkvkvvvvh
GRZEGORZ DRZYMAŁA GRUPA NR 10
Rok akademicki 2001/02
1. Część teoretyczna
Równanie Clapeyron'a
Równanie gazu doskonałego, określające związek między jego temperaturą, ciśnieniem i objętością:
PV = nRT
Gdzie:
P- ciśnienie
V - objętość
n - liczba moli gazu
T - temperatura
R - stała gazowa (R = Nk, N - liczba Avogadra - liczba cząstek np. cząsteczek, atomów,
jonów, elektronów, w jednym molu dowolnej substancji:
NA = 6,022137•1023 mol-1 ; k - stała Boltzmanna).
Z równania Clapeyron'a wynikają prawa Boyle'a, Gay-Lussaca, Charlesa. Równanie to opisuje również z dobrym przybliżeniem rozrzedzone gazy rzeczywiste.
Izoprzemiany gazu doskonałego
Gaz doskonały:
objętość cząsteczek gazu jest o wiele mniejsza niż objętość zajmowana przez gaz,
zasięg sił działających między dwoma cząstkami jest o wiele mniejszy niż średnia odległość międzycząsteczkowa.
Wyróżniamy następujące izoprzemiany gazu doskonałego:
przemiana izotermiczna - przemiana gazowa zachodząca przy stałej temperaturze (ciepło właściwe przemiany izotermicznej), gdzie gęstość gazu jest wprost proporcjonalna do ciśnienia. Opisuje ją równanie:
PV = constans
(gdzie: P - ciśnienie, V - objętość), opisuje ją prawo Boyle'a-Mariotte'a. Praca układu w trakcie przemiany izotermicznej równa jest zmianie energii swobodnej.
przemiana izobaryczna - przemiana gazowa zachodząca przy stałym ciśnieniu p (ciepło właściwe przemiany izobarycznej), gdzie objętość określonej ilości gazu jest wprost proporcjonalna do jego temperatury bezwzględnej. Opisuje ją równanie:
![]()
= constans
gdzie:
V - objętość
T - temperatura
Zależność ta nosi nazwę prawa Gay-Lussaca.
Praca L w przemianie izobarycznej wyraża się wzorem:
L=pΔV
gdzie ΔV równe jest zmianie objętości.
przemiana izochoryczna - przemiana gazowa zachodząca przy stałej objętości (ciepło właściwe przemiany izochorycznej), gdzie ciśnienie gazu doskonałego jest wprost proporcjonalne do temperatury. Opisuje ją równanie:
![]()
= const.
gdzie:
P - ciśnienie
T - temperatura
Zależność ta nosi nazwę prawa Charlesa.
Układ nie wykonuje pracy w przemianie izochorycznej.
Pierwsza zasada termodynamiki
Zmiana energii wewnętrznej układu równa jest różnicy ciepła
dostarczonego do układu i pracy wykonanej przez ten układ.
To jest po prostu inna wersja zasady zachowania energii, w której mamy rozdzieloną energię ciała na część makroskopową i mikroskopową. Makroskopowa to energia ruchu masy (energia mechaniczna). Mikroskopowa to "ukryta" energia cząstek (energia wewnętrzna).
Zasada ta, równoważna zasadzie zachowania energii, w zarysach sformułowana została w 1842 przez J.R. Mayera, uściślona zaś w 1847 przez H.L.F. de Helmholtza.
Gdy dwa układy (ciała) o różnych temperaturach zetkniemy ze sobą to ciepło Q przepływa z ciała cieplejszego do chłodniejszego. Zgodnie z zasadą zachowania energii, ciepło pobrane przez układ musi być równe wzrostowi energii wewnętrznej układu plus pracy wykonanej przez układ nad otoczeniem zewnętrznym czyli
?U = W + Q
gdzie:
?U - zmiana energii wewnętrznej
W - praca wykonana nad ciałem
Q - ciepło doprowadzone
Zasada ta pracuje "w obie strony" tzn., gdy nad układem zostanie wykonana praca to układ może oddawać ciepło. To równanie bardzo często przybiera postać :
dU = dQ - dW
Praca
W dynamice - skalarna wielkość fizyczna; za miarę pracy W stałej siły F przyjmujemy iloczyn wartości tej siły i wartości przesunięcia r:
![]()
Jednostką pracy w układzie SI jest 1 dżul [ 1 J].
W termodynamice - wielkość fizyczna równa energii, jaką układ termodynamiczny oddaje otoczeniu zmieniając jednocześnie parametry opisujące jego stan. Maksymalną pracę wykona układ izolowany cieplnie w procesie izeontropowym. Jednostką pracy termodynamicznej jest dżul (dawniej kaloria).
Ciepło
Jedna (obok pracy termodynamicznej) z form przekazania energii układowi termodynamicznemu.
Ciepło właściwe
Ilość ciepła pobranego przez jednostkę masy danego układu, powodująca wzrost temperatury układu o jeden stopień Kelvina (1K). Ciepło właściwe definiujemy jako dQ/dT na gram lub mol substancji (ciepło wagowe lub molowe).
Ciepło molowe
Ilość ciepła wymieniana z otoczeniem przez 1 mol danej substancji, powodująca jednostkową zmianę temperatury. W przypadku gazów ciepło molowe przyjmuje odmienne wartości - podczas wymiany ciepła w warunkach stałego ciśnienia lub stałej objętości.
Dla gazu doskonałego różnica ta równa jest stałej gazowej R, natomiast dla substancji skondensowanych można ją pominąć.
Energia wewnętrzna
Jedna z funkcji termodynamicznych, równa całkowitej energii układu (zazwyczaj bez energii kinetycznej i potencjalnej układu jako całości). Jej zmiany określa pierwsza zasada termodynamiki Energia wewnętrzna dla procesów izoentropowych i izochorycznych jest potencjałem termodynamicznym.
Adiabatyczna przemiana gazu i równanie Poissone'a
Przemiana adiabatyczna - proces termodynamiczny, podczas którego układ nie oddaje i nie pobiera ciepła. Proces adiabatyczny realizuje się przez izolowanie cieplne układu, bądź też przeprowadzając go bardzo szybko (np. rozprężanie gazów w silniku o wewnętrznym spalaniu). Jeśli w procesie adiabatycznym układ wykonuje pracę, to odbywa się to kosztem energii wewnętrznej układu, zatem temperatura jego obniża się.
Gdyby w adiabatycznym cylindrze umieścić gaz o masie m, i na tłok wykonany z materiału (również nieprzenikliwego dla ciepła) wywrzeć ciśnienie p, wówczas zostanie wykonana praca:
?W = -pdV
?Q = 0
dV=mCvdT
Zatem z równania wyrażającego I zasadę termodynamiki otrzymamy:
pdV = mCvdT
z równania Clapeyrona możemy określić p
p = (![]()
)·m·(![]()
)
i podstawić do równania :
- pdV = mCvdT
w rezultacie czego otrzymamy
(-![]()
)·m·(![]()
) = mCvdT
Wiedząc, że ![]()
= ![]()
, możemy podstawić tę wartość do powyższego równania i podzieleniu przez T otrzymamy:
-m(Cp - Cv)![]()
= mCv·(![]()
)
Po skróceniu przez m., podzieleniu przez Cv i uporządkowaniu równanie przyjmuje postać:
(Cp /Cv - 1) ![]()
+ ![]()
= 0
Stosunek ![]()
oznaczmy literą И :
(И - 1) ![]()
+ ![]()
= 0
Całkując to równanie otrzymamy:
(И - 1)1nV = 1nT = constans
Stosując znane twierdzenie matematyki elementarnej {(И - 1)nV = nVИ-1} o sumie logarytmów możemy to zapisać jako logarytm iloczynu:
1n(VИ-1T) = constans
Jeżeli logarytm danej wielkości jest stały, znaczy to, iż suma tejże wielkości również jest stała, zatem ostatecznie można zapisać, że:
VИ-1T = constans
Jest to tzw. równanie Poissone'a. Mówi ono, że gdy zmniejszymy adiabatycznie objętość gazu, to jego temperatura będzie się podnosić, a przy adiabatycznym powiększeniu objętości gazu jego temperatura będzie opadała.
Ciepło właściwe gazów można wyliczyć na podstawie znajomości równania stanu gazów. Ciepła właściwe gazów przy przemianie izochorycznej Cp i przy przemianie izobarycznej Cv zdefiniowane są równaniami:
Q = Cv·m(T-Tο) dla v=constans
Q = Cp·m(T-Tο) dla p=constans
Q jest to ilość ciepła wymieniana przez układ przy przechodzeniu od temperatury Tο do
temperatury T.
Zamiast ciepła właściwego na jednostkę masy, można wyliczyć ciepła właściwe Cv i Cp jednego kilomola gazu (Cv = CvM, Cp = CpM, gdzie M jest masą jednego kilomola)
W przemianie izochorycznej, dostarczone układowi ciepło Q, jest równe przyrostowi energii wewnętrznej tego układu.
?U = Q
Z kolei w przemianie izobarycznej wykonana jest jednocześnie praca (L = p?V), a więc,
?U = Q - L = Q - nR·?T
Energia wewnętrzna jednego kilomola gazu doskonałego równa jest iloczynowi średniej energii kinetycznej cząsteczek Ēkin i liczby Avogadra (N)
U = Ē·N = 3/2R·T
Energia ta, dla gazu doskonałego, zależy tylko od temperatury. Dla jednego kilomola gazu w przemianie izochorycznej mamy więc:
3/2R(T-Tο) = Cv(T-Tο)
W przemianie izobarycznej natomiast:
3/2R (T-Tο) = Cp(T-Tο) - R(T-Tο)
W rezultacie otrzymujemy:
Cv =3/2R
Cp = 5/2R
więc:
Cp - Cv = R
Różnica między ciepłem właściwym Cp i Cv kilomola gazu doskonałego, równa jest stałej gazowej R (w układzie SI). Wniosek ten jest zgodny z doświadczeniem dla wszystkich gazów w zakresie ciśnień i temperatur, w którym spełniają one równanie gazu doskonałego.
Metoda pomiaru ![]()
= κ.
W celu pomiaru stosunku ciepła właściwego do ciepła molowego gazu należy wykonać następujące czynności:
Przy użyciu pompy uzyskać w balonie z powietrzem nadwyżkę ciśnienia wynoszącą 8 - 10 cm słupa cieczy w manometrze, po czym zamknąć kran łączący balon z pompą i wyłączyć pompę.
Po ustaleniu poziomu cieczy w manometrze odczytać nadwyżkę ciśnienia h w balonie.
Rozprężyć adiabatycznie powietrze w balonie, otwierając kran łączący balon z otoczeniem, na czas 1-2 sekund. Po wyrównaniu się ciśnienia powietrza w balonie z ciśnieniem atmosferycznym, należy natychmiast zamknąć kran.
Odczeka kilka minut, aż temperatura powietrza w balonie zrówna się z temperaturą otoczenia i poziom cieczy w manometrze ustali się, a następnie odczytać nadwyżkę ciśnienia h1.
Powyższe czynności powtórzyć co najmniej 10 razy.
Uzyskane w ten sposób wyniki zapisać w tabelce.
Korzystając z danych z tabelki obliczyć ![]()
dla każdego pomiaru korzystając ze wzoru:
κ = h/(h - h1)
a następnie obliczyć wartość średnią κśr.
2. Część doświadczalna
Wykonałam trzynaście pomiarów wysokości słupa cieczy. Po uzyskaniu nadwyżki ok. 8cm w manometrze (po ustaleniu się poziomu cieczy) oraz trzynaście pomiarów wysokości słupa cieczy po rozprężeniu adiabatycznym powietrza w balonie. Wyniki pomiarowe zamieszczono w tabeli.
Obliczono wartość Cp/Cv dla każdego pomiaru przy pomocy wzoru :
Cp/Cv =![]()
Wartości obliczone wpisano do tabeli, w odpowiednią rubrykę.
Stosunek ów musiał zawierać się w granicy 1,2 - 1,4, jako że mieliśmy do czynienia z mieszaniną gazów dwuatomowych.
Policzono także wartość średnią ![]()
, która równa się 1,28. Wykorzystując tą daną, dla każdego pomiaru policzono ![]()
, odejmując wartość średnią ![]()
od obliczonej. Wartość ![]()
podniesiono do kwadratu, celem uzyskania niezbędnych danych do wykreślenia krzywej Gaussa.
Uwagi
Metoda pomiarowa przyjęta do wykonania wykresów okazała się dość skomplikowana, choć z pozoru łatwa. Dość trudne z początku okazało się otrzymanie właściwego stosunku Cp/Cv, dopiero po kilku próbnych pomiarach ustalono odpowiednie czynności. Problem wiązał się z niedokładnością przy pomiarze wysokości słupa cieczy w manometrze, a także uzyskiwaniem niedostatecznej nadwyżki. Kolejnym problemem był czas, w jakim należało rozprężyć powietrze w balonie. Instrukcja podawała 1-2 sekund , przyjęto jednak czas minimalnie dłuższy. Dopiero wtedy uzyskiwano rzetelne wartości.
Wnioski
Zbadano zjawisko adiabatycznych przemian gazu w balonie.
Wykonano trzynaście pomiarów wysokości słupa cieczy przed i po otwarciu kranu.
Wyznaczono stosunek Cp/Cv metodą Clementa-Desormensa.
Wykreślono krzywą Gaussa, obrazującą błąd pomiaru.
Dane doświadczalne zaprezentowano w tabeli oraz na wykresie
L.p.Wysokość słupa cieczy K=Cp/Cv ε=K-Kśr ε2h [mm]h1 [mm]1.90231,3432840,0632840,0040052.116291,3333330,0533330,0028443.150281,229508-0,050490,0025494.109271,3292680,0492680,0024275.133281,266667-0,013330,0001786.116251,274725-0,0052707.143301,265487-0,014510,0002118.99211,269231-0,010770,0001169.124281,2916670,0116670,00013610.137271,245455-0,034550,00119311.92181,243243-0,036760,00135112.124291,3052630,0252630,00063813.139271,241071-0,038930,001515Kśr =1,279862? ε2 =0,017165
Błędy
Błąd pomiarowy obliczamy metodą Gaussa - wyznaczamy średni błąd pojedynczego pomiaru δx.
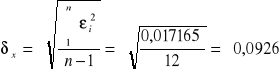
oraz błąd średniej arytmetcznej
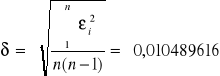
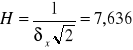
Krzywą Gaussa wykreślamy na podstawie wartości uzyskanych z poniższego wzoru:
![]()
y(ε1)3,41y(ε2)3,65y(ε3)3,71y(ε4)3,74y(ε5)4,26y(ε6)4,3y(ε7)4,25y(ε8)4,28y(ε9)4,27y(ε10)4,02y(ε11)3,98y(ε12)4,15y(ε13)3,94(wartości przybliżone)
Wyszukiwarka
Podobne podstrony:
4143
4143
4143
4143
4143 Lilia haft
praca licencjacka b7 4143
więcej podobnych podstron