Na podstawie wyników pomiarów zestawionych w tabeli sporządzono wykres biegu kalorymetru ![]()
.
Szczecin 28.01.2003
Tomasz Klama
Krzysztof Juszczyk
Gr.♫
Sprawozdanie z ćwiczenia nr 19:
Wyznaczanie ciepła reakcji zobojętniania kwasu siarkowego,
wodorotlenkiem sodowym w roztworze wodnym.
Celem ćwiczenia było wyznaczenie metodą kalorymetryczną ciepła zobojętniania kwasu siarkowego wodorotlenkiem sodowym w roztworze wodnym.
W procesie zobojętniania mocnego kwasu mocną zasadą, nie biorą udziału aniony kwasu i kationy zasady, a obserwowane ciepło reakcji wywiązuje się w wyniku powstawania cząsteczki wody:
H3O+ + OH- = 2 H2O
Badanie polegało na przeprowadzeniu reakcji 450 cm3 NaOH z 25 cm3 H2SO4. Takie proporcje są wystarczające do całkowitego zobojętnienia substancji. Reakcję przeprowadzono w kalorymetrze cieczowym zaopatrzonym w termometr Beckmana, a także w mieszadło i grzałkę o dokładnie znanym oporze. Pomiarów temperatury dokonano według instrukcji wykonania ćwiczenia, a uzyskane wyniki przedstawione zostały w tabeli.
TABELA POMIAROWA
Lp |
Czas[min] |
T[C] |
1 |
1 |
0,91 |
2 |
2 |
0,91 |
3 |
3 |
0,92 |
4 |
4 |
0,92 |
5 |
5 |
0,92 |
6 |
6 |
0,92 |
7 |
7 |
0,92 |
wstrzyknięcie H2SO4 |
||
8 |
7,5 |
2,15 |
9 |
8 |
2,2 |
10 |
8,5 |
2,2 |
11 |
9 |
2,2 |
12 |
9,5 |
2,2 |
13 |
10 |
2,2 |
14 |
10,5 |
2,2 |
|
włączenie grzałki |
|
15 |
11,5 |
2,22 |
16 |
12,5 |
2,27 |
17 |
13,5 |
2,31 |
18 |
14,5 |
2,35 |
19 |
15,5 |
2,4 |
20 |
16,5 |
2,45 |
21 |
17,5 |
2,49 |
22 |
18,5 |
2,53 |
23 |
19,5 |
2,58 |
24 |
20,5 |
2,62 |
25 |
21,5 |
2,67 |
26 |
22,5 |
2,71 |
27 |
23,5 |
2,75 |
28 |
24,5 |
2,79 |
29 |
25,5 |
2,83 |
30 |
26,5 |
2,88 |
31 |
27,5 |
2,92 |
32 |
28,5 |
2,96 |
33 |
29,5 |
3 |
34 |
30,5 |
3,04 |
35 |
31,5 |
3,08 |
36 |
32,5 |
3,12 |
37 |
33,5 |
3,16 |
38 |
34,5 |
3,2 |
39 |
35,5 |
3,24 |
|
po wyłączeniu grzałki |
|
40 |
36,5 |
3,24 |
41 |
37,5 |
3,24 |
42 |
38,5 |
3,23 |
43 |
39,5 |
3,23 |
44 |
40,5 |
3,23 |
45 |
41,5 |
3,22 |
46 |
42,5 |
3,22 |
47 |
43,5 |
3,21 |
OPRACOWANIE WYNIKÓW:
Na podstawie wyników pomiarów zestawionych w tabeli sporządzono wykres biegu kalorymetru ![]()
.
Obliczenie ciepła reakcji zobojętniania:
U=40 V
R=934![]()
T1=2,2 T2=0,92 t3=35,5
T3=3,24 T4=2,2 t4=11,5
![]()
![]()
![]()
![]()
X=(t3-t4)*60
X=24*60=1440[s]
nNaOH=450*10-3*0,1= 0,045 [mol/dm3]
Qp=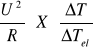
Qp=![]()
Qp=6082,13 [J]
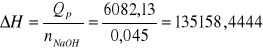
[J/mol*K]
![]()
H=135,1584 kJmol-1K-1
∆H- dla wody wynosi 241988,6664 J/mol, a ∆H entalpia reakcji zobojętniania NaOH roztworem H2SO4 wynosi 135,1584 kJmol-1K-1.
Różnica wyników eksperymentalnych i wartości zaczerpniętych z literatury może być spowodowana błędami pomiarowymi podczas prowadzenia doświadczenia, lub czynnikami wpływającymi na dokładność pomiaru.
2