TEORIA WIĄZAŃ WALENCYJNYCH VB, ORBITALI MOLEKULARNYCH MO (pkt.5), energia wiązania cząsteczki
Kwantowymi teoriami wiązania chemicznego, które wyjaśniają zarówno
charakter i energię wiązań w cząsteczce oraz geometrię cząsteczek, są teoria wiązań walencyjnych i teoria orbitali molekularnych (cząsteczkowych). W wielu punktach są podobne, lecz w różny sposób tłumaczą te same zjawiska.
Teoria wiązań walencyjnych opisuje wiązanie kowalencyjne jako rezultat nałożenia się na siebie dwóch orbitali atomowych z niesparowanym elektronem o spinach przeciwnych, przy czym każdy orbital pochodzi od innego atomu. Sparowane w ten sposób ze sobą dwa elektrony w nałożonych orbitalach są przyciągane do jąder obydwu atomów, ponieważ są uwspólnione przez obydwa atomy i dzięki temu atomy te są połączone. Każdy z połączonych ze sobą atomów zatrzymuje swoje własne orbitale atomowe. Siła wiązania atomowego zależy od stopnia nałożenia się orbitali i jest tym większa, im bardziej orbitale zachodzą na siebie.
Teoria orbitali molekularnych (cząsteczkowych) opisuje tworzenie wiązań atomowych jako rezultat matematycznej kombinacji orbitali atomowych (funkcji falowych), prowadzący do określenia energii i kształtu orbitali cząsteczkowych. Według tej teorii, tworzenie wiązania atomowego jest skutkiem powstania orbitali molekularnych (cząsteczkowych). Powstawanie orbitali molekularnych jest skutkiem kombinacji dwóch lub większej liczby orbitali atomowych. Liczba utworzonych
orbitali molekularnych jest taka sama, jak liczba orbitali atomowych, z których kombinacje te powstały. Orbitale molekularne nazywane są tak, ze względu na ich przynależność do całej cząsteczki, a nie do konkretnego atomu.
Orbital molekularny opisuje tę część przestrzeni w cząsteczce, w której
najprawdopodobniej znajdują się elektrony, charakteryzuje zatem cząsteczkę jako
całość, a nie pojedynczy atom. Orbitale molekularne mają charakterystyczny kształt, wymiar i poziom energetyczny. Orbital cząsteczkowy, którego energia jest niższa od energii orbitali atomowych, z których został utworzony, jest orbitalem wiążącym, tak jak np. w orbitalu H2, mającym kształt jajka. Natomiast orbital molekularny, który ma energię wyższą niż orbitale atomowe, z których został utworzony, jest orbitalem antywiążącym. W orbitalu tym elektrony nie mogą znaleźć się w środkowym obszarze między jądrami atomowymi, gdzie występuje węzeł funkcji falowej, dlatego
nie mogą przyczynić się do utworzenia wiązania. Zatem nakładanie się dwóch orbitali atomowych daje dwa orbitale molekularne, wiążący i antywiążący. Cząsteczki w stanach podstawowych mają obsadzone elektronami tylko orbitale wiążące. Orbitale antywiążące są obsadzone elektronami tylko w stanach wzbudzonych cząsteczek.
TEORIA KOSSELA I LEWISA POWSTAWANIA WIĄZAŃ
Niezwykła bierność chemiczna gazów szlachetnych spowodowana jest oktetem elektronowym na powłoce walencyjnej. Taka konfiguracja elektronowa tych pierwiastków nasunęła Kosselowi i Lewisowi myśl, że inne pierwiastki będą chciały również osiągnąć oktet elektronów na powłoce walencyjnej. Mogą to uczynić na kilka sposobów:
oddać nadmiarowe elektrony innemu pierwiastkowi
przyjąć brakujące elektrony od innego pierwiastka
podzielić się elektronami (uwspólnić je), w ten sposób obydwa łączące się atomy uzyskają oktet
Wiązania według koncepcji Kossela
Pierwsze dwa przypadki należy rozpatrywać wspólnie. Ponieważ gdy jeden z atomów oddaje elektrony, nie mogą one przecież zniknąć, inny atom musi je przyjąć. Powstają w ten sposób jony naładowane dodatnio (kationy) oraz jony naładowane ujemnie (aniony), które przyciągają się wzajemnie siłami elektrostatycznymi. Mówimy, że pomiędzy jonami powstało wiązanie jonowe. Dla uproszczenia przyjmijmy planetarny model atomu z elektronami zmieczczonymi na powłokach.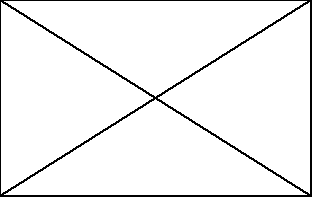
stan początkowy, dwa oddzielne atomy po przejściu elektronu powstały dwa jony (anion i kation)
Wiązanie jonowe powstaje tylko w wyniku spotkania się atomu silnie elektroujemniego z atomem o małej elektroujemności (atomu elektrododatniego). Oczywiście oderwanie elektronu od jednodotatniego jonu (również przyłączenie elektrou do anionu) jest trudniejsze. Dlatego głownie wiązania jonowe powstają pomiędzy jonami o jednostkowym ładunku.
1.1.2. Teoria Lewisa powstawania wiązań - wiązanie kowalencyjne.
W przypadku gdy spotkają się dwa atomy o porównywalnej elektroujemności, lub wręcz identycznej (np. takie same atomy), trudno jest wymagać by jeden z nich zabrał drugiemu elektron. Muszą one sobie radzić w inny sposób. Każdy z nich chce osiągnąć oktet elektronów. Jedynym wyjściem będzie gdy każdy atom “wypożyczy” swój elektron drugiemu atomowi. Mówimy, że uwspólniają one swoje elektrony (oczywiście uwspólniają ich tyle ile potrzeba) tak, by ten drugi atom uzyskał oktet elektronów, czyli uzyskał konfigurację najbliższego gazu szlachetnego. Oczywiście w rachunkach te elektrony (uwspólnione) należy liczyć podwójnie: raz że należą do jednego atomu, a drugi raz do drugiego atomu.

dwa oddzielne atomy, następuje uwspólnienie elektronów, po czym każdy atom posiada oktet elektronów
Rysowanie tego typu modeli jest niepotrzebną stratą czasu i bezcelowe. Prościej jest zamiast modeli atomów pisać symbole pierwiastków. Nie musimy też brać pod uwagę elektronów z powłok wewnętrznych, a jedynie z najbardziej zewnętrznej powłoki - elektrony walencyjne. Takie przedstawienie wzoru cząsteczki nosi nazwę wzoru elektronowego Lewisa:
W celu dalszego uproszczenia, parę elektronów wiążących zastępuje się kreską:
, a dość często każdą parę elektronów zastępuje się kreską:
.
Te wzory z parą elektronów wiążących w postaci kreski są najczęściej stosowane i noszą nazwę wzorów strukturalnych Lewisa.
W początkowym etapie nauki chemii powinniśmy zawsze rysować wzory w postaci wzorów Lewisa, a nie wzorów kreskowych dlatego, że w przeciwieństwie do tych ostatnich, pozwalają one na przewidywanie właściwości chemicznych i fizycznych związków.
Pomiędzy atomami może utworzyć się nie tylko wiązanie pojedyncze, ale również podwójne lub potrójne:

Zauważmy, że aby mogło powstać wiązanaie podwójne lub potrójne atomy muszą się do siebie bardziej zbliżyć, zatem wiązania te są krótsze od wiązań pojedynczych. Jeżeli wiązania powstają pomiędzy identycznymi atomami noszą nazwę wiązań kowalencyjnych atomowych, lub kowalencyjnych homoatomowych.
Wiązania kowalencyjne mogą również powstać pomiędzy atomami o różnej, lecz zbliżonej elektroujemności. Noszą one wtedy nazwę wiązań kowalencyjnych spolaryzowanych, lub wiązań kowalencyjnych heteroatomowych
We wzorach Lewisa fundamentalną zasadą jest, że każdy atom, o ile to możliwe, musi mieć oktet elektronów. Jednakże struktury w których jakiś atom ma więcej niż 8 elektronów są również możliwe, np. dla PCl5, SF6. Reguła oktetu musi być ściśle przestrzegana dla pierwiastków II okresu, nie mogą one posiadać więcej niż 8 elektronów na ostatniej powłoce. Struktury w których pierwiastki II okresu posiadają więcej niż 8 elektronów są niemożliwe. Spowodowane jest to tym, że pierwiastki te nie posiadają niskoenergetycznych orbitali d, na których mogłyby pomieścić nadmiarowe elektrony.
Nie można powiedzieć, że atomy II okresu nie posiadają orbitali d. Tak jak każdy żołnierz nosi w plecaku buławę, tak każdy atom posiada orbitale d, f, g (nawet atom wodoru), tylko, że orbitale te są wysokoenergetyczne i często nie ma możliwości umieszczenia na nich elektronów.
|
Wzór strukturalny kwasu azotowego(V) niepoprawny. Azot jest pierwiastkiem II okresu i nie może posiadać 10 elektronów. |
|
Wzór kwasu siarkowego(VI) mimo, że atom siarki posiada 12 elektronów jest poprawny. Siarka jest pierwiastkiem III okresu, dysponuje niskoenergetycznymi orbitalami d, w związku z tym może nadmiarowe elektrony pomieścić na tych orbitalach. |
Jaki jest więc poprawny wzór strukturalny kwasu azotowego(V), czy można zapisać wzór kwasu siarkowego(VI) zgodnie wymogami stawianymi dla wzorów Lewisa?
W tym celu zapiszmy jeszcze raz atomy wraz ze swoimi elektronami walencyjnymi.
|
połączmy elektrony w pary, by utworzyć wiązania i by każdy atom posiadał oktet (oprócz atomu wodoru) |
|
zauważmy, że dwa atomy tlenu, azot posiadają już oktet (atom wodou dublet) elektronów, są więc "szczęśliwe". pozostał jeden atom tlenu z 6 elektronami. |
|
jeżeli atom azotu uwspólni z atomem tlenu swoje dwa elektrony, pomiędzy atomem azotu a tlenu powstanie wiązanie. Atom azotu nadal będzie miał oktet elektronów, ale oktet uzyska też atom tlenu. Tego typu wiązanie nosi nazwę wiązania koordynacyjnego, donorowo-akceptorowego, lub semipolarnego. Oznacza się je za pomocą strzałki skierowanej od donora do akceptora. |
|
|
Tego typu wiązanie sugeruje, że w cząsteczce kwasu azotowego(V) istnieją trzy różne wiązania N-O. Jedno pojedyncze, jedno podwójne oraz jedno semipolarne. Czy w istocie tak jest? Rozpatrzmy jeszcze raz tworzenie się cząsteczki kwasu azotowego(V) na modelu, a na koniec zabierzmy jon wodorowy od cząsteczki kwasu azotowego(V) i utwórzmy jon azotanowy(V):
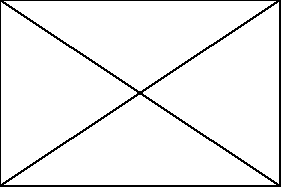
Czy teraz patrząc na końcowy wzór możemy stwierdzić, które wiązanie N-O powstało w wyniku uwspólnienia dwóch elektronów pochodzących od atomu azotu (wiązanie semipolarne)? Czy może każdy atom dostarczył po jednym elektronie „do wspólnego użytku” i powstało wiązanie kowalencyjne.
Rozpatrzmy jeszcze jeden przykład, a mianowicie jon amoniowy NH4+. Utworzenie tego jonu możemy sobie wyobrazić na dwa sposoby:
Jednodotatni jon azotu i cztery atomy wodoru tworzą wiązania kowalencyjne poprzez uwspólnienie elektronów:
W powstałej w ten sposób cząsteczce jonu amoniowego istnieją cztery jednakowe wiązania kowalencyjne.
Do cząsteczki amoniaku zbliża się jon wodorowy (nie posiada elektronów, a chce mieć podobnie jak hel, dwa elektrony). Aby powstało wiązanie między atomem azotu i jonem wodorowym, atom azotu musi uwspólnić swoją parę elektronów z jonem wodorowym:
Więc jak to jest z jonem amoniowym? Istnieją dwa różne jony amoniowe (w zależności od sposobu powatawania, co sprzeczne jest z podstawowym prawem chemii), czy jeden? Odpowiedź jest prosta: wiązanie semipolarne powstaje w inny sposób niż wiązanie kowalencyjne, ale po utworzeniu (po powstaniu) niczym nie różni się od wiązania kowalencyjnego. Jeżeli niczym nie różni się od wiązania kowalencyjnego, to można je zapisać w identyczny sposób jak wiązanie kowalencyjne. Inaczej mówiąc wiązanie semipolarne po utworzeniu staje się wiązaniem kowalencyjnym.
WIĄZANIA JONOWE
Podział wiązań na typy ma charakter formalny, w rzeczywistości między
niektórymi typami brak wyraźnej granicy. Podstawowymi typami wiązań są: wiązania
jonowe (elektrowalencyjne), atomowe, atomowe spolaryzowane, koordynacyjne,
wodorowe oraz wiązania międzycząsteczkowe, czyli siły Van der Waalsa.
Wiązanie jonowe powstaje w wyniku przyciągania elektrostatycznego odmiennych
ładunków. Występuje między dwoma jonami i wynika z przyciągania
elektrostatycznego ich przeciwnych ładunków. Na ogół obecne jest w solach nieorganicznych.
Typowe wiązanie jonowe tworzy się między pierwiastkiem (metalem) silnie
elektrododatnim (należącym do litowców), który oddaje elektron, a pierwiastkiem
(niemetalem) silnie elektroujemnym (należącym do fluorowców), przyjmującym
elektron.
Utworzona wiążąca para elektronowa jest niemal całkowicie przesunięta do
atomu bardziej elektroujemnego, dzięki czemu atomy uczestniczące w tworzeniu
wiązania jonowego osiągają konfigurację oktetową.
Przykładowo, podczas tworzenia NaCl, atom sodu oddaje elektron, przechodząc
w jon Na+, który osiągnął konfigurację neonu. Natomiast atom chloru przyjmuje
elektron, przechodząc w jon Cl-, o konfiguracji argonu. Wytworzony NaCl
określa się jako jonowe ciało stałe, posiadające wiązanie jonowe.
ELEKTROUJEMNOŚĆ W SKALI PAULINGA
Elektroujemność to miara tendencji do przyciągania elektronów przez atomy danego pierwiastka, gdy tworzy on związek chemiczny z atomami innego pierwiastka. Bardziej elektroujemny pierwiastek "ściąga" do siebie elektrony tworzące wiązanie z atomem mniej elektroujemnym, co prowadzi do polaryzacji wiązania. W skrajnym przypadku, gdy elektroujemności obu pierwiastków bardzo się różnią (np. sód i chlor), dochodzi do pełnego przeskoku elektronów na bardziej elektroujemny atom, co prowadzi do powstania wiązania jonowego.
Elektroujemność pierwiastków jest często zależna od układu atomów w danym związku, ich stopnia utlenienia, przyjętej w danym momencie hybrydyzacji i dość często zdarza się, że wiązania polaryzują się odwrotnie niżby to wynikało z formalnej elektroujemności związanych pierwiastków. Mimo to zaproponowano wiele sposobów, aby ilościowo zdefiniować ogólną elektroujemność pierwiastków.
Pierwszą taką propozycją była skala Paulinga oparta na pomiarach energii i polaryzacji wiązań prostych dwuatomowych związków chemicznych. Skala ta jest wciąż najczęściej używana, jednak bardzo mało precyzyjna i często prowadzi do błędnych wniosków.
Grupa → |
|||||||||||||||||||
↓ Okres |
|
||||||||||||||||||
H |
|
|
|||||||||||||||||
Li |
Be |
|
B |
C |
N |
O |
F |
|
|||||||||||
Na |
Mg |
|
Al |
Si |
P |
S |
Cl |
|
|||||||||||
K |
Ca |
Sc |
Ti |
V |
Cr |
Mn |
Fe |
Co |
Ni |
Cu |
Zn |
Ga |
Ge |
As |
Se |
Br |
Kr |
|
|
Rb |
Sr |
Y |
Zr |
Nb |
Mo |
Tc |
Ru |
Rh |
Pd |
Ag |
Cd |
In |
Sn |
Sb |
Te |
I |
Xe |
|
|
Cs |
Ba |
* |
Hf |
Ta |
W |
Re |
Os |
Ir |
Pt |
Au |
Hg |
Tl |
Pb |
Bi |
Po |
At |
Rn |
|
|
Fr |
Ra |
** |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
* |
La |
Ce |
Pr |
Nd |
Pm |
Sm |
Eu |
Gd |
Tb |
Dy |
Ho |
Er |
Tm |
Yb |
Lu |
|
|
|
|
** |
Ac |
Th |
Pa |
U |
Np |
Pu |
Am |
Cm |
Bk |
Cf |
Es |
Fm |
Md |
No |
Lr |
|
|
|
|
ENERGIA SIECI KRYSTALICZNEJ
Powstawanie sieci krystalicznej zawsze wiąże się z wydzielaniem na zewnatrz kryształu pewnej porcji energii. Układy są tym trwalsze, im niższą energią udało im się osiągnąć-w wypadku kryształu im więcej energii zostało wyzwolonej podczas tworzenia sieci krystalicznej. Aby rozerwać sieć krystaliczną nalezy dostarczyć tyle energii do kryształu, jaka została uwolniona podczas jego tworzenia. Aby stopić kryształ nalezy go rozgrzać. Niektóre ciała stałe są łatwo topliwe(ołów, lód) a inne trudno(chlorek sodu) oznacza to, że energia sieci krystaliczej NaCl jest duzo większa od energii Pb i lodu. Odmiany alotropowe tego pierwiastka różnią się między sobą stopniem topliwości.
WŁAŚCIWOŚCI ZWIĄZKÓW JONOWYCH
Stałe substancje jonowe są zbudowane z kationów i anionów tworzących uporządkowany układ przestrzenny. Substancje takie to przykłady kryształów, czyli substancji zbudowanych z atomów, cząsteczek lub jonów tworzących uporządkowaną sieć przestrzenną. Typowe ich właściwości to: wysokie temperatury topnienia i wrzenia, czy kruchość. Dopiero w wys. temp. możliwe jest przemieszczanie się jonów wzgl siebie i utworzenie cieczy. Nie rozpuszczają się w wodzie: silne przyciąganie między kationami i anionami tych związków uniemożliwia ich rozpad na jony. Jony tworzą uporządkowane struktury krystaliczne. Substancje jonowe mają z reguły wys. tem. topnienia i wrzenia, są kruche, a jeżeli rozp. się w wodzie tworzą r-ry elektrolitów (jonowe).
ŁADUNEK FORMALNY
Ładunek formalny atomów wchodzących w skład cząsteczki określa różnica
między liczbą elektronów na powłoce walencyjnej danego atomu w cząsteczce,
a liczbą elektronów posiadanych przez ten sam atom w stanie pierwiastkowym.
Można go określić, korzystając z następującego wzoru:
ładunek formalny = A - B - C
gdzie:
A - liczba elektronów walencyjnych,
B - połowa elektronów wiążących,
C - liczba elektronów niewiążących.
przykładowo, obliczając ładunek formalny:
⇒ dla atomu azotu w grupie nitrowej, np. nitrometanu:
H O
H C N
H O
elektrony walencyjne atomu azotu = 5
elektrony wiążące atomu azotu = 8
elektrony niewiążące atomu azotu = 0
ładunek formalny atomu azotu = 5 - 8/2 - 0 = +1
⇒ dla atomu tlenu pojedynczo związanego w grupie nitrowej:
elektrony walencyjne atomu tlenu = 6
elektrony wiążące atomu tlenu = 2
elektrony niewiążące atomu tlenu = 6
ładunek formalny atomu tlenu = 6 - 2/2 - 6 = -1
Z powyższego przykładu wynika, że grupa nitrowa, choć jako całość jest
obojętna, to na atomie azotu ma dodatni ładunek formalny, a na atomie tlenu ujemny.
Ładunek formalny jest szczególnie istotny dla atomów, które mają pozornie
„nienormalną” liczbę wiązań, jak np. atom azotu w jonie nitroniowym, w grupie
nitrowej, w czwartorzędowych solach amoniowych, w tym w cholinie lub acetylocholinie.
W związkach tych atom azotu zaangażowany jest w cztery wiązania chemiczne,
a nie w trzy - jak zazwyczaj - dlatego musi być przedstawiany z formalnym
ładunkiem dodatnim. W tabeli 2 przedstawiono przypadki, w których ładunki
formalne występują (lub nie) na atomach: węgla, azotu i tlenu.
Cząsteczki, które jako całość są obojętne, ale na poszczególnych atomach
mają formalny ładunek dodatni i ujemny, nazywają się cząsteczkami dipolowymi.
Dipole przyciągają się elektrostatycznie tworząc asocjaty, charakterystyczne dla
wody i innych cieczy dipolowych. Pod wpływem pola elektrycznego cząsteczki
dipolowe, szczególnie w cieczach, ulegają orientacji równoległej do linii sił pola.
Po usunięciu zewnętrznego pola elektrycznego cząsteczki dipolowe z powrotem
przechodzą w stan nieuporządkowany.
Wyszukiwarka