Wykresy:
Wstęp teoretyczny:
Szczególny przypadkiem korozji jest korozja kontaktowa. Występuje ona w przypadku, gdy dwa metale (lub metal i elektronowy przewodnik niemetaliczny jak np. grafit, magnetyt) stykają się ze sobą i jednocześnie pozostają w kontakcie z elektrolitem. Kontakt dwóch metali z reguły zwalnia szybkość korozji jednego metalu, przyśpiesza zaś korozję drugiego.
Reakcje anodowe w tego typu reakcjach przedstawiają równania stechiometryczne:
MA → MAa+ + a⋅e-
MB → MBb+ + b⋅e-
Proces anodowy sprowadza się tu do roztwarzana metali, a szybkość tego procesu jest szybkością korozji.
Reakcję katodową w silnie kwasowych roztworach opisuje równanie:
H+ + e- → ½ H2 jest to tzw. depolaryzacja wodorowa
Korozję kontaktową metali A i B można opisać sumarycznymi równaniami stechometrycznmi:
MA + aH+ → MAa+ + a/2 H2
MB + bH+ → MBb+ + b/2 H2
Gdy korodujące metale są bardziej elektroujemne od wodoru (mniej szlachetne), wówczas będą korodować jednocześnie. Suma ilości przekorodowanych metali A i B musi być równa ilości wydzielonego na katodzie wodoru. Podobnie suma prądów anodowych jest równa sumie prądów katodowych. Proces anodowy jednak przebiega szybciej na metalu bardziej elektroujemnym , proces katodowy na metalu bardziej elektrododatnim.
Cel ćwiczenia:
Celem tego ćwiczenia jest ustalenie wpływu kontaktów: żelazo-cynk, żelazo-miedź oraz stosunku wielkości powierzchni pozostających w kontakcie metali na szybkość korozji
w 10% kwasie siarkowym.
Opracowanie wyników:
Wyniki pomiarów korozji kontaktowej w układach Fe - Zn, Fe - Cu
10% roztwór kwasu siarkowego t0 [oC]
1 |
2 |
3 |
4 |
7 |
8 |
9 |
10 |
11 |
12 |
|||||||
nr |
powierzchnia czynna Fe |
powierzchnia czynna Zn |
SFe / SZn |
czas trwania korozji |
masa próbki żelaznej |
masa próbki cynkowej (miedzianej) |
średnia szybkość korozji żelaza |
średnia szybkość korozji cynku (miedzi) |
sumaryczny średni prąd korozyjny w układzie |
|||||||
|
SFe [cm2] |
SZn [cm2] |
|
t [min] |
Przed |
po |
ubytek masy |
przed |
po |
ubytek masy |
IFe [A] |
na jedn. pow. |
IZn [A] |
na jedn. pow. |
I = IFe + IZn |
|
|
|
|
|
|
m1 Fe [g] |
m2 Fe [g] |
၄ၭၥ၆ ၝၧၛ |
m1 Zn [g] |
m2 Zn [g] |
၄ၭၮၚ ၝၧၛ |
|
iFe |
|
iZn |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[A/cm2] |
|
[A/cm2] |
|
|
1 |
6,44 |
38,40 |
0,1 |
45 |
5,16780 |
5,16730 |
0,00050 |
5,22680 |
4,56370 |
0,66310 |
0,00064 |
0,00010 |
0,72510 |
0,01888 |
0,72574 |
|
2 |
40,18 |
38,40 |
1 |
45 |
16,48550 |
16,47110 |
0,01440 |
4,92740 |
3,55290 |
1,37450 |
0,01843 |
0,00046 |
1,50302 |
0,03914 |
1,52145 |
|
3 |
38,40 |
9,30 |
10 |
45 |
6,44620 |
6,44400 |
0,00220 |
4,43960 |
3,70560 |
0,73400 |
0,00282 |
0,00007 |
0,80263 |
0,08630 |
0,80545 |
|
|
|
SCu [cm2] |
SFe / SCu |
|
|
|
|
m1 Cu [g] |
m2 Cu [g] |
၄ၭၵ၃ ၝၧၛ |
|
|
ICu [A] |
iZn |
I = IFe + ICu |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[A/cm2] |
|
|
4 |
5,80 |
42,00 |
0,1 |
45 |
4,4398 |
4,4305 |
0,0093 |
11,4676 |
11,4672 |
0,0004 |
0,0119 |
0,00205 |
0,00045 |
0,000011 |
0,01236 |
|
5 |
42,00 |
43,86 |
1 |
45 |
16,8638 |
16,8151 |
0,0487 |
10,9210 |
10,9209 |
0,0001 |
0,0623 |
0,00148 |
0,00011 |
0,000003 |
0,06245 |
|
6 |
44,72 |
6,24 |
10 |
45 |
16,6444 |
16,5872 |
0,0572 |
3,4786 |
3,4782 |
0,0004 |
0,0732 |
0,00164 |
0,00045 |
0,000072 |
0,07367 |
|
|
korozja bez kontaktów |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
7 |
Fe |
41,00 |
|
|
45 |
17,4210 |
17,3608 |
0,0602 |
|
|
|
0,0771 |
0,0019 |
|
|
|
8 |
Zn |
38,40 |
|
|
45 |
10,5342 |
4,9638 |
5,5708 |
|
|
|
6,09167 |
0,15864 |
|
|
|
9 |
Cu |
43,86 |
|
|
45 |
11,5728 |
11,5720 |
0,0008 |
|
|
|
0,00090 |
0,000021 |
|
|
|
Przykład obliczeń:
blaszka żelazna posiada wymiary 41 [mm] x 50 [mm]
S = 2 ⋅ 4,1 ⋅ 5,0 = 41,0 [cm2]
m1 Fe = 17,4210 [g]
m2 Fe = 17,3608 [g]
ΔmFe = m1 Fe - m2 Fe = 17,4210 - 17,3608 = 0,0602
czas korozji t = 45 [min] = 2700 [s]
Z pierwszego prawa Faradaya m = k⋅I⋅t obliczmy natężenie I = m / kt
F = 96500 [C] - stała Faradaya
MFe = 55,847 [g] - masa molowa
KFe = 55,847 / (2 ⋅ 96500) = 2,89 ⋅ 10-4
IFe = ΔmFe / (kFe⋅t) = 0,0602 / (2,89 ⋅ 10-4 ⋅ 2700) = 0,0771
iFe = IFe / SFe = 0,0771 / 41,0 = 0,0019

Wykresy:
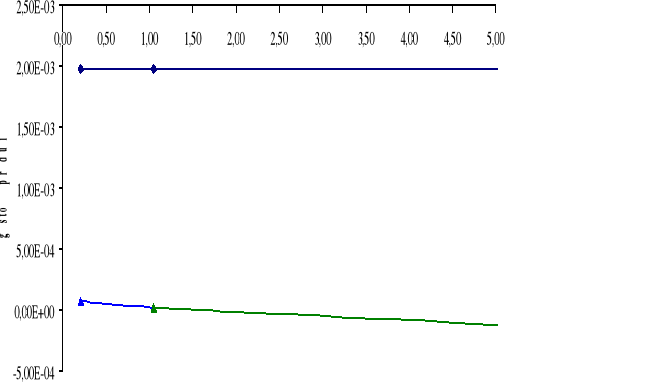
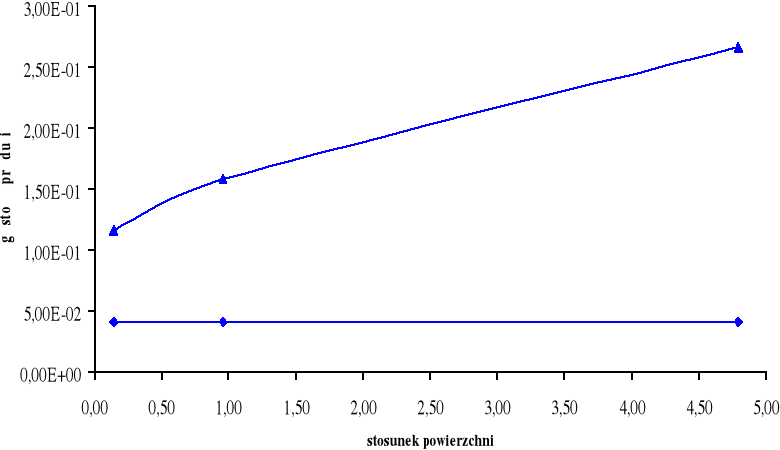
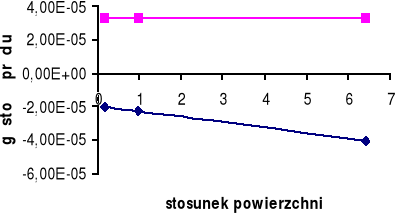
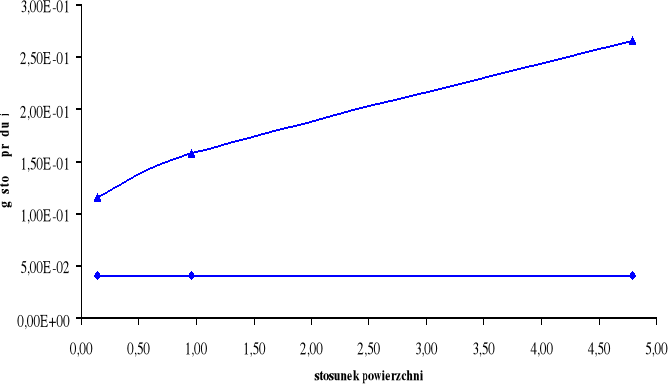
Górny wykres obrazuje zależność gęstości prądu i dla cynku Zn w zależności od stosunku powierzchni SFe / SZn.
Dolny wykres obrazuje zależność gęstości prądu i dla żelaza Fe w zależności od stosunku powierzchni SZn / SFe.
A: Zn → Zn2+ + 2e-
K: H+ + e- → ½ H2
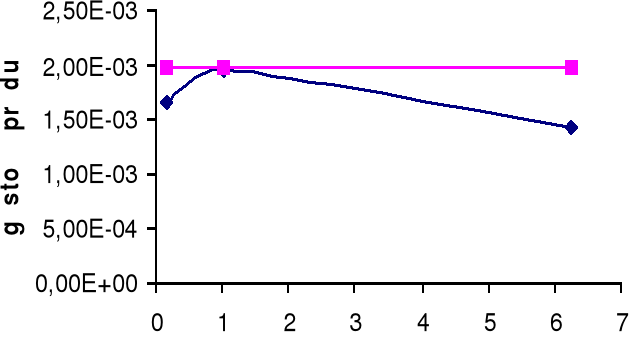
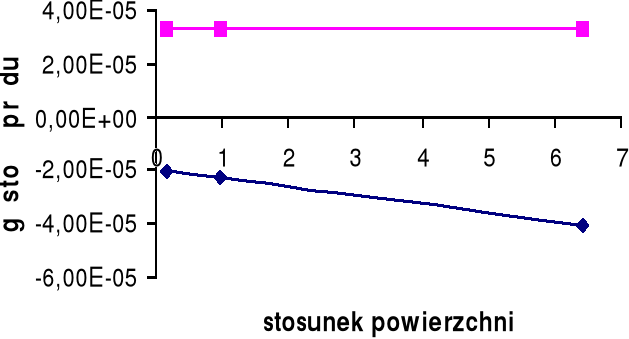
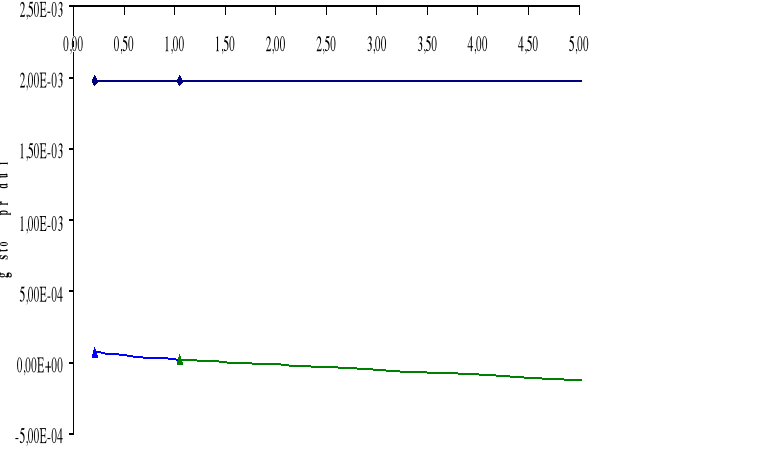
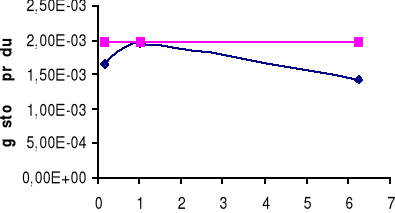
Górny wykres obrazuje zależność gęstości prądu i dla żelaza Fe w zależności od stosunku powierzchni SCu / SFe.
Dolny wykres obrazuje zależność gęstości prądu i dla miedzi Cu w zależności od stosunku powierzchni SFe / SCu.
A: Fe → Fe2+ + e-
K: H+ + e- → ½ H2
Wnioski:
W układzie Fe - Zn możemy zaobserwować zmniejszenie korozji żelaza, w wyniku kontaktu z cynkiem. Wynika to z tego, iż cynk jest bardziej elektroujemny od żelaza i przez chroni je przed korozją (cynk stanowi anodę, a żelazo katodę).
W układzie Fe - Cu możemy zaobserwować, iż w tym przypadku anodę stanowi blaszka żelazna, a katodę stanowi blszka miedziana (blaszka miedziana pokrywa się nalotem). Wynika to z teog, iż żelazo jest bardziej elektroujemne od miedzi.
Pod wpływem kontaktu żelaza z cynkiem lub miedzią można zaobserwować zmniejszenie korozji, bowiem w przypadku gdy żelazo pozostaje bez kontaktu z tymi metalami, wówczas koroduje ono bardziej (o 1-2 rzędy wielkości).
Pod wpływem kontaktu cynku z żelazem, można zaobserwować, iż cynk (stanowiący wówczas anodę) ulega korozji. Wynika to z tego, iż jest on bardziej elektroujemny od żelaza.
Pod wpływem kontaktu miedzi z cynkiem można zaobserwować, iż miedź (stanowiąca wówczas katodę) pokrywa się nalotem. Wynika to z tego, iż miedź jest bardziej elektrododatnia od żelaza.
W układzie Fe - Zn możemy zaobserwować, iż korozja żelaza zależy od stosunku powierzchni SFe / SZn. Im większy stosunek powierzchni SFe / SZn tym mniejsza korozja żelaza. Im większy stosunek SZn / SFe tym większa jest korozja cynku.
W układzie Fe - Cu możemy zaobserwować, iż korozja żelaza zależy od stosunku powierzchni SFe / SCu. Dla małych stosunku powierzchni można zaobserwować, iż korozja żelaza wzrasta, a dopiero po przekroczeniu pewnej wartości SFe / SCu korozja żelaza zmniejsza się.
Aby chronić żelazo przed korozją w silnie kwaśnym środowisku bardzo często blachę żelazną pokrywa się cienką warstwą cynku lub miedzi. Wynika to z tego, iż cynk zmniejsza korozyjność żelaza. Pokrywanie blachy żelaznej miedzią również chroni ją przed korozją, bowiem miedź ulega korozji wolniej niż żelazo.