Wydział Metali Nieżelaznych
Inżynieria Materiałowa
Rok III
STOPY MIEDZI I ANALIZA UKAŁADÓW PODWÓJNYCH
Piotr Janik
Podstawowe przemiany w układach podwójnych:
a ) przemiana eutektyczna:
Przykładowy wykres przemiany eutektycznej w układzie o całkowitym braku rozpuszczalności w składników w stanie stałym.
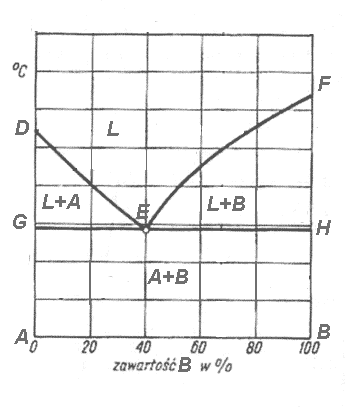
Ciecz o składzie punktu E jest nazywana cieczą eutektyczną, natomiast jej skład - składem eutektycznym. Stopy o składach leżących na lewo od składu eutektycznego są nazywane stopami podeutektycznymi, natomiast leżące na prawo - stopami nadeutektycznymi. Z cieczy o składzie eutektycznym wydzielaja się jednocześnie kryształy składnika A i B, gdyz skład eutektyczny leży zarówno na linii początku wydzielania się kryształów A (linia DE), jak i wydzielania się kryształów B, ( linia EF). Podczas krzepnięcia cieczy o składzie eutektycznym w stopie współistnieją trzy fazy ( zero stopni swobody) i w rezultacie ciecz eutektyczna krzepnie w stałej temperaturze. Dalsze obniżanie się temperatury stopu będzie możliwe dopiero po całkowitym skrzepnięciu cieczy. Powstająca z cieczy o składzie eutektycznym mieszanina kryształów A i B jest nazywana eutektyką lub mieszaniną eutektyczną. Eutektyki są drobnoziarniste, gdyż tworzą się w najniższych temperaturach krzepnięcia, a rozsegregowanie składników następuje w wyniku dyfuzji, której szybkośc maleje wykładniczo wraz z obniżeniem temperatury. Eutektyka składa się z tworzących się jednocześnie kryształów czystych składników A i B. Podczas chłodzenia stopu od temperatury eutektycznej do temperatury otoczenia jej mikrostruktura nie ulega już zmianie.
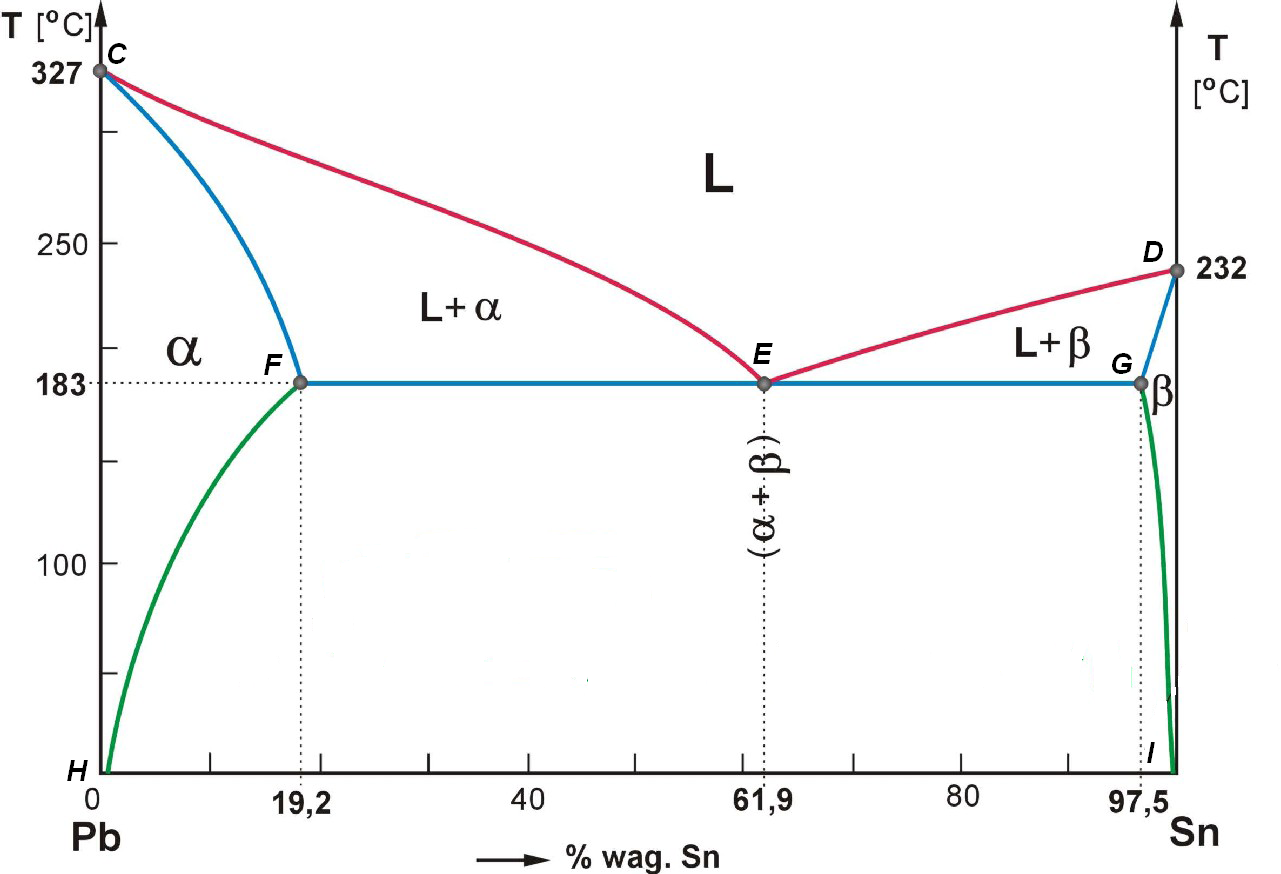
Przykładowy wykres przemiany eutektycznej ( Pb - Sn) dla składników tworzących w stanie stałym roztwory.
E
Jak składnika b, gdyz składnik A jest w fazie
Struktura krystaliczna fazy jest zawsze taka sama jak składnia A, a fazy jak składnika B, gdyż składnik A jest w fazie rozpuszczalnikiem dla składnika B, natomiast w fazie - składnik B dla A. W dyskutowanym układzie zachodzi następująca przemiana eutektyczna:
LE = F + G
Utworzona podczas powolnego chłodzenia mikrostruktura stopu eutektycznego składa się z na przemian ułożonych płytek faz i Nie zawsze fazy eutektyki mają kształt płytek. Czasami czastki jedne z faz mogą mieć kształt listew lub nawet kształt zbliżony do równoosiowego, a druga faza tworzy wtedy osnowę. Podczas obniżania temperatury, w eutektyce poprzednio dyskutowanego układu, ilość faz i ich składy nie ulegały zmianie. W obecnie omawianej eutektyczna skutek zmiany rozpuszczalności granicznej składników wraz ze zmianą temperatury względne ilości faz oraz ich składy ulegają zmianie.
b) przemiana eutektoidalna:
Z porównania przemiany eutektoidalnej z eutektyczną wynika, że podczas przemiany eutektycznej przemianie ulega roztwór ciekły, natomiast podczas przemiany eutektoidalnej - roztwór stały. Mikrostruktury eutektoidalne są zwykle znacznie bardziej drobnoziarniste niż mikrostruktury eutektyczne, gdyż powstaja z roztworu stałego, w którym dyfuzja jest znacznie wolniejsza oraz przemiana zachodzi w niższych temperaturach.
Przykład wykresu z przemianą eutektoidalną:
c ) przemiana perytektyczna
Przykładowy wykres z przemianą perytektyczną:
Likwidusem dla tego wykresu jest linia EDC, natomiast solidusem linia ABPC. Na tym wykresie dla linii BPD zachodzi następując przemiana perytektyczna:
LD + αB = βP
Podczas przemiany perytektycznej z cieczy o składzie punktu D i kryształów roztworu stałego α o składzie punktu B tworzą się kryształy roztworu stałego β o składzie punktu P. Jeżeli stop ma skład punktu P, to w temperaturze przemiany perytektycznej stosunek ilości cieczy L do ilości fazy α wynosi:
Ilośc L/ilość = PB/DP
I po zakończeniu przemiany perytektycznej stop składa się jedynie z kryształów β.
W stopach o składach miedzy punktami D i P przemiana perytektyczna kończy się wyczerpaniem kryształów α, gdyż jest nadmiar cieczy. Dlatego w polu leżacym bezpośrednio poniżej odcinka DP występuje pozostała ciecz i kryształy β powstałe w wyniku przemiany perytektycznej. Podczas dalszego chłodzenia ulega zmianie skład kryształów β oraz wzrasta ich ilość przy zmniejszeniu się ilości cieczy, aż do chwili, gdy osiągną one skład stopu i zniknie ciecz. Jeżeli skład stopu jest zawarty miedzy punktami P i B to przemiana perytektyczna prowadzi do wyczerpania się cieczy, dlatego tez w obszarze leżącym poniżej linii PB występują kryształy faz β i α.
Produktem przemiany perytektycznej może niekiedy być faza pośrednia charakteryzująca się właściwą sobie strukturą krystaliczną.
d ) przemiana perytektoidalna
Przebiega analogicznie do przemiany perytektycznej. Jedyna róznica tak jak w przypadku przemiany eutektoidalnej jest fakt, że przemiana perytektoidalna zachodzi w stanie stałym.
e ) przemiana monotektyczna:
Przykładowy wykres z przemiana monotektyczną:
Dwuskładnikowy układ równowagi fazowej z monotektyka tworzą składniki rozpuszczające się częściowo w stanie ciekłym i nie rozpuszczające się wzajemnie w stanie stałym lub wykazujące małą rozpuszczalność w stanie stałym. Obniżenie temperatury roztworu ciekłego L o składzie chemicznym zawartym miedzy punktem monotektycznym M a punktem N do lini granicznej powoduje utworzenie mieszaniny dwuch roztworów ciekłych L1 i L2, bogatych odpowiednio w metale A i B. Mieszanina roztworów ciekłych L1 i L2 jest trwała do temperatury monotektycznej TM. W wyniku przemiany monotektycznej, która ma charakter przemiany eutektycznej:
L1 = + L2
Roztwór ciekły L1 ulega przemianie w fazę stała oraz roztwór ciekły L2 bogaty w składnik B. Dalsze obniżenie temperatury powoduje krystalizacje stopów, przebiegającą podobnie jak w poprzednio opisanych przypadkach.
2. Reguły Hume-Rothery'ego
a) Czynnik wielkości atomu, (Jeżeli różnica wielkości atomów jest < 15% sprzyja to
powstawaniu roztworów stałych z nieograniczona rozpuszczalności
b) Jednakowy typ sieci krystalicznej składników (izomorfizm)
c) Bliskie sąsiedztwo pierwiastków tworzących roztwór w układzie okresowym (podobna
struktura elektronowa i zbliżone właściwości fizyczne
d) Efekt względnej wartościowości (pierwiastek o wyższej wartościowości lepiej rozpuszcza
się w pierwiastku o niższej rozpuszczalności
Wyszukiwarka