Ćwiczenie nr 6
mgr Anna Bielenica
Lipidy
Repetytorium
Ogólne wiadomości o lipidach.
Podział lipidów.
Kwasy tłuszczowe.
Tłuszcze właściwe (triglicerydy, triacyloglicerole).
Lipidy złożone - fosfolipidy, glikolipidy.
Hormony sterydowe.
Kwasy żółciowe.
Prostaglandyny - prostanoidy (ejkozanoidy).
Część praktyczna
Rozpuszczalność tłuszczów.
Zmydlanie tłuszczów.
Wykrywanie kwasów żółciowych - próba Haya.
Wykrywanie steroli metodą Liebermanna-Burcharda i Salkowskiego.
Oznaczanie cholesterolu metodą Allain-Roeschlau.
Oznaczanie liczby jodowej.
Repetytorium
1. Ogólne wiadomości o lipidach
Lipidy stanowią dużą i bardzo zróżnicowaną pod względem chemicznym grupę naturalnych związków organicznych, których wspólną cechą jest lipofilowość - rozpuszczalność w rozpuszczalnikach niepolarnych (np. eter, chloroform, benzyna). Jest to zatem całkowicie inne kryterium, niż stosuje się do definiowania większości grup naturalnych związków organicznych, gdzie o przynależności do danej grupy decyduje ich budowa chemiczna (grupa funkcyjna). Lipidy wydobywa się z materiałów biologicznych poprzez ekstrakcję niepolarnymi lub słabo polarnymi rozpuszczalnikami organicznymi.
2. Podział lipidów
Lipidy proste
, np.
5. Lipidy złożone - fosfolipidy, glikolipidy
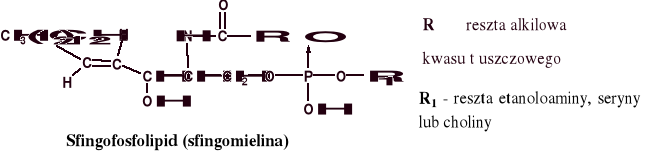
Plazmalogeny
7. Kwasy żółciowe
8. Prostaglandyny - prostanoidy (ejkozanoidy)
Rozpuszczalność tłuszczów.
Zmydlanie tłuszczów.
Wykrywanie kwasów żółciowych - próba Haya.
Wykrywanie steroli metodą Liebermanna-Burcharda i Salkowskiego.
Oznaczanie cholesterolu metodą Allain-Roeschlau.
Oznaczanie liczby jodowej metodą Morgoschesa..
Reakcja Salkowskiego
Oznaczanie cholesterolu metodą Allain-Roeschlau
a) Tłuszcze - estry glicerolu i kwasów tłuszczowych
b) Woski - estry wyższych kwasów tłuszczowych i wyższych alkoholi
2. Lipidy złożone - zawierają oprócz reszt kwasów tłuszczowych i alkoholi reszty innych związków. Dzielą się na:
a) Fosfolipidy - lipidy zawierające oprócz kwasów tłuszczowych resztę kwasu fosforowego; dzielą się na glicerofosfolipidy, sfingofosfolipidy i plazmalogeny
b) Glikosfingolipidy (glikolipidy) - lipidy zawierające kwas tłuszczowy, sfingozynę i węglowodany; są wśród nich cerebrozydy i gangliozydy
c) Inne lipidy złożone - sulfolipidy i aminolipidy
3. Prekursory i pochodne lipidów - modyfikowane chemicznie naturalne lipidy.
Zaliczamy do nich m. in. kwasy tłuszczowe, sterydy i steroidy, lipidy izoprenowe (terpenoidy) np. witaminy rozpuszczalne w tłuszczach,
wyższe alkohole.
3. Kwasy tłuszczowe
Kwasami tłuszczowymi nazywane są alifatyczne, lipofilowe kwasy monokarboksylowe, od kwasu masłowego wzwyż. Posiadają różną długość łańcucha (najczęściej 14-24 atomy C), przeważnie proste, nierozgałęzione łańcuchy, nasycone i nienasycone.
Nomenklatura kwasów tłuszczowych. Nazwy zwyczajowe najczęściej pochodzą od nazwy surowca, z którego kwas został wyodrębniony po raz pierwszy. W literaturze spotyka się skrótowy zapis nazw kwasów tłuszczowych, polegający na użyciu samych liczb z powinięciem nazw. Według tej zasady skrócony zapis kwasu linolowego to 18:2 (9, 12) lub 18:2 (9c, 12c), gdzie pierwsza liczba oznacza liczbę atomów węgla, liczba po dwukropku - liczbę wiązań podwójnych, natomiast zapisane w nawiasie kursywą liczby to numery nienasyconych atomów węgla. Naturalne kwasy tłuszczowe występują głównie w postaci izomerów cis (w zapisie skróconym: c, cis lub Z). Kwasy trans (t, trans lub E) powstają z izomerów cis w obecności katalitycznych ilości utleniaczy (np. HNO3, NO2), światła, pod wpływem podwyższonej temperatury, jako uboczny produkt uwodornienia.
Kwasy tłuszczowe są dla organizmu głównym źródłem energii, stanowią substraty w syntezie tłuszczów, fosfolipidów, lipoprotein, ejkozanoidów i liposacharydów. Przechowywane są przede wszystkim w formie związanej jako triacyloglicerole oraz fosfolipidy, a także w komórkach tłuszczowych w postaci wolnej.
Właściwości fizyczne kwasów tłuszczowych zależą od długości łańcucha i stopnia nienasycenia łańcucha węglowego.
Niezbędne nienasycone kwasy tłuszczowe (NNKT, ang. EFA) to nienasycone kwasy tłuszczowe wykorzystywane do syntezy innych związków koniecznych do prawidłowego funkcjonowania organizmu, nie syntetyzowane przez organizm, dostarczane wraz z pożywieniem. Służą one m.in. jako substraty do syntezy lipidowych składników błon komórkowych i ejkozanoidów. Do NNKT należą kwasy polienowe, zawierające przynajmniej dwa wiązania podwójne, przy czym jedno w położeniu C3 lub C6, licząc od końcowej grupy CH3. NNKT dzielą się na dwie grupy. Prekursorem grupy kwasów omega-3 (n-3) jest kwas α-linolenowy, a omega-6 (n-6) kwas linolowy. Kwasy te są zwane podstawowymi kwasami NNKT. W organizmach ssaków nie dochodzi do transformacji NNKT jednej rodziny w drugą.
Tabela 1. Najpopularniejsze nasycone kwasy tłuszczowe
Nazwa kwasu |
Wzór sumaryczny |
Występowanie |
|
zwyczajowa |
systematyczna |
|
|
masłowy |
butanowy |
C3H7COOH |
masło, olej palmowy i kokosowy |
kapronowy |
heksanowy |
C5H11COOH |
|
kaprylowy |
oktanowy |
C7H15COOH |
|
laurowy |
dodekanowy |
C11H23COOH |
nasiona laurowe, masło, olej palmowy |
palmitynowy |
heksadekanowy |
C15H31COOH |
praktycznie wszystkie tłuszcze roślinne i zwierzęce |
stearynowy |
oktadekanowy |
C17H35COOH |
|
arachidowy |
ejkozanowy |
C19H39COOH |
orzeszki ziemne, tran |
Tabela 2. Najpopularniejsze nienasycone kwasy tłuszczowe
Nazwa kwasu |
Wzór sumaryczny |
Występowanie |
|
zwyczajowa |
systematyczna |
|
|
oleinowy |
(Z)-9-oktadekaenowy
|
C17H33COOH |
najpopularniejszy kwas tłuszczowy |
erukowy |
(Z)-13-dokosaenowy
|
C21H41COOH
|
olej rzepakowy i nasturcjowy |
nerwonowy |
(Z)-15- tetrakosenowy |
C23H45COOH |
składnik mielin |
linolowy |
(Z,Z)-9,12-oktadekadienowy
|
C17H31COOH
|
powszechny składnik lipidów |
linolenowy (α-linolenowy) |
(Z,Z,Z)-9,12,15-oktadekatrienowy
|
C17H29COOH |
olej lniany i konopny |
arachidonowy |
(Z,Z,Z,Z)-5,8,11,14-ejkozatetraenowy
|
C19H31COOH
|
niektóre tkanki zwierzęce |
Oleje schnące stosowane są do wyrobu farb olejnych. Najlepsze farby otrzymuje się z olejów zawierających ok. 50 % kwasu linolowego i 25 % kwasu linolenowego (np. z oleju lnianego lub konopnego). Proces wysychania (utwardzania) olejów schnących polega na utlenianiu tlenem z powietrza podwójnych wiązań występujących w łańcuchach kwasów tłuszczowych. Następuje wtedy przestrzenne sieciowanie łańuchów reszt kwasowych, w wyniku czego zmienia się konsystencja oleju - tworzy się twarda, błyszcząca powłoka.
Diglicerydy (DAG) i monoglicerydy (MAG) nazywane są niepełnymi glicerydami i nie są wliczane do tłuszczów właściwych. W świeżych tłuszczach naturalnych występują w ilościach śladowych, ich stężenie wzrasta podczas przechowywania w warunkach narażonych na hydrolizę. MAG mają zdolności emulgujące i w przemyśle spożywczym wykorzystywane są jako stabilizatory emulsji. Monoacyloglicerole występują głównie w postaci pochodnych sn-1, ponieważ pierwszorzędowe grupy hydroksylowe są bardziej reaktywne niż drugorzędowe, a ponadto pochodne sn-2 łatwo izomeryzują do pochodnych sn-1.
4. Tłuszcze właściwe (triglicerydy, triacyloglicerole)
Tłuszcze właściwe ze względu na pochodzenie można podzielić na naturalne (roślinne i zwierzęce) i modyfikowane (syntetyczne), które otrzymywane są z tłuszczów naturalnych w wyniku uwodornienia (utwardzania) i transestryfikacji (przeestryfikowania).
Otrzymywanie tłuszczów właściwych
1) w reakcji estryfikacji
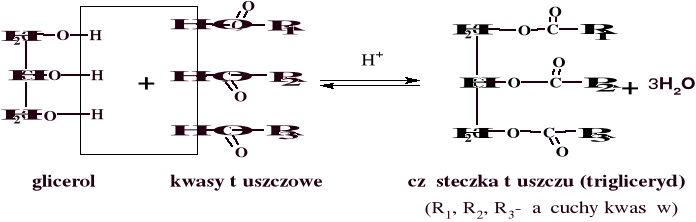
Nazewnictwo i stereochemia tłuszczów. Stereoizomery tłuszczów można przedstawić za pomocą projekcji Fischera, przy czym przyjmuje się umownie, że grupa znajdująca się przy C2 przybiera zawsze konfigurację L. Numery atomów węgla podaje się w nawiasach lub zapisuje z przedrostkiem sn (ang. stereospecific numbering). Według innych, starszych zasad pozycje grup acyloksylowych w cząsteczce glicerolu oznaczało się za pomocą liter greckich, przy czym pozycji 1 odpowiadała litera α, 2 - β, a 3 - α'.
Przykładowe nazewnictwo tłuszczów:
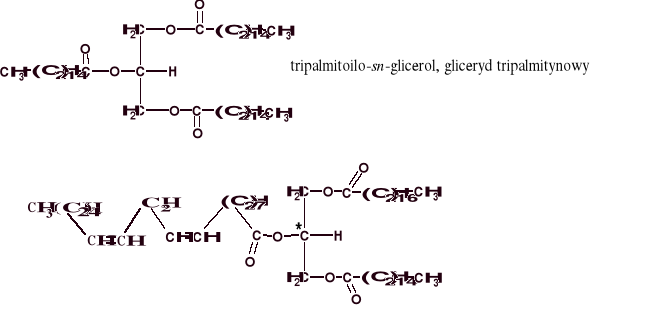
1- stearoilo -2- linoleoilo -3-palmitoilo-sn-glicerol (dawniej: α- stearoilo -β- linoleoilo -α'-palmitoiloglicerol)
Właściwości chemiczne tłuszczów właściwych
1) ulegają reakcjom hydrolizy w środowisku kwaśnym, zasadowym i enzymatycznym
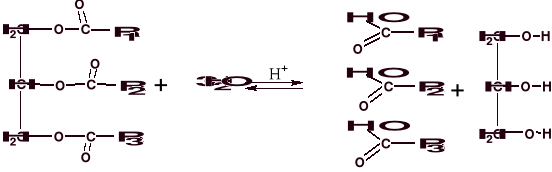
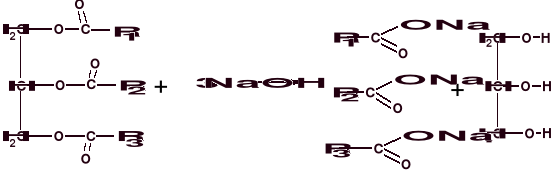
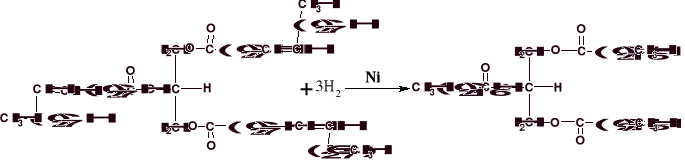
2) aby poprawić przydatność konsumpcyjna tłuszczów i zmniejszyć podatność na utlenianie, poddaje się je reakcjom utwardzania (uwodornienia). Najszybciej ulegają wysyceniu trieny w pozycjach skrajnych sn-1 i sn-3.
3) polepszenie wartości odżywczej tłuszczu osiąga się również w reakcji transestryfikacji (przeestryfikowania), która może zachodzić na drodze: alkoholizy, acydolizy lub transestryfikacji właściwej (wymiany reszt acylowych w wyniku reakcji dwóch lub więcej estrów)
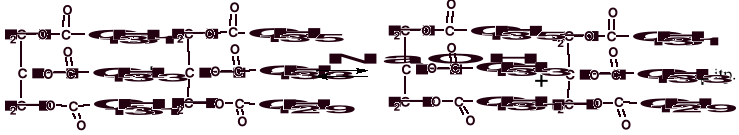
Podobnie jak reakcje hydrolizy, transestryfikacja katalizowana jest przez kwasy, zasady i enzymy z grupy lipaz.
4) tłuszcze zawierające reszty kwasów nienasyconych odbarwiają roztwór wody bromowej i reagują z KMnO4
Liczby określające przydatność spożywczą tłuszczów
Liczba kwasowa - liczba mg KOH potrzebna do zobojętnienia wolnych kwasów tłuszczowych zawartych w 1 g tłuszczu.
Liczba zmydlania - liczba mg KOH potrzebna do zobojętnienia kwasów tłuszczowych wolnych i powstałych w wyniku hydrolizy 1 g tłuszczu.
Liczba jodowa - liczba g wolnego jodu przyłączanego przez wiązania podwójne zawarte w 100 g tłuszczu.
Liczba Lea - liczba cm3 0,002 M tiosiarczanu sodu potrzebna do redukcji jodu wydzielonego z KI przez nadtlenki obecne w 1 g tłuszczu.
Liczba Reicherta-Meissla - liczba cm3 0,1 M KOH zużytego do zobojętnienia lotnych kwasów tłuszczowych oddestylowanych z parą wodną z 5 g tłuszczu. Pozwala określić zawartość kwasów tłuszczowych o długości łańcucha C4-C8.
Do fosfolipidów zalicza się glicerofosfolipidy (glikolipidy) i sfingofosfolipidy (sfingolipidy). Znajdują się one w każdej komórce, a w szczególnie dużym stężeniu występują w tkankach nerwowych, błonie komórkowej i dojrzałych nasionach oleistych.
Glicerofosfolipidy pochodzą od kwasu glicerofosforowego (fosforanu sn-3-glicerolu). 1,2-diacylowany kwas glicerofosforowy nosi nazwę kwasu fosfatydowego. Cząsteczka glicerofosfolipidu zawiera estrowo związany z resztą kwasu ortofosforowego aminoalkohol (np. etanoloaminę, cholinę) lub inny hydroksyzwiązek - serynę, treoninę, inozytol.
Wśród glicerofosfolipidów wyróżniamy m.in. lecytyny (inaczej fosfatydylocholiny, zawierające aminoalkohol cholinę) oraz kefaliny (fosfatydyloetanoloaminy oraz fosfatydyloseryny, zawierające, odpowiednio, etanoloaminę albo serynę).
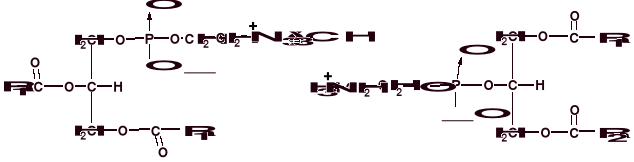
α- fosfatydylocholina (α-lecytyna)
β-fosfatydyloetanoloamina (β- kefalina)
(gdzie R1, R2 - reszty kwasów tłuszczowych)
Składnikiem błon komórkowych są również sfingofosfolipidy, a wśród nich sfingomieliny i cerebrozydy (glikolipidy). To analogi glicerofosfolipidów zawierające aminoalkohol sfingozynę zamiast glicerolu.
Ceramid to N-acylowana sfingozyna. Sfingomieliną natomiast nazywamy ceramidy zestryfikowane kwasem fosforowym, zawierającym przyłączone, również estrowo, cholinę, etanoloaminę lub serynę. Sfingomieliny (fosfatydy) tworzą tzw. mielinę, zewnętrzną osłonkę włókien nerwowych białej substancji mózgu. Wchodzące w skład sfingomielin kwasy tłuszczowe to głównie kwas lignocerowy i nerwonowy.
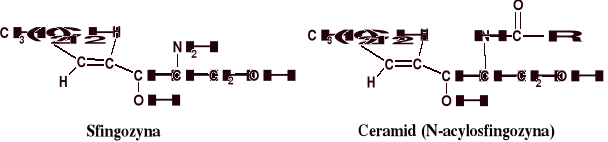
To diglicerydy stanowiące około 10 % fosfolipidów mózgu i mięśni. Swoją budową przypominają kefaliny ale zamiast wiązania estrowego mają przy węglu C1 wiązanie eterowe z resztą wyższego nienasyconego alkoholu. Aminoalkoholem przy węglu C3 połączonym estrowo przez kwas fosforowy może być etanoloamina, cholina, seryna lub inozytol.
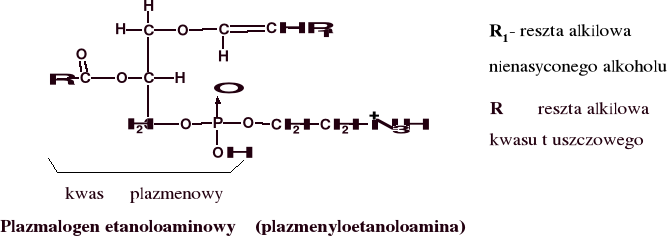
Glikolipidy
Glikosfingolipidy, zwane cerebrozydami występują głównie w mózgu. Są to ceramidy, w których grupa hydroksylowa sfingozyny połączona jest z resztą cukrową (glukoza albo galaktoza) lub łańcuchem oligocukrowym. Bardziej złożone cerebrozydy to gangliozydy - zawierają łańuchy polisacharydowe, często rozgałęzione, złożone z kilku (do siedmiu) reszt cukrów prostych oraz reszty kwasu N-acetyloneuraminowego, zaliczanego do kwasów sjalowych.
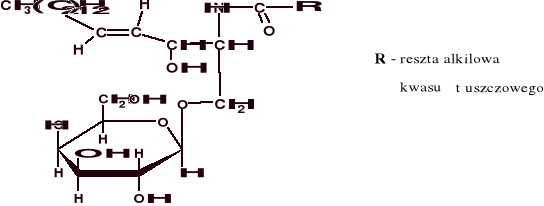
Galaktocerebrozyd (galaktozyloceramid)
Glaktozyloceramid łatwo może być przekształcony w sulfogalaktozyloceramid (przez zestryfikowanie grupy OH przy C3 galaktozy kwasem siarkowym), występującym w mielinie. Związek ten należy do sulfolipidów (sulfatydów).
6. Hormony sterydowe
Sterydy stanowią dużą grupę naturalnych związków organicznych pochodzenia zarówno roślinnego i zwierzęcego, jak i mikroorganicznego. Ich wspólną cechą jest obecność szkieletu węglowego pochodzącego od steranu (1,2-cyklopentano-perhydrofenantrenu).
Przedstawicielem steroli (steroidów zawierających grupę OH w położeniu C3) jest
cholesterol.
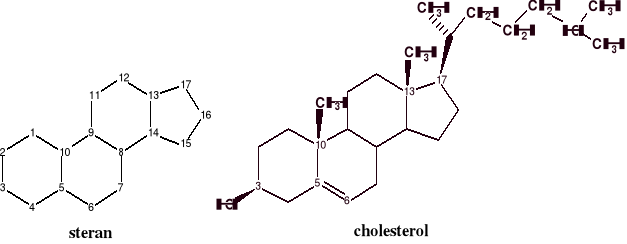
W postaci wolnej lub związanej, cholesterol jest składnikiem błon komórkowych (nadaje im pożądaną płynność i elastyczność), jest podstawowym substratem w syntezie kwasów żółciowych, hormonów płciowych i hormonów kory nadnercza, w tkankach nerwowych wchodzi w skład otoczki mielinowej, stanowiąc 10-15 % suchej masy mózgu. W stanach patologicznych tworzy złogi w postaci kamieni żółciowych oraz odkłada się w ścianach tętnic, co prowadzi do miażdżycy i zawałów serca.
Cholesterol jest sterolem pochodzenia zwierzęcego; jego odpowiednikiem u mikroorganizmów jest ergosterol.
Hormony sterydowe
Należą do nich hormony kory nadnerczy (kortykosterydy) i hormony płciowe gonad.
Kortykosterydy (hormony adrenokortykoidowe) dzielą się na :
mineralokortykosterydy - utrzymują odpowiednie stężenie jonów sodowych i potasowych wpływając na równowagę osmolarną pomiędzy komórką i płynami międzykomórkowymi. Najbardziej znanym hormonem tej grupy jest aldosteron.
glikokortykosterydy - mające wpływ na przemianę węglowodanową, białkową i tłuszczową. Wzmagają odkładanie glikogenu w wątrobie i mięśniach, ułatwiają spalanie glukozy - podnosząc jej poziom we krwi, są antagonistami insuliny. Utrudniają także spalanie tłuszczów oraz działają silnie przeciwobrzękowo, przeciwzapalnie i przeciwreumatycznie. Mają także korzystny wpływ na objawy wywołane wstrząsem, stąd ich zastosowanie w medycynie stanów nagłych. Głównym przedstawicielem glikokortykosterydów jest kortyzol (hydrokortyzon).
Hormony płciowe, wytwarzane przez gruczoły płciowe, dzielą się na: androgeny (hormony męskie) i ginogeny (hormony żeńskie).
Androgeny powodują dojrzewanie płciowe i stymulują męskie wtórne cechy płciowe. Wykazują też działanie anaboliczne pobudzając syntezę białek, powodują więc wzrost masy mięśniowej. Mają zastosowanie w stanach wyniszczenia ustroju po długotrwałych chorobach, po zabiegach chirurgicznych itp. Do androgenów zaliczamy testosteron i produkt jego metabolizmu - androsteron.
Hormony żeńskie - estrogeny (np. estradiol) powodują dojrzewanie płciowe oraz rozwój wtórnych żeńskich cech płciowych. Wspólnie z gestagenami (hormonami ciążowymi, do których należy progesteron), regulują procesy cyklu miesiączkowego.
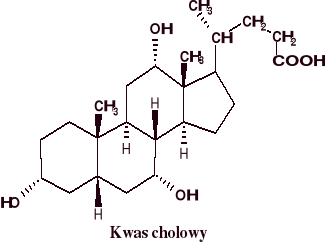
Kwasy żółciowe to steroidy zawierające od 1 do 3 grup hydroksylowych i grupę karboksylową w łańcuchu bocznym. Znanych jest kilka kwasów żółciowych różniących się liczbą grup -OH i ich położeniem. 60 % ogółu kwasów żółciowych człowieka stanowi kwas cholowy (3,7,12-trihydroksycholanowy).
Kwasy żółciowe występują w żółci w formie związanej peptydowo z tauryną jako kwas taurocholowy lub z glicyną (kwas glikocholowy). Do woreczka żółciowego transportowane są w postaci soli sodowych. Sole te, podobnie jak mydła i detergenty, mają właściwości powierzchniowo czynne. Nierozpuszczalne w wodzie składniki pokarmu tworzą z solami kwasów tauro- lub glikocholowych kompleksy, tzw. kwasy choleinowe, mające zdolność do przechodzenia przez ściany jelit.
Prostaglandyny to cykliczne 20-węglowe kwasy karboksylowe, należące do bardzo aktywnych przekaźników biologicznych. Obok prostaglandyn w organizmach ssaków występują podobne do nich związki - prostanoidy, do których należą prostacykliny, tromboksany i leukotrieny. Prekursorami wszystkich tych związków jest kwas arachidonowy i jego analogi.
Prostaglandyny i ich ejkozanowe analogi nazywane są hormonami lokalnymi, ponieważ spełniają funkcję hormonów, ale z powodu niezbyt dużej trwałości mogą oddziaływać tylko lokalnie - na komórki, w których powstały i na komórki leżące w najbliższym sąsiedztwie.
Szkielet prostaglandyn wywodzi się od niewystępującego w naturze kwasu prostanowego:
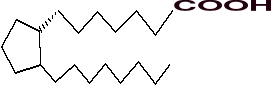
Prostanoidy
Biosynteza prostaglandyn i innych ejkozanoidów zachodzi w mikrosomach. Pierwsza prostaglandyna PGH2, która powstaje z kwasu arachidonowego w obecności cyklooksygenazy, jest bardzo nietrwała i szybko ulega przekształceniu w inne prostaglandyny, prostacykliny i tromboksany.
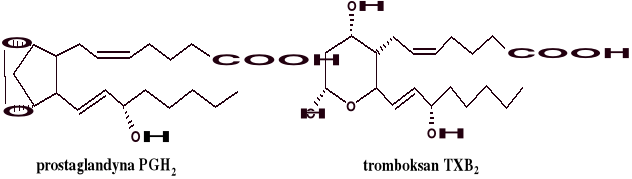
Istnieje kilka głównych grup prostaglandyn. Ich działanie jako regulatorów procesów fizjologicznych jest bardzo zróżnicowane, często antagonistyczne w stosunku do znanych hormonów lub innych prostaglandyn. Prostaglandyna PGF zwęża naczynia krwionośne i oskrzela, hamuje wydzielanie kwasu żołądkowego. Prostaglandyna PGE oraz PGI2 (prostacyklina) rozszerzają naczynia krwionośne i oskrzela. Prostacyklina hamuje agregację krwinek, rozszerza tętnice, uczynnia cyklazę adenylową, zapobiega miażdżycy, przedłuża krwawienie, działa antagonistycznie w stosunku do tromboksanu A2 (TXA2). Prostaglandyny PGE i PGF wywołują skurcz macicy i rozpoczynają akt porodowy. Zaburzenia w wydzielaniu prostaglandyn w czasie ciąży są powodem poronień. Wydzielanie kwaśnego soku żołądkowego hamuje także prostaglandyna PGA. Prostaglandyny odgrywają ważną rolę w pękaniu i wydalaniu pęcherzyków jajnikowych w czasie owulacji. PGF jest powodem bolesnego miesiączkowania. Prostaglandyna PGE hamuje aktywację cyklazy adenylowej w tkance tłuszczowej, zapobiegając lipolizie; zwiększa przepuszczalność naczyń krwionośnych, sprzyja powstawaniu wysięku i stanów zapalnych, wzbudza migrację leukocytów do ogniska zapalnego, zwiększa wrażliwość zakończeń nerwowych na ból. Ponadto zwiększa ciśnienie śródgałkowe, sprzyja powstawaniu stanów zapalnych oka.
Tromboksan A2 zwiększa agregację trombocytów sprzyjając powstawaniu zakrzepów oraz ognisk miażdżycowych, ponadto obkurcza oskrzela. Małe dawki salicylanów zmniejszają syntezę tromboksanu, co zostało wykorzystane w zapobieganiu zakrzepów i zawałów serca.
Niesteroidowe leki przeciwzapalne i przeciwbólowe (np. salicylamid, kwas acetylosalicylowy, propyfenazon, fenylobutazon, ibuprofen) działają leczniczo przez zahamowanie cyklooksygenazy prostaglandynowej, a zatem uniemożliwienie wytwarzania prostaglandyn.
Leukotrieny
Powstają z 20-węglowych kwasów polienowych. Nie należą do prostanoidów, ponieważ nie mają struktury kwasu prostanowego.
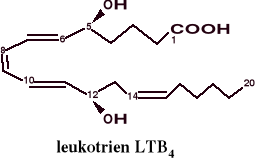
Leukotrieny obkurczają naczynia krwionośne i oskrzela, są przekaźnikiem stanów alergicznych, indukują migrację leukocytów, zwiększają przepuszczalność śródbłonków, uczestniczą w tworzeniu stanów zapalnych w tkankach.
Część praktyczna
1. Rozpuszczalność tłuszczów
Ze względu na obecność długich hydrofobowych łańcuchów kwasów tłuszczowych oraz mało polarnych wiązań estrowych tłuszcze są w wodzie nierozpuszczalne, natomiast dobrze rozpuszczają się w rozpuszczalnikach niepolarnych lub słabo polarnych.
W 5 suchych probówkach umieścić po 5 kropli oleju jadalnego. Następnie do poszczególnych probówek dodać po 1 cm3 wody, acetonu, etanolu, benzenu i chloroformu. Zawartość probówek wymieszać. Określić rozpuszczalność tłuszczu w poszczególnych rozpuszczalnikach.
2. Zmydlanie tłuszczów
Ogrzewanie tłuszczu w środowisku alkalicznym prowadzi do hydrolizy wiązań estrowych w wyniku czego powstają gliceryna i sole kwasów tłuszczowych (mydła).
Do kilku kropli oleju dodać 3-4 cm3 alkoholowego roztworu NaOH i mieszaninę ogrzewać kilka minut we wrzącej łaźni wodnej mieszając. Do mieszaniny dodać 10 cm3 wody destylowanej i silnie wytrząsnąć. Pienienie się roztworu świadczy o obecności mydeł.
3. Wykrywanie kwasów żółciowych - próba Haya
Wysokie napięcie powierzchniowe wody powoduje utrzymanie się na jej powierzchni substancji o ciężarze właściwym większym od wody (np. siarka). Związkami które silnie obniżają napięcie powierzchniowe wody są kwasy żółciowe, które posiadają kilka hydrofilowych grup OH oraz polarną grupę karboksylową.
W jednej probówce umieścić 5 cm3 wody, w drugiej 5 cm3 roztworu żółci. Na powierzchnię obu cieczy nasypać niewielką ilość kwiatu siarczanego (siarki sublimowanej). Początkowo nie mieszać. Zaobserwować różnicę w zachowaniu siarki.
4. Wykrywanie steroli metodą Liebermanna-Burcharda i Salkowskiego
Sterole pochodzenia zwierzęcego i roślinnego zawierające w cząsteczce wiązania podwójne tworzą ze stężonymi kwasami produkty o charakterystycznych barwach. Pod wpływem stężonego kwasu siarkowego (odczyn Salkowskiego) dochodzi do eliminacji dwóch cząsteczek wody i powstania czerwonego kwasu disulfonowego bicholestadienu.
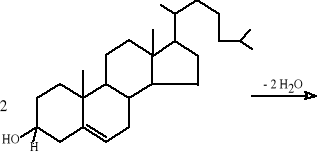
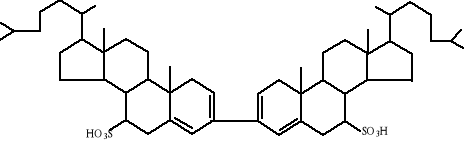
cholesterol _→ kwas disulfonowy bicholestadienu
W obecności stężonego kwasu siarkowego i bezwodnika octowego (odczyn Liebermanna-Burcharda) tworzy się zielono zabarwiony kwas monosulfonowy bicholestadienu.
Reakcja Liebermanna-Burcharda
Do suchej probówki wprowadzić 5 kropli oleju 1 cm3 chloroformu i 0,25 cm3 bezwodnika octowego, wymieszać i podwarstwić 5 kroplami stężonego kwasu siarkowego. Warstwa chloroformowa barwi się na kolor zielony.
Do suchej probówki wprowadzić 5 kropli oleju, 1 cm3 chloroformu i delikatnie podwarstwić kilkoma kroplami stężonego kwasu siarkowego. Warstwa chloroformowa barwi się na kolor brunatno-czerwony.
Metoda ta służy do ilościowego, diagnostycznego oznaczania poziomu cholesterolu w ludzkiej surowicy. W wyniku tej metody wolny cholesterol jest utleniany przez oksydazę cholesterolową do cholest-4-en-3-onu i nadtlenku wodoru. Utworzony nadtlenek wodoru łączy się z 4-aminoantypiryną i kwasem p-hydroksybenzoesowym tworząc czerwony barwnik chinonoiminę. Intensywność powstałego różowego zabarwienia jest wprost proporcjonalna do stężenia cholesterolu w badanej próbce.
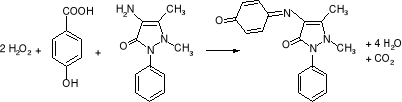
Do suchej probówki wprowadzić 5 cm3 odczynnika CHOLESTEROL DST, a następnie 0,1cm3 (100 l przy użyciu pipety automatycznej) roztworu badanego. Całość probówki wymieszać i inkubować przez 5 minut w łaźni wodnej w temperaturze 37 C. Zmierzyć absorbancję próby badanej względem próby ślepej (5 cm3 odczynnika Cholesterol dst), przy długości fali 520 nm.
Uzyskane zabarwienie jest stabilne przez 30 minut.
Wynik odczytać z krzywej wzorcowej.
6. Oznaczanie liczby jodowej metodą Morgoschesa.
Nienasycone kwasy tłuszczowe mogą przyłączać w miejsce podwójnego wiązania chlorowiec: jod lub brom. Reakcja jodowania jest wykorzystywana w analizie ilościowej tłuszczu (oznaczanie liczby jodowej). Im wyższa liczba jodowa tym silniejszy charakter nienasycony tłuszczu. W przypadku, gdy reakcja jodowania zachodzi w środowisku wodno-alkoholowym do wiązania podwójnego przyłączają się także grupy hydroksylowe:
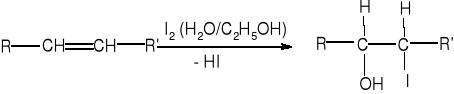
Nadmiar wolnego jodu odmiareczkowujemy mianowanym roztworem tiosiarczanu. W tej metodzie addycja jodu następuje w czasie 4-5 minut. Po dłuższym czasie uzyskuje się wartości wyższe.

Wykonanie oznaczenia:
W zlewce umieścić 15 cm3 roztworu badanego tłuszczu w alkoholu. W przypadku obecności nierozpuszczonego tłuszczu, zlewkę ogrzewać na łaźni wodnej do momentu rozpuszczenia się tłuszczu. Do roztworu dodać 10 cm3 0,2 M alkoholowego roztworu jodu. Dokładnie wymieszać roztwór, natychmiast dodać 100 cm3 wody destylowanej i odstawić pod przykryciem na 4-5 min (nie dłużej!). Po tym czasie nadmiar jodu odmiareczkować 0,1M Na2S2O3 wobec 2 cm3 skrobi, którą należy dodać pod koniec miareczkowania (gdy roztwór uzyska jasnożółtą barwę). Koniec miareczkowania określa nam mleczna barwa roztworu.
Próba kontrolna: w kolbie umieścić 10 cm3 0,2 M alkoholowego roztworu jodu i postępować jak powyżej.
Liczbę jodową Lj obliczamy z uwzględnieniem wartości gramorównoważnika jodu (126.92 g) w odniesieniu do 100 g tłuszczu:
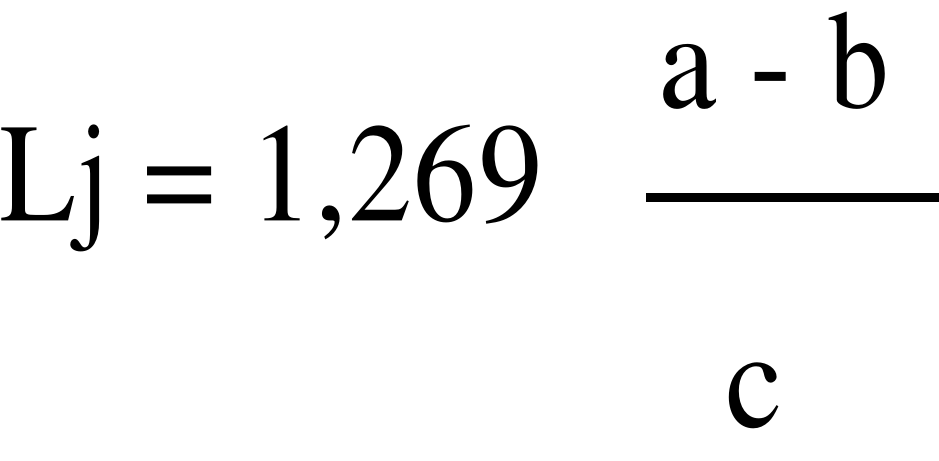
gdzie: a - liczba cm3 0,1 M Na2S2O3 zużyta w próbie kontrolnej
b - liczba cm3 0,1 M Na2S2O3 zużyta w oznaczeniu właściwym
c - ilość tłuszczu w gramach zawartego w badanej próbce (przeliczyć z zawartości w roztworze - oznaczenie na butelkach z roztworami tłuszczów).
Przykładowe wartości liczby jodowej zgromadzono w tabeli.
Nazwa tłuszczu |
Liczba jodowa (środowisko bezwodne) |
Łój barani |
38 - 46 |
Olej słonecznikowy |
119 - 135 |
Olej palmowy |
51.5 - 57 |
Oliwa z oliwek |
79 - 88 |
Smalec |
46 - 70 |
Mleko |
26 - 50 |
Tran |
121 - 146.6 |
Masło |
25-40 |
5
Wyszukiwarka