000Entalpia - sposób obliczania
-ciała stałe i ciecze i=u+pv, gdzie v - obj. właść., p - bezwzględne ciśnienie statyczne, u - właściwa energia wewnętrzna
-gaz doskonały (funkcja tylko temp, nie zależy od ciśnienia i objętości) i=cpT+uo, gdzie cp - ciepło wł. przy stałym ciśnieniu, T - temp, uo - energia otoczenia
-gaz półdoskonały (funkcja tylko temp)
; gdzie
- średnie ciepło właściwe od 0 doT, T - temp
-para nasycona mokra i=i`+x(i``-i`), gdzie i - entalpia pary nasyc. mokrej, i` - entalpia cieczy, i`` - ilość pary suchej nasyconej, x - stopień wilgotności
-para przegrzana i=i``qp, gdzie qp - ciepło przegrzania pary
-para mokra nasycona i=q+r+pr, gdzie r - entalpia parowania
Układ termodynamiczny to dowolnie wybrana część wszechświata, której zachowanie jest rozpatrywane na podstawie zasad termodynamiki. Pozostały świat to Otoczenie termodynamiczne.
000 Roztwory gazów dosk:
Gazy mieszają się dokładnie tworząc roztwory. Przykładami takich roztworów są: powietrze, spaliny. Każdy gaz wchodzący w skład roztworu znajdującego się w stanie równowagi td jest w nim równomiernie rozmieszczony w całej przestrzeni o objętości V zajętej przez roztwór i ma temperaturę T jednoznaczną z temperaturą całego roztworu. Własności roztworów zależą bezpośrednio od ich składu chemicznego. Skład chemiczny roztworu określa się za pomocą udziałów składników. Udział składnika zdefiniowany jest jako stosunek ilości składnika do ilości całego roztworu. W zależności od sposobu określania ilości substancji tworzy się różnego rodzaju udziały:
Udział masowy składnika i roztworu- gi = mi / m
jest stosunkiem ilości tego składnika mi, określonej za pomocą masy, do ilości m całego roztworu wyrażonej w tych samych jednostkach.
Udział molowy składnika i roztworu - zi = ni / n
Jest stosunkiem liczby kilomoli ni tego składnika do liczby kilomoli roztworu n , równej sumie kilomoli wszystkich składników n=∑ni
Udział objętościowy składnika i roztworu- jest to stosunek objętości samego tylko składnika Vi do objętości całego roztworu V wziętych przy tych samych ciśnieniach i temperaturach:
- ri = Vi/V przy: p,T- constans
Stężenie roztworu c=n/V
Ciśnienie składnikowe pi składnika roztworu gazów doskonałych jest ciśnieniem składnika, jakie wywierałby na on gdyby sam zajmował całą objętość roztworu V w tej samej temperaturze co roztwór. Zgodnie z równaniem stanu gazów dosk.:
piV=niRT -----pV=nRT czyli udział molowy lub objętościowy wynosi zi=ri=pi/p
000 Co to jest strumień czynnika termodynamicz.?
Obliczamy za pomocą średniej prędkości przepływu. Jeżeli na przykład przewodem rurowym o przekroju F [m2] płynie strumień z szybkością w [m/s] to wzór na strumień objętości wygląda
Strumień substancji
[kg/s] oblicza się mnożąc objętość przez gęstość substancji
gdy
= idem to jest to warunek ciągłości strugi.
000 Parametry układu termodynamicznego:
Objętość właściwa-objętość zajmowana w dowolnych warunkach przez substancję o masie 1 kg, wyrażona w metrach sześciennych na kilogram. Jest odwrotnością gęstości.Objętość właściwa odnosi się zwykle do gazów i jest jedną z funkcji stanu. Znając jej wartość i wartość dowolnego innego parametru stanu, można wyznaczyć pozostałe funkcje i parametry stanu.
Gęstość-masa jednostki objętości, dla substancji jednorodnych określana jako stosunek masy m do objętości V:
Gęstość jest cechą charakterystyczną substancji, a w określonych warunkach standardowych stanowi jedną z najważniejszych cech substancji - służy do obliczania masy i ciężaru określonej objętości substancji.
Ciężar właściwy-γ, stosunek ciężaru ciała do jego objętości:
W odróżnieniu od gęstości, ciężar właściwy zależy też od siły ciążenia, czyli w warunkach nieważkości wynosi zero, gdy gęstość pozostaje taka sama (podobnie jak masa). γ stanowi ciężar odniesiony do jednostki objętości płynu:γ = ρ g. Jednostką ciężaru właściwego jest 1kg / (m2 s2 ), co wynika z poniższego zapisu:(kg/m3 )(m/s2) = (N m)(g m3 s2) = (N m s2)/(m m3 s2) = (N/m2)(1/m) = Pa/m
Temperatura- jest miarą stanu cieplnego danego ciała. Temperaturę można ściśle zdefiniować tylko dla stanów równowagi termodynamicznej, z termodynamicznego bowiem punktu widzenia jest ona wielkością reprezentującą wspólną własność dwóch układów pozostających w równowadze ze sobą. Temperatura jest związana ze średnią energią kinetyczną ruchu i drgań wszystkich cząsteczek tworzących dany układ i jest miarą tej energii.
5Ciśnienie-to wielkość skalarna określona jako wartość siły działającej prostopadle do powierzchni podzielona przez powierzchnię na jaką ona działa, co przedstawia zależność:
W przypadku gazów w stanie ustalonym w spoczynku, ciśnienie jakie gaz wywiera na ścianki naczynia jest funkcją objętości, masy i temperatury i dlatego w termodynamice traktowane jest jako funkcja stanu.
Strumień objętościowy-(objętościowe natężenie przepływu) - iloczyn prędkości (v) czynnika przepływającego przez przewód rurowy (rurę) i powierzchni przekroju S tego przewodu.Q = vS
7.Gaz doskonały definiować można zarówno na poziomie mikroskopowym (przez podanie właściwości elementów, z których jest zbudowany), jak i na poziomie makroskopowym (poprzez podanie jego właściwości jako całości). Równanie stanu - równanie Clapeyrona
Pełna postać równania stanu gazu doskonałego jest następująca:p V = n R T i nazywane jest ono równaniem Clapeyrona. Przy czym p oznacza ciśnienie gazu, V - objetość, T - temperaturę, n - liczbę moli gazu a R jest tzw. stałą gazową równą R = 8, 314 J/mol·K. Nic nie przeszkodzi, używając związku R = NA k zapisać równania następująco:p V = N k T gdzie k = R / NA jest stałą Boltzmanna.Na uwagę zasługuje fakt, że wymiarem prawej (i lewej) strony jest wymiar energii.
8.Gaz pół doskonały-Gaz półdoskonały różni się tym od gazu doskonałego, że w jego drobinach występują drgania atomów. Gaz rzeczywisty zachowuje się jak gaz półdoskonały lub doskonały pod dostatecznie niskim ciśnienie.
9.Prawa do gazu doskonałego-1) Boylea Mariottea Jeżeli w =idem to p*V=idem 2)GayLussaca- Charlesa
Jeżeli p= idem to objętość właściwa to objętość właściwa V=V0(1+T);V/T=idem V0-obj.wł gazu w temp 00C -termiczny wsp rozszerzalności objętości gazu odniesiony do obj V0 jest ustalony eksperymentalnie (1/273,15) *(1/K)Założymy że t=idem
p-stałe ciśnienie bezwzgl [N/m2] V- objętość właściwa [m3/kg] R-indywidualna stała gazowa [Nm/kgK]T-t emp benzyny 3)Awogadra liczba drobin zawartych w jednakowej objętości różnych gazów doskonałych w tych samych warunkach termicznych (temp i ciśnienie gazów jest takie same)
(MR) jedn indywidualnej stałej gazowej 8314 [J/kmolK]
R=(MR)/M
M1*R1= M2*R2= M*R
P*V=R*Tp(MV)=MR*T
P*V=m*R*Tp*V=n(MR)*T
MV;(MR)(B)nie zależy od rodzaju gazu
n,m- masy
10.Prawo Daltona-Prawo ciśnień cząstkowych zostało opublikowane przez Daltona w 1810 r. Głosi ono:"Ciśnienie wywierane przez mieszaninę gazów jest równe sumie ciśnień wywieranych przez składniki mieszaniny, gdyby każdy z nich był umieszczany osobno w tych samych warunkach objętości i temperatury, jest ono zatem sumą ciśnień cząstkowych." W formie matematycznej można je wyrazić jako:
p=pps+ph ps-pow. Suchego h- porcjalne pary wodnej.
11.Ciepło właściwe- Całkowite ciepło przejęte przez ciało o masie m podczas podgrzewania od T1 do T2 jest równe ciepłu dostarczonemu z zewnątrz i ciepłu tarcia (ciepło wewnątrz ciał) Qc 1-2 =Q1-2+Qf przy czym ![]()
przekształcając wg. ![]()
![]()
![]()
Średnie ciepło właściwe ![]()
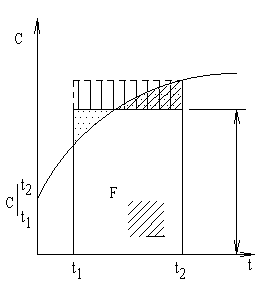
jest to ilość ciepła jaką należy dostarczyć jednej jednostce ilości substancji, aby zmienić temperaturę o 1K w całym rozpatrywanym okresie temp. Zależy od:rodzaju ciała ,temperatury t1 t2,warunków ogrzewania ciał. Stosunek Cp/Cv=χ Jeżeli mam ciało masie m i podgrzewam od t do Δt+t to nastąpi przyrost ciepła ΔQc ![]()
![]()
![]()
-rośnie wraz ze wzrostem t i jest wysokością prostokąta o szerokości (t2-t1). F pole figury nieregularnej równe polu prostokąta o wysokości. Wielkości ciepła właściwego C i szerokości t2-t1. Pole figury F=(t2-t1)*c
12..I zasada termodynamiki- W układzie odosobnionym tzn. osłoniętym osłoną adiabatyczną, ilość energii wewnętrznej układ jest stała Ed=ΔEu+Ew [J] ⇒ równ bilansu energetycznego można traktować jako I zasadę termodynamiki dot. Układu zamkniętego. Energia doprowadzona do układu wyodrębnionego osłoną adiabatyczną pozostaje częściowo w układzie a część jest wyprowadzona z układu. Interpretacja graficzna - wykr. Sankeya
Jeżeli układ działa w sposób ustalony (jego energi nie zmienia się w czasie lub zmienia się w sposób periodyczny i po skończonej liczbie cykli wraca do wart. Początkowych) to bilans energetyczny przyjmuje postać ![]()
ponieważ ![]()
to do czynnego silnika ![]()
że jest rzeczą niemożliwą skonstruowanie perpetum mobile pierwszego rodzaju (silnika pracującego bez zasilania energią z zewnątrz). ![]()
![]()
Zmiana energii wewnętrznej układu zamkniętego jest równa energii, która przepływa przez jego granice na sposób ciepła lub pracy. [1]
dQ=dV+pdV dQ=dV+dL - 2 postacie
13.Pojęcie pracy bezwzględnej- Jest to praca wykonana przez czynnik termodynamiczny wtedy gdy ciśnienie otoczenia jest równe zero. Pracę tę można obliczyć rozpatrując układ cylinder - tłok
Przy ∞ małym dx czynnik wykonuje pracę dl=kdx, gdzie k - siła, dx droga. Przy pracy bez tarcia siłę k równoważy ciśnienie działające na tłok. Stąd: k=pA, gdzie p - ciśnienie, A- przekrój, dl=p A dx ⇒ dl=p dv, p - bezwzględne ciśnienie statyczne wewn. Cylindra, dv - przyrost objętości w cylindrze
14.Praca bezwzględna ![]()
; interpr. graficzna (założenie - znam zależność p od v)
L1-2 - zależy od drogi przemiany a nie tylko od stanu początkowego i końcowego
L1-2 - dotyczy przemian zachodzących bez strat na rzecz tarcia (wtedy dl <pdv)
Zastosowanie: w układach otwartych i zamkniętych, pseudoodwr. dl = p dv - dlt = p dv - dQf stąd dl < p dv
dlt - praca na rzecz tarcia, dQf - ciepło na rzecz tarcia
15.Praca techniczna-
Pracę fizyczną rozpatrujemy wg idealnej maszyny przepływowej tzn.
nie występuje tarcie poruszających się względem siebie powierzchni
zawory nie stawiają oporu
w wewnętrznym zwrotnym położeniu tłok dotyka cylindra
Praca techniczna element. dLt = -Vdp, Lt>0 gdy dp<0
Praca skończona Lt 1-2 = ![]()
dLt>0 gdy dp<0; dLt<0 gdy dp>0
16.Przemiany termodynamiczne gazów doskonałych: Przemiany termodynamiczne
izobaryczna (p=const)
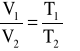
, ![]()
![]()
, Lt1,2 = 0, , ![]()
izochoryczna (V=const)
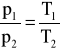
,![]()
, ![]()
, ![]()
, ![]()
c) izotermiczna (T=const)
![]()
, ![]()
, ![]()
, ![]()
d) adiabatyczna (Q=const)
![]()
![]()
, ![]()
![]()
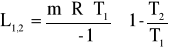
, ![]()
![]()
politropowa
![]()
![]()
, ![]()
,
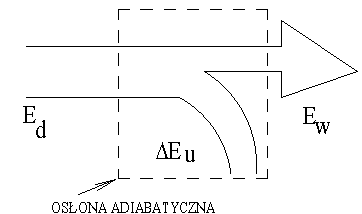
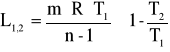
, ![]()
, 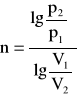
![]()
![]()
, ![]()
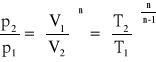
17.II zasada termodynamiki
Clausjusa ciepło nie może przejść samorzutnie od ciała o temp niższej do ciała o temp wyższej. Aby spowodować taki przepływ ciepła musimy zastosować lewo bieżną maszynę cieplną i wkładać do niej energię z zewnątrz, tzn. wywoływać zmiany w innych ciałach
Cornota-niemożliwy jest proces którego jedynym efektem jest zamiana ciepła pobranego ze żródła na równoważną mu prace.
ENTROPIA `S' Jest to funkcja stanu termodynamicznego, której zmiana równa się ilorazowi dostarczonego ciepłą i temperatury ![]()
; S - entropia całkowita
![]()
; s - entropia właściwa w odniesieniu do 1kg czynnika; dla źródła ΔS = - ![]()
źródło oddaje energię więc przyrost entropii jest ujemny. Entropia mówi nam o kierunku przemian zachodzących w przyrodzie.
Jeżeli układ jest jak na rys. i założenie: do tłok + cylinder możemy doprowadzić ciepło Q ze źródła ciepłą, przy czym Q = idem. Do cylindra mogę doprowadzić substancję o ilości dm i entropii właściwej s.
Wyróżniamy dwa przypadki:
I przemiana odwracalna
Tcz = Tźr ; b) brak tarcia dQt = 0
przyrost entropii układu odosobnionego Δs = π, natomiast elementarny przyrost ozn. dπ = ds.u+dsot
![]()
- przyrost entropii układu
![]()
- przyrost entropii otoczenia
![]()
![]()
Wniosek: W układzie odosobnionym sumą przyrostów entropii wszystkich ciał uczestniczących w zjawisku odwracalnym jest = 0. Warunek ten jest spełniony nawet w najmniejszej części zjawiska.
II przemiana nieodwracalna tzn. tźr≠tcz
18.Obieg termodynamiczny
Obieg prawobiezny- praca jest dodatnia czyli urządzenie wytwarza energię. Qz=Lob+Qotocz. W cylindrze którego zawory są zamknięte trzyatomowy gaz doskonały podlega trzem przemianom. 1-2 adiabata, 2-3 izobara, 3-1 izochora.
Obieg lewobrzeżny-do urządzenie doprowadzana jest energia. Qd+|Lob|=Qw E-wydajność urządzenia chłodniczego. Ech=Qd/|Lob|
Obieg sprężarki chłodniczej gazowej `'parowej'', pompy ciepła
Obieg Carnota:
1-2 izotermiczna ekspansja następuje pobór ciepła
2-3 izentropowa ekspansja
3-4 kompresja izotermiczna następuje oddanie ciepła
4-1 kompresja izentropowa
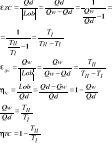
19.Zmiana stanu skupienia
Stopień suchości- jest to stosunek masy nasyconej suchej do pary mokrej.
Objętość właściwa pary mokrej- suma objętości cieczy w punkcie pęcherzyków i pary suchej nasyconej.
Entalpia właściwa-Dla entalpii właściwej można zapisać wzór definicyjny w następującej postaci:
gdzie:
— energia wewnętrzna właściwa
— objętość właściwa.
20.Powietrze wilgotne
Wilgotność bezwzględna-(gęstość wilgotności)- ro= mw/V
Wilgotność względna- fi=mw/mwn w-pary wodnej wn-pary w. nasyconej
Wilgotność właściwa- x=mpw/mps
Entalpia pary wilgotnej- jest równa sumie entalpi pow. Suchego i pary wodnej. i=(cp+xcpw)t+xr (cp+xcpw)=c
21.Elementy techniki cieplnej-
przewodzenie ciepła - przenoszenie ciepła w obrębie danego ciała od jednych drobin do drugich lub przez dyfuzję
konwekcja - (unoszenie ciepła) ciepło płynie z cząsteczkami płynu od ściany przegrody do rdzenia strumienia lub odwrotnie
promieniowanie - ciepło przenosi się od jednego ciała do drugiego w postaci energii promienistej (za pośrednictwem fal elektromagnet)
![]()
Prawo FOUTIERA-gęstość przewodzonego strumienia ciepła jest wprost proporcjonalna do gradientu temperatury
lub w postaci skalarnej
Prawo NEWTONA- Q =A-α(tf - tw)τ, gdzie tw - temp pow ciała stałego, tf - temp opływającego płynu, α - współczynnik, τ - czas, A - powierzchnia
α - ozn. ilość wymienionego podczas przejmowania przez jednostkę powierzchni w ciągu jednostki czasu.Przewodzenie - polega na przenoszeniu ciepła w obrębie danego ciała od jednych drobin do drugich, odbywa się tylko gdy drobiny ciała nie podlegają przesunięciom makroskopowym. Warunek spełniony podczas przepływu ciepła przez ciała stałe
Prawo PLANCA- prawo opisujące emisję światła przez ciało doskonale czarne znajdujące się w danej temperaturze.Zgodnie z nim emisja (i absorpcja) światła odbywa się w porcjach (kwantach) o energii hν, gdzie h - stała Plancka, ν - częstotliwość fali światła, a zależność zdolności emisyjnej ε od częstotliwości fali ν i temperatury T wyrażona jest wzorem (tzw. wzór Plancka):
gdzie c - prędkość światła, k - stała Boltzmanna.
E=(C1lambdat-s)/(ec2/lambdatT-1)
Prawo STEFANO-BALTZMANA- opisuje całkowitą moc wypromieniowywaną przez ciało doskonale czarne w danej temperaturze. Zostało opracowane w 1879 przez Jožefa Stefana i Ludwiga Boltzmanna.
gdzie, Φ - strumień energii wypromieniowywany w kierunku prostopadłym do powierzchni ciała [W / m2] , σ - stała Stefana-Boltzmanna , T - temperatura w skali Kelvina E=Co(T/100)
Prawo LAMBERTA- opisuje pochłaniane promieniowania elektromagnetycznego przy przechodzeniu przez częściowo absorbujący i rozpraszający ośrodek.Prawo może być matematycznie sformułowane na kilka sposobów: Absorpcja promienia światła przechodzącego przez kuwetę o na odcinku o długości l. Efi=Eocos(fi)
MECHANIKA PŁYNÓW
27.TEMPERATURA - jest miarą średniej energii kinetycznej atomów lub molekuł płynu. Do pomiaru temperatury można użyć przyrządu opartego na zależności temperatury od określonej właściwości płynu ( objętość , ciśnienie , przewodność cieplna i inne ).Podstawową jednostką temperatury bezwzględnej jest KELWIN [ K ].Dopuszcza się stopnie CELCJUSZA [0C ] przy czym: 0 0C = 273,16 K (zero stopni Kelwina w skali Celsjusza wynosi -273,16 0C).
28.CIŚNIENIE - stanowi sumaryczny efekt zderzeń molekuł z powierzchnią ściany lub powierzchnią zanurzonego ciała w płynie. W ujęciu fenomenologicznym, tzn. bazującym na molekularnej strukturze płynów, ciśnienie p, mierzone w [Pa ] wynosi p = F / A , F - parcie, [N], A - powierzchnia działania parcia, [m2]
Jednostką ciśnienia w układzie jednostek SI jest PASKAL [Pa]
29.GĘSTOŚĆ - przez gęstość ρ rozumiemy masę płynu odniesioną do jednostki objętości stąd:ρ = lim (Δm/ΔV) = dm/dV. Dla płynu w równowadze termodynamicznej gęstość wyraża zależność:ρ = m / VJednostką gęstości w układzie SI jest 1 kg/m3.
30.LEPKOŚĆ - czyli TARCIE WEWNĘTRZNE jest to zdolność płynu do przenoszenia naprężeń stycznych między sąsiednimi warstwami płynu, poruszającymi się z różnymi prędkościami względem siebie. Naprężenia styczne w płynie powstają także między płynem a ciałem stałym, np. ścianką zbiornika lub przewodu. Naprężenia stycznie nie występują w stanie spoczynku płynu. Miarą lepkości jest - DYNAMICZNY WSPÓŁCZYNNIK LEPKOŚCI - μ (mi) ![]()
31.RÓWANIE RÓWNOWAGI STATYCZNEJ:
Równowaga dotyczy równoważenia się sił masowych i sił powierzchniowych, co zapisuje się w postaci:
Fxdx+Fydy+Fzdz=dp/ro
![]()
,gdzie
i, j, k - wektory jednostkowe osi współrzędnych (wersory),
∂p/∂x, ∂p/∂y, ∂p/∂z - pochodne cząstkowe.
ρFm = gradp = 0
Jest to wektorowy zapis równania równowagi płynu w postaci różniczkowej.
W układzie współrzędnych kartezjańskich równanie (6) można zapisać w postaci trzech równań skalarnych, a mianowicie ![]()
w których X, Y, Z stanowią składowe jednostkowej siły masowej Fm w kierunkach trzech osi współrzędnych x, y, z. Mnożąc stronami równania (7) odpowiednio przez dx, dy, dz otrzymuje się:
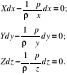
Z kolei, sumując te równania stronami, dostaje się; ρ( Xdx + Ydy + Zdz ) = (∂p/∂x)dx + (∂p/∂y)dy + ∂p/∂z)dz .Prawa strona zależności (9) jest różniczką zupełną dp, co można zapisać to krócej:
ρ( Xdx + Ydy + Zdz) = dp
32.Napór na powierzchnie płaskie siła nacisku jaką płyn wywiera na daną powierzchnię. Siła ta jest normalna do danej powierzchni.Parcie jest związane z ciśnieniem wzorem
gdzie:
- wektor powierzchni nieskończenie małego fragmentu ds powierzchni S, p - ciśnienie hydrostatyczne panujące na poziomie, na którym znajduje się powierzchnia ds. Dla powierzchni płaskich i stałego ciśnienia w każdym punkcie powierzchni, wzór na parcie upraszcza się do postaci
Płyn w stanie spoczynku wywiera napór hydrostatyczny zarówno na dno jak i ścianę naczynia.Parcie na ścianę poziomą można zapisać
33.Wypór hydrostatyczny- siła stanowiąca wypadkową naporów hydrostatycznych działających na ciało częściowo lub całkowicie zanurzone w cieczy. Wypór skierowany jest przeciwnie do siły ciężkości, a jego wartość określa prawo Archimedesa. Zaczepiony jest umownie w tzw. środku wyporu, który pokrywa się ze środkiem masy wypartej cieczy. W przypadku statku lub jachtu wypór w warunkach statycznych równa się wyporności.
34.Równowaga wzgledna cieczy Równowaga względna. Jeżeli punkt materialny jest w równowadze (czyli spoczynku) względem układu ruchomego, to przyśpieszenie względne jest pw=0, a prędkość względna t>(O=0.Wynika stąd, że również przyśpieszenie Coriolisa jest pc=0, a zatem i siła Coriolisa Pc=0. Z równania (II), str. 137, otrzymamy więc (I) Pb + Pu=0. A więc: gdy punkt jest w równowadze względnej, silą bezwzględna równoważy się z silą unoszenia. Równowaga względna cieczy jest w przypadku, gdy ciecz jest spoczynku względem własnych cząstek.
35.Pochodna substancjonalna Ta pochodna dH/dt nosi nazwę pochodnej substancjonalnej dowolnej wielkości fizycznej. Pochodna ta jest sumą pochodnej lokalnej ∂H/∂t i pochodnej konwekcyjnej (v⋅∇)H. Pochodna ∂H/∂t oznacza zmianę wielkości H w czasie
36) POCHODNA SUBSTANCJALNA
Niech będzie rozważana wielkość fizyczna H, tzn. taka że:
H = f ( x, y, z, t ). V=(Vx, Vy, Vz)
Różniczkując cząstkowo tę zależność, otrzymuje się:
dH = (∂H/∂t)dt + (∂H/∂x)dx + (∂H/∂y)dy + (∂H/∂z)dz
Dzieląc stronami przez dt, dostaje się:
dH/dt = ∂H/∂t + (∂H/∂x)(dx/dt) + (∂H/∂y)(dy/dt) + (∂H/∂z)(dz/dt)
Zauważmy, że dx/dt = vx; dy/dt = vy; dz/dt = vz, tj. są to odpowiednie składowe prędkości v w kierunku osi współrzędnych x, y, z.
Wobec tego zapis wyrażenia (5) upraszcza się do postaci:
dH/dt = ∂H/∂t + (∂H/∂x)vx + (∂H/∂y)vy + (∂H/∂z)vz
∂H/∂t - pochodna lokalna
(∂H/∂x)vx + (∂H/∂y)vy + (∂H/∂z)vz - pochodna konwekcyjna
Pochodna ∂H/∂t oznacza zmianę wielkości H w czasie.
![]()
,![]()
-przyśpieszenia lokalne
![]()
- przyspieszenia unoszenia
37) POLA FIZYCZNE
POLEM FIZYCZNYM nazywamy obszar, w którym każdemu punktowi w każdej chwili czasu jest jednoznacznie przyporządkowana określona wartość wielkości fizycznej (parametru) płynu. Mogą być różne pola fizyczne, jak pole ciśnienia, temperatury, prędkości i inne. Zespół pól określa przepływ płynu, stąd wynika klasyfikacja przepływów:
pole ustalone, jeśli wielkość fizyczna nie zależy od czasu: ∂H/∂t = 0
![]()
H = f (x, y, z );
pole nieustalone, jeśli wielkość fizyczna zależy od czasu: ∂H/∂t ≠ 0 i wobec tego H = f ( x, y, z, t );
pole jednorodne i niejednorodne, gdy wielkość fizyczna jest stała lub niestała;
pole ciągłe i nieciągłe;
pole źródłowe i nieźródłowe;
pole wirowe i bezwirowe (potencjalne ): wirowe - u ≠ 0; ω ≠ 0;
bezwirowe - u ≠ 0; ω = 0 (ω - prędkość kątowa);
pole skalarne, wektorowe, tensorowe; jeśli wielkość fizyczna jest skalarem lub wektorem, lub tensorem;
pole jedno-, dwu- i trójwymiarowe (liniowe, płaskie, płaskie osiowo-symetryczne i przestrzenne).
Równanie ciągłości:
Dla osi x:
![]()
Dla osi y:
![]()
Dla osi z:
![]()
![]()

R+A=0
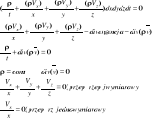
DYNAMIKA PŁYNU DOSKONAŁEGO
38) Równanie Eulera, równanie ruchu Eulera, siły działające w płyn
Siły powierzchniowe i siły masowe
![]()
39) Równanie bernulliego
Założenia
-ciecz jest nieściśliwa
- ciecz nie jest lepka
- przepływ jest stacjonarny i bezwymiarowy
Wyprowadzenie wzoru bernulliego
- przepływ jednowymiarowy, przepływ bezwirowy
![]()
równanie Eulera dla przepływu jednowymiarowego
przepływ ustalony
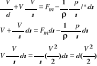
siły masowe są potencjalne
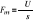
U-potencjał
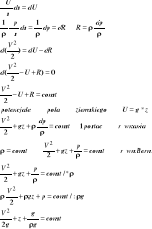
Interpretacja graficzna
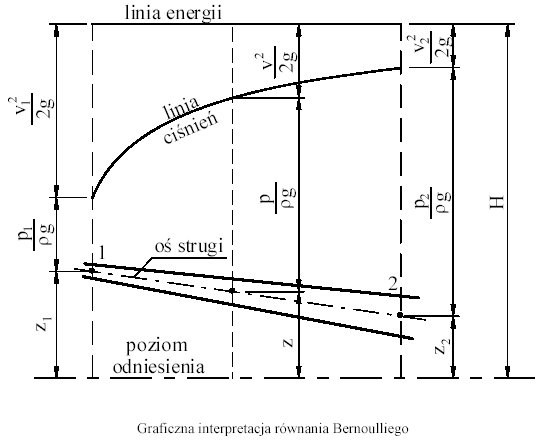
DYNAMIKA PŁYNÓW RZECZYWISTYCH
40) Prawo Hagena-Poiseuille'a
gdzie poszczególne symbole oznaczają:
ΦV - strumień objętości przepływu,
V, dV/dt - objętość, pochodna objętości względem czasu,
z - współrzędna walcowa, długość liczona wzdłuż osi przewodu,
vs - średnia prędkość płynu w kierunku z,
r - promień wewnętrzny przewodu,
η - współczynnik lepkości dynamicznej płynu,
p - ciśnienie uśrednione w przekroju przewodu,
-dp/dz - gradient ciśnienia wzdłuż osi z,
Δp - różnica ciśnień na końcach przewodu,
l - długość przewodu.
równanie Hagena-Poiseuille'a - przepływ laminarny w przewodzie kołowym
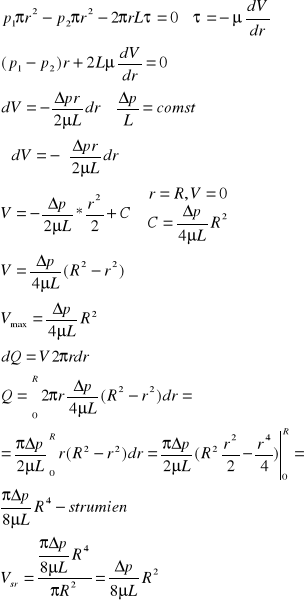
![]()
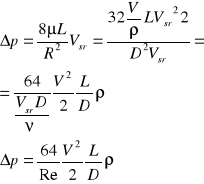
41) Istota przepływu laminarnego i turbulentnego
Ruch laminarny (warstwy się nie nakładają) tory cząstek mało różnią się od siebie. Pozostające w ruchu medium można traktować jako zbiór oddzielnych warstw, poruszających się względem siebie z różną prędkością i nie mieszających się ze sobą. Ruch taki występuje w mediach o dużej lepkości (μ), np. lawa wulkaniczna. Re<2300
Ruch turbulentny ( warstwy mieszają się ze sobą) ruch cząstek płynu powoduje mieszanie się ze sobą rożnych warstw, Ruch ten występuje w mediach o względnie malej lepkości (μ), np. woda, powietrze. Re>50000
42) Równanie Darcyego-Weisbacha-równanie opisujące spadek ciśnienia płynu na skutek oporów jego przepływu w przewodzie.
![]()
λ - współczynnik oporu - f(Re)
v - prędkość płynu
ρ - gęstość płynu
Porowatość ośrodka w ogólności ![]()
Porowatość powierzchniowa ![]()
Przepływ w ośrodku porowatym (prawo Darcyego)
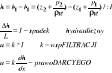
Dopływ do rowu
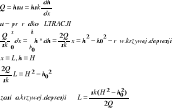
Dopływ do studni
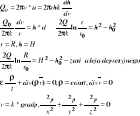
43) opory przepływu, opór tarcia i miejscowy (od czego zależą od Re i chropowatości - współczynnik oporu λ(Re, ε)
- poszukujemy funkcję zależną od zjawisk fizycznych
![]()
n=6, i=3 => n-i=3 poszukujemy funkcji o 3 wielkościach f(π1, π2, π3)=0
-poszukujemy funkcji o wielkościach (ρ, V, D)
ρa1 Va2 Da3=1
- parametry bezwymiarowe z pozostałych wielkości
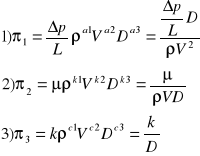
- poszukujemy funkcji
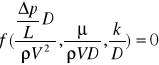
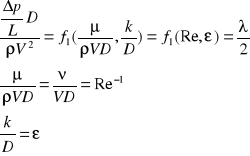
44) uogólnione prawo Bernoulliego + ze stratami
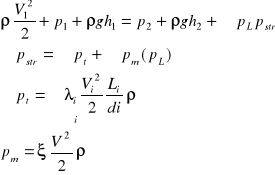
- współczynnik ξ możemy obliczyć dla nagłego rozszerzenia przewodu
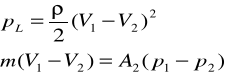
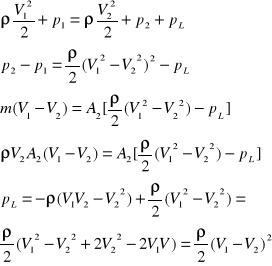
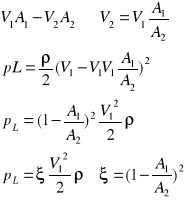
45) przepływy w kanałach otwartych, równanie jednostronne, prędkość, przekrój optymalny, wzór chezy'ego
- wzór chezy'ego
![]()
- przekrój optymalny- max strumień objętości przepływający kanałem o stałym nachyleniu i stałym przekroju poprzecznym- kształt okrągły będzie najbardziej optymalny
46) Opadanie swobodne cząstek

47) Siła oporu profilowanego - występuje zawsze gdy V>0
![]()
Rotametr - przyrząd do pomiaru strumienia objętości

dx - odległość przesunięcia tłoka
Jeżeli:
dv>0 to dl>0
dv<0 to dl<0
Lt=Ln+L1-2+Lw+L1-2+p1v1-p2v2
Ln - praca napełniania
L1-2 - praca przemiany zamknietej
Lw - praca wytłaczania
zał. p1>p2
w.z.p. - przemiana napełniania
z.z.p. - ilość czynnika = const
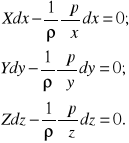
Wyszukiwarka