Węglowodany
CUKRY - SACHARYDY Cn(H2O)n
to polihydroksydyaldehydy lub ketony lub związki, które po hydrolizie dają wyżej wymienione.
PODZIAŁ:
kryterium stanowi ilość jednostek cukrowych budujących cząsteczkę
I cukry proste II di (bi) sacharydy III polisacharydy
kryterium stanowi liczba atomów węgla w pojedynczym łańcuchu cząsteczki cukru prostego
triozy, tetrozy, pentozy i.t.d.
Cukry proste - reaktywność
Reakcje z wodorotlenkiem miedzi (II):
na zimno - sąsiednie grupy - OH tworzą wiązania donorowo - akceptorowe z wodorotlenkiem miedzi (II)
na gorąco - biegnie utlenienie do kwasu aldonowego - ulegają tej reakcji zarówno aldozy jak i ketozy.
CHO C HOH CH2OH
║
CHOH COH C=O keton i aldehyd ulegając enolizacji (w środowisku zasadowym dają
ten sam enol - dają ten sam produkt utlenienia - kwas aldonowy
Cukry proste mają własności utleniające - ulegają próbie Tollensa, Trommera, Fehlinga (Cu 2+ w wodnym roztworze winianu sodu), Benedicta (Cu 2+ w wodnym roztworze cytrynianu sodu) - niektóre testy dla diabetyków wykorzystują test Benedicta - czułość do 0,1 % glukozy w moczu.
Wydłużanie łańcucha cukru: synteza Kilianiego - Fischera.
CHO + HCN CN
CHOH CHOH (dwie cyjanohydryny - po stronie prawej i lewej grupa - OH)
CHOH
COOH CHO
CHOH CHOH
CHOH CHOH
Skracanie łańcucha: degradacja Wohla - odwrotnośc syntezy.
(cukier, oksym, cyjanohydryna, skrócenie łańcucha)
CHO CH=NOH C≡N
CHOH CHOH CHOH CHO
CHOH CHOH
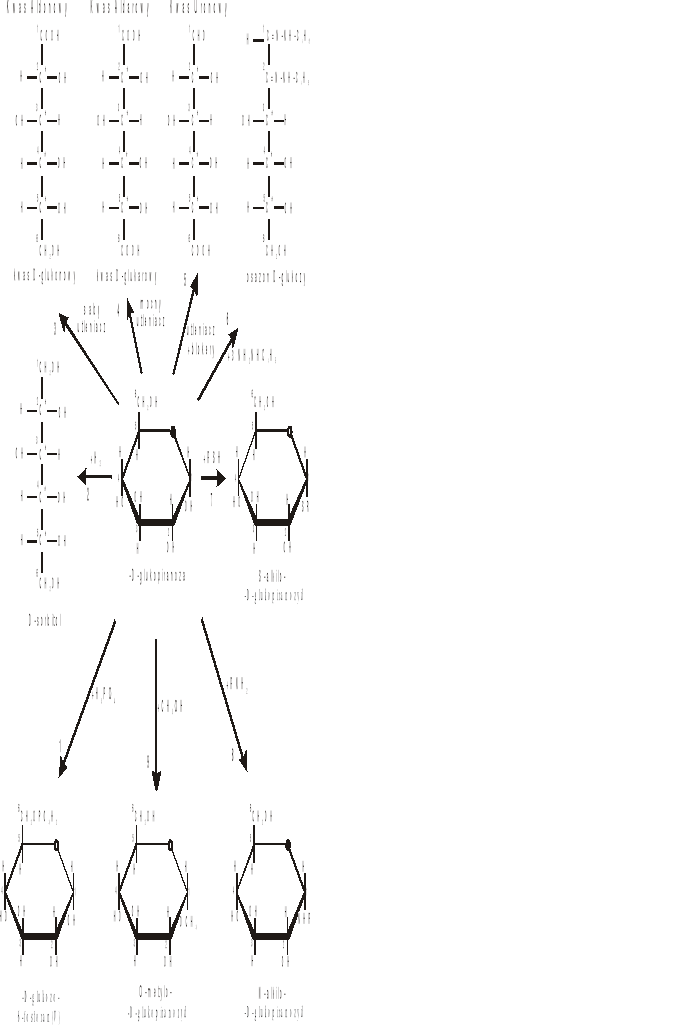
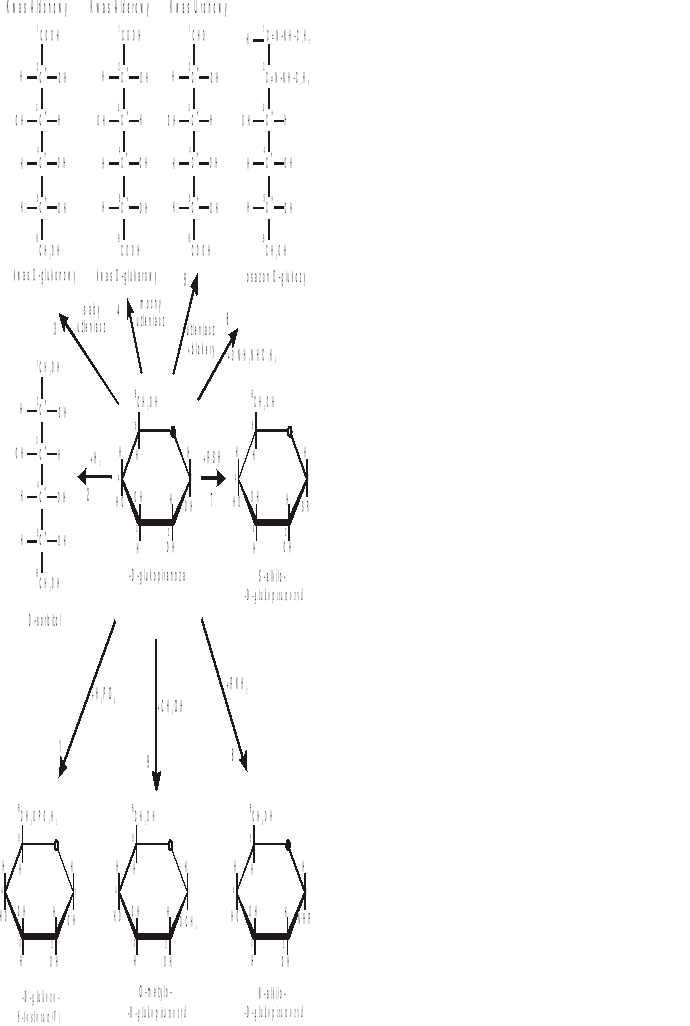
1. Reakcja estryfikacji - -OH + HOPO3 H2O + - O - PO3
2. Redukcja grupy aldehydowej do alkoholowej - -CHO + H2 CH2OH
3, 4, 5. Reakcje utlenienia - słaby utleniacz - utlenia tylko grupę aldehydową; mocny utleniacz utlenia grupę aldehydową i alkoholową do grupy karboksylowej; w obecności blokerów utlenia się tylko grupa alkoholowa do karboksylowej a aldehydowa jest zablokowana.
6. Reakcja identyfikacji cukrów prostych - tworzenie kryształów osazonów, łatwych do odróżnienia pod mikroskopem. Nie da się tylko zidentyfikować takich diastereoizomerycznych aldoz, które różnią się pomiędzy sobą konfiguracją wokół drugiego węgla w łańcuchu (pierwszego atomu asymetrycznego).
7, 8, 10. Tworzenie glikozydów - blokowanie grupy aldehydowej - cukier traci własności redukujące (zmiana końcówki -oza na - zyd). Powstają O - glikozydy (reakcje z alkoholami); N - glikozydy (reakcje z amoniakiem lub aminami); S - glikozydy (reakcje z tiolami (merkaptanami)).
Dwucukry i wielocukry
Dwucukry
(pochodne heksoz - C12H22O11)
glukoza + glukoza = maltoza (wiązanie α - 1,4 - O - glikozydowe; ma własności redukujące)
glukoza + galaktoza = laktoza (wiązanie α - 1,4 - O - glikozydowe; ma własności redukujące)
glukoza + fruktoza = sacharoza (wiązanie α -1,2 - O - glikozydowe; nie ma własności redukujących; hydroliza nosi nazwę - inwersji - podczas hydrolizy następuje odwrócenie kąta skręcalności płaszczyzny światła spolaryzowanego)
wielocukry
(pochodne heksoz - (C6H10O5)n)
skrobia:
zbudowana z amylozy - frakcja nierozpuszczalna w wodzie (80%) o budowie liniowej i wiązaniach α - 1,4 - O - glikozydowe i amylopektyny - frakcja w wodzie rozpuszczalna - 20% i wiązaniach α - 1,4 - O - glikozydowym i α - 1, 6 - O - glikozydowym.
Hydroliza skrobi: skrobia dekstryny maltoza glukoza
(C6H10O5)n (C6H10O5)m (m<n) C12H22O11 C6H12O6
glikogen:
materiał zapasowy wątroby, podobny do amylopektyny ale bardziej rozgałęziony.
celuloza:
materiał budulcowy roślin, podobny do amylozy ale o wiązaniach β - 1,4 - O glikozydowych (nie trawionych przez człowieka; ewentualnie przez enzym zwany emulsyną)
Aglikon - nie ma budowy cukru - GLIKOZYDY WŁAŚCIWE
Aglikon - ma budowę cukru - GLIKOZYDY NIEWŁAŚCIWE
(dwucukry i wielocukry)
H3O +
H2NOH
(CH3CO)2O
CH3COONa
Na +, CH3O -
CHOH
CHOH
OH
OH
OH
Aglikon
H
H
H
H
H
CHOH
2
O
Glikozydy nie mają własności redukujących i nie ulega mutarotacji
(czyli zmianie kąta skręcalności kąta skręcalności płaszczyzny światła spolaryzowanego przez świeżo sporządzony roztwór cukru)
Wyszukiwarka