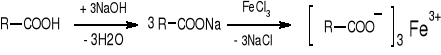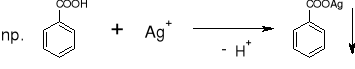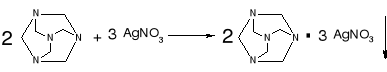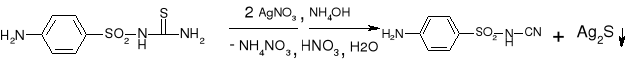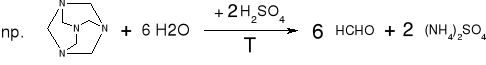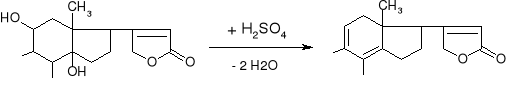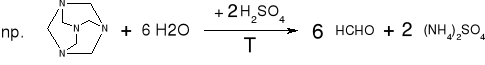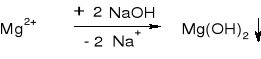Substancje reagujące: |
Reakcja: |
Wynik: |
||
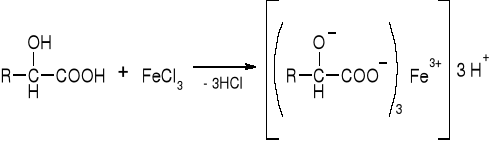
1) Reakcje z 10% roztworem chlorku żelazowego (FeCl3) |
||||
- Hydroksykwasy: cytrynowy, winowy, mlekowy, glukonowy (str. 117) |
|
Żółte zabarwienie |
||
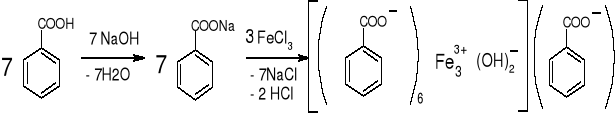
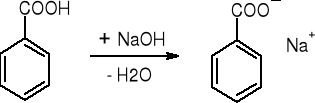
- Benzoesany: (str. 116) |
|
Cielisty osad, rozpuszczalny w nadmiarze odczynnika |
||
- Mrówczany, octany, propioniany, aminobenzoesany: (str. 116) |
|
Czerwone zabarwienie |
||
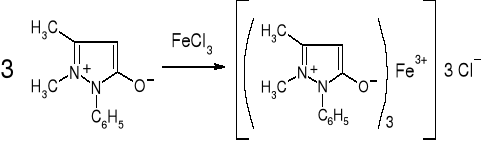
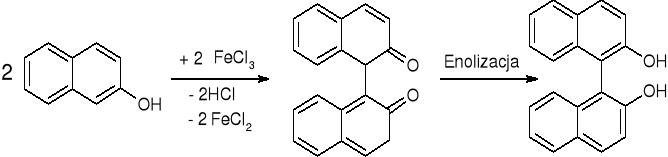
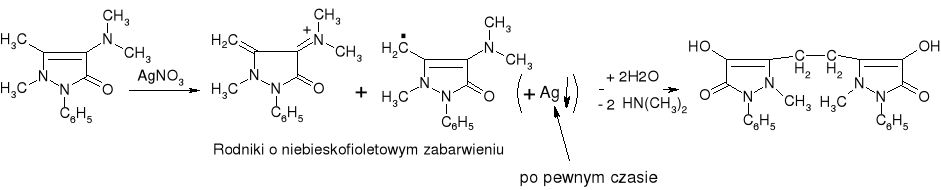
- Enole: fenazon (str. 276)
|
|
|
||
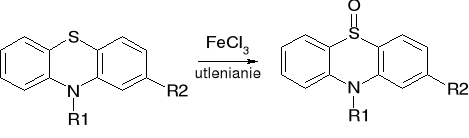
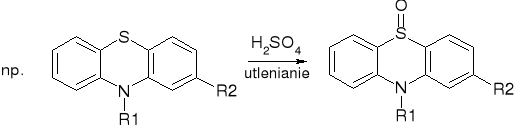
- Pochodne fenotiazyny: (str. 348)
|
(produkt pośredni - rodnik semichinonowy - daje to zabarwienie) |
|
||
- Neoarsfenamina; (str. 357) |
- brak reakcji |
|
||
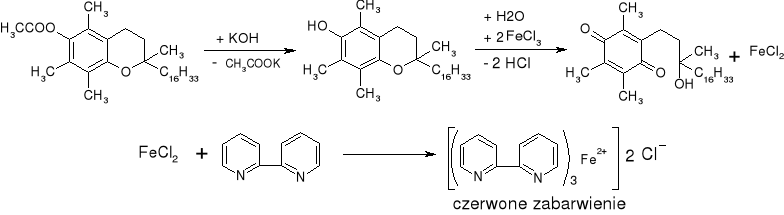
- Tokoferol: (str. 150)
|
|
|
||
- Rodanki: |
|
|
||
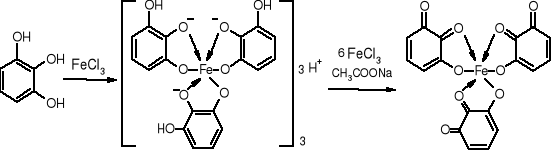
- Pirogalol (str. 90) |
|
Czerwonobrunatne zabarwienie, przechodzące w ciemnofioletowe po dodaniu 20% CH3COONa |
||
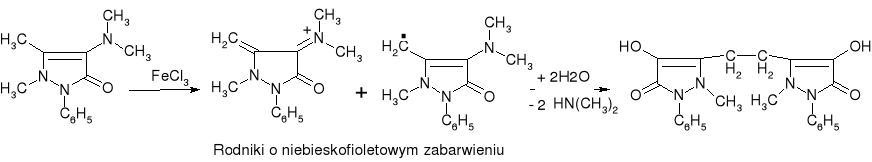
- Amninofenazon (str. 276), noraminofenazon:
|
|
Niebieskie lub niebieskofioletowe zabarwienie |
||
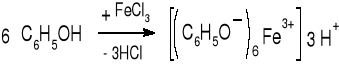
- Fenole: chlorofenol, krezol, trójkrezol, tymol, eugenol, morfina |
- Jak fenole (patrz niżej) |
|
||
- Fenole: fenol, rezorcynol, sulfoguajakol, salicylamid (str. 77) |
|
Fioletowe zabarwienie |
||
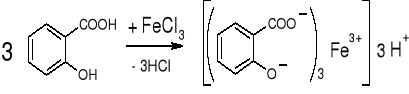
- Fenolokwasy i ich estry: kwas salicylowy, aminosalicylowy, salicylan metylu, salicylan fenylu; hydroksybenzoesan etylu, metylu i propylu (str. 131) |
|
|
||
- tiosiarczany: ? |
? |
|
||
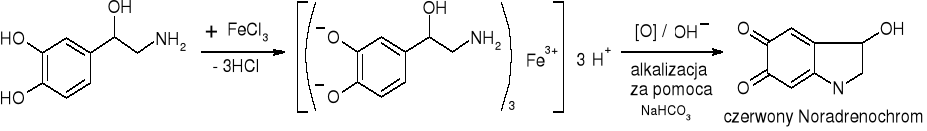
- Adrenalina, noradrenalina, izoprenalina, korbadryna: (str. 202) |
|
Zielone zabarwienie (w niektórych przypadkach po alkalizacji czerwone zabarwienie) |
||
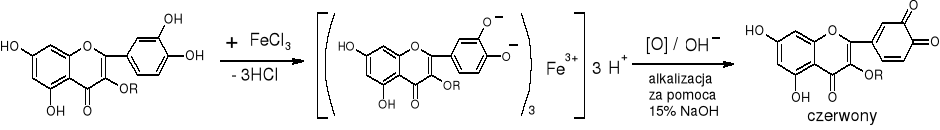
- Rutozyd: (str. 263)
|
|
|
||
- 2-naftol: (str. 88)
|
|
|
||
- Kreozot - mieszanina fenoli:
|
- jak fenole (patrz wyżej) |
|
||
Reakcje z 10% roztworem chlorku żelazowego (FeCl3) dodatnia po hydrolizie (estry fenoli): |
||||
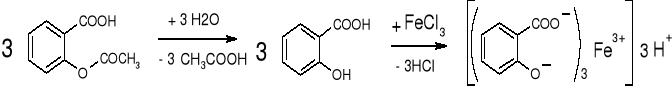
- Kwas acetylosalicylowy
|
|
Fioletowe zabarwienie |
||
- Edan: (str. 156) |
- po hydrolizie reaguje jak fenolokwasy (patrz wyżej) |
|
||
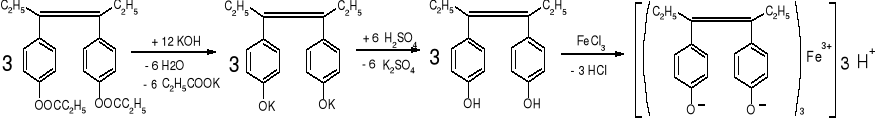
- Dwupropionian dwuetylostylbestrolu (str. 149)
|
|
Zielone zabarwienie |
||
- Benzoesan naftylu: (str.147) |
/najpierw hydroliza związku, a później jak dla 2-naftolu (patrz wyżej)/ |
|
||
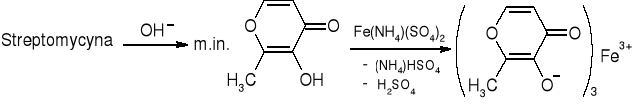
- Streptomycyna: (str. 185) |
|
Czerwone zabarwienie |
||
2) Reakcja z azotanem srebrowym (AgNO3): |
||||
- Sole nieorganiczne: Cl-, CN-, SCN-, Fe(CN)64-SO32-, BO32-, HPO32- (str. 31) |
|
Biały osad |
||
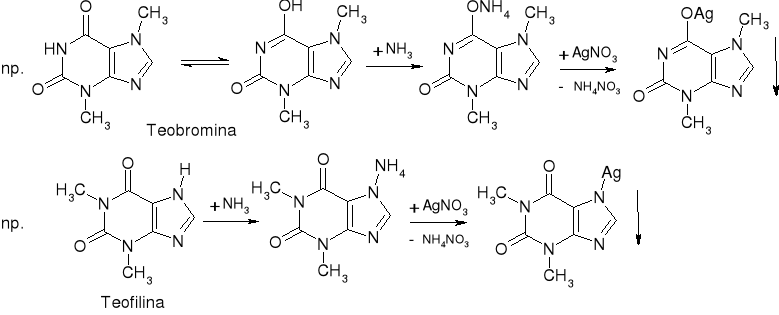
- Sole kwasów, enoli i iminów: szczawiany, winiany, benzoesany, salicylany, barbiturany, sulfonamidy, sacharyna, fenytoina, teofilina, teobromina, aminofilina, fenylobutazon, tiomersal
(Kofeina nie reaguje ponieważ nie ulega tautomerii i zablokowana jest pozycja 7) |
|
|
||
- Metenamina: (str. 107) |
|
Biały osad, rozpuszczalny w nadmiarze odczynnika |
||
- Tiosiarczany: ? |
?: biały osad to chyba Ag2S2O3, a czarny osad to wydzielająca się wolna siarka z rozpadu tego związku. |
Biały osad → czernieje |
||
- Br-, J-, PO43-, AsO33-:
|
|
Żółty osad |
||
- Fe(CN)63-:
|
|
Czerwonoomarańczowy osad |
||
- CrO42-, Cr2O72-: |
|
Czerwony osad |
||
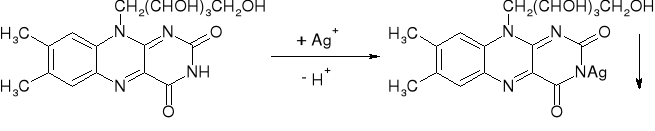
- Ryboflawina: (str. 316) |
|
Czerwone zabarwienie po kilku minutach |
||
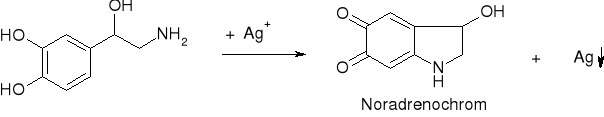
- Adrenalina, Noradrenalina, Izoprenalina, Korbadryna: |
|
Czerwone zabarwienie i czarny osad Ago |
||
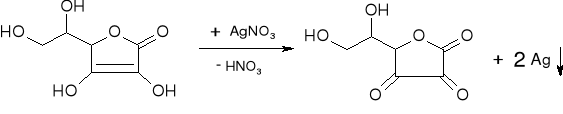
- Kwas askorbowy: (str. 135)
|
|
czarny osad Ago |
||
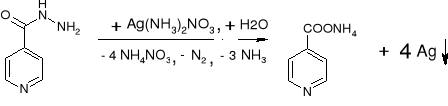
- Izoniazyd (po ogrzaniu): (str. 217)
|
|
|
||
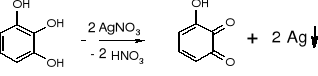
- Pirogalol: (str. 90) |
|
|
||
- Mrówczany (po ogrzaniu): (str. 119) |
|
|
||
- Aminofenazon (str. 276), Noraminofenazon: |
|
Fioletowe zabarwienie, po pewnym czasie czarny osad Ago |
||
Amoniakalny roztwór AgNO3: |
||||
- Kwas askorbowy, izoniazyd, pirogalol: |
- reakcje j.w. |
czarny osad Ago |
||
- w temp. 80oC: kwas winowy, aldehydy, chloroform, chlorobutanol, glicerol, sorbitol, sterydy z ugrupowaniem β-ketolowym |
- wszystkie te związki redukują na ciepło amoniakalny roztwór AgNO3 (do Ago)
|
|
||
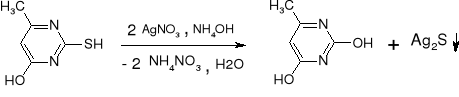
- Metylotiouracyl: (str. 324)
|
|
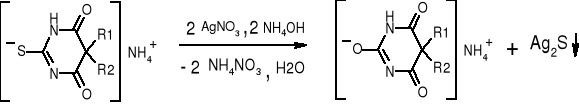
czarny osad Ag2S |
||
- Sulfatiokarbamid: (str. 332) |
|
|
||
- Tiopental: (str. 326) |
|
|
||
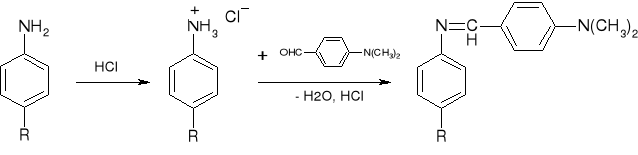
3) Reakcja z odczynnikiem Ehrlicha (HCl i aldehyd p-dwumetylo-aminobenzoesowy): |
||||
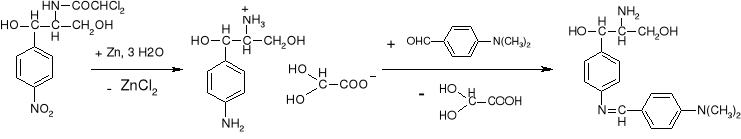
- I rzędowe amin aromatyczne: sulfonamidy, kwas aminobenzoesowy, kwas aminosalicylowy, aminobenzoesan etylu, prokaina, prokainamid, dwuchlorofenarsyna neoarsfenamina, etakrydyna i izoniazyd: (str. 189) |
|
Czerwonoomarańczowy osad lub zabarwienie |
||
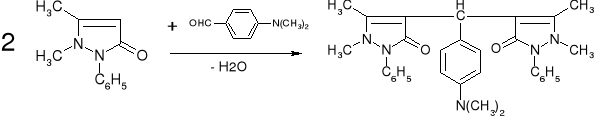
- Fenazon: (str. 276) |
|
Różowe zabarwienie |
||
- Tetracyklina: (str.234), mocznik (str. 170), uretan (str. 163), meprobamat (str. 164) |
- brak reakcji - nie znalazłem reakcji w książce, która nas obowiązuje, więc chyba trzeba tylko znać co z czym reaguje i jakiego koloru produkt powstaje.
|
Żółte zabarwienie, a po ogrzaniu brunatne |
||
- Chlortetracyklina: (str. 235) |
- brak reakcji |
Żółte, a po ogrzaniu niebieskozielone zabarwienie |
||
- Oksytetracyklina: (str. 235) |
- brak reakcji |
Fioletowe, a po ogrzaniu niebieskie zabarwienie |
||
- Antazolina: (str. 284) |
- brak reakcji |
Fioletowe zabarwienie po podgrzaniu |
||
- Ergometryna, ergotamina: (str, 265) |
|
Niebieskie zabarwienie po kilku minutach |
||
- Rezerpina: (str. 269) |
- brak reakcji |
Zielone zabarwienie |
||
- Tolazolina: (str. 283) |
- brak reakcji |
Zielone zabarwienie po ogrzaniu |
||
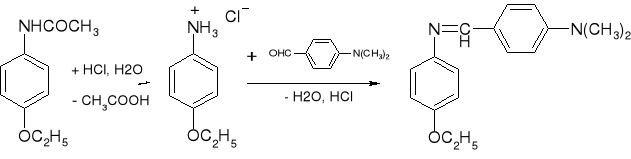
Reakcja z odczynnikiem Ehrlicha po hydrolizie za pomocą 15% HCl: |
||||
- Fenacetyna: (str. 222) acetarsol, lidokaina, fenylobutazon, pochodne benzotiadiazyny |
(ogólnie chodzi o to, aby za pomocą HCl, zhydrolizować te amidy do wolnej I aminy aromatycznej, która może już ulec reakcji z odczynnikiem Ehrlicha) |
Żółte zabarwienie |
||
Reakcja z odczynnikiem Ehrlicha po redukcji za pomocą Zn i 10% HCl: |
||||
- Chloramfenikol: (str. 227) |
(poprzez redukcję grupy nitrowej uzyskujemy I rzędową aminę aromatyczną) |
Żółte zabarwienie |
||
4) Reakcja z kwasem siarkowym (VI) (H2SO4): |
||||
16% H2SO4: |
||||
- Mleczan etakrydyny: (str, 303) |
|
Żółty osad |
||
- Chinina: (str. 293) |
- brak reakcji |
Niebieska fluorescencja |
||
- Hydrochlorotiazyd, metenamina, neoarsfenamina, noraminofenazon: (str.107) |
|
Po ogrzaniu zapach formaldehydu (HCHO), a po dodaniu NaOH zapach amoniaku (NH3) |
||
96% H2SO4: |
||||
- Kwas dehydrocholowy: (str. 242) |
- brak reakcji (dodajemy oprócz kwasu siarkowego jeszcze HCOOH) |
Żółte zabarwienie z zieloną fluorescencją |
||
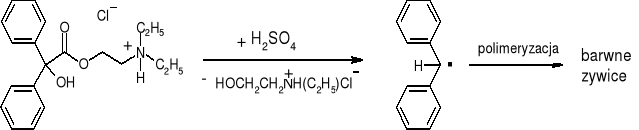
- Benaktyzyna: (str. 152) |
|
Żółte zabarwienie szybko przechodzące w czerwono-amarantowe (chyba kobieta pisała ten skrypt - naszukałem się co to za kolor...) |
||
- Cyklobarbital, heksobarbital: (str. 177) |
- brak reakcji |
Żółte zabarwienie → pomarańczowe → czerwone |
||
- Chlorpromazyna: (str. 348), prometazyna, difenydramina, oksytetracyklina, hydrokortyzon, prednisolon, cholesterol, cholekalcyferol, dezoksykorton (temp.), meprobamat (temp.) |
(produkt pośredni - rodnik semichinonowy - daje to zabarwienie)
|
Czerwone zabarwienie |
||
- Uabaina: (str. 258) |
|
Różowe zabarwienie |
||
- Dwuetylostylbestrol: (str. 147) |
- brak reakcji |
Żółtopomarańczowe - pod wpływem wody przechodzi w różowe |
||
- Tetracyklina: (str.234) |
- brak reakcji |
Fioletowe zabarwienie |
||
- Chlorotetracyklina: (str.234) |
- brak reakcji |
Niebieskie zabarwienie przechodzące w oliwkowozielone |
||
- Estradiol: (str. 241) |
- brak reakcji |
Żółtozielone zabarwienie z zieloną fluorescencją, po dodaniu wody zabarwienie pomarańczowe |
||
- Metenamina: (str 107) hydrochlorotiazyd, primidon, noraminofenazon, neoarsfenamina |
|
Po ogrzaniu zapach formaldehydu (HCHO), |
||
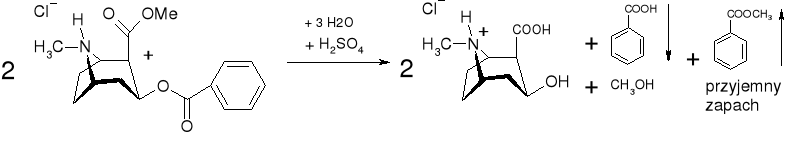
- Kokaina: (str. 302) |
|
Po ogrzaniu przyjemny estrowy zapach benzoesanu metylu |
||
5) Reakcja z kwasem azotowym (V) (HNO3): |
||||
10% HNO3: |
||||
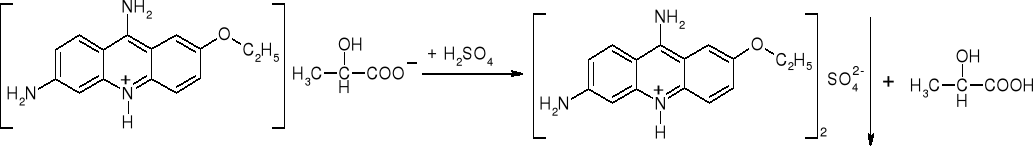
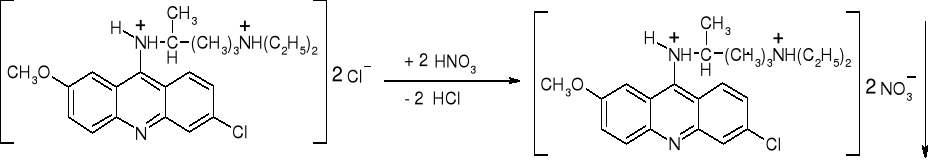
-Chlorowodorek mepakryny: (str. 305) |
|
Żółty osad |
||
65% HNO3: |
||||
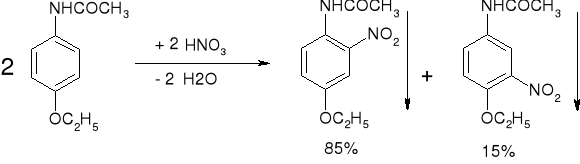
- Fenacetyna: (str. 222) |
|
Pomarańczowy osad |
||
- Apomorfina, antazolina, morfina: (str. 289) |
- brak reakcji |
Czerwone zabarwienie |
||
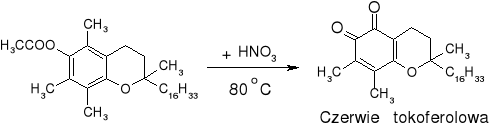
- Tokoferol: (str. 149) |
|
Czerwone zabarwienie po ogrzaniu (80oC) |
||
6) Reakcja z wodorotlenkiem sodowym (NaOH): |
||||
10% NaOH: |
||||
- Substancje o charakterze kwasów organicznych: |
|
Substancja nierozpuszczalna w H2O rozpuszcza się w 10% NaOH |
||
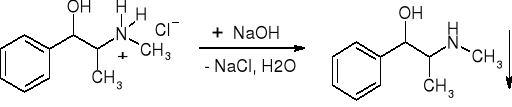
- Sole zasad organicznych: np. Efedryna (str. 199)
|
|
Z wodnego roztworu wytrąca się osad |
||
- Sole Ca2+, Mg2+, Zn2+, Pb2+, Fe2+: |
|
|
||
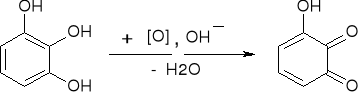
- Pirogalol, rezorcynol: (str. 90) |
|
Żółte zabarwienie |
||
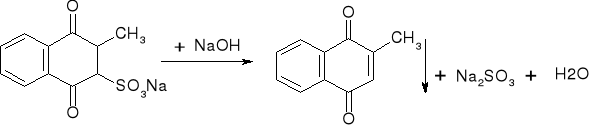
- Menadion: (str. 99) |
|
Żółty osad |
||
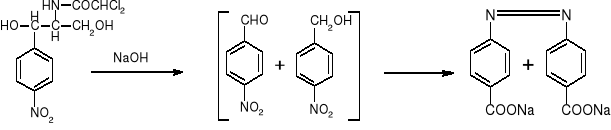
- Chloramfenikol: (po ogrzaniu) (str. 228)
|
|
Pomarańczowe zabarwienie |
||
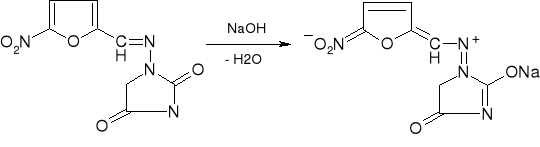
- Nitrofurantoina: (str. 230)
|
|
|
||
- Dianton: (str. 100) |
- brak reakcji
|
Czerwone zabarwienie |
||
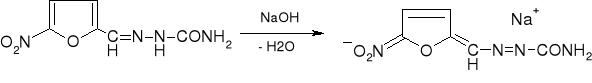
- Nitrofural: (str. 229)
|
|
|
||
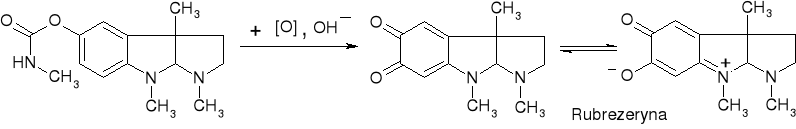
- Fizostygmina: (str. 167) |
|
|
||
15% NaOH: |
||||
- Wodzian chloralu: (str. 108)
|
|
Zapach chloroformu |
||
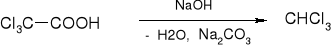
- kwas trójchlorooctowy: (str. 122)
|
|
|
||
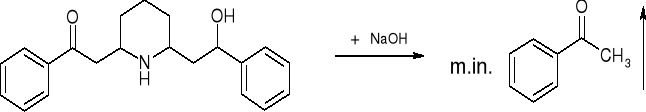
- Lobelina:
|
|
Zapach acetofenonu |
||
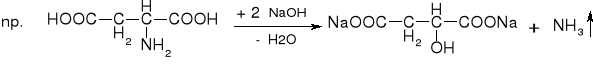
- Kwas glutamowy: (str. 209), uretan, meprobamat, sulfoguanidyna, ureidy o łańcuchu otwartym
|
Ogólnie wszystkie podczas reakcji z 15% NaOH tracą NH3 |
Zapach amoniaku |
||
Stapianie z NaOH: |
||||
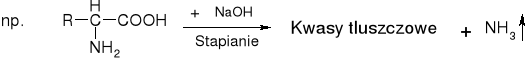
- Aminokwasy: (str. 206), amidy, imidy, ureidy, uretany, sulfonamidy, piramidon, streptomycyna
|
Ogólnie wszystkie podczas stapiania z NaOH tracą NH3 |
Zapach amoniaku |
||
Wyszukiwarka