arkusz aI + odpowiedzi0002

Zadanie 5. (2 pkt.)
Określ rodzaj reakcji, przyjmując jako kryterium klasyfikacji:
a) liczbę reagentów.....................................
b) zmiany energii wewnętrznej układu ..................
Zadanie 6. (2 pkt.)
Oblicz, jaką objętość w warunkach normalnych zajmie gaz powstały w wyniku przemiany 0,5 mola HgO.
Zadanie 7. (1 pkt)
Dany jest zbiór procesów: I — rdzewienie żelaza, II spalanie metanu, III — tworzenie osadu AgCI w roztworze: wodnym, IV — czernienie srebrnych przedmiotów, V — tworzenie NaOH w reakcji sodu z wodą, VI — fotosynteza węglowodanów w roślinach. Wskaż zestaw, w którym podano tylko reakcje powolne:
D. IV, V, VI.
A. I, II, III, B. II, IV, V, C. I, IV, VI,
Zadanie 8. (1 pkt)
Podaj 2 czynniki pozwalające zwiększyć szybkość: reakcji cynku z kwasem solnym:
Zadanie 9. (2 pkt.)
W pewnej temperaturze stężenie procentowe nasyconego wodnego roztworu AgNO, wynosi 68,3%. Oblicz rozpuszczalność tej soli w wodzie.
Zadanie 10. (6 pkt.)
Przeprowadzono doświadczenie przedstawione za pomocą rysunków:
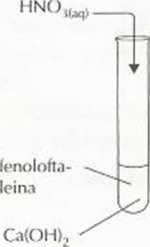
II

NaOH
NH«CIW

Ułóż równania reakcji zachodzących w probówkach, w formie cząsteczkowej i jonowej (pełnej i skróconej).
8
I
Wyszukiwarka
Podobne podstrony:
arkusz dI + odpowiedzi0002 Zadanie 7. (2 pkt.) Określ, jak zmieni się wydajność reakcji I 2CO,pl +&n
arkusz aI + odpowiedzi0005 Zadanie 30. (1 pkt) Podano określenia pojęć: A wzrost zawartośc i gazów s
arkusz aI + odpowiedzi0004 Zadanie 17. (1 pkt) Dany jest wzór sumaryczny związku: C,H,Br.. Podaj wzo
arkusz cI + odpowiedzi0002 Zadanie 7. (2 pkt.) W celu otrzymania wodoru można przeprowadzić reakcję
arkusz aII + odpowiedzi0003 Zadanie 9. (1 pkt) Wyjaśnij, jak rozumiesz stwierdzenie: „Reakcja syntez
arkusz bII + odpowiedzi0002 Zadanie 5. (4 pkt.) Przeprowadzono doświadczenie przedstawione za pomocą
arkusz aII + odpowiedzi0002 Zadanie 5. (2 pkt.) Wyjaśnij, dlaczego objętość mieszaniny etanolu z wod
arkusz bII + odpowiedzi0003 Zadanie 8. (4 pkt.) W trzech elektrolizerac h z elektrodami platynowymi
więcej podobnych podstron