arkusz dII + odpowiedzi0003

Zadanie 10. (4 pkt.)
W stanic równowagi reakcji
N2<s> + 3H2Ik, ► 2NH3<8>
w określonej temperaturze stężenia reagentów wynoszą: cH, = 2 mol-Hm \ cNi = 1 mol • dm \ cN11( --- 4 mol dm Oblicz stałą równowagi reakcji oraz początkowe stężenia substratów tej re
Zadanie 11. (3 pkt.)
Na podstawie energii wiązań:
C< „ = 412 kj-mol Fc_c = 830 k) • mol \ fn_n = 420 kj • mol'1, wyznacz zmianę entalpii reakcji:
2CH4(8) —«► 11-CsC Hfel + 3H,;k)
Zadanie 12. (3 pkt.)
Ułóż równania połówkowe i dobierz współczynniki w równaniu:
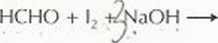
HCOONa
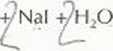
• Informacja do zadań 13 i 14
W celu zbadania mocy kwasów wykonano doświadczenie zilustrowane rysunkiem:
II
h2so4
III
CH,C(X)H

Cl tjCOONd.j
Zaobserwowano: pojawienie się zapachu charakterystycznego dla octu (I); wydzielanie się bezbarwnego i bezwonnego gazu (II) oraz wydzielanie się bezbarwnego gazu o charakterystycznym zapachu (III).
78
Wyszukiwarka
Podobne podstrony:
arkusz dII + odpowiedzi0004 Zadanie 13. (4 pkt.) Ułóż równania reakcji wykonanych w doświadczeniu i
arkusz eI + odpowiedzi0003 Zadanie 10. (4 pkt.) Ustal, ile dmł wodv i ile gramów 98-orocentowego roz
arkusz bII + odpowiedzi0005 Zadanie 17. (4 pkt.) Zaproponuj cykl reakcji prowadzących do otrzymania
arkusz cI + odpowiedzi0006 Zadanie 26. (2 pkt.) Ułóż równanie reakcji, w której wyniku otrzymasz dip
arkusz dII + odpowiedzi0002 Zadanie 5. (2 pkt.) Wyjaśnij, dlaczego cząsteczki wody w stanic stałym t
2009 05 25!;39;32 Materiał diagnostyczny Arkusz - poziom podstawowy 6 Zadanie 10. (1 pkt) Rower kosz
więcej podobnych podstron