P1100264
chemiczny rozkład pod wpływem strumienia elektronów. W tym przypadku efced^j o proces chemiczny. Powstanie widma masowego wywołane jest pracz wiązki joofc, utworzone z jonów o różnych masach. Powstają one w źródle jonowym spektra metru masowego po rozłożeniu cząsteczek silnym strumieniem elektronów; po\wt* wanie jonów zachodzi zgodnie ze złożonymi mechanizmami stopniowymi.
Spektrometr masowy (rys. 28.1) w zasadzie składa się z trzech cletneiufoy; źródła jonowego, analizatora i układu rejestracji różnych jonów. W dalszej części
/
|
Cżątiectfi otójełm |
My mmdHelow } |
Jony rozdzieleń* | ||
|
im |
1 |
3 |
tgź'—-<*r |
4 |
|
'Sk, | ||||
Rys. 28.1. Blokowy schemat spektrometru masowego / - doprowadzenie próbki, 2 — źródło Jonów, 2 — analizator, 4 — rejestracja
rozdziału zostanie opisany mechanizm powstawania widma masowego i funkcje poszczególnych części składowych spektrometru.
Próbka, która musi być w stanic gazowym, podawana jest do próżniowej Vx-mory jonizacyjnej, gdzie cząsteczki związku bombardowane są elektronami emitowanymi z rozżarzonego włókna wolframowego. Elektrony te o dużej energii tire-tycznej powodują rozkład cząsteczek na fragmenty, a powstające fragmenty jsi i jiierozłolone cząsteczki są jonizowane. Jony (zazwyczaj tylko jony dodatnie) $j następnie przyspieszane i ogniskowane tak, że powstaje wąska wiązka przechodząc* do analizatora. W analizatorze wiązka jonów ulega rozdzieleniu na poszczegóte wiązki zgodnie zc stosunkiem ich masy i ładunku (m/e), przy czym jony różnią saę między sobą energią uzyskaną w polu magnetycznym i elektrycznym.
Po wyjścia z analizatora wiązki jonowe kierowane są do kolektora speforc-roetni, gdzie prąd jonowy zostaje wzmocniony I zarejestrowany fotograficznie lub fotoelektrycznie.
Położenie linii na fotografii lub położenie maksimum na taśmie rejestracyjnej określone jest przez rozdzielenie jonów według ich mas. Zaczernienie linii lub wysokość maksimów odpowiada względnej zawaitości poszczególnych jonów.
28.1.1. Procesy jonizacyjne
Powstawanie jonów podczas rozkładu cząsteczek, który zachodzi w komora jonizacyjnej, ma pierwszorzędne znaczenie w spektrometrii masowej.
Do zjonizowania cząsteczki, tj. do oderwania jednego lub więcej elektronów od cząsteczki, potrzebna jest określona praca, którą określa się jako energię jonteż Energia jonizaęp różnych cząsteczek jest różna i w przypadku cząsteczek organice nych wynosi 8-13 eV. Aby prawdopodobieństwo jonizacji było jak największe, cwp jonizacji powinna być istotnie wyższa od wartości potencjału jonizucyjncgo cząstek
Energię potrzebną do jonizacji uzyskuje się w zderzeniach z elektronami, fotonami (focojonizacju), -/.jonizowanymi cząsteczkami (jonizacja chemiczna), albo W polu elektrycznym (lO^-lO1 V/cm).
W analitycznych zastosowaniach spektrometrii masowej najodpowiedniejsza jest jonizacja pod wpływem bombardowania cząsteczek gazu elektronami emitowanymi przez rozżarzoną katodą. Energia elektronów (70-100 eV) odpowiada dla większości gazów maksymalnej wydajności jonizacyjnej. Zastosowanie takiego źródła jest ograniczone do substancji, które pod ciśnieniem 1,33 • 10 * Pa mogą wystosować w sianie gazowym.
Elektrony o energii kilkudziesięciu cV przekazują cząsteczce tylko część swojej energii. Jeżeli otrzymana energia jest nieco większa od potencjału jonizacyjnego cząsteczki, to zachodzi wybicie elektronu z cząsteczki i powstaje jon cząsteczkowy według schematu
Me-re — Me+4-2* (28.1)
Energia wzbudzenia jonu cząsteczkowego ma przeważnie charakter elektronowy i stosunkowo szybko maleje w wyniku przejść bezprotnienistych zwiększając energię wewnętrzną (oscylacyjno-rotacyjną). Ze wzrostem energii elektronów wzrasta prawdopodobieństwo jonizacji oraz wewnętrzna energia jonu cząsteczkowego. Jeżeli na pewnym oscylacyjnym stopniu swobody zgromadzi się więcej energii, niż wynosi energia dysocjacji, fo jon cząsteczkowy rozpadnie sio w miejscu najsłabszego wiązaniu i powstanie zjonizowany fragment, obojętna cząsteczka lub rodnik
MeX* -> Mc+ +X (28.2)
gdzie X — obojętna cząsteczka lub rodnik.
Wzbudzone jony, powstałe w wyniku rozkładu, owy starczającej energii wewnętrznej ulegają dalszemu podobnemu rozkładowi tak, że wzrost energii elektronów powoduje powstanie bardziej złożonego widma substancji. Na przykład w wyniku rozkładu tak prostej cząsteczki, jak cząsteczka metanu, może powstać aż siedem różnych fragmentarycznych jonów: CH*, CH+, CHJ, CH\C\HJ, H*; w przypadku bardziej złożonych cząsteczek liczba ich jest o wiele większa. Równowaga ®*ędzy tymi procesami rozkładu jest osiągana dla bardzo dużych energii elektronów (ponad 50 eV), gdy względne natężenia prądów jonowych nic ulęgają zmianie, lab zmieniają się bardzo mało.
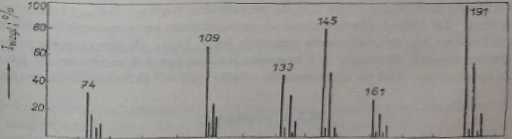
60 80 100 120 1*0 100 160 200
■ •-
Rys. 28.2. Widmo masowe 2, S-dwuchlóro nitrobenzenu
399
Wyszukiwarka