P1100288
domieszek gran uhreyjny cli oraz od sposobu granulacji. Pory wo wtórnej struktura* porowatej są nkjednnkowc i ich rozmiary wynoszą 1-1000 nm. W pierwotnej *lruk-turze porowatej adsorpcja zachodzi selektywnie, wo wtórnej — jest nic selektywna. Adsorbują się także substancje, które nie mogą wniknąć do pierwotnej struktury porowatej. Transport masy do struktury pierwotnej odbywa się zu pośrednictwem struktury wtórnej, która dzięki temu może częściowo wpływać na dynamiczne wla-saości adsorpcyjnc granulowanych sit molekularnych.
33J.6. Krytyczne rozmiary cząsteczek
Krytyczne rozmiary cząsteczek udsorbatu można obliczyć np. stosując wartości promieni atomowych van der Waolsa. W adsorbentach «> okrągłym kształcie otworu porów (neolity typu A, X, Y) wystarczy wyznaczyć tylko jedną wartość krytycznego rozmiaru cząsteczki.
Wewnętrzna powierzchnia pierwotnej struktury porowatej jest dostępna dla cząsteczek adsorbatu. których rozmiar krytyczny jest mniejszy albo równy efektywnemu przekrojowi porów. Ze względów sferycznych nic jest ona dostępna dla czą-
Tablica 33.2. Średnice krytyczne cząsteczek substancji
|
Cząsteczka |
średnica krytyczna nm |
Cząsteczka |
Średnica b>iycai om | |
|
He |
0-2 |
CaH* |
0,425 | |
|
Ne |
0.32 |
CjH, |
0,444 | |
|
Ar |
0.33.1 |
HaO |
0.26 | |
|
Kr |
0,394 |
CHjOH |
0.30 | |
|
Xe |
0,437 0.40 |
CO |
0.32 | |
|
Clh |
GOa |
0.2S | ||
|
CF* |
0.533 |
CaF* |
0.533 | |
|
ca |
0,688 |
Ca CI. |
0,688 | |
|
CBr. |
0.746 |
c,n. |
0.489 | |
|
C(CH,)4 |
0.688 |
/n>-C«Hie |
0,558 | |
|
Hj |
0,24 |
c/ś/o>C|H ■ 0 |
0.435 | |
|
O, N, |
0.2S 0.30 |
c.h6 |
0l56 |
sieczek adsorbatu, których kry tyczne rozmiary bardzo znacznie przekraczają efektywne przekroje porów adsorbentów.
Krytyczne rozmiary cząsteczek niektórych substancji przedstawiono w tabl. 33.2.
33J.7. Izoterma adsorpcji Petersona-Redlicha
Najważniejszą Informacją do opisu adsorpcji na zeolitach jest izoterma adsorpcji. W większości przypadków izotermy to są wypukłe w stosunku do osi stężenia i ze wzrostem stężenia osiągają graniczne wartości adsorpcji Vm. Graniczna wartość adsorpcji jest określona tym, że pory sit molekularnych mają ograniczoną objętość. Po wypełnieniu tej objętości adsorpcja już nic może zachodzić. Grankaow wartości Km są stałymi o dużym znaczeniu, których znajomość jest ważna do inter-
prctocj* wyników adsorpcji. Stalą tę nic zawsze można okfcfiić eksperymentalnie, pa przybliżonego obliczenia można stosować zależność
Vmx Li - K.2 Lj (33.1)
gdac: ymi — graniczna objętość substancji, dla której można tę wielkość zmierzyć, — długość cząsteczki substancji; Vm^ — graniczna objętość substancji, której wielkości zmierzyć nie można, Lj — długość cząsteczki tej substancji.
W prnktycc często jest bardzo trudno znaleźć izotermę, która ujmowała by x dostateczną dokładnością zachowanie się adsorbatu r.a sitach molekuł ornych \v szerokim zakresie warunków pracy. W tych przypadkach można dla całej grupy substancji wybrać postępowanie analogiczne do tego, które zastosowali Petersem i Redlicli. Do opisu izoterm adsorpcji n-parafin na sitach molekularnych użyli oni wzór empiryczny
*» 11Si 0Ł2)
pod warunkiem, żc O < </ < 1, gdzie m — masa adsorhntu, p — ciśnienie adsorbatu. A. B, g — odpowiednie stałe specyficzne.
Dla małych ciśnień izoterma jest prostoliniowa, dla stężeń większych niewiele przewyższa wartości izotermy Langmuira i odpowiada krzywej m — A]Bp1'9. Po uzyskaniu ciśnienia nasycenia pm i granicznej wartości adsorpcji n\ (adsorpcja odpowiadająca ciśnieniu pj można izotermę przedstawić w postaci
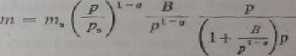
która dla g = 1 przekształca się w równanie Langmuira. Z równania (33.3) wynika, It liczba efektywnych miejsc adsorpcji rośnie zc wzrostem ciśnienia (stopniowo są obsadzane miejsca o coraz mniejszej energii adsorpcji) oraz 2c ciepło adsorpcji naleje ze wzrostem ciśnienia.
Autorzy wykazali, że ich teorię można rozszerzyć do opisu adsorpcji mieszanin j adsorpcji roztworów.
33.3. ORGANICZNE SITA MOLEKULARNE. ROZDZIELANIE SUBSTANCJI O DUŻYCH CZĄSTECZKACH
Pierwsze pomyślne wyniki rozdzielania substancji o dużych cząsteczkach me-I todą „przesiewania cząsteczek** uzyskano przez zastosowanie żelu skrobii. Roz-I gałęzione łańcuchy amylopcktyn w napęczniałych granulkach tworzą jakby sito. I do którego mogą wchodzić cząsteczki o masie cząsteczkowej do 5000, a dla nic-I których specjalnie preparowanych skrobii nawet do 60 000. Efekt sitowy stwicr-] dzono także w żelach agaru i żelatyny. Żele substancji naturalnych (skrobia, agar.
I żelatyna) mają jednak wiele wad. jak np. łatwe uszkodzenie enzymami.
Duży postęp w dziedzinie techniki przesiewania makrocząsteczek jest związany z wprowadzeniem syntetycznych sit molekularnych w oparciu o dekstran, poli-

447
Wyszukiwarka